糖皮质激素规律治疗与成人免疫性血小板减少症近期复发的关系
高亚玥,马一盖
(中日友好医院 血液科,北京 100029)
免疫性血小板减少症 (immune thrombocytopenia,ITP)是一种自身免疫性疾病,其特点为正常血小板免疫性破坏,最常发生于针对一种不明原因刺激的反应。过去称为免疫性或特发性血小板减少性紫癜(immune or idiopathic thrombocytopenic purpura)。ITP分为原发性和继发性2种,前者为单独的血小板减少,后者包括自身免疫性疾病、病毒感染和某些药物。糖皮质激素、切脾和免疫抑制剂是目前治疗原发性ITP的主要选择,而糖皮质激素仍然是首选治疗,有效率为2/3。如何正规使用糖皮质激素、如何规律减量和治疗至少持续多长时间,目前尚无统一的认识。本研究通过我院门诊和住院ITP患者糖皮质激素治疗后长期随访分析,旨在探讨糖皮质激素治疗的剂量和持续时间与复发率的关系,期望进一步规范ITP的糖皮质激素治疗。
1 材料和方法
1.1 病例选择
1994年8月~2012年4月在我院血液科门诊和住院新诊断的ITP患者,包括原发性和继发性,共101例,其中男23例、女78例;平均年龄46.3岁。诊断原发性ITP 94例、继发性ITP干燥综合征1例、B细胞淋巴瘤2例、Evans综合征4例。随访日期截止至2013年2月31日,中位随访时间63个月(10~336个月)。
1.2方法
血小板<30×109/L伴出血患者开始糖皮质激素治疗。90例给予强的松1mg/kg,3~4周(个别患者给予地塞米松10~15mg,5~7d后改为相应剂量的强的松),在起始剂量基础上减量1/3,2~3周,此后均在现剂量基础上减量1/4,2~3周、1/5 2~3周、1/6 2~3周,之后每 3~4周减量 1/8至停药,激素治疗至少6个月以上。举例:体重60kg患者,开始给予强的松 60mg/d,3~4 周, 此后 40mg/d,2~3周、30mg/d 2~3 周、25mg/d,2~3 周、20mg/d,2~3周、17.5mg/d,2~3 周、15mg/d,2~3 周等。 采用上述治疗方案的患者称为常规治疗组。开始激素治疗3~4周部分有效患者,也按上述方法逐渐减量;无效患者也逐渐减量,并同时加用其他(如环孢霉素A)治疗,减量速度缩短1倍以上。11例患者未按上述原则治疗,激素自行停用或随意减量,为非常规治疗组。
1.3 诊断和疗效标准[1,2]
1.3.1 原发性ITP诊断标准
至少2次检查血小板计数减少,血细胞形态无异常;脾脏一般不增大;骨髓检查:巨核细胞数增多或正常、有成熟障碍;须排除其他继发性血小板减少症。
1.3.2 疗效标准
(1)完全反应(CR):治疗后 PLT≥100×109/L,且没有出血。 (2)有效(R):治疗后 PLT>30×109/L,并且比基础血小板计数增加2倍,且没有出血。(3)无效(NR):治疗后 PLT<30×109/L 或者血小板计数增加不到基础值的2倍或者有出血。(4)复发:有以下情况之一者:①患者CR后,血小板计数<100×109/L或者出血;②患者CR后,血小板计数<30×109/L或者血小板计数增加不到基础值的2倍或者有出血。(5)糖皮质激素依赖:指患者需要继续或反复给予糖皮质激素治疗>2个月,以维持血小板计数>30×109/L,避免出血。
1.4 统计学方法
应用SPSS 13.0软件进行相对和危险度检验,独立样本采用t检验及χ2检验。
2 结果
2.1 2组患者的基线情况
2组患者的基线临床资料比较见表1。
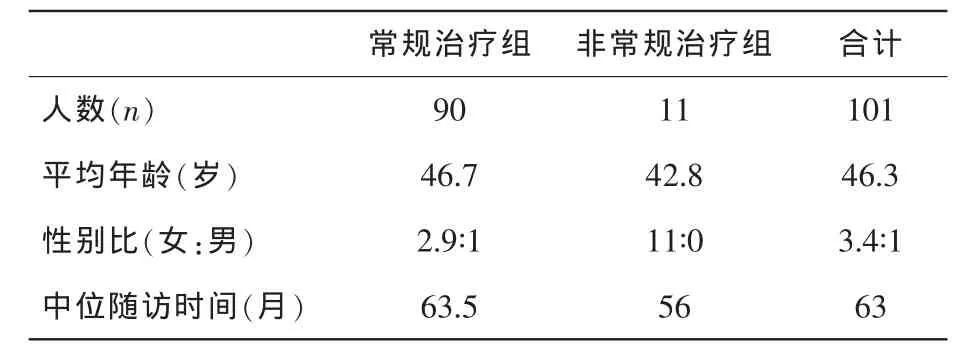
表1 2组患者的临床资料
2.2 2组激素疗效比较
按医嘱应用糖皮质激素治疗并逐渐减量的常规治疗组与自行停用或随意减量的非常规治疗组比较,其初始有效率均较高,无统计学差异(均P>0.05)。初始激素治疗总有效率66.3%,见表2。
2.3 2组复发率比较
本次研究中位随访时间为63个月,常规治疗组与非常规治疗组比较,复发率显著减少(17.9%vs 81.8%,P<0.01),且平均复发时间显著延长(44.8个月 vs 4.8个月,P<0.05)。非常规治疗组复发的相对危险度是常规治疗组的20.7倍,见表3。
2.4 2组并发症和生存率比较
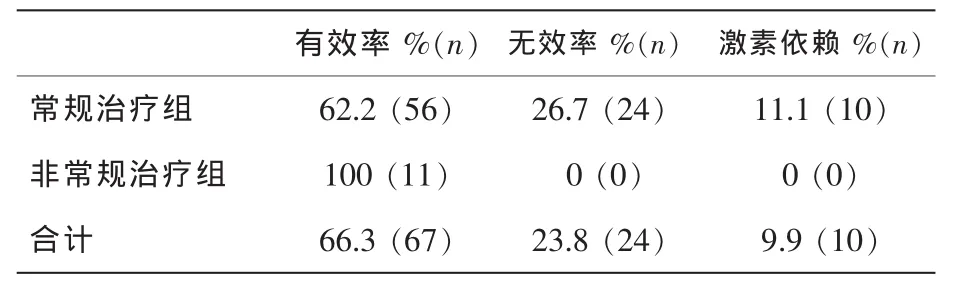
表2 2组激素疗效比较
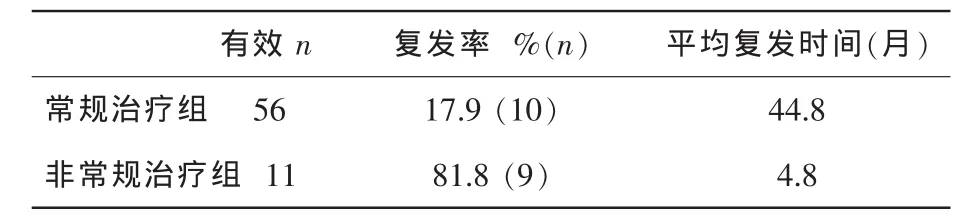
表3 2组复发率比较
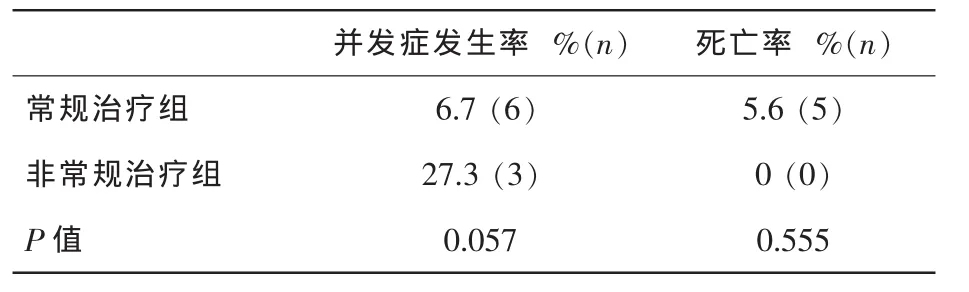
表4 2组并发症和死亡率比较
并发症主要指出现颅内出血、消化道出血、股骨头坏死等严重并发症。2组的并发症发生率及死亡率比较无显著性差异,见表4。
3 讨论
3.1 糖皮质激素治疗的有效率与长期复发率
综合文献显示,强的松或强的松龙1mg/kg Qd,连续2~4周,血小板上升后逐渐减量,有效率可达 50%~60%,但长期有效率仅有 10%~25%[3~6]。
本次研究初始激素治疗总有效率可达66.3%,长期复发率为28.4%,与文献相符,无论常规治疗组还是非常规治疗组,初始激素治疗有效率均很高,但非常规治疗组复发率81.8%,明显高于常规治疗组12.9%,近似估计其复发相对危险度是正规治疗组的20.7倍,且平均复发时间4.8个月(0.5~14个月)明显短于常规治疗组44.8月(2~139个月),均具有明显统计学意义。2组的并发症发生率及死亡率无显著性差异。
3.2 影响糖皮质激素疗效的原因
3.2.1 血小板膜糖蛋白
ITP患者自身抗体破坏血小板主要是自身抗体与血小板抗原靶位-血小板膜糖蛋白(platelet membrane glycoprotein,GP, 主要是 GPⅡb/Ⅲa 和GPIb-Ⅸ)特异性结合,通过抗体的Fc段与巨噬细胞的受体(FcγR)结合,在网状内皮系统被吞噬和破坏,也可通过细胞毒性T细胞的直接杀伤或由补体介导的溶解破坏[7]。研究表明:针对血小板GPⅡb/Ⅲa和GPIb-Ⅸ的自身抗体在ITP中引起血小板清除的机制不同。抗GPIIb/Ⅲa抗体通过Fc途径清除血小板,而抗GPIb-Ⅸ抗体清除血小板不依赖Fc途径,尽管这种不依赖Fc途径清除血小板的机制尚未完全阐明,但研究证明,抗GPIbα抗体通过Ashwell-Morell受体和 MAC-1整合素,诱导GPIbα去涎酸化,使血小板活化和凋亡增加,由巨噬细胞吞噬清除,是GP I b抗体引起血小板清除的主要途径[8,9]。
Zeng等研究发现,抗GPIbα抗体阳性患者大剂量地塞米松治疗反应率明显低于抗GP1Ib/Ⅲa抗体阳性患者(26.5%vs 72.1%,P<0.05),并且抗GPⅡb/Ⅲa与抗GPIbα抗体双阳性的患者,对大剂量地塞米松治疗的反应率也明显下降(29.6%)[10]。Go等研究发现抗GPIb-IX抗体阴性ITP患者对IVIG的反应率高于阳性患者 (100%vs 30%,P<0.01)[11]。 有研究显示,血小板膜糖蛋白特异性抗体GPⅡb/Ⅲa和GPIb-Ⅸ在不同ITP患者中分布不同,新诊断ITP患者以GPⅡb/Ⅲa抗体为主,而慢性、持续性ITP患者以GPIb-Ⅸ抗体为主,GPⅡb/Ⅲa抗体阳性的患者对激素治疗反应率高与阴性患者[12]。
3.2.2 糖皮质激素受体
糖皮质激素(glucocorticoid,GC)发挥作用主要是通过与糖皮质激素受体 (glucocorticoid receptor,GR)结合实现的,目前已发现GR经选择性剪接可产生 5种亚型:GRα、GRβ、GRγ、GRP 和GRA。GRα有50个氨基酸,GRβ有15个氨基酸,与GRα的50个氨基酸完全不同源,不能与GC结合,且对GRα介导的基因转录起抑制作用[13]。
GR与GC结合之前,GR在胞质内与HSP90、HSP70等Hsp90共同伴侣结合在一起,形成GR复合物,GC与GR的最佳结合以及随后的转录反应活性都要求GR复合物的成熟完整,GR复合物中伴侣蛋白异常可能会改变患者对GC的敏感性。GC与GR结合后,以GC-GR二聚体的形式进入细胞核,与糖皮质激素反应元件结合调控靶基因的转录,同时还受某些核转录因子的调节,如NF-κB、AP-1等,这些转录因子的表达异常也可能参与GC抵抗的产生。GR基因突变可以破坏GC信号转导途径,降低组织、细胞对GC的敏感性[14],以上均可导致患者对糖皮质激素抵抗。
本次研究未能对ITP患者进行血小板膜糖蛋白及GR的类型进行检测,以后应尽可能开展上述两项检查,预测患者对激素治疗的反应,查找激素疗效欠佳的原因,更好的个体化治疗ITP。
3.3 激素治疗时间长短与复发率的关系
2011年美国血液病学会推荐成人ITP一线治疗方案,较长时间的糖皮质激素治疗效果优于较短时间的治疗[15],可以获得更长的缓解时间,此推荐是基于一项静脉甲强龙40mg Qd 4d后,继续口服强的松或停止治疗的研究结果[16]。也有试验表明,短期大剂量静脉地塞米松40mg Qd连用4d,每4周1次,共6次,有效率 89.2%,90%的患者可维持15个月不复发,若连用4d,每2周1次,共4次,有效率85.6%,81%的患者可维持15个月不复发,复发率22%[17],但该研究随访时间仅15个月,尚不足以说明复发与否。另外,还有试验显示,短期大剂量静脉地塞米松40mg Qd连用4d,只用1次,6个月内复发率可达50%,中位复发时间为 45d(14~129d)[18]。
本研究中位随访时间达到63个月,常规治疗组糖皮质激素应用时间至少达到6个月,其复发率显著小于非常规治疗组 (17.9%vs 81.8%,P<0.01),且非常规治疗组复发的相对危险度是常规治疗组的20.7倍,提示糖皮质激素规律减量应用6个月以上可以明显降低ITP复发的风险。
[1]中华医学会血液学分会血栓与止血学组.成人原发免疫性血小板减少症诊治的中国专家共识 [J].中华血液学杂志,2011,32(3):214-216.
[2]杨仁池.免疫性血小板减少症的命名、定义与疗效评价的标准化——关于ITP国际工作组报告的解读[J].中华血液学杂志,2009,30(3):215-216.
[3]Cines DB,Blanchette VS.Immune thrombocytopenic purpura[J].N Engl J Med,2002,346:995-1008.
[4]GeorgeJN,el-HarakeMA,Raskob GE.Chronicidiopathic thrombocytopenic purpura[J].N Engl J Med,1994,331:1207-1211.
[5]George JN,Woolf SH,Raskob GE,et al.Idiopathic thrombocytopenic purpura:a practice guideline developed by explicit methods for the American Society of Hematology[J].Blood,1996,88:3-40.
[6]Portielje JE,Westendorp RG,Kluin-Nelemans HC,et al.Morbidity and mortality in adults with idiopathic thrombocytopenic purpura[J].Blood,2001,97:2549-2554.
[7]Johnsen J.Pathogenesis in immune thrombocytopenia:new insights [J].Hematology Am Soc HematolEdue Program,2012,2012:306-312.
[8]Li J,van der Wal DE,Zhu I,et al.Fc-independent phagocytosis:implications for IVIG and other therapies in immunemediated thrombocytopenia [J].Cardiovasc HematolDisord Drug Targets,2013,13:50-58.
[9]Jansen AJ,Josefsson EC,Rumjantseva V,et al.Desialylation accelerates platelet clearance after refrigeration and initiates GPlbαmetalloproteinase-mediated cleavage in mice[J].Blood,2012,1(19):1263-1273.
[10]Zeng Q,Zha I,Tao l,et al.Relative efficacy of steroid therapy in immune thrombocytopenia mediated by anti-platelet GPIIb/Ⅲ a versus GP Iα antibodies[J].Am J Hematol.2012.87:206.208.
[11]Go RS,Johnston KL,Bruden KC.The association between plateletautoantibody specificity and response to intravenous immunoglobulin G in the treatment of patients with immune thrombocytopenia[J].Haematologica.2007,92:283-284.
[12]刘晓帆,薛峰,张磊,等.血小板膜糖蛋白特异性抗体在原发免疫性血小板减少症患者中的分布与疗效的关系[J].中华血液学杂志,2013,34(7):610-613.
[13]Kino T,Su YA,Chrousos GP.Human glucocorticoid receptor isoform b:recent understanding of its potential implications in physiology and pathophysiology[J].Cell Mol Life Sci,2009,66:3435.3448.
[14]Charmandari E,Chrousos GP,Kino T.Identification of natural human glucocorticoid receptor (hGR)mutations or polymorphisms and their functional consequences at the hormone-receptorin teraction level[J].MethodsMoIBiol,2009,590:33-60.
[15]Cindy Neunert,Wendy Lim,Mark Crowther,et al.The american society of hematology 2011 evidence-based practice guideline for immune thrombocytopenia[J].blood,2011,117:4190-4207.
[16]Godeau B,Chevret S,Varet B,et al.Intra venous immunoglobulin or high-dose methylpred nisolone,with or without oral prednisone,for adults with untreated severe autoimmune thrombocytopenic purpura:a randomised, multicentre trial[J].Lancet,2002,359(9300):23-29.
[17]Mazzucconi MG,Fazi P,Bernasconi S,et al.Therapy with high-dose dexamethasone (HD-DXM) in previously untreated patientsaffected by idiopathic thrombocytopenic purpura:a GIMEMA experience [J].Blood,2007,109 (4):1401-1407.
[18]Cheng Y,Wong RS,Soo YO,et al.Initial treatment of immune thrombocytopenic purpura with high-dose dexamethasone[J].N Engl J Med,2003,349:831-836.

