RP-HPLC法测定贝那普利氢氯噻嗪片的含量
苏 敏,章志强,邓玉清,郝 程(.陕西方舟制药有限公司,西安 70075;.陕西省体育科学研究所,西安 70065;.西安天一秦昆制药有限责任公司,西安 70077)
贝那普利氢氯噻嗪片是一种治疗高血压的化学药物复方制剂,适用于用贝那普利和氢氯噻嗪单一治疗不能达到满意疗效的病人[1-2]。关于其含量测定方法,国外文献报道有薄层色谱法和高效液相色谱法[3-4],国内到目前为止还没有高效液相色谱法的相关报道。为了更好地控制其质量,本文对盐酸贝那普利和氢氯噻嗪的HPLC含量测定方法进行了提升,对其线性、重复性、稳定性等进行了可行性研究。
1 仪器与材料
1.1仪器 高效液相色谱仪(戴安U3000)。
1.2试药 四氢呋喃(色谱纯);冰醋酸(分析纯);四丁基溴化铵(分析纯);盐酸贝那普利对照品(按C24H28N2O5·HCl计,供HPLC法测定,含量为99.5%);氢氯噻嗪对照品(按C7H8ClN3O4S2计,含量为99.8%);贝那普利氢氯噻嗪片样品(自制)。
2 方法与结果
2.1色谱条件 色谱柱:Ultimate AQ-C18柱(250 mm×4.6 mm,5 μm);流动相:四氢呋喃-水-冰醋酸(250 mL+750 mL+4 mL,加入四丁基溴化铵1.0 g);检测波长:240 nm;流速:1.5 mL·min-1;进样量:20 μL。
2.2系统适用性实验 取有关物质CGS 14831对照品20 mg,精密称定,置于50 mL量瓶中,加溶剂使溶解并稀释至刻度,摇匀,作为杂质对照品储备液Ⅰ;取有关物质SU5683对照品适量,精密称定,加溶剂制成0.25 mg·mL-1的溶液,作为杂质对照品储备液Ⅱ;另取氢氯噻嗪对照品约6 mg和盐酸贝那普利对照品约5 mg,精密称定,置于25 mL量瓶中,精密加入杂质对照品储备液Ⅰ、Ⅱ分别为1 mL和1 mL,加溶剂稀释至刻度,作为系统适用性溶液[5]。
2.3方法学验证
2.3.1线性实验 取盐酸贝那普利对照品20 mg和氢氯噻嗪对照品25 mg,精密称定,置于50mL量瓶中,加溶剂溶解并稀释至刻度,摇匀,作为储备液。精密量取1,2.5,4,5,7.5和10 mL储备液,置于10 mL量瓶中,用溶剂(乙腈-水-冰醋酸(100∶150∶1)稀释至刻度,摇匀,作为供试液。分别精密量取上述溶液各20 μL注入高效液相色谱仪。以峰面积为纵坐标、质量浓度为横坐标作图,进行线性回归[6]。盐酸贝那普利质量浓度在41.2~412.3 μg·mL-1范围内呈线性,回归方程为y=14 731x-88 403,r=0.999 5,氢氯噻嗪质量浓度在51.0~509.6 μg·mL-1范围内呈线性,回归方程为y=5 816.6x+9 053.9,r=0.999 8。
2.3.2精密度实验 取盐酸贝那普利对照品20 mg和氢氯噻嗪对照品25 mg,精密称定,置于100 mL量瓶中,用溶剂溶解并稀释至刻度,摇匀,作为对照品溶液。精密量取20 μL上述溶液,注入高效液相色谱仪,在相同条件下,由同一分析人员对同一瓶样品重复进样6次,以峰面积的偏差为目标,考察进样精密度,记录色谱图。同一溶液连续进样6次,两主药氢氯噻嗪和盐酸贝那普利的峰面积的RSD均1.01%,0.71%和0.76%,0.69%,均小于2%,表明进样精密度良好。
2.3.3稳定性实验 将对照品和样品均配制成质量浓度约为盐酸贝那普利0.2 mg·mL-1、氢氯噻嗪0.25 mg·mL-1的溶液作为供试品溶液,分别于第0,2,4,6,8和12 h进样测定[7]。结果对照品溶液、供试品溶液中两成分峰面积在12 h内RSD值氢氯噻嗪和盐酸贝那普利分别为1.04%,0.66%,1.01%和0.84%,均小于2%,表明对照品溶液与供试品溶液均在12 h内稳定。
2.3.4重复性实验 取盐酸贝那普利对照品20 mg和氢氯噻嗪对照品25 mg,精密称定,置于100 mL量瓶中,加溶剂溶解并稀释至刻度,摇匀,即得。取本品20片,精密称定,研细,分别取6份等量的样品,精密称取(约相当于盐酸贝那普利10 mg),置于50 mL量瓶中,加溶剂40 mL,超声处理10 min,振摇15 min,放冷至室温,用溶剂稀释至刻度,摇匀,用0.45 μm的滤膜过滤,弃去初滤液6 mL,取续滤液,即得。平行操作配制6份,精密量取20 μL上述溶液,注入高效液相色谱仪,记录色谱图。以外标法按峰面积计算含量。两主成分氢氯噻嗪和贝那普利含量的RSD分别为1.00%和0.90%,均小于2%,表明进样重复性良好。
2.3.5准确度实验 取氢氯噻嗪对照品25 mg和盐酸贝那普利对照品20 mg,精密称定,置于100 mL量瓶中,加溶剂溶解并稀释至刻度,摇匀,即得。以此为基础分别配制80%~120%的对照品溶液,计算80%~120%范围内回收率,考察该方法测定的结果与真实值接近的程度。实验结果显示,盐酸贝那普利平均回收率在99.6%~101.6%之间,RSD小于2%,氢氯噻嗪平均回收率在99.3%~100.7%之间,RSD小于2%,符合平均回收率在98.0%~102.0%的要求,证明此方法准确度良好。
2.3.6回收率实验 对照品溶液:分别取氢氯噻嗪和盐酸贝那普利对照品约25和20 mg,置于100 mL量瓶中,加5 mL甲醇使溶解,并用0.1 mol·L-1盐酸溶液稀释至刻度;再精密量取5 mL,置于200 mL量瓶中,加0.1 mol·L-1盐酸溶液稀释至刻度,摇匀,即得。50%供试品溶液:取氢氯噻嗪和盐酸贝那普利对照品约12.5和10 mg,精密称定,置于同一含有约0.217 5 g空白辅料的100 mL量瓶中,加少量溶剂使其溶解,并用0.1 mol·L-1盐酸溶液稀释至刻度,摇匀,过滤;精密量取续滤液5 mL,置于200 mL量瓶中,加0.1 mol·L-1盐酸溶液稀释至刻度,摇匀,即得,共制备3份。同理,再分别配制80%供试品溶液和100%供试品溶液[8],精密量取对照品溶液和供试品溶液各50 μL,分别注入液相色谱仪,记录色谱图。结果见表1和表2及图1。
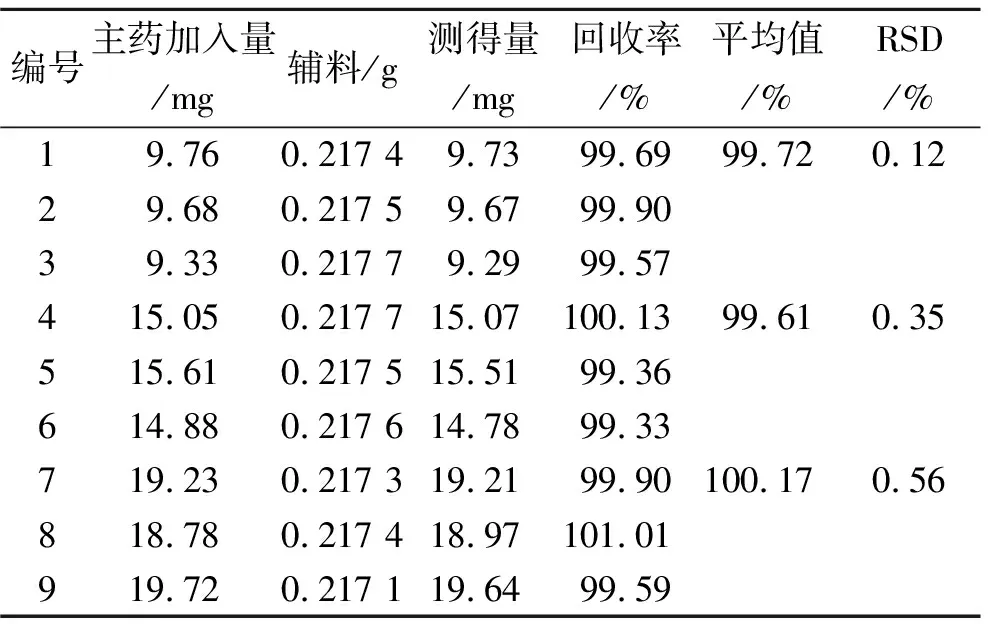
表1 盐酸贝那普利回收率实验结果
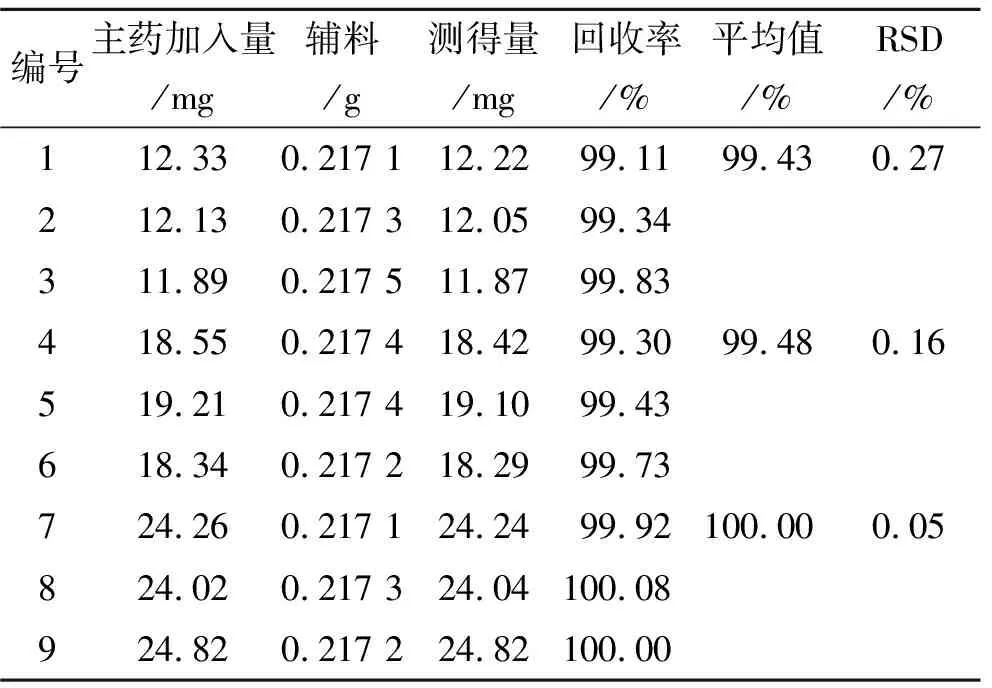
表2 氢氯噻嗪回收率实验结果
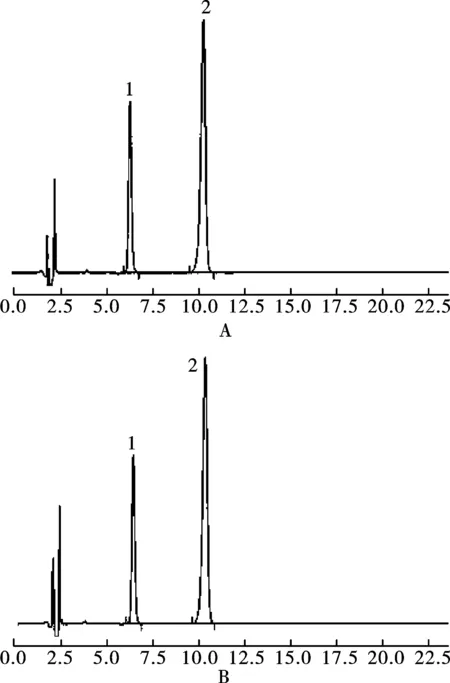
图1 HPLC图
实验结果表明,3个不同质量浓度的供试品溶液中,氢氯噻嗪和盐酸贝那普利的回收率RSD分别为0.35%和0.51%,均小于2%,回收率良好。
2.3.7样品测定 取本品20片,精密称定,研细,分别取6份等量的样品,精密称取(约相当于盐酸贝那普利10 mg),置于50 mL量瓶中,加溶剂40 mL,超声处理10 min,振摇15 min,放冷至室温,用溶剂稀释至刻度,摇匀,用0.45 μm的滤膜过滤,弃去初滤液6 mL,取续滤液,即得。分别取2份等量的对照品,氢氯噻嗪25 mg和盐酸贝那普利20 mg,精密称定,置于100 mL量瓶中,加溶剂溶解并稀释至刻度,摇匀,即得。实验结果表明,本品3 批含氢氯噻嗪分别为98.8%,99.6%和98.9%,均在标示量的95.0%~105.0%范围内,盐酸贝那普利含量分别为99.7%,100.5%和100.3%,均在标示量的92.0%~105.0%范围内,符合规定。
3 讨论
3.1色谱条件的选择 本品氢氯噻嗪、盐酸贝那普利的最大吸收波长分别为238,242和317 nm,故确定含量的检测波长为240 nm。四氢呋喃-水-冰醋酸(250 mL+750 mL+4 mL,加入四丁基溴化铵1.0 g)时主峰理论板数不低于2 000,与杂质峰分离度不小于1.5,未检出不纯物,故确定为该品种的流动相。色谱柱为Ultimate AQ-C18(250 mm×4.6 mm,5 μm)时主峰理论板数不低于2 000,与杂质峰的分离度不小于1.5,故确定为该品种的色谱柱。
3.2四氢呋喃用量 在本品检测中四氢呋喃用量相对较大,可适当调节流动相中的四氢呋喃量,使CGS 14831, SU 5683与氢氯噻嗪的分离度符合要求。所用四氢呋喃应保证其纯度,应临用开瓶,否则会引起色谱峰的增加。
参考文献:
[1] 尹欢招.贝那普利加小剂量氢氯噻嗪治疗高血压病的临床疗效[J].浙江中医药大学学报,2009,33(4): 549-550.
[2] 陈源源, 孙宁玲, 余振裘,等.国产复方贝那普利/氢氯噻嗪治疗轻中度高血压的随机双盲多中心平行对照临床研究[J].中国临床药理学杂志, 2007,23(6): 407-410.
[3] El-Gindy A, Ashour A, Abdel-Fattah L, et al. Application of LC and HPTLC-densitometry for the simultaneous determination of benazepril hydrochloride and hydrochlorothiazide[J]. J Pharm Biomed Anal,2001, 25(2): 171-179.
[4] Panderi IE,Parissi-Poulou M. Simultaneous determination of benazepril hydrochloride and hydrochlorothiazide by micro-bore liquid chromatography[J]. J Pharm Biomed Anal,1999,21(5): 1017-1024.
[5] 国家药典委员会.中国药典2010年版[S].一部.北京:中国医药科技出版社,2010: 130-131.
[6] 李媛,林青.厄贝沙坦氢氯噻嗪片的含量测定研究[J]. 当代医学,2013,19(20): 18-19.
[7] 惠芳,宋敏,杭太俊,等. 厄贝沙坦氢氯噻嗪片的含量测定和有关物质研究[J]. 中国新药杂志, 2010,19(3): 236-245.
[8] 陈玉璞. HPLC法测定复方卡托普利片中氢氯噻嗪的含量[J]. 西北药学杂志,2010,25(1): 14-15.

