硫辛酸注射液与木糖醇和果糖注射液的配伍稳定性考察
甘惠贞,林淑瑜,潘丹婷,杨昌云
0 引言
糖尿病患者长期高血糖造成微血管内皮病变,导致神经缺血、缺氧,引起氧化应激增强,自由基生成增加,引发一系列氧化反应,最终导致神经损伤[1]。硫辛酸(ALA)是一种独特的氧化-还原双向氧化应激强效抑制剂,可清除氧化应激的终末产物,清除自由基等其他抗氧化剂[2-4]。ALA主要通过抑制脂质过氧化,改善血管内皮细胞功能,增加神经营养血管的血流量,增加神经Na+-K+-ATP酶的活性等机制,改善糖尿病周围神经病变的症状[5-6],改善氧化应激状态,对糖尿病慢性并发症的防治具有良好效果[7]。硫辛酸注射液的活性成分含有二硫键,因此,说明书用法是加入生理盐水静脉滴注,配好的输液用铝铂纸包裹避光,6 h内可保持稳定[7]。且不能与葡萄糖溶液、林格氏溶液及所有可能与巯基或二硫键起反应的溶液配伍使用。但是在临床应用过程中常遇见糖尿病合并高钠血症,单一溶媒的要求让硫辛酸的使用受到了限制。为了能满足这些特殊病理生理需求的患者用药,本试验通过高效液相色谱法来测定硫辛酸与木糖醇注射液或果糖注射液配伍后硫辛酸的含量变化,以探索其配伍的稳定性,为临床用药提供参考。
1 仪器与材料
1.1 仪器 Ultimate3000高效液相色谱仪(赛默飞中国有限公司);JA2003电子分析天平(上海方瑞仪器有限公司);PHS-3C型实验室pH计(上海诚宁环保科技有限公司)。
1.2 药品与试药 硫辛酸注射液(上海现代哈森药业有限公司,规格:20 mL∶0.6 g,批号:11060621);硫辛酸对照品(中国药品生物制品检定所,批号:MUST-11072905,HPLC纯度≥98%);10%果糖注射液(四川科伦药业股份有限公司,规格:250 mL,批号:F11040913-1);木糖醇注射液(上海华中药业有限公司,规格:250 mL,批号:F11030504);0.9%氯化钠注射液(浙江天瑞药业有限公司,规格:250 mL,批号:211062303);乙腈(美国进口Fisher 色谱醇)、磷酸二氢钾(美国进口MREDA色谱醇);水为超纯化水(本院消毒供应室提供)。
2 方法与结果
2.1 色谱条件[8]色谱柱:Acclaim C18(250 mm×4.6 mm,5 μm);流动相:0.005 mol/L磷酸二氢钾溶液(磷酸调节pH=3.0)-乙腈(50∶50);流速:1.0 mL/min;柱温:30 ℃;检测波长:212 nm;进样量:5 μL。
2.2 对照品及样品溶液的制备
2.2.1 对照品储备溶液的制备 精密称取硫辛酸对照品200 mg,置于10 mL量瓶中,加流动相稀释至刻度,摇匀,避光、即得。
2.2.2 对照品溶液的制备 精密吸取对照品储备液1 mL,置于10 mL量瓶中,加流动相稀释至刻度,摇匀,避光、即得。
2.2.3 供试品溶液的制备 取硫辛酸注射液1 支(600 mg),置于30 mL容量瓶中,加流动相稀释至刻度,0.22 μm的微孔滤膜滤过,避光。精密吸取续滤液1 mL,置于10 mL量瓶中,加流动相稀释至刻度,摇匀,避光、即得。
2.2.4 配伍溶液的制备 模拟临床应用配制,将硫辛酸注射液1支(600 mg)分别加入溶媒0.9% NS 250 mL、木糖醇注射液250 mL及果糖注射液250 mL中并混合均匀,避光、即得。
2.3 方法专属性考察 酸破坏:取制备对照品溶液10 mL,加0.1 mol/L HCL溶液1.0 mL溶解,放置6 h,用0.1 mol/L NaOH溶液调pH至中性。碱破坏:取制备对照品溶液10 mL,加0.1 mol/L NaOH 溶液1.0 mL溶解,放置6 h,用0.1 mol/L HCL溶液调pH值至中性。高温破坏:取制备对照品溶液10 mL,80 ℃水浴加热6 h,冷却至室温。光照破坏:取制备对照品溶液10 mL,强光(4 500 Lx)照射6 h。分别将以上破坏后的溶液按“2.1”色谱条件进样测定。由破坏试验结果表明,本品经酸、碱、光照、高温破坏后,样品杂质峰均有所增加,且所产生的杂质与主峰充分分离,其保留时间与未破坏样品溶液色谱图中的吸收峰一致。见图1。
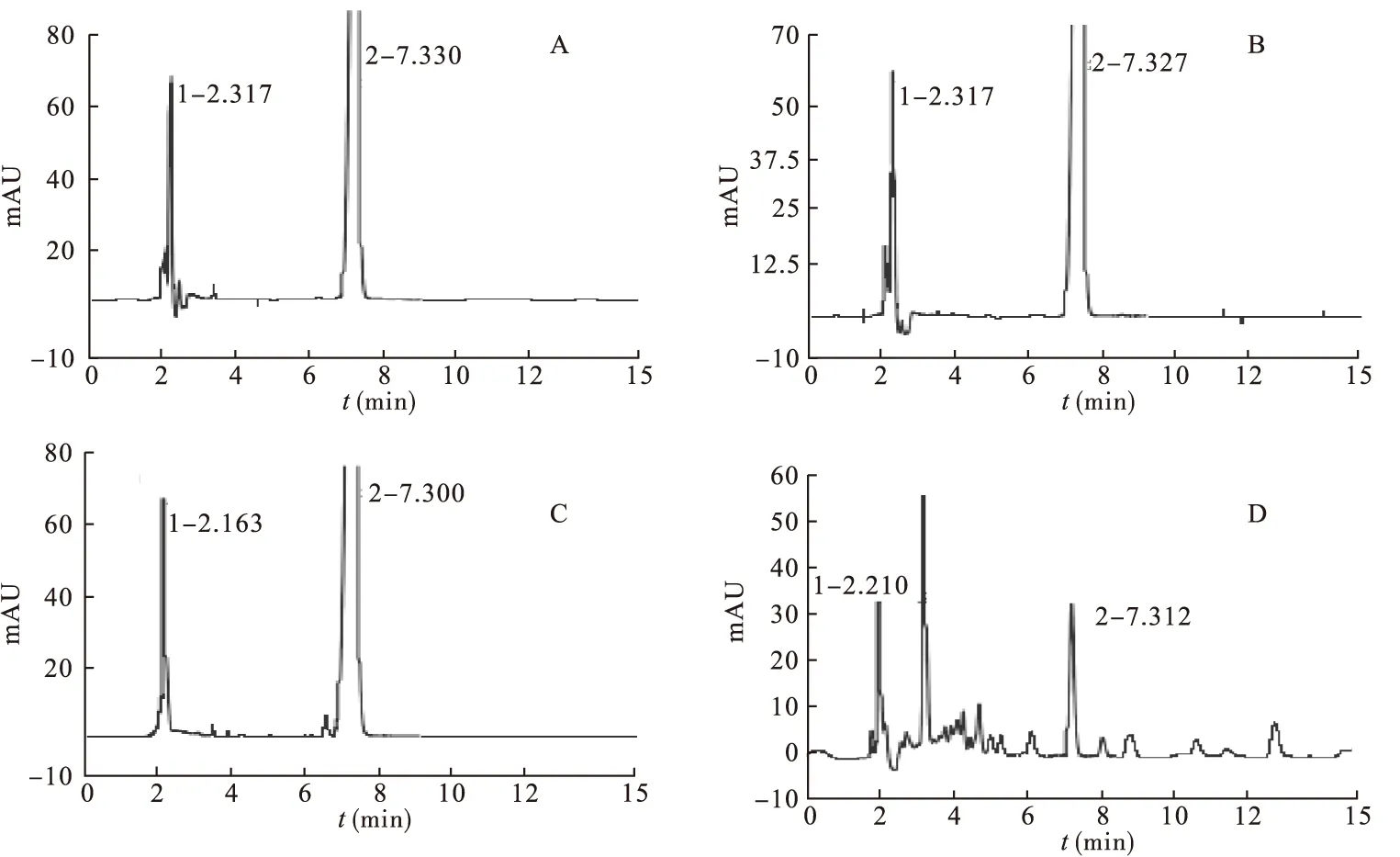
图1 破坏性试验结果
2.4 线性关系考察 精密吸取硫辛酸储备液适量,加流动相定量稀释制成系列浓度为2.00、1.00、0.50、0.25、0.12、0.06 mg/mL的溶液,分别进样5 μL。以硫辛酸的质量浓度(C)为横坐标、峰面积(A)为纵坐标,绘制标准曲线,得回归方程为:A=70.225 C+1.557 5(r=0.999 7)。表明硫辛酸检测质量浓度线性范围为0.06~2.00 mg/mL。
2.5 精密度试验 精密吸取硫辛酸对照品储备液适量,制成高、中、低3种不同浓度(2.0、1.0、0.5 mg/mL)的标样液各5份,同日测定并连续测定5 d,计算峰面积,得日内RSD分别为0.166%、0.212%、0.339%;日间RSD分别为0.655%、0.397%、0.514%,结果表明精密度良好。
2.6 重复性试验 按照供试品溶液制备方法制备成浓度为2.0 mg/mL的供试品溶液6份,进样测定,测得峰面积RSD=0.215%,结果表明重复性良好。
2.7 加样回收率试验 精密量取浓度为1.102 6 mg/mL的供试品溶液100、500、800 μL各3份,分别置于10 mL容量瓶中,分别加入浓度为0.313 7 mg/mL的对照品溶液500、1 000、1 500 μL,每个浓度平行3份,加流动相稀释至刻度,摇匀,取5 μL进样,计算回收率和RSD,见表1。
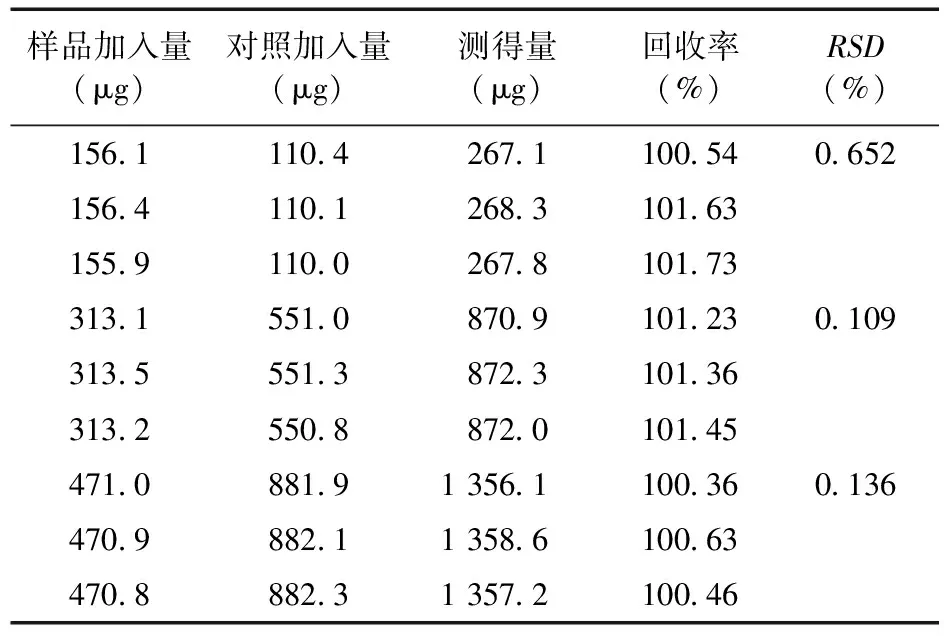
表1 回收率试验结果
2.8 稳定性试验 硫辛酸注射液供试溶液在避光和不避光(供试液不套用避光袋,放置在室内)的条件下于0、1、2、3、8、24 h分别进行测定,以(0 h)的含量为100%,换算出百分含量,结果显示,在避光的条件下硫辛酸注射液在24 h内稳定,不避光的条件下,在第3小时时硫辛酸的含量为86.45%,已降解低于90%。见表2。
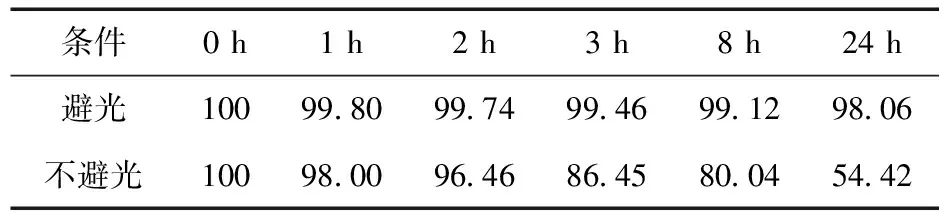
表2 硫辛酸稳定性测定结果(%)
2.9 硫辛酸与木糖醇、果糖配伍稳定性试验 取配好后的配伍药液(避光)即刻(0 h)及加药后不同时间(1、2、4、6、8、12、24 h)取样进行药液pH值和硫辛酸含量测定。从含量测定的结果得出,硫辛酸在0.9%生理盐水和木糖醇注射液两种溶媒中24 h内含量几乎无变化;但是在果糖注射液中不稳定,4 h时降解至89.98%,24 h后降解至64.47%。溶液pH值、颜色的测定结果得出,在3种溶媒中,溶液的pH值均无明显变化,在生理盐水、木糖醇溶液中的pH分别是7.9、7.7,与硫辛酸注射液(pH=8.0)接近,但果糖溶液中的pH值为7.1,比生理盐水、木糖醇溶液的pH值低,且24 h内溶液的颜色澄清度由无色变为淡黄色、棕黄色、红棕色、红棕色絮状物。图2-D和图2-E色谱图结果比较显示,硫辛酸与果糖配伍24 h后,硫辛酸的最大吸收峰明显下降,保留时间在3~5 min处增加了许多小分解峰。见表3~表5、图2。
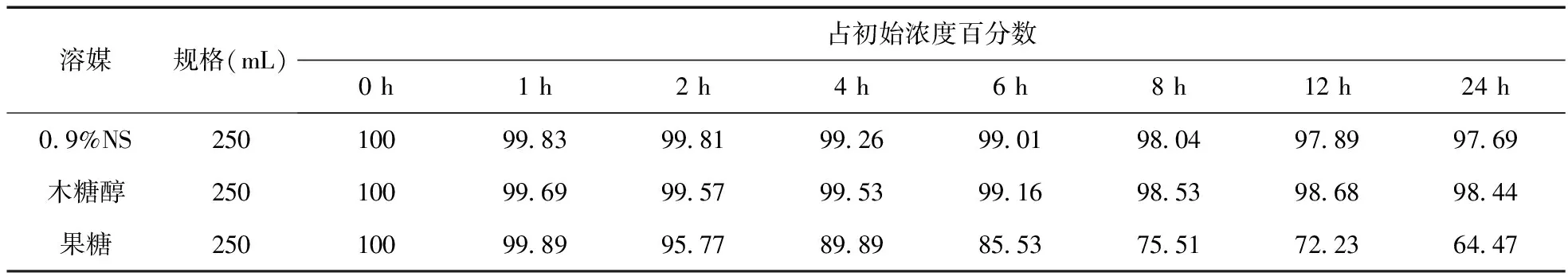
表3 硫辛酸与不同溶媒配伍后含量变化(%)

表4 硫辛酸与不同溶媒配伍pH值变化

表5 硫辛酸与不同溶媒配伍后颜色变化
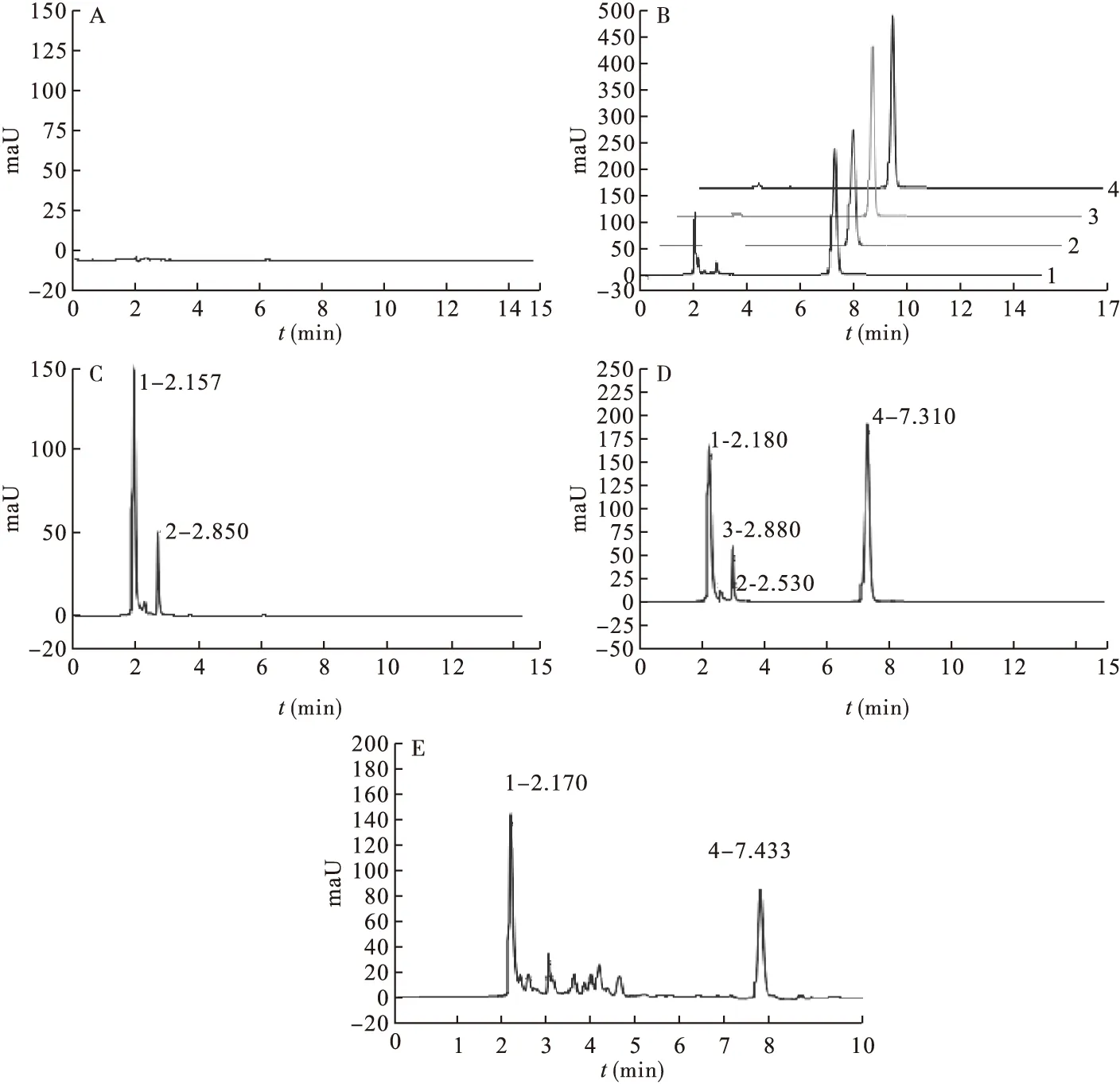
图2 各类型的色谱吸收图谱
3 讨论
3.1 色谱条件的选择 参考文献[9],选择“2.1”色谱条件,在该色谱条件下(见图2-B~图2-E),保留时间7.3 min处为硫辛酸的吸收峰,图2-A和图2-B分别为木糖醇和果糖在该色谱条件下的吸收峰,在2.1~3.0 min处的吸收峰为果糖的吸收峰。
3.2 硫辛酸与木糖醇、果糖的配伍稳定性 硫辛酸注射液在0.9%生理盐水、木糖醇注射液中的配伍含量24 h内几乎无变化,pH值几乎无变化。从含量、pH值、颜色澄清度及色谱图测定结果可得出,硫辛酸在0.9%生理盐水和木糖醇注射液的溶媒中24 h内稳定好;而在果糖注射液中不稳定,因果糖的pH=3.68为弱酸性,易引起硫辛酸中的巯基或二硫键的分解,导致溶液颜色的变化,所以不适宜与果糖配伍。因此对于限制钠摄入的糖尿病患者使用硫辛酸可选择木糖醇注射液作为溶媒。
4 结论
本文采用HPLC法的色谱条件可以用于测定硫辛酸含量,来考察硫辛酸与木糖醇注射液、果糖注射液配伍稳定性,操作简便、准确、重复性好。硫辛酸注射液可与0.9%生理盐水、木糖醇注射液配伍,不宜与果糖注射液配伍,并且使用精密过滤避光输液器输注,可有效减少药液中的微粒,避免输液反应的发生[10]。
参考文献:
[1] 张孝丽,郭晖.α-硫辛酸治疗糖尿病周围神经病变的研究进展[J].医学综述,2011,17(2):281-282.
[2] 宋效成,凌桂梅,谢秋平.α-硫辛酸治疗糖尿病周围神经病变84例临床观察[J].内科,2011,6(5):413-414.
[3] 韩静,卜一珊.α-硫辛酸对糖尿病周围神经病变的治疗效果分析[J].中国新药杂志,2013,22(6):695-697.
[4] 邱春娟,吕肖锋,赵晶.α硫辛酸对早期糖尿病肾病患者氧化应激水平的影响及对肾脏的保护作用[J].中国医药,2013,8(9):124-1248.
[5] Jain SK,Lim G.Lipoic acid decreases lipid peroxidation and protein glycosylation and increases(Na+-K+)-and Ca2+-ATPase activities in high glucose treated human erythrocytes[J].Frc Radic Biol Med,2000,29(11):1122-1128.
[6] 韩隆元.硫辛酸与依帕司他联合门冬胰岛素30治疗2型糖尿病周围神经病变疗效观察[J].中国医药,2012,7(2):163-165.
[7] 唐果,张蕾,曹秀堂.α-硫辛酸治疗糖尿病周围神经病变的Meta分析[J].中国药物应用与监测,2012,9(1):12-13.
[8] 杜洪洋.硫辛酸注射液质量研究[J].黑龙江医药,2013,26(2):218-220.
[9] 甘惠贞,林淑瑜,李玉堂.高效液相色谱法测定硫辛酸注射液含量[J].医药导报,2012,11(31):1494-1496.
[10]杨金芬,雷薇.精密避光输液器预防α-硫辛酸液输液反应的效果研究[J].实用临床医药杂志,2013,17(2):60-61.

