Na3AlF6-Al2O3系熔盐结构的计算模拟与高温拉曼光谱
刘晓伟,尤静林,王媛媛,王晨阳,刘 钦,王 静,赵 婷
(上海大学 上海市现代冶金与材料制备重点实验室,上海 200072)
当代铝电解工业普遍采用霍尔−埃鲁铝电解法[1],选取冰晶石(Na3AlF6)作助熔剂,氧化铝在高温状态下溶解于冰晶石,电导性和稳定性较好,因此,霍尔−埃鲁法电解铝在铝电解工业中使用越来越广泛。
在铝电解过程中,目前存在阳极效应、电导率降低、电流效率较低和溶解度下降等诸多问题[2−3],它们与冰晶石−氧化铝熔体中形成的复杂络合离子的微观结构密不可分。熔体中络合离子的种类及结构决定了熔盐的物化性能,所以探究熔体中络合离子的存在形式,有助于改善铝电解的环境条件,进一步提高电解效率。
在过去相当长的一段时间内,已有研究者通过高温拉曼光谱[4−5]、X 射线衍射[6]和统计力学方法[7−8]对冰晶石−氧化铝系熔盐结构进行了深入研究,认为熔盐主要以铝氟络合离子和铝氟氧络合离子等形成存在,但目前对络合离子的研究仍未达成共识,关键是缺乏合适的实验甄别和理论模拟方法。随着现代计算机模拟技术的发展,量子化学ab initio计算方法已经越来越多地应用到熔盐结构的研究中,肖丽等[9]利用此方法对铝氟酸盐体系的典型晶体进行了研究,与拉曼光谱实验结果吻合较好,同时也得出冰晶石在常温下主要以 AlF63−形式存在的结论。赵婷等[10]也利用此方法研究了熔盐中铝氟络合离子的结构,发现拉曼振动频率能较好地反映微环境的差异。当前铝电解工业主要面对重要的 Na3AlF6-Al2O3体系[11]和更为复杂的NaF-AlF3-Al2O3体系[12−13],由于高温熔体状态复杂,对于其中含有的络合离子种类及结构许多研究者仍持不同的观点。本文作者则采用量子化学 ab initio和DFT(Density function theory,DFT)计算方法对Na3AlF6-Al2O3体系可能出现的络合离子进行计算模拟,同时与高温拉曼光谱实验相互佐证,诊断熔盐中的络合离子。
在Na3AlF6-Al2O3体系研究过程中,考虑到电解效率等因素对实验研究有所限制,阚洪敏等[14]、黄有国等[15]以及丁吉林等[16]研究发现,铝电解工业中添加助熔剂(如LiF和CaF2等)具有一定的优越性,它们能够降低熔点以及增加电导率,所以本文作者通过高温拉曼光谱实验研究添加助熔剂和不添加助熔剂两种情况。
1 计算模拟
1.1 团簇结构模型
考虑到铝氟键和铝氧键的连接角度、桥氟和桥氧数目、桥接形式等的不同,以及铝氟四面体和氧桥所受周围微环境的不同[17],构建了铝氟四配位结构模型,如图 1所示。至于铝氟六配位结构,肖丽等[9]已进行过计算模拟,可以作为本研究的参考。
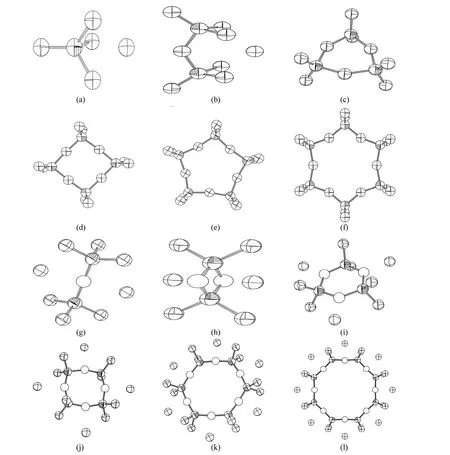
图1 团簇离子的结构模型Fig. 1 Model clusters (Element labels to Al, F, Na, O): (a)NaAlF4; (b)NaAl2F7; (c)Al3F9; (d)Al4F12; (e)Al5F15;(f)Al6F18; (g)Na2Al2OF6; (h)Na2Al2O2F4; (i)Na3Al3O3F6; (j)Na4Al4O4F8; (k)Na6Al6O6F12; (l)Na8Al8O8F16
图1中构建的团簇(a)~(f)为铝氟系结构,其中团簇(a)为铝氟四面体结构,团簇(b)为两个铝氟四面体结构通过氟原子桥接的氟桥结构,团簇(c)则表示3个铝氟四面体通过氟原子桥接的环状结构,团簇(d)~(f)分别表示4、5、6个铝氟四面体通过氟原子桥接的环状结构,其桥接形式为—AlF2—F—AlF2—。团簇(g)~(l)为铝氟氧系结构,其中团簇(g)为铝氟四面体通过单个氧原子桥接的氧桥结构,团簇(h)为两个铝氟四面体通过两个氧原子桥接的双氧桥结构,团簇(i)~(l)则分别表示3、4、6、8个铝氟四面体通过氧原子桥接成的环状结构,其桥接形式为—AlF2—O—AlF2—。
1.2 计算方法
采用量子化学ab initio和ADF(DFT中的阿姆斯特丹密度泛函方法)计算方法对图 1中的团簇进行结构优化和频率计算,其中 ab initio计算方法选取6-31G(d)基组,ADF计算方法选取广义梯度近似(GGA)中的Becke交换泛函和Perdew相关泛函、TZP基组。
1.3 计算结果及其分析
1.3.1 铝氟系团簇计算结果分析
图2所示为团簇a~f的量子化学ab initio和ADF计算方法的计算结果,并将其光谱强度以单位铝原子进行归一化处理(本研究所有计算模拟结果归一化方法与此相同)。
图2所示为图1中团簇a~f的ab initio计算方法和ADF计算方法的计算结果。表1所列为通过计算得到各团簇模型的拉曼活性振动频率,其中νAl-F,nb表示非桥氟键的伸缩振动频率,vAl-F,b表示桥氟键的对称伸缩振动频率。
由图2(a)可知,单个铝氟四面体团簇a铝氟键的伸缩振动频率为674.3 cm−1;单氟桥团簇b中,非桥氟的伸缩振动频率为734.7 cm−1,桥氟的对称伸缩振动频率为498.4 cm−1;铝氟环状团簇c~f中,非桥氟的伸缩振动频率在880 cm−1左右,桥氟的对称伸缩振动频率在437~471 cm−1之间,环状团簇模型的计算模拟结果显示,不同环状团簇的同一振动模差别不大,因此认为计算结果受环的大小影响不敏感。
由图2(b)可知,团簇a铝氟键的伸缩振动频率为607 cm−1;团簇b中,非桥氟的伸缩振动频率为681 cm−1,桥氟的对称伸缩振动频率为470 cm−1;团簇c~f中,非桥氟的伸缩振动频率在780~816 cm−1之间,桥氟的对称伸缩振动频率在385~413 cm−1之间,环状团簇模型的ADF计算模拟结果与量子化学ab initio模拟结果趋势基本一致。
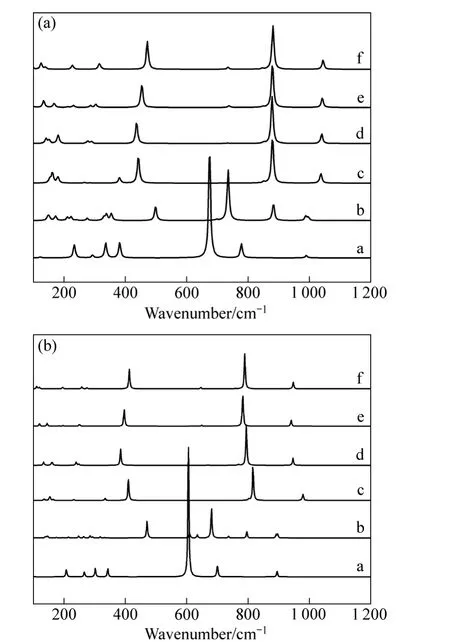
图2 采用ab initio(a)和ADF(b)计算铝氟四面体团簇a~f的拉曼光谱Fig. 2 Calculated Raman spectra of aluminum-fluorine tetrahedral model clusters a~f simulated by ab initio(a)and ADF(b)
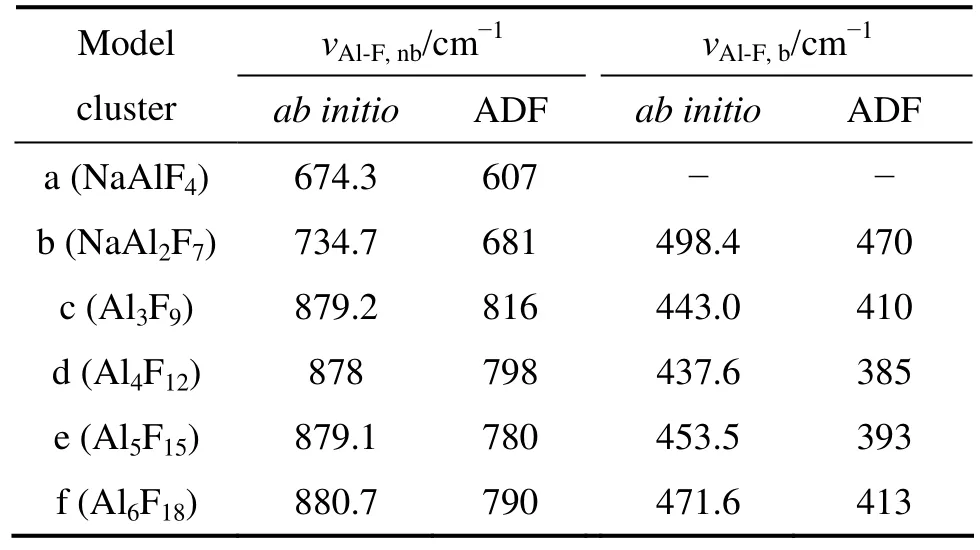
表1 团簇a~f结构的拉曼活性振动频率Table 1 Raman active vibrational wavenumber of model clusters a−f
综上所述,两种方法计算模拟得到的拉曼光谱基本一致,就同一振动模而言,前者频率略高于后者的。图3所列为两种计算方法的振动频率,并对其进行线性拟合,得到拟合函数为y=1.083 47x+12.811 63。其中横坐标x表示ADF计算方法计算模拟结果,纵坐标y表示ab initio计算方法计算模拟结果。由图3可以看出,两种方法的计算模拟结果吻合较好,虽然计算结果存在较小的系统误差,但可以采用ADF计算方法模拟较大的团簇结构,因为 ADF的时间效率远高于ab initio计算方法的。
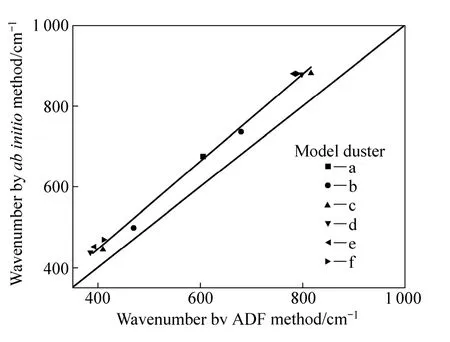
图3 ab initio和ADF计算结果对比Fig. 3 Comparison of wavenumber calculation results by ab initio and ADF methods
1.3.2 铝氟氧系团簇计算结果分析
图4表示团簇g~l通过ab initio计算方法和ADF计算方法得到的归一化计算结果。
图4表示图1中团簇g~l两种方法的计算结果,其中图4(a)表示ab initio计算方法计算铝氟氧系团簇的拉曼光谱,图4(b)则表示ADF计算方法得到的拉曼光谱。计算得到的各团簇模型的拉曼活性振动参数如表2所列,其中νAl-F,nb表示铝氟键的伸缩振动频率,νAl-O,b表示桥氧键的对称伸缩振动频率,νAl-O,b,sw表示整体离子的摇摆振动。
由图4(a)知,单氧桥团簇g铝氟键的伸缩振动频率为297 cm−1,桥氧的对称伸缩振动频率为502 cm−1;双氧桥团簇h中,铝氟键的伸缩振动频率为309 cm−1,桥氧的对称伸缩振动频率为417 cm−1,整体离子的摇摆振动频率为 769 cm−1;团簇 i~l为环状的—AlF2—O—AlF2—形式,桥氧的对称伸缩振动频率基本保持在430~490 cm−1的范围内,不同环状团簇模型的同一振动模差别不大。
由图4(b)知,团簇g铝氟键的伸缩振动频率为267 cm−1,桥氧的对称伸缩振动频率为461 cm−1;团簇h中,铝氟键的伸缩振动频率为316 cm−1,桥氧的对称伸缩振动频率为405 cm-1,整体离子的摇摆振动频率为780 cm−1;团簇i~l中,桥氧的对称伸缩振动频率在390~450 cm−1范围内,此计算模拟结果与量子化学ab initio模拟结果趋势基本一致。
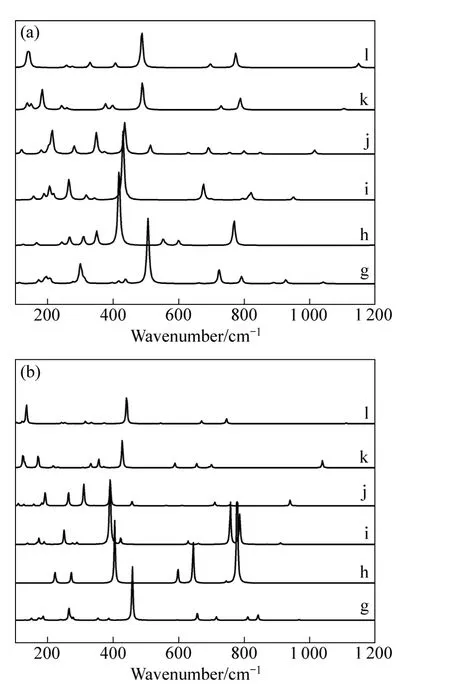
图4 ab initio(a)和ADF(b)计算铝氟氧系团簇g~l的拉曼光谱Fig. 4 Calculated Raman spectra of aluminum-fluorineoxygen model clusters g~l simulated by ab initio (a)and ADF(b)
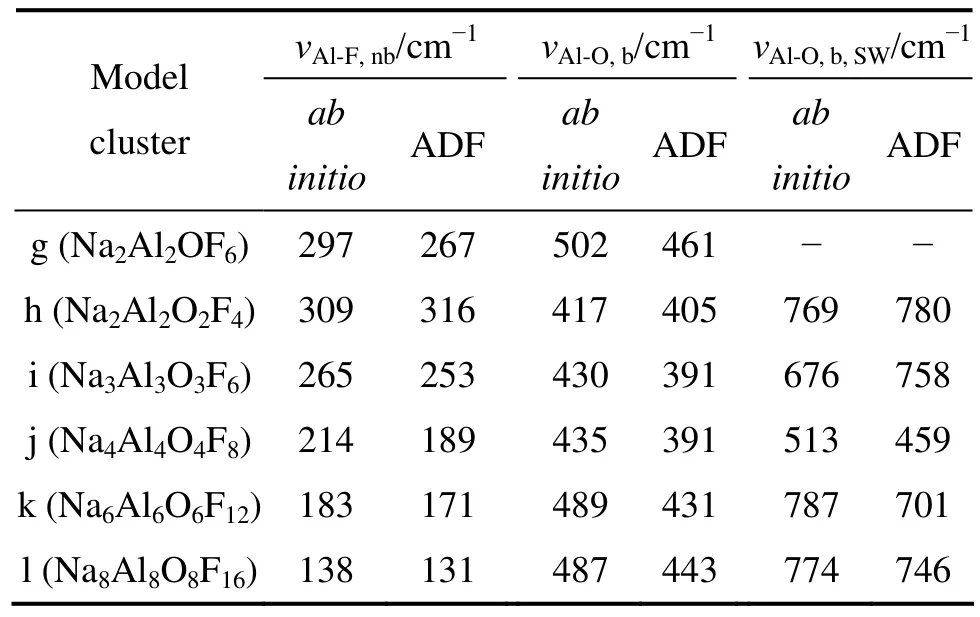
表2 团簇g~l结构拉曼活性的振动频率Table 2 Raman active vibrational wavenumber of model clusters g~l
综上所述,结果显示两种方法计算结果吻合较好,相对于铝氟体系,铝氟氧体系两种方法计算结果存在的系统误差更小。图5左上方曲线表示振动频率的拟合曲线,拟合函数为y=0.977 38x+32.764 85,其中横坐标x表示ADF计算方法计算模拟结果,纵坐标y表示ab initio计算方法计算模拟结果。对于铝氟氧体系较大团簇结构,可以通过ADF计算方法进行计算模拟。
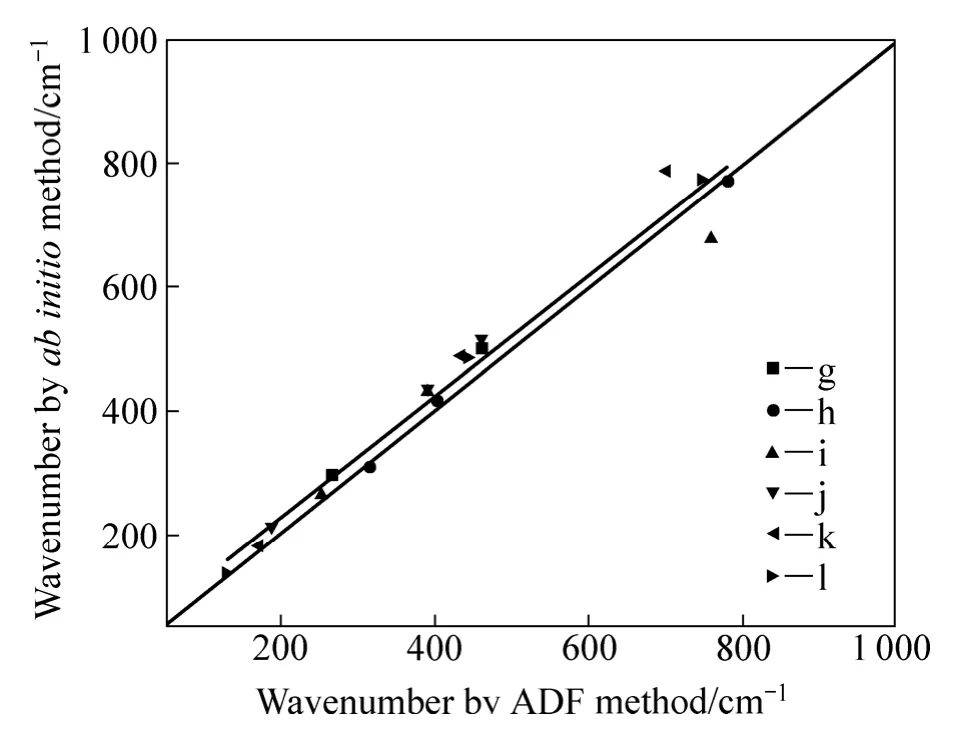
图5 ab initio和ADF计算结果对比图Fig. 5 Comparison of wavenumber calculation results by ab initio and ADF methods
2 高温拉曼光谱实验
2.1 样品制备
本研究中将Na3AlF6和Al2O3在烘箱中以473K保温2 h,按照一定的成分比(Al2O3含量为6%(质量分数))将两者均匀混合并在玛瑙研钵中研磨3 h。然后将其置于铂金坩埚中,放入马弗炉预熔,1 h后取出放入玛瑙研钵中研磨2 h,此样品标为样品A;在以上Na3AlF6和Al2O3混合物中添加4.1%的CaF2和4.4%的LiF(质量分数),重复上述预熔实验,得到样品B。
2.2 实验方法
将制得样品置于铂金坩埚中,在样品周围放置缠绕的高温耐材,将中间带有小孔的陶瓷片盖在上面,将其放置在高温热台中,通过拉曼光谱与高温热台相结合,在升温的过程中选取不同的温度点进行拉曼测试,观察拉曼谱图上的谱峰变化情况。
实验选用Horiba Jobin Y’von LabRAM HR 800型激光共焦拉曼光谱仪,采用脉冲激光器作为光源。高温热台采用TMS94/1500型热台。实验条件为激光波长为355 nm,激光功率约100 mW,扫描范围为100~1 200 cm−1,升温速率为30 K/min。
2.3 实验结果及讨论
考虑到铝电解过程中 Al2O3的溶解度与添加剂的密切关系,以及以往实验经验,参考 Na3AlF6-Al2O3二元系相图,从熔体开始选取不同的温度点进行拉曼数据采集,对于样品A和B进行原位升温拉曼光谱实验,如图6所示。

图6 样品A和样品B(含有CaF2、LiF)升温拉曼实验谱Fig. 6 Raman spectra of samples A (a)and B (b)(Containing CaF2 and LiF)with temperature increasing
从图 6可知,常温下,Na3AlF6占主导地位,其结构的ab initio计算结果与拉曼光谱实验吻合[9], 345 cm−1和394 cm−1处谱峰分别代表了Al—F弯曲振动和反对称伸缩振动,553 cm−1表征为Al—F键的伸缩振动。随着温度的升高,样品A和样品B在Al2O3溶解过程中出现明显的差异。
从图6(a)看出,1 263 K以下,样品A的实验谱峰随温度变化较小,温度为1 403 K时,553 cm−1处的谱峰逐渐消失,582 cm−1左右谱峰出现。单冰晶石结构的拉曼光谱实验与ab initio计算表明582 cm−1左右谱峰为 AlF4−离子的特征峰[18],据此可推断实验熔体中出现 AlF63−→AlF4−的转化,DANEK 等[19]认为此过程存在 AlF63−=AlF52−+F−和 AlF52−=AlF4−+F−反应,但是对于熔体中是否存在 AlF52−,研究者们尚未达成共识,因此,本研究不能确定是否存在 AlF52−。随着温度的升高,1 443 K时,谱峰410 cm−1和772 cm−1同时出现,说明两谱峰可能表征一种物质,与标准谱图对比证实其为 α-Al2O3,结构为 Al—O—Al六元环状结构,其中Al是六配位结构,O是四配位结构,整体结构呈六方晶型[20−21],此现象说明Al2O3并没有完全溶解。
图7比较样品 A在 1523K时的实验谱图与α-Al2O3常温时的标准谱图,两者吻合较好,谱峰410和772 cm−1分别代表Al—O—Al键的扭摆振动和对称伸缩振动。特别指出 1523K的实验谱图在波数 590 cm−1左右谱峰较宽,其原因在于样品中含有大量的AlF4−离子。HU 等[4]和 DANEK 等[19]研究表明,在AlF63−→AlF4−的反应过程中,F−与 O2−半径接近,F−易被Al2O3中较多的O2−取代,在熔体中形成一定数量的含氧质点,发生了如下反应:A12O3+4A1F63−=3A12OF62−+6F−,温度高于1 443 K以后,熔体中开始出现Al2OF62−离子。随着温度的上升,Al2O3特征峰一直存在,说明 Al2O3尚未完全溶解,但在含有助熔剂CaF2和LiF的实验(见图6(b))中,Al2O3溶解较好。随着温度的升高,从973K到1 023 K,553 cm−1谱峰转化为553 cm−1与627 cm−1左右谱峰共存,同样体现了AlF63−→AlF4−的转化反应。1 023 K 时,出现 428 cm−1谱峰,温度升至1 173 K时,发现其与341 cm−1融为包络状,这一过程显示是 Na3AlF6发生相变,键长变短,结构更加紧密,其中波数976 cm−1左右表征样品中含有CaF2(参照标准谱图)。1 223 K时,388 cm−1处谱峰呈现较大的包络状,表明熔体状态多元结构共存,其内部除了含有 Na+、AlF63−、AlF4−、F−等简单离子外,还含有较复杂的 Al2OF62−等络合离子。以 Al2O3开始溶解为起点,温度逐渐升高,A12OF62−离子特征峰出现在460 cm−1左右,与图1团簇g的计算模拟结果(特征峰500 cm−1左右)存在一定偏差,主要是因为随着温度的升高,其发生红移,表明桥氧键变长,键角变大,其计算结果显示500 cm−1左右谱峰表征桥氧的对称伸缩振动,290 cm−1左右谱峰表征铝氟键的摇摆振动。1 233 K以上,对比实验谱图与和计算谱图(见图4),发现实验谱峰与图1中团簇k和l计算模拟得出的计算谱峰吻合较好,说明高温状态下,熔体中已含有结构形式为—AlF2—O—AlF2—的离子。温度继续升高,α-Al2O3迅速溶解。从以上结果可知,CaF2和LiF的添加促进了 α-Al2O3的熔化,同时有助于降低铝电解的温度。因此在工业铝电解过程中,一般的会选用一些类似于CaF2、LiF等的助熔剂添加在电解池中。
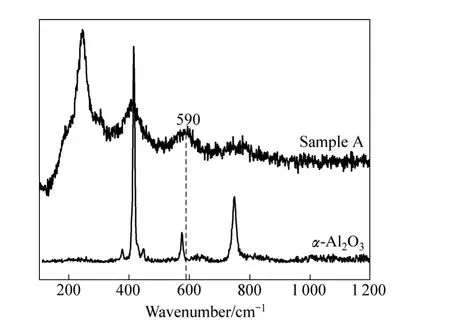
图7 样品A在1 523 K实验谱图与α-Al2O3谱图对比Fig. 7 Comparison of experimental Raman spectra of sample A melting at 1 523 K with the of α-Al2O3
3 结论
1) 铝氟系和铝氟氧系中络合离子的拉曼频率计算结果表明,量子化学ab initio和ADF两种计算方法用于同类离子团簇计算模拟时,其计算结果基本一致,还可以通过 ADF计算方法计算模拟一些较大的团簇结构。
2) 铝电解过程中,在没有添加剂的情况下,Al2O3溶解效率较低,但添加助熔剂CaF2、LiF后,溶解效率提高,这说明CaF2、LiF对Al2O3的溶解具有促进作用。
3) 两种方法计算铝氟氧体系的模拟结果与实验结果表明,对于样品B,在1 173 K以上,熔体中出现 Al2OF62−离子,其结构为 AlF3—O—AlF3形式,但未有数据表明熔体中存在双氧桥结构。
[1]邱竹贤. 铝电解原理与应用[M]. 北京: 中国矿业出版社,1998: 4−8.QIU Zhu-xian. Textbook of Principle and application of aluminium electrolysis[M]. Beijing: China University of Mining and Technology Press, 1998: 4−8.
[2]李继东, 张明杰, 张廷安, 杨少华. Na3AlF6-Al2O3二元系熔度与熔盐结构[J]. 材料与冶金学报, 2007, 6(4): 269−273.LI Ji-dong, ZHANG Ming-jie, ZHANG Ting-an, YANG Shao-hua. Fusibility of Na3AlF6-Al2O3binary system and fused salt structure[J]. Journal of Materials and Metallurgy, 2007, 6(4):269−273.
[3]狄鸿利, 张明杰. Na3AlF6-Al2O3二元系熔度与 Al2O3在熔融Na3AlF6中的溶解机理[J]. 东北工学院报, 1985(4): 37−42.DI Hong-li, ZHANG Ming-jie. On the dissolution mechanism of Al2O3in Na3AlF6melt[J]. Journal of Northeast Institute of Technology, 1985(4): 37−42.
[4]HU Xian-wei, QU Jun-yue, GAO Bing-liang, LIU Feng-guo,WANG Zhao-wen. Raman spectroscopy and ionic structure of Na3AlF6-Al2O3melts[J]. Transactions of Nonferrous Metals Society of China, 2011, 21(2): 402−406.
[5]GILBER B, MAMANTOV G, BEGUN G M. Raman spectra of aluminum fluoride containing melts and the ionic equilibrium in molten cryolite type mixtures[J]. Journal of Chemical Physics,1975, 62(3): 940−955.
[6]黄子卿. 熔盐结构[J]. 科学通报, 1975(3): 112−119.HUANG Zi-qing. The structure of molten salt[J]. Chinese Science Bulletin, 1975(3): 112−119.
[7]侯怀宇, 谢 刚, 陈书荣, 张雄飞. NaF-AlF3系熔盐结构的分子动力学计算[J]. 中国有色金属学报, 2000, 10(6): 914−918.HOU Huai-yu, XIE Gang, CHEN Shu-rong, ZHANG Xiong-fei.Structure of molecular dynamics simulated NaF-AlF3melt[J].The Chinese Journal of Nonferrous Metals, 2000, 10(6):914−918.
[8]ROBERT E, OLSEN J E, DANEK V, TIXHON E, STVOLD T,GILBERT B. Structure and thermodynamics of alkali fluoride-aluminum fluoride-alumina melts. vapor pressure,solubility and raman spectroscopic studies[J]. Journal of Physical Chemistry B, 1997, 101(46): 9447−9457.
[9]肖 丽, 尤静林, 蒋国昌. 氟铝酸盐离子团簇微环境与拉曼光谱表征[J]. 中国有色金属学报, 2008, 18(6): 1164−1170.XIAO Li, YOU Jing-lin, JIANG Guo-chang. Characteristic Raman spectra of micro environment of fluoroaluminate structural units[J]. The Chinese Journal of Nonferrous Metals,2008, 18(6): 1164−1170.
[10]赵 婷, 尤静林, 王媛媛, 汪 磊, 马 兰. NaF-AlF3二元系铝氟四面体团簇结构的拉曼光谱表征与量子化学从头计算[J].光散射学报, 2012, 24(1): 1−7.ZHAO Ting, YOU Jing-lin, WANG Yuan-yuan, WANG Lei, MA Lan. Characteristic Raman spectra and quantum chemistry ab initio calculation on aluminum-fluorine tetrahedral model clusters of NaF-AlF3binary[J]. Journal of Light Scattering, 2012,24(1): 1−7.
[11]BROOKER M H, BERG R W, VON BARNER J H, BJERRUM N J. Raman study of the hexafluoroaluminate ion in solid and molten flinak[J]. Inorganic Chemistry, 2000, 39(16): 3682−3689.
[12]YUNSHU Z, GUPTA S, SAHAI Y, ROBERT A. Modeling of the solubility of alumina in the NaF-AlF3system at 1300 K[J].Metallurgical and Materials Transactions B, 2002, 33B(2):315−319.
[13]NAZMUTDINOV R R, ZINKICHEVA T T, VASSILIEV S Y,GLUKHOV D V, TSIRLINA G A, PROBST M. A spectroscopic and computational study of Al(Ⅲ)complexes in sodium cryolite melts: Ionic composition in a wide range of cryolite ratios[J].Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2010, 75(4): 1244−1252.
[14]阚洪敏, 班允刚, 邱竹贤, 王兆文. 低温铝电解的研究[J]. 中国有色冶金, 2007(2): 16−19.KAN Hong-min, BAN Yun-gang, QIU Zhu-xian, WANG Zhao-wen. Manufacture and application of the flat interface tray of zinc rectifying furnaces[J]. China Nonferrous Metallurgy,2007(2): 16−19.
[15]黄有国, 田忠良, 赖延清, 李 劼, 刘业翔. LiF对Na3AlF6-K3AlF6-AlF3熔体初晶温度和Al2O3溶解度的影响[J].中国有色金属学报, 2010, 20(5): 903−907.HUANG You-guo, TIAN Zhong-liang, LAI Yan-qing, LI Jie,LIU Ye-xiang. Effect of LiF on liquidus temperature and solubility of Al2O3in Na3AlF6-K3AlF6-AlF3melts[J]. The Chinese Journal of Nonferrous Metals, 2010, 20(5): 903−907.
[16]丁吉林, 田 永, 杨叶伟, 李 钊, 杨 钢. 大型铝电解槽添加锂盐工业试验及应用[J]. 有色金属: 冶炼部分, 2006(2):27−29.DING Ji-lin, TIAN Yong, YANG Ye-wei, LI Zhao, YANG Gang.Industrial test & application of adding LiF3in large-scale aluminum electrobath[J]. Nonferrous Metals: Extractive Metallurgy, 2006(2): 27−29.
[17]王艳玲. 无机化学[M]. 北京: 高等教育出版社, 2008: 14−41.WANG Yan-ling. Textbook of inorganic chemistry[M]. Beijing:Higher education press, 2008: 14−41.
[18]戴苏娟, 尤静林, 王媛媛, 王 威, 王志超, 牛玉静. 单冰晶石微结构与拉曼光谱特征研究[J]. 光散射学报, 2010, 22(3):276−280.DAI Su-juan, YOU Jing-lin, WANG Yuan-yuan, WANG Wei,WANG Zhi-chao, NIU Yu-jing. Study of micro structure and Raman spectroscopic characteristics of sodium aluminum tetrafluoride[J]. Journal of Light Scattering, 2010, 22(3):276−280.
[19]DANEK V, GUSTAVSEN O T, OSTVOLD T. Structure of the MF-AlF3-Al2O3(M = Li, Na, K)melts[J]. Canadian Metallurgical Quarterly, 2000, 39(2): 153−162.
[20]谭训彦, 王 昕, 尹衍升, 刘英才, 张金升, 孟繁琴. α-Al2O3的晶体结构与价电子结构[J]. 中国有色金属学报, 2002,12(S1): s18−s23.TAN Xun-yan, WANG Xin, YIN Yan-sheng, LIU Ying-cai,ZHANG Jin-sheng, MENG Fan-qin. Crystal structure and valence electron structure of a-Al2O3[J]. The Chinese Journal of Nonferrous Metals, 2002, 12(S1): s18−s23.
[21]MARIOTTO G, CAZZANELLI E, CARTURAN G, DI MAGGIO R, SCARDI P. Raman and X-ray diffraction study of boehmite gels and their transformation to α- or β-alumina[J].Journal of Solid State Chemistry, 1990, 86(2): 263−263.

