利用铅冶炼烟尘制备超细氧化铅粉末
杨 勰 李宏煦 李 超 王 帅 王喻玥
(1.北京科技大学冶金与生态工程学院,北京 100083;2.稀贵金属绿色回收与提取北京市重点实验室,北京 100083;3.生态与循环冶金教育部重点实验室,北京 100083)
·综合利用·
利用铅冶炼烟尘制备超细氧化铅粉末
杨 勰1,2,3李宏煦1,2,3李 超1,2,3王 帅1,2,3王喻玥1
(1.北京科技大学冶金与生态工程学院,北京 100083;2.稀贵金属绿色回收与提取北京市重点实验室,北京 100083;3.生态与循环冶金教育部重点实验室,北京 100083)
河南某底吹炉炼铅烟尘Pb含量达44.99%,可作为生产高质量超微细氧化铅粉末的重要资源。试验采用硫酸化焙烧预处理—NaCl浸出酸浸渣—氧化铅前驱体合成—氧化铅粉末生成工艺对超微细氧化铅粉末加工技术条件进行了研究。结果表明:试验确定条件下硫酸化焙烧预处理—水浸工艺的Pb、Cd、As去除率分别达2.67%、96.98%、100.00%,初步实现了铅与镉、砷等杂质元素的分离;NaCl浸出酸浸渣工艺的铅、镉作业浸出率为97.89%和98.12%;氧化铅前驱体合成工艺的铅转换率为97.88%;氧化铅粉末生成工艺彻底改变了晶体的形貌,生成物具有短棒状海绵疏松的微观形貌,长度小于2 μm,氧化铅含量达98.31%,属优质超细氧化铅粉末。因此,该工艺为铅冶炼烟尘的回收和超细氧化铅粉末的制造提供了一种新的思路。
铅冶炼烟尘 硫酸化焙烧 NaCl溶液浸出 氧化铅前驱体合成 超细氧化铅粉末
据统计,2012年全世界产铅量达1 056万t,中国约占世界总产铅量的43%,成为世界第一铅生产和消费国[1-3]。富氧底吹炼铅工艺是我国火法炼铅的主要工艺之一,在高温强化熔炼过程中,会有大量的铅等金属挥发,造成烟尘率较高,国内炼铅企业为了减少资源流失、控制烟尘对环境的污染,通常将这些烟尘返回与原料混合继续冶炼,如此循环往复,将造成富氧底吹炉烟尘中多种有价元素大量富集[4-7],进而影响炼铅原料的品质。随着近年炼铅用铅精矿品位的下滑、杂质含量的上升,烟尘返回冶炼对炉况的影响越来越严重。因此,对含铅烟尘进行单独处理意义重大。
氧化铅在工业上有广泛的用途,可用作颜料铅白、铅皂、冶金助溶剂、油漆催干剂、陶瓷原料、铅盐塑料稳定剂、铅玻璃工业原料以及铅盐类工业的中间原料等。随着经济的发展,氧化铅的需求也随之增长[8-10]。目前从固体废物中提取氧化铅的方法有火法和湿法,而湿法冶金技术有较强的选择性,在水溶液中可通过控制生产条件实现不同元素的有效分离,且生产环境友好、生产成本低[11-13]。李磊等人[14-15]在低温下用柠檬酸与铅膏反应合成柠檬酸铅,再焙烧得到氧化铅;朱新锋等人[16]以Na2CO3、NaHCO3和(NH4)2CO3为脱硫剂与铅膏反应制得碱式碳酸铅,再焙烧得氧化铅;Hassam Karami等人[17]用硝酸铅与氢氧化钠反应得到氢氧化铅,焙烧得氧化铅。然而,以铅冶炼烟尘为原料生产氧化铅的研究却未见报道。考虑到铅烟尘中的铅化合物组成与铅膏相似,因此,本试验采用湿法冶金工艺,以铅冶炼烟尘为原料,对通过合成前驱物、再焙烧脱水来制备氧化铅的工艺进行了研究。
1 试验原料
试验原料为河南某底吹炉炼铅烟尘,主要化学成分分析结果见表1,XRD分析结果见图1,SEM图片见图2。

表1 试验原料主要化学成分分析结果

图1 试验原料的XRD图谱
从表1可以看出,试验原料中Pb、Cd含量高,分别为44.99%和39.48%;非金属S、As含量次之,分别为8.38%和5.87%;其他金属元素Na、Cu、Zn等含量较低,均在0.23%~0.26%之间。
从图1可以看出,试验原料的XRD图谱中主要可见Pb3O4、Pb2O3、PbO以及PbSO4和PbCl2等铅矿物的衍射峰;镉矿物中CdS、CdSO4和CdAs的衍射峰也较强。

图2 试验原料的SEM图片
从图2可以看出,试验原料大多由聚合物组成,经高温冷凝后相互黏结,粒度在1~10 μm之间。
2 试验步骤及原理
氧化铅粉末制备主要分硫酸化焙烧预处理、NaCl浸出酸浸渣、氧化铅前驱体合成和氧化铅粉末的生成等4大步。
(1)硫酸化焙烧预处理。铅冶炼烟尘中主要为金属氧化物和金属硫化物、砷化物,其中部分金属氧化物可用酸浸出、部分硫化物和砷化物难溶于酸。要高效实现铅与其余金属的分离,必须完成金属硫化物和砷化物的氧化,且使铅保留在渣相中,其余金属尽可能进入溶液中,最有效的办法是硫酸化焙烧—水浸。该部分的主要反应有(Me代表Pb、Cd、Zn):
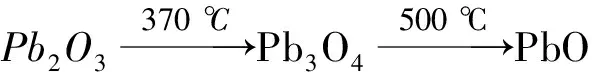
(1)
MeO+H2SO4=MeSO4+H2O,
(2)
2MeS+2H2SO4+3O2=2MeSO4+2SO2+2H2O,
(3)
Me3As2+3H2SO4+3O2=3MeSO4+As2O3+3H2O,
(4)


(5)
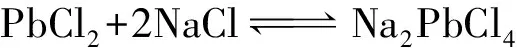
(6)
(3)氧化铅前驱体合成。PbCl2冷却结晶后从溶液中析出,结晶后溶液返回继续浸出,析出的PbCl2,经洗涤,得到的纯度较高的PbCl2与NaOH反应生成Pb(OH)2,其反应式为

(7)
(4)氧化铅粉末的生成。Pb(OH)2在一定条件下焙烧后得到氧化铅粉末,其反应式为

(8)
3 试验结果与讨论
3.1 硫酸化焙烧预处理—水浸试验
由于镉和砷是制备硫酸铅渣的主要杂质元素,氯盐、钠盐为可溶盐,而铜、锌、铟含量远小于镉、砷,因此不予研究。硫酸化焙烧采用浓硫酸,焙烧产物水浸的液固比为30mL/g、水浸温度为60 ℃、时间为120min。
3.1.1 焙烧温度对铅、镉、砷去除率的影响
硫酸化焙烧温度对铅、镉、砷去除率影响试验的酸料比为0.6mL/g,焙烧时间为120min,试验结果见表2。
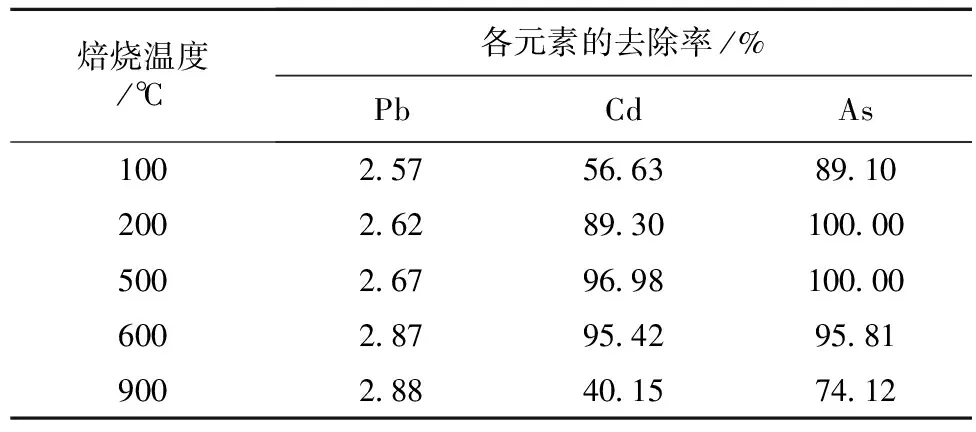
表2 硫酸化焙烧温度试验结果
从表2可以看出,升高焙烧温度,铅去除率微幅上升,但镉、砷的去除率先显著上升后显著下降,高点在500 ℃时。这是因为,一方面,温度升高有利于镉的氧化物、硫化物或砷化物在空气中与硫酸反应生成易溶的硫酸镉;另一方面,浓硫酸的沸点为330 ℃,高于此温度会加速硫酸分解为三氧化硫和水,温度不太高的情况下,硫酸分解生成的三氧化硫可继续发挥硫酸的作用,与反应对象发生化学反应,但温度过高,三氧化硫会大量挥发,从而影响易溶硫酸镉的生成。因此,确定焙烧温度为500 ℃。
3.1.2 酸料比对铅、镉、砷去除率的影响
酸料比对铅、镉、砷去除率影响试验的焙烧温度为500 ℃,焙烧时间为120 min,试验结果见表3。

表3 酸料比试验结果
从表3可以看出,提高酸料比,镉、砷的去除率先上升后维持在高位,铅去除率变化很小。因此,确定酸料比为0.6 L/g。
3.1.3 焙烧时间对铅、镉、砷去除率的影响
焙烧时间对铅、镉、砷去除率影响试验的焙烧温度为500 ℃,酸料比为0.6 mL/g,试验结果见表4。
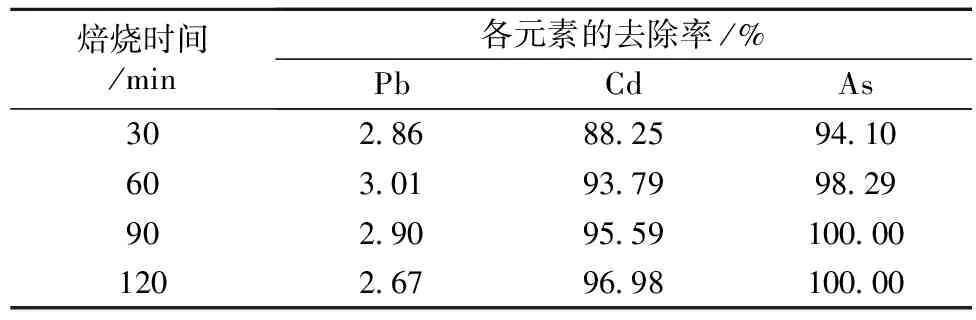
表4 焙烧时间试验结果
从表4可以看出,延长焙烧时间,镉、砷的去除率上升,铅去除率变化很小。因此,确定焙烧时间为120 min。
3.1.4 硫酸化焙烧—水浸试验结果
在酸料比为0.6 mL/g、焙烧温度为500 ℃、焙烧时间为120 min情况下的焙烧产物,在60 ℃下搅拌水浸120 min,浸出渣主要化学成分分析结果见表5。

表5 硫酸化焙烧—水浸渣主要化学成分分析结果
从表5可以看出,硫酸化焙烧—水浸具有较好的除杂效果,但酸浸渣中仍含有少量的镉。
在酸料比为0.6 mL/g、焙烧温度为500 ℃、焙烧时间为120 min情况下的焙烧产物,在60 ℃下搅拌水浸120 min,Pb、Cd、As的去除率分别达2.67%、96.98%、100.00%,产物中Pb、Cd、As的含量分别为67.10%、0.68%、0.03%。
3.2 酸浸渣NaCl溶液浸出—结晶试验
将酸浸渣烘干、研磨、过200目筛,讨论在氯化钠浓度、浸出温度、浸出时间、液固比等不同反应条件对铅、镉浸出率的影响。反应控制溶液的pH在4以下(防止水解),浸出完成后,浸出液趁热过滤,滤渣用与反应温度相同的热水冲洗3次,滤液经室温静置12 h结晶,得氯化铅。
3.2.1 NaCl溶液浓度对铅、镉浸出率的影响
NaCl溶液浓度试验的浸出温度为90 ℃、浸出时间为90 min、液固比为30 mL/g,试验结果见图3。
从图3可以看出,随着氯化钠浓度的提高,硫酸铅不断转化为溶解度更大的铅配合物Na2PbCl4,由于镉含量远低于铅,氯化镉的溶解度又高于氯化铅,所以镉的浸出更易达到平衡,因此镉、铅浸出率呈幅度不同的上升趋势。为了获得较高的铅浸出率,确定氯化钠溶液的浓度为250 g/L。
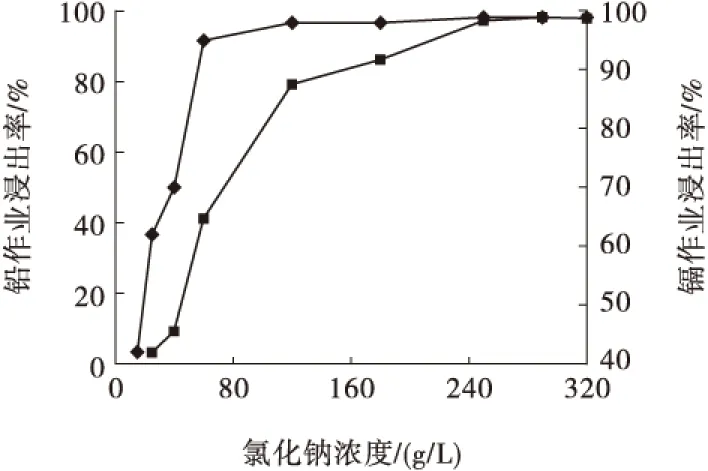
图3 NaCl浓度对铅、镉浸出率的影响
3.2.2 浸出温度对铅、镉浸出率的影响
浸出温度试验的NaCl溶液浓度为250 g/L、浸出时间为90min、液固比为30 mL/g,试验结果见图4。

图4 浸出温度对铅、镉浸出率的影响
从图4可以看出,随着浸出温度的升高,铅、镉浸出率均上升。温度升高有利于提高氯化铅的溶解度,对镉的浸出影响较小。综合考虑,确定浸出温度为90 ℃。
3.2.3 浸出时间对铅、镉浸出率的影响
浸出时间试验的NaCl溶液浓度为250 g/L、浸出温度为90 ℃、液固比为30 mL/g,试验结果见图5。
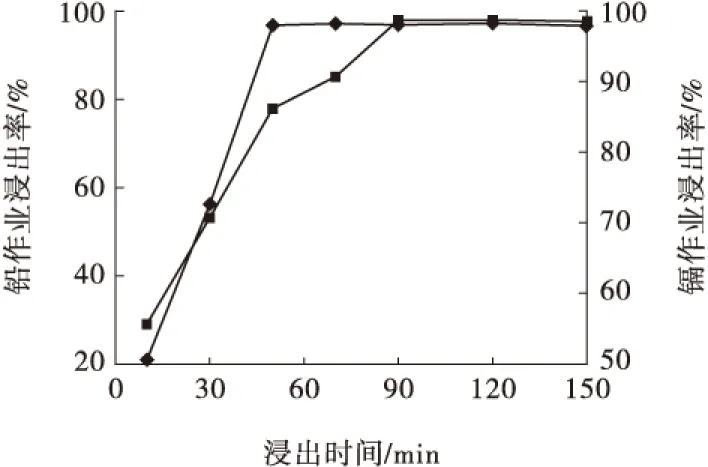
图5 反应时间对铅、镉浸出率的影响
从图5可以看出,随着浸出时间的延长,铅、镉浸出率均上升。综合考虑,确定浸出时间为90 min。
3.2.4 液固比对铅、镉浸出率的影响
液固比试验的NaCl溶液浓度为250 g/L、浸出温度为90 ℃、浸出时间为90 min,试验结果见图6。
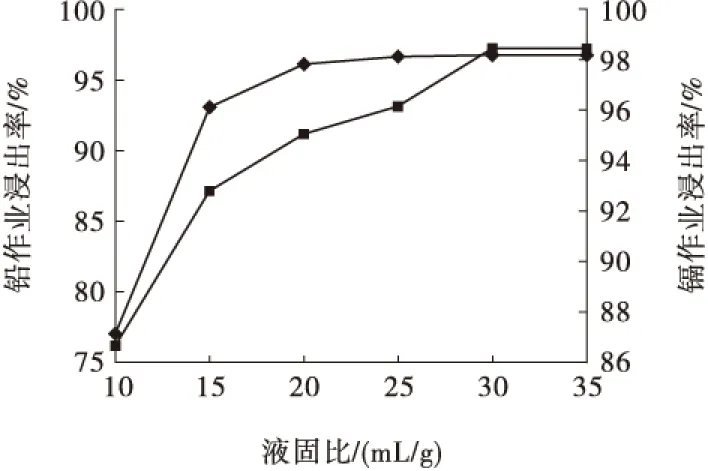
图6 液固比对铅、镉浸出率的影响
从图6可以看出,随着液固比的增大,铅、镉浸出率上升。因为反应式(5)是可逆反应,溶液不断积累的硫酸根离子会抑制反应进行,液固比增大,有利于缓冲溶液中硫酸根离子浓度的上升。综合考虑,确定液固比为30 mL/g,对应的铅、镉浸出率为97.89%和98.12%。
3.2.5 氯化铅结晶试验
酸浸渣用浓度为250 g/L的NaCl溶液按液固比30 mL/g、在90 ℃、浸出90 min,将滤液室温下静置12 h进行结晶,结晶率为92.13%,结晶体的SEM图片见图7。

图7 氯化铅结晶体的SEM图片(放大500倍)
从图7可以看出,氯化铅结晶体微观形貌为细棒状,长度在10~200 μm之间。
3.3 氧化铅前驱体合成中氢氧化钠用量试验
氯化铅与氢氧化钠反应生成的氢氧化铅属两性化合物,与过量的碱溶液反应生成可溶盐Na2PbO2,因此,控制氢氧化钠的用量非常重要。
将干燥后的氯化铅晶体磨细、过200目筛,加入氢氧化钠溶液,液固比为30∶1,反应温度为90 ℃、反应时间为60 min,反应结束后过滤,所得沉淀在80 ℃下真空烘干24 h,称重并分析其中氯、铅含量,氢氧化钠实际用量与理论用量之比(r)对氧化铅前驱体合成试验结果见表6,XRD图谱见图8。
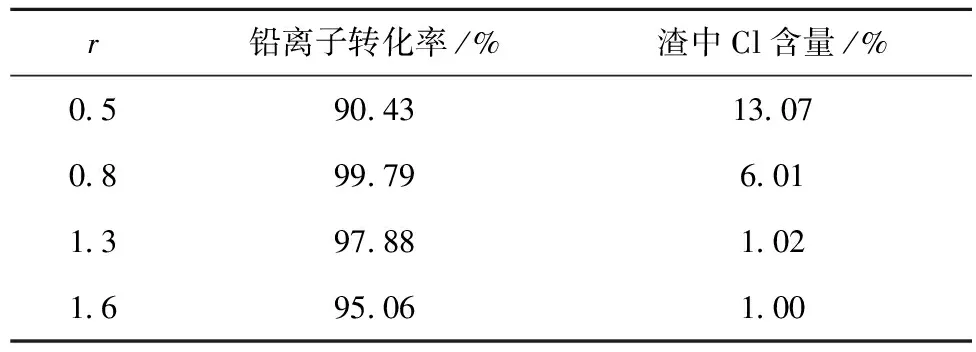
表6 氢氧化钠用量对氧化铅前驱体合成的影响
注:铅离子的转化率是指所得产物中铅总量与反应之前氯化铅中铅总量的比值。

图8 不同氢氧化钠用量情况下沉淀物的XRD图谱
从表6可以看出,随着氢氧化钠用量的增大,铅转化率先上升后下降,而产物中的氯离子含量先下降后维持在低位。综合考虑,确定氢氧化钠的实际用量为理论用量的1.3倍。
从图8可以看出,当r=0.5时,由于碱量不足,反应生成了PbCl(OH);而当r=0.8时,碱式氯化铅衍射峰减少,出现了所需产物Pb(OH)2和3PbO·H2O的衍射峰,少量的氯以PbOHCl形式存在;而当r=1.3~1.6时,PbOHCl的衍射峰也不可见,产物中仅可见Pb(OH)2和3PbO·H2O的衍射峰,产物的分子形式可表示为mPbO·nH2O,因而氯的含量很低,这一结论与表6的结果一致。
3.4 氧化铅粉末的制备
用差热分析仪分析合成的氧化铅前驱体在25~800 ℃下的热反应变化,结果见图9。
从图9可以看出,在25~800 ℃范围内,共出现2个吸热峰,分别对应着2个明显的热重变化,对应的温度分别为102 ℃和504 ℃,推测这2个温度下发生了脱水反应。因此,用马弗炉分别在102 ℃和504 ℃下,对氧化铅前驱体加热焙烧120 min,所得产物的XRD图谱见图10。
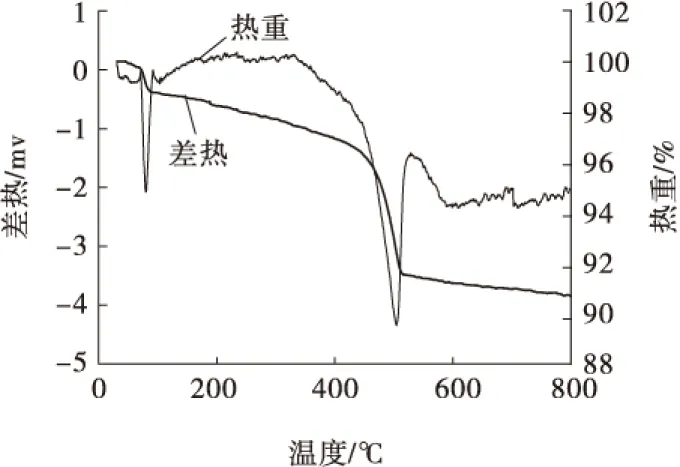
图9 氧化铅前驱体的差热分析结果

图10 不同温度下焙烧产物的XRD图谱
从图10可以看出,不同焙烧温度下,产物的特征峰单一:102 ℃时呈现出Pb(OH)2的特征峰,说明该温度下氧化铅前驱体mPbO·nH2O脱除了部分结晶水;504 ℃时Pb(OH)2的特征峰消失,出现了PbO的特征峰,说明在此温度下Pb(OH)2进一步发生脱水反应,得到最终所需的产物PbO粉末。因此,氧化铅前驱体制备PbO的适宜焙烧温度为504 ℃。
氧化铅前驱体、102 ℃和504 ℃焙烧产物的SEM照片见图11。
从图11可以看出,从氧化铅前驱体到504 ℃的焙烧产物氧化铅,产品的粒度越来越小,结晶形态越来越不规则。图11(a)、图11(d)中的前驱体的形状类似图5中氯化铅晶体的棒状,但尺寸明显变少,长度一般为10 μm,这种形貌的形成是由于在前驱物的合成过程中,有氯化钠产生,而氯离子有很强的配位能力,能吸附在产物的晶体表面,阻止这些晶面的生长,使得晶体的生长有了定向性,从而产物分子被有序排列成棒状,这也就是前驱物中一直有1%左右氯离子存在的原因。图11(b)、图11(e)为氧化铅前驱体脱除部分结晶水的产物,因而尺寸较前驱体有所减小,但没有打乱晶体排布的规律,颗粒长约2 μm。图11(c)、图11(f)为氧化铅前驱体完全脱水的产物,晶体的形貌改变很彻底,规律排布的短棒状消失,呈现的是海绵状疏松的微观形貌,长度小于2 μm,主要化学成分分析结果见表7。

图11 氧化铅前驱体及不同温度下焙烧产物的SEM照片

表7 超细氧化铅粉末的主要化学成分分析结果
从表7可以看出,超细氧化铅粉末纯度较高,氧化铅含量达98.31%。
4 结 论
(1)河南某底吹炉炼铅烟尘Pb含量达44.99%,是重要的二次资源,其中杂质Cd、As的含量为39.48%、5.87%,采用硫酸化焙烧预处理—NaCl浸出酸浸渣—氧化铅前驱体合成—氧化铅粉末生成工艺可获取高质量的超微细氧化铅粉末,实现二次铅资源的高效利用。
(2)硫酸化焙烧预处理—水浸工艺的焙烧过程酸料比为0.6 mL/g、焙烧温度为500 ℃、焙烧时间为120 min,焙烧产物水浸过程的液固比为30 mL/g、水浸温度为60 ℃、水浸时间为120 min,该工艺的Pb、Cd、As去除率分别达2.67%、96.98%、100.00%,产物中Pb、Cd、As的含量分别为67.10%、0.68%、0.03%,初步实现了铅与镉、砷等杂质元素的分离。
(3)NaCl浸出酸浸渣工艺的NaCl溶液浓度为250 g/L、浸出温度为90 ℃、液固比为30∶1 mL/g、浸出时间为90 min,对应的铅、镉作业浸出率为97.89%和98.12%。
(4)氧化铅前驱体合成工艺中氯化铅晶体与氢氧化钠溶液的液固比为30∶1、氢氧化钠实际用量与理论用量之比为1.3、反应温度为90 ℃、反应时间为60 min,产物中仅可见Pb(OH)2和3PbO·H2O的衍射峰,铅转换率为97.88%,氯含量很低。
(5)氧化铅粉末生成工艺的适宜焙烧温度为504 ℃,脱水过程使晶体的形貌发生了彻底改变,具有短棒状海绵疏松的微观形貌,长度小于2 μm,氧化铅含量达98.31%,属优质超细氧化铅粉末。
[1] 李卫锋,张晓国,郭学益,等.我国铅冶炼的技术现状及进展[J].中国有色冶金,2010,4(2):29-33. Li Weifeng,Zang Xiaoguo,Guo Xueyi,et al.Status and process of lead smelting technology in China[J].China Nonferrous Metallurgy,2010,4(2):29-33.
[2] 李卫锋,杨安国,郭学益,等.河南铅冶炼的现状及发展思考[J].中国金属通报,2009(15):34-37. Li Weifeng,Yang Anguo,Guo Xueyi,et al.The present situation and development of Henan lead smelting industry[J].China Metal Bulletin,2009(15):34-37.
[3] 崔雅茹,李凯茂,何江山,等.液态高铅渣还原过程炉渣熔化温度的研究[J].稀有金属,2013,37(3):473-478. Cui Yaru,Li Kaimao,He Jiangshan,et al.Melting point of molten high-lead slag in direct reduction process [J].Chinese Journal of Rare Metals,2013,37(3):473-478.
[4] 李卫锋,贾著红.硫化铅精矿富氧底吹及富氧顶吹熔炼技术[M].长沙:中南大学出版社,2010. Li Weifeng,Jia Zhuhong.Smelting Technology of Lead Sulfide Concentrate Rich Oxygen Bottom Blowing Top-blown[M].Changsha:Central South University Press,2010.
[5] 邵 戈,曾小冬.水口山炼铅底吹炉烟灰综合回收试验研究[J].中国有色冶金,2010,8(4):43-45. Shao Ge,Zeng Xiaodong.Test of comprehensive recovery ash from bottom-blowning furnace of lead smelting in Shuikoushan[J].China Nonferrous Metallurgy,2010,8(4):43-45.
[6] 郑时路.复杂铅烟尘湿法处理新工艺研究[D].长沙:中南大学,2004. Zheng Shilu.New Technology of Complex Lead Smoke Wet Processing Research[D].Changsha:Central South University,2004.
[7] Martins F M,Neto J M d R,Cunha C J d.Mineral phases of weathered and recent electric arc furnace dust[J].Journal of Hazardous Materials,2008,154:417-425.
[8] 钟 晨.从硫化铅精矿中制备红丹和黄丹[J].有色冶炼,1997,12(4):52-54. Zhong Chen.The preparation of yellow lead and red lead from the lead sulfide concentrate[J].China Nonferrous Metallurgy,1997,12(4):52-54.
[9] 宋剑飞,李立清,李 丹.用废铅蓄电池制备黄丹和红丹[J].化工环保,2004,24(1):52-54. Song Jianfei,Li Liqing,Li Dan.Preparation of yellow lead and red lead from used lead batteries[J].Environmental Protection of Chemical Industry,2004,24(1):52-54.
[10] 陈槐隆.综合利用铅渣湿法生产优质黄丹[J].有色金属:冶炼部分,1992,25(1):5-8. Chen Kuilong.The comprehensive utilization of lead slag to produce quality yellow lead[J].Nonferrous Metals:Extractive Metallurgy,1992,25(1):5-8.
[11] 李洪桂.湿法冶金学[M].长沙:中南大学出版社,2011. Li Honggui.Hydremetallurgy[M].Changsha:Central South University Press,2011.
[12] Havlik T,Bernardes A M,Schneider I A H,et al.Hydrometallurgical processing of carbon steel EAF dust[J].Journal of Hazardous Materials,2006,135(1) :311-318.
[13] Jha M K,Kumar V,Singh R.Review of hydrometallurgical recovery of zinc from industrial wastes[J].Resources,Conservation and Recycling,2001,33(2):1-22.
[14] Li L,Zhu X,Yang D,et al.Preparation and characterization of nano-structured lead oxide from spent lead acid battery paste[J].Journal of Hazardous Materials,2012,203:274-282..
[15] 朱新锋,刘万超,杨海玉,等.以废铅酸电池铅膏制备超细氧化铅粉末[J].中国有色金属学报,2010,20(1):133-135. Zhu Xinfeng,Liu Wanchao,Yang Haiyu,et al.Preparation of ultrafine PbO powders from lead paste in spent lead acid battery[J].The Chinese Journal of Nonferrous Metals,2010,20(1):133-135.
[16] Zhu Xinfeng,Li Lei,Sun Xiaojiao,et al.Preparation of basic lead oxide from spent lead acid battery paste via chemical conversion[J].Hydrometallury,2012(117/118):24-31.
[17] Karami H,Karimi M A,Haghdar S,et al.Synthesis of lead oxide nanoparticles by sonochemical method and its application as cathode and anode of lead-acid batteries[J].Materials Chemistry and Physics,2008,108:7-9.
[18] Turan M D,Altundogan H S,Tümen F.Recovery of zinc and lead from zinc plant residue[J].Hydrometallurgy,2004,75:169-176.
[19] Guo Zhaohui,Pan Fengkai,Xiao Xiyuan,et al.Optimization of brine leaching of metals from hydrometallurgical residue[J].Transactions of Nonferrous Metals Society of China,2010(10):2000-2005.
[20] Farahmand F,Moradkhani D,Safarzadeh M S,et al.Brine leaching of lead-bearing zinc plant residue:process optimization using orthogonal array design methodology[J].Hydrometallurgy,2009,95(3):316-324.
(责任编辑 罗主平)
Preparation of Ultrafine PbO Powders with Lead Smelting Dust
Yang Xie1,2,3Li Hongxu1,2,3Li Chao1,2,3Wang Shuai1,2,3Wang Yuyue1
(1.SchoolofMetallurgicalandEcologicalEngineering,UniversityofScienceandTechnologyBeijing,Beijing100083,China; 2.BeijingKeyLaboratoryofGreenRecoveryandExtractionofPreciousMetals,Beijing100083,China;3.MinistryofEducationKeyLaboratoryofEcologyandCycleMetallurgy,Beijing100083,China)
A lead dust of bottom blowing furnace,Henan province,contains Pb 44.99%,which can be used as significant resource for preparing high quality ultrafine PbO powders.The optimal technological condition for preparing ultrafine PbO powders are investigated by adopting the process of sulfuric acid roasting-sodium chloride leaching-lead oxide precursor synthesis-generation of lead oxide powder.The results showed that the removing rate of Pb,Cd,As reached 2.67%,96.98%,100.00% through the process of pre-treatment of sulfuric acid roasting-water leaching process,preliminarily removing the impurities of Pb,Cd,As.The leaching rate of Pb and Cd were 97.89% and 98.12% separately by sodium chloride leaching acid process.The conversion rate of Pb was 97.88% by PbO precursor synthesis process.The product crystal morphology was thoroughly changed during generation process of PbO powder,and the product had short clavite sponge porous microstructure,with length of less than 2 μm and PbO of 98.31%,which is considered as high quality of ultrafine PbO powders.To sum up,this process provides a new idea for recycling of lead dust and preparation of ultrafine PbO powders.
Lead smelting dust,Sulfuric acid roasting,Sodium chloride leaching,Lead oxide precursor synthesis,Ultrafine PbO powder
2014-06-06
国家自然科学基金资助项目(编号:51234008) 。
杨 勰(1989—),女,硕士研究生。通讯作者 李宏煦(1971—),教授,博士研究生导师。
TF812
A
1001-1250(2014)-09-165-07

