云铜降低阴极铜中银含量的生产实践
马 军, 李 坚, 罗劲松, 叶文淳
(1.云南铜业(集团)有限公司, 云南 昆明 650051; 2.昆明理工大学冶金与能源工程学院, 云南 昆明 650093;3.云南铜业股份有限公司, 云南 昆明 650102;4.昆明冶金高等专科学校, 云南 昆明 650033)
云铜降低阴极铜中银含量的生产实践
马 军1, 李 坚2, 罗劲松3, 叶文淳4
(1.云南铜业(集团)有限公司, 云南 昆明 650051; 2.昆明理工大学冶金与能源工程学院, 云南 昆明 650093;3.云南铜业股份有限公司, 云南 昆明 650102;4.昆明冶金高等专科学校, 云南 昆明 650033)
阴极铜含银高不仅影响高纯阴极铜的性能,也给铜电解企业造成经济损失。本文分析了银在铜电解过程中的行为和进入阴极铜的途径,明确了银在铜电解过程中可能发生多种反应,并通过电化学沉积和机械粘附两种途径进入阴极铜;阐述了影响阴极铜银含量的主要因素。云铜从生产实际出发,采取了一系列有效措施,使阴极铜中银含量降低并连续保持在10×10-6左右。
铜电解; 阴极铜; 银
全球铜产量的80%左右产自硫化铜矿,而硫化铜矿经火法冶炼产出的阳极铜中含铜通常只有99.0%~99.5%,须经过电解精炼获得高纯阴极铜。硫化铜矿在造锍熔炼、转炉吹炼及火法精炼过程中,矿物中的银绝大部分被富集在阳极铜中。在铜电解精炼过程中,阳极铜中的杂质主要进入阳极泥和电解液,极少量进入阴极铜。虽然银的标准电极电位较正,但因银主要是以固溶体的形式存在于阳极铜中,在铜电化学溶解的同时,银也溶解进入电解液,此后经过多种复杂的化学反应,绝大部分的银进入阳极泥中,但仍有少量银不可避免地进入阴极铜。国家标准(GB/T467—2010)对阴极铜中银含量的要求较为宽泛(≤25×10-6),正常生产时阴极铜中的银含量均能达到此要求,并保持低于15 ×10-6,因而控制阴极铜含银量方面的研究报道较少。然而,银与铜的市场价格相差近百倍,这就意味着阴极铜中银含量越高,铜电解生产企业的经济损失越大;其次,对于下游铜加工企业,银往往属于有害杂质,希望原料(阴极铜)的银含量控制在一个较低的范围内,所以阴极铜中银含量也是衡量铜电解生产企业产品质量的重要指标之一。另外,金属回收率是反映冶炼企业生产经营及管理水平的一个重要技术经济指标,是企业的生命线。
云南铜业股份公司冶炼加工总厂(简称云铜)历年的铜电解生产中,阴极铜产品的银含量基本维持在10×10-6左右。2011年阴极铜含银平均为9.7×10-6, 2012年1~2月份分别为10.8×10-6和10.3×10-6;然而3~5月份阴极铜的银含量突然升高了30%~50%,分别达到15.2×10-6、15.1×10-6和13.2×10-6。云铜从生产实际出发,对铜电解生产系统进行较全面的分析,明确银在铜电解过程中的行为和进入阴极铜的途径,并采取有效措施降低阴极铜的银含量,提高了银等有价金属的回收率,从而降低了企业的生产成本。
1 银在铜电解过程中的行为
1.1 银在阳极铜中的存在形式
有研究表明[1],杂质在阳极铜中以两种形式存在:其一是以固溶体的形式存在于铜晶体中,如银和镍几乎全部是以固溶体的形式存在于铜的基体中,含量在各区域分布不均,呈现较大差异;其二是以单独的夹杂物沿着铜的晶界存在,主要包括Cu2O、Cu2Se、Cu- Pb- As 的氧化物和Cu- Pb- As- Sb- Bi的氧化物。图1为阳极铜的矿相结构(背散射电镜照片),图2呈现了杂质粒子在阳极铜中的分布及矿相结构[2]。

1-Cu2O; 2-Cu- Pb- As- Sb- Bi的氧化物或Cu- Pb- As的氧化物; 3-Cu; 4-Cu- Cu2O共晶结构
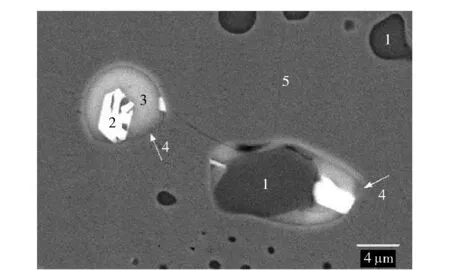
1-Cu2O; 2-Cu- Pb- As的氧化物;3-Cu- Pb- As- Sb- Bi的氧化物; 4-Cu2Se; 5-Cu
阳极铜中95%以上的银是与铜形成亚稳态的固溶体存在于铜基体中,只有很少量的银以Cu- Pb- As- Sb- Bi复杂氧化物或Cu- Ag合金微粒的形式固溶于Cu2(Se,Te)夹渣中,固溶体中银的浓度很小,若浓度较高,则形成过饱和固溶体。而Cu2Se或Cu2(Se,Te)相则以不连续的圆边包裹在夹渣颗粒的外缘(见图2)。
1.2 银在阳极铜电化溶解时的行为
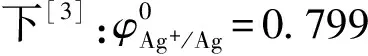
可以看出,与铜相比,银具有较大的正电性,但在阳极铜中固溶的银浓度很小,因此固溶体的平衡电极电位值应与铜接近。在铜电解精炼过程中,铜在阳极发生电化学溶解的同时,铜基体中的银也通过电化学溶解或被溶有氧的电解液所溶解,继而快速发生多种复杂反应而从电解液中沉出。

(1)

(2)
(1)部分溶解的Ag+被电解液中的Cu+还原,形成银粉存在于阳极表面,更典型的是这些银粉在阳极表面形成的Cu2O薄层上沉积,如图3所示[1]。但沉淀出来的大部分金属银粉又会被含氧的电解液再次溶解。

(3)

(4)

(5)

1-金属Ag; 2-Cu2O层; 3-阳极铜
(2)另一些溶解的Ag+以Cu- Ag- Pb- As- Se复杂氧化物颗粒聚集于阳极泥中。
(3)还有一些Ag+与从阳极泥中脱落的Cu2(Se,Te)夹渣反应而形成载银硒化铜或载铜硒化银AgCuSe 和Ag2Se,如图4[2]所示。这类反应的程度取决于阳极或银粉与电解液的接触时间以及银与硒在阳极铜中的含量。随着电解时间延长,Cu2(Se,Te)中的Cu将更多地被Ag+离子所置换(取代),致使阳极泥中的Cu2(Se,Te)含量减少,同时Ag2Se含量增加。

(6)

(7)

1-Pb5(AsO4)3(OH, Cl); 2-PbSO4; 3-(Cu,Ag)2Se;4-AgCuSe;5-Ag粉; 6-Pb- As- Sb- Bi- S- O相;7-Cu- Ag- AsO4- SO4氧化物相
因此,阳极泥硒化物颗粒中银的富集是一个变化过程,阳极泥中的含银硒化物包括(Cu2-xAgx)Se、AgCuSe和Ag2Se[1,4]。
1.3 银在铜阳极泥中的存在形式
铜电解精炼所产阳极泥的组成(物种)很大程度上取决于初始阳极铜的组成,通常含有硒化物(银、铜)、PbSO4、CuSO4·5H2O、NiO、Cu3Ni2-xSbO6-x(x=0.1~0.2,Kupferglimmer)、SbAsO4、BiAsO4、多种Sb- Bi- As- Pb氧化物、砷酸铜、砷酸锡、CuSeO3·2H2O、金属银,并伴有少量的Cu2O、SnO2、CuCl、金属铜、硅胶、重晶石、石英、金和其他贵金属等。
尽管在已溶阳极铜的表面总是有银粉,但大部分的银粉在含氧的电解液中被溶解成为Ag+,而溶解了的Ag+又与硒化铜发生反应生成各种富含银的硒化物。除了金属银和少量存在于氧化物物相中的银以外,有时也会存在Cu- Ag的硫酸盐、AgCl。因此,在阳极泥中以金属态存在的银含量就取决于阳极铜中Ag/Se的摩尔比(或Ag/(Se+Te)),当Ag/Se的摩尔比小于1时,硒化物的主要存在形式为(Cu2-xAgx)(Se,Te)、Cu(Se,Te)和较少量的AgCu(Se,Te);当Ag/Se的摩尔比接近1时,以AgCu(Se,Te)为主要物相;当Ag/Se的摩尔比大于1时,含银的物相除AgCu(Se,Te)以外,还增加了Ag2(Se,Te),并存在金属银;当Ag/Se的摩尔比大于3时,金属银成为阳极泥中主要的银物相,同时存在少量Ag2Se[1]。
1.4 银在阴极铜中析出的机理
银可能以两种方式进入阴极铜:其一是通过Ag+离子放电析出进入阴极铜;其二是以金属Ag或含银化合物的胶体粒子或微细粒子通过机械夹杂、粘附进入阴极铜。
根据能斯特方程,以溶液中离子浓度代替活度计算电极电位分别为[3]:
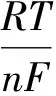
(8)
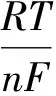
(9)
按照实际生产时的铜电解液,其中Cu2+浓度为 50 g/L左右,Ag+浓度约1 mg/L,电解液温度为60 ℃,则Cu2+和Ag+在阴极还原析出的平衡电极电位分别为:φCu2+/Cu=0.337 V和φAg+/Ag≈0.466 V。可见φAg+/Ag>φCu2+/Cu,因此,电解液中即使Ag+浓度为1 mg/L仍可在阴极放电析出;只有当电解液中Ag+浓度≤0.01 mg/L时,φAg+/Ag≤0.337 V,才可避免Ag+在阴极放电析出。
云铜实际生产中,铜电解液中富余的铜离子以两种方式脱除:一部分电解液中的铜通过结晶硫酸铜脱除;另一部分电解液则以电积生产阴极铜(电积铜)的方式进行脱铜。而电积铜中的银含量一直比电解精炼所产阴极铜(电解铜)的银含量要高,如2013年1~6月份所产电积铜的银含量为13.1×10-6,而电解铜的银含量却为8.4×10-6。值得关注的是,电积脱铜所采用的阳极板为不含银的铅基合金惰性阳极,而且电积脱铜时电解液中的固体悬浮物含量也比电解精炼时要低,然而电积脱铜时的槽电压比电解精炼时高8倍左右,同时电积液中Cu2+浓度降低,增加了阴、阳极的极化,使电解液中相同浓度的Ag+更加容易在阴极放电析出。因此,可以认为银的放电沉积是污染阴极铜的主要原因。但若电解液中固体悬浮物浓度增加,将进一步增加银进入阴极铜的几率,导致阴极铜银含量增加。通过各种手段减少电解液中悬浮微粒(漂浮阳极泥、银粉微粒、含银化合物微粒等)的含量,必然有利于降低阴极铜中银的含量。
2 影响阴极铜含银的因素及降低阴极铜含银的措施
生产实践表明,阴极铜的银含量主要与阳极铜的银含量、阳极泥浆过滤质量、电解液的精细过滤程度以及电解液中氯离子浓度等因素有关。此外,铜电解生产的电流密度、电解液组成、电解液流量、电解液温度、电解液粘度、电解槽面管理以及所产阴极铜结晶的致密程度等因素对阴极铜的银含量也有一定的影响。
2.1 阳极铜银含量
生产实践表明,阴极铜的银含量与阳极铜的银含量存在正相关的关系。在60 ℃时,当阳极铜的银含量从0.3%增加至1.0%时,阴极铜的银含量几乎增加1倍,如图5[5]所示。

图5 阴极铜中银含量与阳极铜中银含量的关系(60 ℃)
阳极铜的银含量升高,阳极溶解过程中铜和银均发生电化学溶解,随后在阳极表面和电解液中生成较多的银粉、硒化银和氯化银微粒悬浮于电解液中,这些微粒使电解液变得浑浊,而含银的悬浮物将有更多机会粘附于阴极表面,被新沉积的铜包裹,最终导致阴极铜的银含量偏高、阴极结晶组织疏松、表面粗糙。用高银阳极铜生产的阴极铜,往往会出现阴极铜含银显著增加,而其它杂质含量正常的现象。
广西河池铜厂因所处理的铜原料含银高达0.20%,所产阳极铜的银含量高达0.50%~0.65%,为维持正常生产并获得质量较好阴极铜,该厂采取了将铜电解的电流密度降低至160 A/m2左右、降低电解液中Cu2+浓度、适当升高电解液温度等措施,产出的阴极铜中Cu+Ag含量为99.97%,银含量为18×10-6[6]。加拿大铜精炼厂(CCR)的阳极铜中银含量平均为0.25%~0.3%,有时高达0.4%,电解生产过程中阳极钝化现象严重,为此,该厂用银含量分别为(%):0.37、0.41、0.47、0.55、0.65及0.88的阳极铜进行小型试验研究,结果表明只有控制合理的电解工艺条件,如Cu2+浓度低于43 g/L、Ni2+浓度低于8 g/L、电流密度低于257 A/m2、电解液温度维持在65 ℃左右,才能有效地避免电解过程中阳极发生钝化[7]。
云铜主要以硫化铜矿为原料生产阳极铜,继而产出高纯阴极铜,所产阳极铜的成分见表1。

表1 云铜所产阳极铜的成分 %
云铜2012年以来阳极铜的成分与表1中各项指标相近,基本可以排除阳极铜成分波动造成阴极铜含银的影响。
2.2 电解液中悬浮颗粒物含量
生产实践表明,当电解液中悬浮颗粒物(漂浮阳极泥)含量大于30 mg/L时,阴极铜表面会产生斑点,而且银含量增加。云铜电解生产采用板框压滤机进行阳极泥浆液的固液分离,滤液直接用泵送至铜电解生产的循环槽。在阴极铜银含量突然升高的生产期间,板框过滤机的过滤后液有浑浊现象,过滤后的电解液中有肉眼可见的灰白色分散颗粒;从电解槽中取出的阴极铜(烫洗前)上沿有黑色阳极泥颗粒附着,烫洗后的阴极铜表面颜色较暗;在阴极铜板面生长的突瘤(庖丁)与板面接触处,有阳极泥颗粒。因此,自2012年5月1日起,将提高电解液的过滤质量作为降低阴极铜银含量的主要措施:①及时更换板框过滤机的破损板、框和滤布;②增加板框过滤机数量,增加过滤面积,并在阳极泥浆泵上增设变频器,以降低板框过滤机单位面积的过滤速度,提高阳极泥浆液的过滤质量;③加大对板框过滤机过滤后液的检查力度,发现过滤后液跑浑及时进行处理,严防跑浑液进入生产电解液体系;④加大对电解液精细过滤的LAROX过滤机滤布的更换频率。
上述措施使电解液中悬浮颗粒物含量从43 mg/L降低至14 mg/L,显著提高了电解液的澄清度。5月1日~10日,阴极铜平均银含量为14.9×10-6,而5月11日~20日所产阴极铜的银含量则下降至10.6×10-6,下降了29%。
2.3 电解液组成
电解液中Cu2+或杂质离子浓度的增加,会使电解液的粘度和密度增大,不利于电解液中阳极泥的沉降,并增加悬浮颗粒物粘附阴极的几率,从而使阴极铜中的银含量增大。此外,云铜近年来电解液中Ni2+浓度长期高达20~25 g/L,也是电解液粘度和密度增加大的又一重要因素。因此,云铜加大净化系统对铜、镍、砷、锑等杂质离子的脱除力度,将电解液中Cu2+浓度从50.24 g/L降低至43.7 g/L,Ni2+浓度从23.2 g/L降低至15.24 g/L,有效降低电解液粘度和密度,为阳极泥沉降创造良好的条件。
2.4 电流密度
电流密度是影响金属沉积物结构和性质的一个主要因素。一般来说,电流密度低,容易形成细粒粘附阴极沉积物;电流密度高,易产生粗粒不粘附的多孔沉积物。
实际生产中提高电流密度,首先会增加阴、阳极的极化电位,更有利于电极电位比铜正的金属杂质(如银)的析出;其次需要相应地改变铜电解生产的工艺条件(如增加电解液的循环速度和添加剂的加入量等);再者阴极表面的粗糙程度会随之增加,给电解液中的含银微粒在阴极板面上粘附增加更多的机会。因此,电流密度增大,会使阴极铜中银含量升高。为此,云铜铜电解的电流密度总体控制在300 A/m2以下,2011年电流密度为273 A/m2,2012年5月起将电流密度降至263 A/m2。
2.5 电解液流量及均匀性
在电解生产过程中,某些情况下(如提高电流密度等)需要增大电解液循环流量以避免阴极表面铜离子浓度贫化而引起的浓差极化,然而电解液循环流量的增大又将使阳极泥的沉降速度减慢,并使电解液中悬浮颗粒物含量增加,从而使阴极铜的银含量增加。曾有生产实践表明,电解液流量从30 L/(min·槽)增加到35 L/(min·槽)时,阴极铜的银含量增加了1.2×10-6。为此,云铜将传统铜电解系统和艾萨铜电解系统的电解液流量分别下调至25~30 L/(min·槽)和30~35 L/(min·槽),并加强电解槽循环流量的监测,确保每个电解槽电解液流量均匀稳定,有利于阳极泥的沉降。
2.6 电解液温度
电解液温度升高,将加速阳极铜固溶体中银的溶解,并有利于Cu+浓度的提高[5],而Ag+与Cu+能快速反应生成单质银粉,Ag+也能与Cu2(Se,Te)反应生成AgCu(Se,Te)、Ag2(Se,Te)等,综合的结果可能会增加电解液中银粉和含银化合物微粒的含量,相应地增加了银粉和含银化合物微粒通过机械夹杂进入阴极铜的几率;然而,电解液温度升高,也将使电解液的密度和黏度降低,有利于加快电解液中悬浮颗粒物的沉降,减少银粉和含银化合物微粒通过机械夹杂进入阴极铜的几率,从而减少贵金属的损失。生产实践表明:当电解液温度低于50 ℃时,电解液会出现浑浊现象,而温度上升至55~60 ℃时,浑浊现象逐渐消失,这是由于一些细微的阳极泥粒子在温度低、粘度大的电解液中不易沉降所至。因此,温度对阴极铜中银含量的影响较为复杂,应综合考虑。为此,云铜将传统法铜电解生产系统的电解槽出口温度由60 ℃提高到62 ℃,而将艾萨法铜电解生产系统的电解槽出口温度由64 ℃降低到62 ℃。云铜经过35 d的生产,数据表明,阴极铜平均银含量从电解液温度为64 ℃时的9.9×10-6降低至62 ℃时的8.3×10-6,平均降低了1.6×10-6。
2.7 其他因素
云铜的生产实践表明,阴极铜结晶的致密、光滑程度对阴极铜中银含量有一定影响。结晶致密、表面平整光滑的阴极铜不易粘附和夹杂阳极泥粒子。因此,实际生产中根据情况,对添加剂明胶、硫脲和盐酸的配比以及添加量进行及时调整,确保阴极铜产品结晶致密。
此外,云铜加强了电解槽的槽面及阳极泥浆过滤岗位管理,一是减少传统法铜电解生产系统在槽面挑拣不良残极的数量,由原来的约150块/d降低到80块/d左右,减少对电解液的搅动以及由此带来的阳极泥机械污染阴极铜的几率;二是定期(大约三个月)对阳极泥浆过滤系统的后液池(清液池)和电解液安全储槽进行清洗除泥,很大程度上降低了电解液中悬浮颗粒物的浓度。
2.8 降低阴极铜银含量的效果
通过以上一系列措施,2012年6月份起云铜阴极铜中的银含量大幅下降,统计数据见图6。
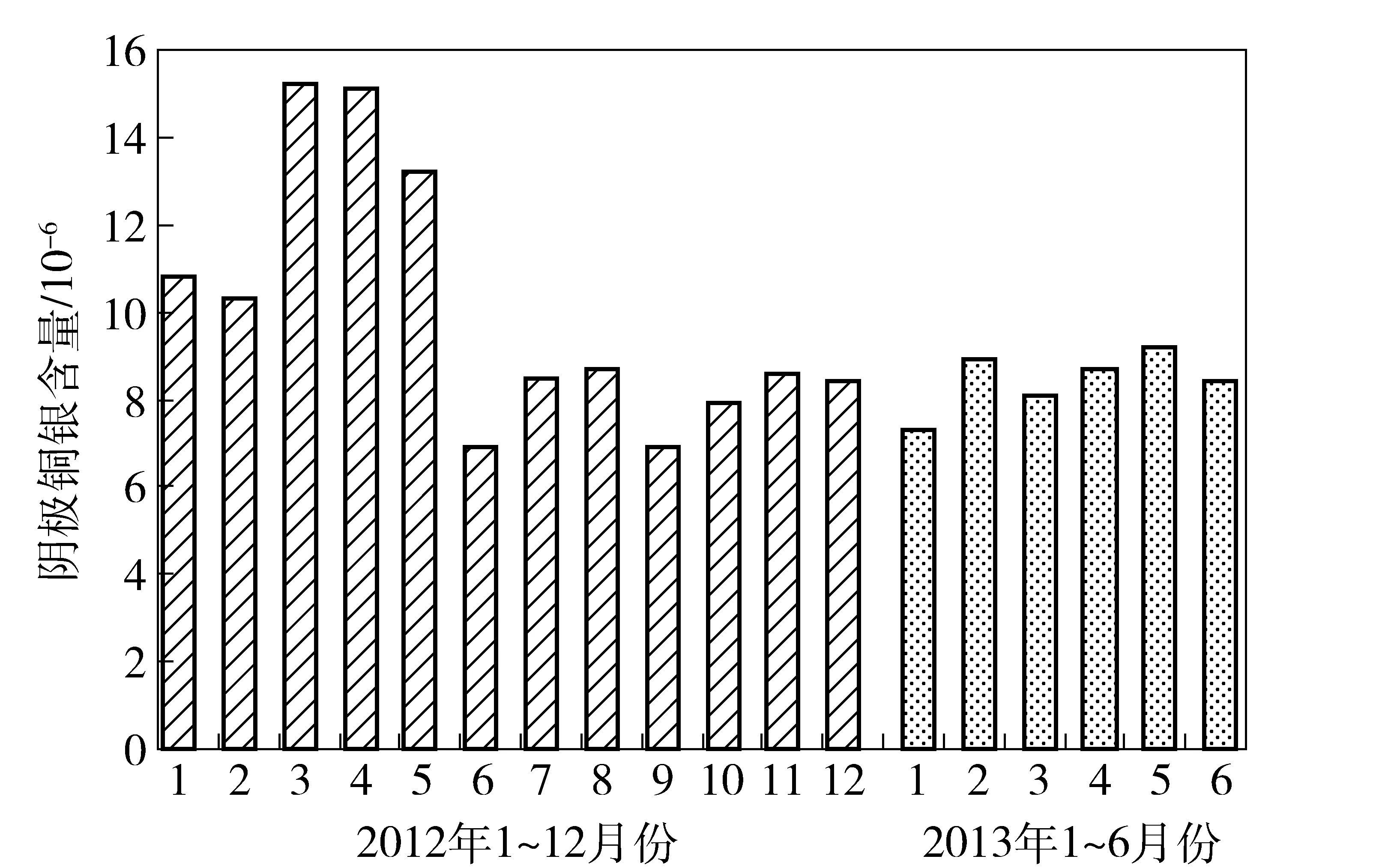
图6 2012年1月至2013年6月云铜所产阴极铜的银含量
从图4可以看出,通过采取一系列措施,2012年6~12月份阴极铜的银含量平均为8.0×10-6,较2012年1~5月份的平均12.9×10-6下降了4.9×10-6,下降幅度达38%;而且2013年1~6月份阴极铜的银含量也一直保持较低水平,平均为8.4×10-6,较2012年全年阴极铜的平均银含量10.1×10-6降低了1.7×10-6。
2013年1~6月份,云铜阴极铜累计产量为147.8 kt,上述措施实际减少了进入阴极铜的银总量为251 kg,按银价4 360元/kg(不含税价)计算,减少了阴极铜因含银高而造成的损失约100万元。
3 结论
铜电解生产中,银以电化学沉积和机械粘附两种方式进入阴极铜。而阳极铜的银含量、电解液的组成、悬浮颗粒物的浓度、电流密度、电解液温度、电解液循环流量等多种因素均可能对阴极铜的银含量产生影响。为避免阴极铜的银含量增高给铜电解生产企业造成经济损失,并为下游的铜加工企业提供优质铜原料,需要综合考虑上述各影响因素,制定系统合理的生产方案,控制适当的电解技术条件以降低阴极铜中银的含量。经过一年的探索及生产实践,云铜2013年1~6月份阴极铜的银含量显著降低并保持在8.4×10-6左右,提高了阴极铜的质量,同时为企业带来良好的经济效益。
[1]T T Chen, J E Dutrizac. A mineralogical study of the deportment and reaction of silver during copper electrorefining[J]. Metallurgical and Materials Transactions B, 1989, 20(3) : 345-361.
[2]T T Chen and J E Dutrizac. Mineralogical characterization of a copper anode and the anode slimes from the La Caridad copper refinery of Mexicana de Cobre[J]. Metallurgical and Materials Transactions B, 2005, 36B(4): 229-240.
[3]J G SPEIGHT. Lang’s Handbook of Chemistry[M]. Sixteenth Edition, McGraw-Hill Companies, Incorporated, 2004.
[4]T T Chen, J E Dutrizac. The deportment of selenium and tellurium during the electrorefining of copper. Minor Elements 2000[C], C Young, Ed., Processing and Environmental Aspects of As, Sb, Se, Te, and Bi. Society for Mining, Metallurgy, and Exploration, Inc. (SME), Littleton, Colorado, 199-212.
[5]朱祖泽, 贺家齐. 现代铜冶金学[M]. 北京 : 科学出版社, 2003.
[6]张继荣, 林忠. 高银阳极铜电解精炼的生产实践[J]. 有色金属(冶炼部分), 1997,(5): 6-7.
[7]史有高译. 高银铜阳极的电解精炼[J]. 有色冶炼,1994,(3): 11-16.
PracticeofreducingcontentsofsilverincathodecopperinYunnanCopperIndustryCo.,Ltd.
MA Jun, LI Jian, LUO Jin-song, YE Wen-Chun
The high content of silver in cathode copper affects the performance of high-purity cathode copper, and leads to economic loss of copper electrolysis enterprise. The behaviors of silver in copper electrolysis process and the ways to enter into cathode copper were analyzed, various reaction of silver that maybe occurred in the copper electrolysis process were determined, the two ways of silver to enter into the cathode copper including electrochemical deposition and mechanical adhesion were proposed, the key factors that influence the content of silver in cathode copper were introduced. According to the production practice, some effective measures to reduce the content of silver in cathode copper were adopted, and the content of silver maintained about 10×10-6.
copper electrolysis; cathode copper; silver
马 军(1974—),男,云南昆明人,云南铜业(集团)有限公司,工程师。

TF811
B


