V-M/TiO2(M=Cu、Cr、Ce、Mn、Mo)催化燃烧含氯有机废气
黄海凤,宁星杰,蒋孝佳,顾 蕾,卢晗锋
(1.浙江工业大学生物与环境工程学院,浙江 杭州 310014;2.浙江工业大学化学工程与材料科学学院,催化反应工程研究所,浙江 杭州 310014)
V-M/TiO2(M=Cu、Cr、Ce、Mn、Mo)催化燃烧含氯有机废气
黄海凤1,宁星杰1,蒋孝佳1,顾 蕾1,卢晗锋2*
(1.浙江工业大学生物与环境工程学院,浙江 杭州 310014;2.浙江工业大学化学工程与材料科学学院,催化反应工程研究所,浙江 杭州 310014)
以TiO2为载体,采用浸渍法制备V-M/TiO2(M=Cu、Cr、Ce、Mn、Mo)双金属氧化物催化剂,考察其催化燃烧氯苯、二氯甲烷等含氯有机废气(CVOCs)的性能,并通过XRD、BET、H2-TPR和NH3-TPD对催化剂进行了表征.结果表明,V-Mo/TiO2催化剂比表面积最大,催化剂表面活性组分的高分散性和良好的酸性分布使得V-Mo/TiO2能够在260oC将氯苯完全转化为CO2和HCl.而V-Mn/TiO2则具有丰富的活性氧,可显著提高催化剂深度氧化二氯甲烷的能力,在380℃时二氯甲烷即可完全燃烧,并且反应对CO2有着很高的选择性.
含氯有机废气(CVOCs);V-M/TiO2双金属催化剂;催化燃烧
含氯有机废气(CVOCs)广泛存在于机械、石油化工、制药、涂料装饰业等生产过程中,其排放对大气环境和人类健康会造成严重危害[1-2].常见的CVOCs处理方法有直接燃烧法、光催化法[3-4]、溶剂吸收法、催化燃烧法[5]等.其中,催化燃烧法在处理CVOCs时具有起燃温度较低、能耗小、便于工业化应用及有效避免二等剧毒物质产生的优点,被认为是治理 CVOCs的有效方法之一[6-9].氯苯和二氯甲烷是工业上常见的含氯有机废气,V2O5/TiO2催化剂在处理氯苯、二氯苯等芳烃类CVOCs时显示良好的催化活性和抗氯中毒能力,但对CO2选择性不高,在催化燃烧过程中易产生大量的CO[10];此外,V2O5/TiO2很难在低温条件下将二氯甲烷、二氯乙烷等较稳定的烷烃类氯化物完全转化,并且燃烧过程中容易生成一氯甲烷、甲醛等有害的中间产物,造成二次污染.含氯有机废气的催化燃烧中,不仅要求催化剂有着较高活性和稳定性,还需避免CO、一氯甲烷等有害中间物质的大量产生.为此,研究者通常采用制备双金属氧化物催化剂来提高V2O5/TiO2的催化性能[11].
据文献报道[12-14],CrOχ具有催化活性高、选择性高的优点,能够将二氯甲烷等烷烃类氯化物转化为 CO2、H2O、HCl,副产物较少;MnOχ有着较好的活性氧迁移能力[5,15],Mn和Zr的混合氧化物种可以促使二氯乙烷、三氯乙烯的起燃温度向低温偏移,促进CO向CO2的转化[16]; CeO2具有良好储放氧能力和催化活性,据报道[17],在MnOχ/Al2O3中添加适量Ce可提高催化剂对甲苯的氧化活性.此外,Casagrande等[18]报道,在SCR脱硝中,Mo氧化物掺杂的V2O5/TiO2催化剂增强了活性组分与载体之间的相互作用,增加催化剂表面酸量,并且抑制锐钛矿相的TiO2向金红石相转变,进而提高了催化剂的脱硝性能.Huang等[19]研究发现,CeO2-USY催化剂中,添加一定量Cu氧化物可以增加催化剂表面强酸中心的数目,促进二氯乙烷(DCE)的深度氧化.
目前,V-Mo/TiO2、V-W/TiO2、V-Cu/TiO2等双金属催化剂在SCR脱硝中已得到广泛应用,但 V与 Mn、Mo等制成双金属催化剂来处理CVOCs的研究报道并不是很多,且很少有研究者采用V-Mn/TiO2来处理二氯甲烷.基于以上分析,本文尝试以TiO2为载体,采用浸渍法制备了一系列V-M/TiO2(M= Cu、Cr、Ce、Mn、Mo)双金属氧化物催化剂,考察催化剂对氯苯和二氯甲烷的催化活性和产物选择性,并借助 XRD、BET、H2-TPR和NH3-TPD等表征手段,对双金属氧化物催化剂的催化燃烧机制进行了探讨.
1 材料与方法
1.1 催化剂制备
采用浸渍法制备一系列V-M/TiO2(M=Cu、Cr、Ce、Mn、Mo)双金属氧化物催化剂.以V-Cr/TiO2催化剂为例,取一定量的催化剂前驱体 Cr(NO3)3·9H2O和 NH4VO3于烧杯中,加入100mL去离子水,60℃搅拌溶解,再向溶液中加入2g TiO2载体,磁力搅拌20min,置于旋转蒸发仪中于70℃水浴蒸干,在110℃干燥12h,置于马弗炉于500℃焙烧5h,得到所需的V-Cr/TiO2催化剂.催化剂活性组分理论负载量为10wt%,V与M的质量比约为1:2(通过物质的量折算).采用上述相同方法制备V-Cu/TiO2、V-Ce/TiO2、V-Mn/TiO2、V-Mo/TiO2和V2O5/TiO2催化剂,其中Cu、Ce、Mn、Mo的前驱体分别为 Cu(NO3)2·3H2O、Ce(NO3)3·6H2O、Mn(NO3)2和H32Mo7N6O28. 1.2 催化剂活性评价
催化剂的氯苯、二氯甲烷活性测试在固定床反应器中进行.反应管内径为 10mm,催化剂用量为0.2g,用0.8g石英砂稀释.有机气体发生器置于冰水混合物(0℃)中,通过调节质量流量计上鼓泡气和稀释气流量(鼓泡气和稀释气均为空气),控制氯苯和二氯甲烷的进料浓度为5000mg/m3,反应空速(GHSV)为15000mL/(g·h),氯苯、二氯甲烷转化率采用GC9790型气相色谱仪分析.
1.3 催化剂表征
X射线衍射(XRD,X-ray Diffraction)测试采用瑞士ARL公司SCINTAG XTRA高分辨多晶X射线衍射仪,Ni滤波,Cu靶,Ka辐射源,管电压为40kV,管电流为50mA.
比表面积测试采用Micromeritics ASAP2010物理吸附仪,吸附测定之前,样品于 250℃下真空脱气3h,在-196℃下N2吸附-脱附.样品的比表面积采用BET法计算.
氢程序升温还原(H2-TPR,H2-temperature programmed reduction)测 试 采 用 FINE SORB-3010E型程序升温化学吸附仪.称取样品200mg,先在高纯 Ar中加热到 200℃预处理 1h,再降至50℃,通10%H2/Ar,以10℃/min速率升温至 800℃,热导检测器测量消耗的 H2(柱温恒定60℃),记录电信号.
氨程序升温脱附(NH3-TPD,NH3-temperature programmed desorption)测 试 采 用 FINE SORB-3010E型程序升温化学吸附仪.称取样品200mg,先在高纯He中加热到500℃并预处理1h,再降至50℃,通NH3吸附1h后,用高纯He恒温吹扫1h,最后以10℃/min速率升温至800℃,热导检测器测量脱附的 NH3(柱温恒定 60℃),记录电信号.
2 结果与讨论
2.1 催化剂的表征分析
结果如图 1所示 V2O5/TiO2催化剂在 2θ= 25.3、37.8、48.1、53.89和 55.1°处有明显的衍射峰,归属于锐钛矿的 TiO2特征峰;V2O5晶相则在 20.3°、26.1°处出现其衍射特征峰.Ce、Mn、Mo等元素分别与V共同负载在TiO2载体上时,催化剂上25.3°、37.8°等处的TiO2衍射峰的位置和强度没有发生明显的变化,说明 V-Ce/TiO2、V-Mn/TiO2等催化剂上TiO2的结构没有遭到破坏;XRD图谱中没有被检测到 CeO2、Mn2O3、MoO3和V2O5氧化物的晶相,只是在2θ=24.03°、21.5°等处出现了微弱的 CeVO4,MoV2O8氧化物的衍射峰,表明Ce、Mn、V等活性物种在载体表面呈无定型态或分散度较高.上述实验现象说明Ce、Mo、Mn等元素与V之间的相互作用在一定程度能够抑制V2O5晶相的形成以及晶相在载体表面的聚集,有利于 V活性组分的分散[20].对于V-Cr/TiO2和V-Cu/TiO2催化剂,TiO2在25.3°、48.1°处的特征峰变的窄而尖锐,并且在 27.4°、36.1°处出现了金红石型的TiO2衍射峰,说明Cr、Cu与 V的共同作用在一定程度上改变了 TiO2的结构,导致锐钛矿的 TiO2向金红石型转变.此外,在36.1°、39.2°处检测到了CrO3的特征峰[13],并且V2O5晶相在 20.3°处的特征峰变的明显,说明在V-Cr/TiO2和V-Cu/TiO2中,活性组分主要以单一的氧化物形式存在,V2O5晶相容易在催化剂表面发生团聚现象.
如表1所示,相比于纯TiO2载体,负载活性组分后,催化剂的比表面积和孔容呈减小趋势,这可能是由氧化物在催化剂表面沉积导致,此外锐钛矿 TiO2转变为金红石型也会降低催化剂的比表面积[21-22].V-Cr/TiO2和 V-Cu/TiO2比表面积最小,这可能与大量V2O5、CrO3晶相在催化剂表面聚集以及部分金红石型 TiO2的形成有关.V-Mn/TiO2和V-Mo/TiO2的比表面积分别为67.01m2/g和40.28m2/g,相对于TiO2载体,比表面积损失较少,结合之前的 XRD表征,说明 Mn、Mo与V共同负载TiO2上在一定程度上抑制V物种在催化剂表面的聚集和 TiO2载体晶型的转变,提高活性组分在载体表面的分散度.

图1 催化剂的XRD谱图Fig.1 XRD patters of the catalysts
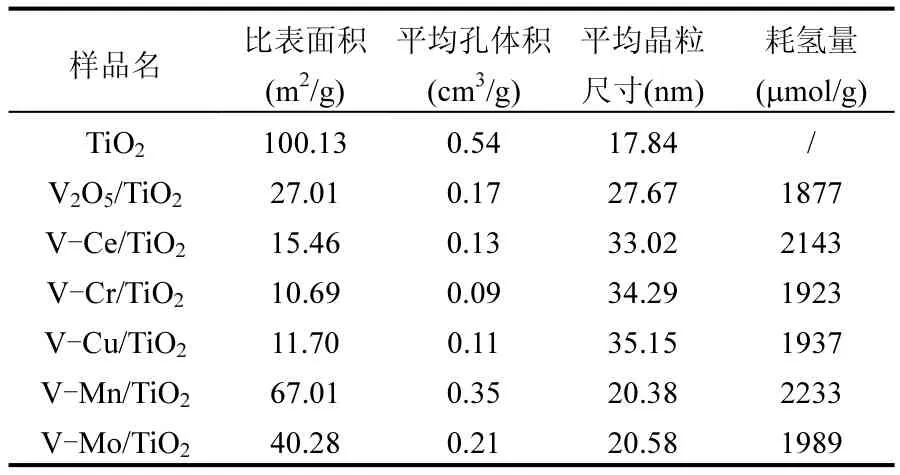
表1 催化剂的物理化学性质Table 1 The physical and chemical properties of catalysts
2.2 H2-TPR表征分析
在含氯有机废气的催化燃烧中,一般来说,催化剂的氧化性能越强,越有利于有机物的降解.为此,我们对双金属氧化物催化剂进行了 H2-TPR表征,结果如图2所示.V2O5/TiO2催化剂在530℃左右出现一个宽的还原峰,可归属为 V5+物种的还原[23].V-Cr/TiO2、V-Ce/TiO2和V-Cu/TiO2都显示单一的还原峰,V-Cr/TiO2中氧化物还原峰温度向高温偏移,说明Cr的存在抑制了V氧化物的还原;而Ce、Cu与V的之间的相互作用则提高了催化剂的氧化还原性,使得催化剂的起始还原温度向低温偏移.V-Mn/TiO2和V-Mo/TiO2催化剂在 300~550℃之间出现 2个明显的还原峰,低温还原峰分别归属于 Mn4+[24]和 Mo6+的还原
[25],V5+的还原温度降低到了475℃和510℃,表明Mn、Mo与V之间的相互作用促进了钒氧化物的还原,有利于催化剂表面活性氧的转移.各催化剂的耗氢量如表1所示,V2O5/TiO2催化剂耗氢量为1877μmol/g,Ce、Mn等金属与V共同负载于TiO2上后,耗氢量明显增加.V-Mo/TiO2催化剂中,Mo和 V氧化物的耗氢量分别为 1141和1265μmol/g,而在V-Mn/TiO2中,H2消耗量达到了2233μmol/g,催化剂在350℃和475℃处还原峰耗氢量分别为1209μmol/g和1024μmol/g,活性氧数量有了大幅度提升,可为 CVOCs的氧化提供更多的活性氧.

图2 催化剂的H2-TPR谱图Fig.2 H2-TPR patterns of the catalysts
2.3 NH3-TPD表征分析
含氯有机废气的催化燃烧中,氯苯、二氯甲烷等首先吸附在催化剂表面的 L酸或者Brønsted酸性位上发生脱氯作用,然后在表面活性氧和晶格氧的作用下进一步氧化成 CO2、HCl[14,26],催化剂表面酸性分布对催化剂活性有一定的影响.如图 3所示,V2O5/TiO2催化剂在160℃左右出现一个宽的脱附峰,可认为是催化剂表面对 NH3物理吸附的结果,670℃左右出现的单一脱附峰,归属于吸附在L酸位上的NH3脱附结果[27],较大的峰面积说明 V2O5/TiO2催化剂上存在较多的L酸.对于V-Ce/TiO2、V-Cr/TiO2和V-Mn /TiO2,催化剂在160℃左右的脱附峰变弱甚至消失,只是在 650~700℃这一温度段出现一个L酸的脱附峰,并且脱附温度有所偏移,催化剂表面L酸量减少,这可能是由金属氧化物将酸性位覆盖导致.V-Cu/TiO2在650℃左右两边各出现一个小的肩峰,说明 Cu的引入影响了催化剂上L酸分布.V-Mo/TiO2催化剂TPD谱图中出现3个脱附峰,相比于V2O5/TiO2,催化剂在430℃形成一个新的脱附峰,可认为是吸附在催化剂表面Brønsted酸性位上NH3脱附的结果,说明Mo与V或者V-Mo与TiO2之间的相互作用在一定程度上促进了Brønsted酸的形成,有利于CVOCs在催化剂表面的吸附和脱氯反应的进行.

图3 催化剂的NH3-TPD谱图Fig.3 NH3-TPD patterns of the catalysts
2.4 催化剂的活性评价
由图4可见,V2O5/TiO2在低温段处理氯苯的活性较差,200℃只有 32%左右的转化率.当温度继续升高时,其催化活性迅速提高,T90约为325
℃.V-Ce/TiO2处理氯苯的燃烧曲线与 V2O5/ TiO2大致相同,说明Ce与V的共同负载对催化剂处理氯苯的性能影响不大.V-Mn/TiO2处理氯苯时,其低温活性有一定的提升,200℃氯苯转化率为 30.4%,但随着温度继续升高,氯苯的转化率缓慢增加.双金属Mo与V共同负载于TiO2上后,催化剂处理氯苯的活性有着明显的提升,200℃时氯苯的转化率为45.3%,T90约为260oC,相比于V2O5/TiO2,转化温度下降了 65℃左右,说明V-Mo/TiO2对氯苯有着很好的处理效果,相比于目前文献报道的MnCe、Ru/TiO2等催化剂,活性并没有太大的差异.而 V-Cr/TiO2和 V-Cu/TiO2处理氯苯的活性反而弱于单金属的V2O5/TiO2催化剂,尤其是V-Cu/TiO2催化剂,氯苯在200℃时转化率只有 18.8%,当温度升高到 350℃时,也只有50%左右的氯苯被转化.
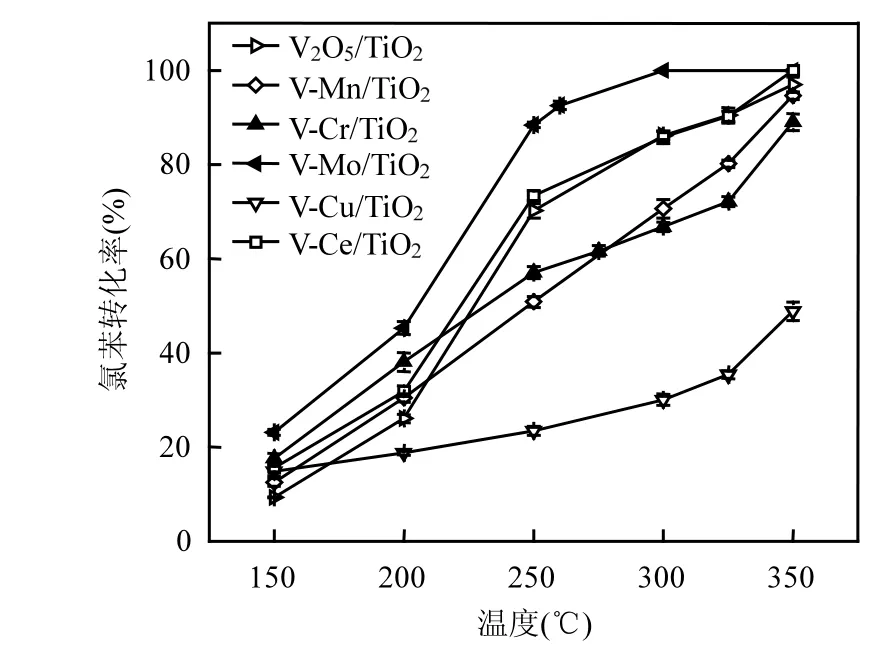
图4 催化剂对氯苯转化率的影响Fig.4 The conversion of chlorobenzene over different catalysts

图5 催化剂对二氯甲烷转化率的影响Fig.5 The conversion of dichloromethane over different catalysts
二氯甲烷属于烷烃类氯化物,相比于氯苯,断裂其C—Cl、C—H键需要更多的能量,并且在催化燃烧中容易产生更难降解的CH3Cl、CHCl3等中间产物,因此二氯甲烷比氯苯更难降解[28-29].本实验中各催化剂处理二氯甲烷的燃烧曲线如图5所示,与氯苯相比,催化剂的起燃温度均向高温偏移.V2O5/TiO2在处理二氯甲烷时拥有一定的活性,450℃时二氯甲烷的转化率约为60%.Mn、Ce、Mo分别与V共同作用在TiO2上后,催化剂催化燃烧二氯甲烷的活性有明显的提升,300oC时,二氯甲烷在 V-Mn/TiO2、V-Ce/TiO2和V-Mo/TiO2的转化率分别为77.4%,37.2%和41%. V-Mn/TiO2催化剂在处理二氯甲烷时拥有最佳的催化性能,T90约为 380℃.目前文献报道的Pt/Al2O3、Pd/TiO2-Al2O3、Cr2O3/A2lO3等催化剂完全转化 DCM的温度在350℃左右,活性较好,但是贵金属容易发生氯中毒而导致催化剂失活,而 Cr是重毒物质,需避免使用,在相同的测试条件下,本论文制备的V-Mn/TiO2催化活性与贵金属和铬系催化剂相差不大,并且其抗氯中毒能力强,对环境毒害作用较小,是一种环境友好型催化剂.对于V-Cr/TiO2和V-Cu/TiO2,催化剂催化燃烧二氯甲烷的活性反而呈下降趋势,450℃时,二氯甲烷的转化率分别为24.1%,31.1%,活性较差.
据文献[30]报道,V2O5/TiO2在催化燃烧CVOCs的过程中,V2O5晶相和金红石TiO2的形成不利于催化反应的进行.由XRD分析可知,Cr、Cu与V共同负载在TiO2上时,Cr、V等活性元素主要以CrO3、V2O5单一氧化物形式团聚于催化剂表面,分散性较差,并且有一定量的锐钛矿相TiO2转化为金红石相,导致催化剂比表面积大量减小,进而影响了催化剂表面氧化物的还原和酸性分布,导致V-Cr/TiO2和V-Cu/TiO2在处理氯苯、二氯甲烷时活性较差.对于 V-Mo/TiO2和V-Mn/TiO2催化剂,活性元素主要以混合氧化物的形式高度分散于催化剂表面,一定程度上抑制了 V2O5晶相的形成和 TiO2晶型的转变,催化剂比表面积损失较小.在V-Mo/TiO2双金属催化剂中,活性组分高度分散于催化剂表面,V与Mo之间的相互作用促进了钒氧化物的还原以及Brønsted酸的形成,催化剂表面较多的 L酸和Brønsted酸位点有利于氯苯的吸附和脱氯作用的进行,使得V-Mo/TiO2在处理氯苯时拥有较好的活性.而V-Mn/TiO2催化剂拥有良好的比表面积,Mn与V之间的强相互作用使得V2O5的还原温度向低温偏移,促进了催化剂表面活性氧的转移,为二氯甲烷的深度氧化提供了大量活性氧,增强了催化剂的氧化性能,进而提高了催化剂催化燃烧二氯甲烷的性能.

二氯甲烷浓度为5000mg/m3,反应温度350℃,空速为15000mL/(g· h)
含氯挥发性有机化合物的催化燃烧中,催化剂不仅要具有较高的催化活性和稳定性,还需对CO2和HCl有着较高的选择性.与氯苯相比,二氯甲烷在催化燃烧中容易产生 CH2O、CH3Cl、CHCl3等中间产物,易造成二次污染.为此,测试了V-Mn/TiO2、V-Mo/TiO2和V2O5/TiO2催化燃烧二氯甲烷时的产物分布情况,实验条件为 DCM浓度 5000mg/m3,空速 15000mL/(g·h),反应温度350℃,测试结果如图6所示.V2O5/TiO2处理二氯甲烷时活性较差,350℃时催化燃烧的产物为CO、CO2和CH3Cl,产生大量二次污染,几乎没有HCl的形成.V-Mn/TiO2催化燃烧二氯甲烷的主要产物为CO2,CH3Cl,CO和HCl的含量约为125和280mg/m3.V-Mn/TiO2催化剂表面存在大量的活性氧,能够将CO深度氧化为CO2,使得催化剂对CO2有着较好的选择性,但是其不能进一步脱去 CH3Cl上的氯元素,导致 HCl生成量较少.而V-Mo/TiO2催化剂表面存在较多的酸性位,有利于脱氯反应的进行,将氯元素以HCl的形式从催化剂表面转移出去,使得催化剂对HCl有着较好的选择性,350℃时HCl的生成量约为1500mg/m3,明显高于V-Mn/TiO2.
4 结论
4.1 V-Mn/TiO2和V-Mo/TiO2催化剂活性组分主要以混合氧化物的形式高度分散在催化剂表面,比表面积损失较少;Mo与V之间的相互作用使得催化剂表面形成一定量的 Brønsted酸性位点,有利于 CVOCs在催化剂表面的吸附和脱氯反应的进行,提高了V-Mo/TiO2催化燃烧氯苯的活性,且对HCl的选择性较好;V-Mn/TiO2催化剂存在大量的活性氧,氧化性能较强,在催化燃烧二氯甲烷时拥有最佳的活性,并且对CO2选择性高.
4.2 V2O5/TiO2催化剂中Cr、Cu的引入导致部分锐钛矿的TiO2向金红石型转变,活性元素主要以CrO3、V2O5等晶相存在,很大程度上减小了催化剂的比表面积和酸量,并且抑制了V氧化物种的还原,导致催化剂处理氯苯和二氯甲烷的活性下降.
[1]Davy C. Legislation with respect to dioxins in the workplace[J]. Environment International, 2004,30,(2):219-233.
[2]Quaß U, Fermann M, Bröker G. The European Dioxin Air Emission Inventory Project--Final Results [J]. Chemosphere, 2004,54(9):1319-1327.
[3]刘 鸿,成少安,张鉴清,等.无水条件下气相三氯乙烯的光催化降解研究 [J]. 中国环境科学, 1998,18(2):144-147.
[4]李 佳,傅平丰,张彭义,等.纳米 Au/TiO2薄膜真空紫外光催化降解甲醛 [J]. 中国环境科学, 2010,30(11):1441-1445.
[5]Zhang C, Hua W, Wang C, et al. The effect of A-site substitution by Sr, Mg and Ce on the catalytic performance of LaMnO3catalysts for the oxidation of vinyl chloride emission [J]. Applied Catalysis B: Environmental, 2013,(134/135):310-315.
[6]周 瑛,卢晗锋,陈银飞,等.LaBO3钙钛矿催化剂的 VOCs催化燃烧特性 [J]. 中国环境科学, 2012,32(10):1772-1777.
[7]Dai Q, Bai S, Wang J, et al. The effect of TiO2doping on catalytic performances of Ru/CeO2catalysts during catalytic combustion of chlorobenzene [J]. Applied Catalysis B: Environmental, 2013,(142/143):222-233.
[8]Maghsoodi S, Towfighi J, Khodadadi A, et al. The effects ofexcess manganese in nano-size lanthanum manganite perovskite on enhancement of trichloroethylene oxidation activity[J]. Chemical Engineering Journal, 2013,(215/216):827-837.
[9]Chen Q Y, Li N, Luo M F, et al. Catalytic oxidation of dichloromethane over Pt/CeO2-Al2O3catalysts [J]. Applied Catalysis B: Environmental, 2012,127:159-166.
[10]Graham J L, Almquist C B, Kumar S, et al. An investigation of nanostructured vanadia/titania catalysts for the oxidation of monochlorobenzene [J]. Catalysis Today, 2003,88(1/2):73-82.
[11]Bertinchamps F, Grégoire C, Gaigneaux E M. Systematic investigation of supported transition metal oxide based formulations for the catalytic oxidative elimination of (chloro)-aromatics [J]. Applied Catalysis B: Environmental, 2006,66:10-22.
[12]Hu R, Jin P, Luo M F, et al. Characterization of CrOx/Al2O3catalysts for dichloromethane oxidation [J]. Catalysis Today, 2011,175:598-602.
[13]Huang Q Q, Meng Z H, Zhou R X, et al. The effect of synergy between Cr2O3-CeO2and USY zeolite on the catalytic performance and durability of chromium and cerium modified USY catalysts for decomposition of chlorinated volatile organic compounds [J]. Applied Catalysis B: Environmental, 2012,(115/ 116):179-189.
[14]Yang P, Meng Z H, Zhou R X, et al. Enhanced catalytic activity and stability of Ce doping on Cr supported HZSM-5catalysts for deep oxidation of chlorinated volatile organic compounds [J]. Chemical Engineering Journal, 2013,234:203-210.
[15]Dai Y, Wang X Y, Dai Q, et al. Effect of Ce and La on the structure and activity of MnOx catalyst in catalytic combustion of chlorobenzene [J]. Applied CatalysisB:Environmental, 2012,(111/ 112):141-149.
[16]Gutierrez J, Rivas B, Martin S,et al. Structure of Mn-Zr mixed oxides catalysts and their catalytic performance in the gas-phase oxidation of chlorocarbons [J]. Chemosphere, 2007,68:1004-1012.
[17]黄学敏,曹 利,杨 全.MnxCe1-x/Al2O3催化剂的制备及其催化甲苯的燃烧性能 [J]. 环境工程学报, 2012,34(12):03-06.
[18]Casagrande L, Lietti L, Nova I, et al. SCR of NO by NH3over TiO2-supported V2O5-MoO3catalysts:reactivity and redox behavior [J]. Applied Catalysis B: Environmental, 1999,22(1):63-77.
[19]Huang Q Q, Xue X M, Zhou R X. Catalytic behavior and durability of CeO2or/and CuO modified USY zeolite catalysts for decomposition of chlorinated volatile organic compounds [J]. Journal of Molecular Catalysis A: Chemical, 2011,344(1/2): 74-82.
[20]秦 昆,刘善堂.钨对 Vox/TiO2催化燃烧氯苯的作用 [J]. 工业催化, 2012,20(6):0015-0019.
[21]许波连,范以宁,刘 浏,等.V2O5TiO2催化剂表面钒氧物种的分散状态和催化性能 [J]. 中国科学, 2002,3203(2):35-0242.
[22]Wang C, Yang S, Chang H, et al. Dispersion of tungsten oxide on SCR performance of V2O5-WO3/TiO2: Acidity, surface species and catalytic activity [J]. Chemical Engineering Journal, 2013, 225:520-527.
[23]Wu M, Dai Q G, Wang X Y. Catalytic combustion of chlorinated VOCs over VOx/TiO2catalysts [J]. Catalysis Communications, 2012,18:72-75.
[24]Wang X Y, Qian K, Dai Q G, et al. Catalytic combustion of chlorobenzene over MnOx-CeO2mixed oxide catalysts [J]. Applied Catalysis B: Environmental, 2009,86(3/4):166-175.
[25]Zhang D H, Li X J,Xu L Y, et al. Investigations into the C4olefin metathesis over Mo/Al2O3: effects of support nature and pretreatment conditions on the product distribution [J]. Applied Catalysis A: General, 2014,472:92-100.
[26]Pinard L, Mijoin J, Ayrault P, et al. On the mechanism of the catalytic destruction of dichloromethane over Pt zeolite catalysts [J]. Applied Catalysis B: Environmental, 2005,51(1):1-8.
[27]Albonetti B, Mengou J, Scirè S, et al. The role of acidity in the decomposition of 1,2-dichlorobenzene over TiO2-based V2O5/WO3catalysts [J]. Applied Catalysis A: General, 2008, 341(1/2):18-25.
[28]Dai Q G, Bai S X, Wang X Y, et al. Catalytic combustion of chlorobenzene over Ru-doped ceria catalysts [J]. Applied Catalysis B: Environmental, 2012,126:64-75.
[29]Maupin I, Pinard L, Mijoin J,et al. Bifunctional mechanism of dichloromethane oxidation over Pt/Al2O3: CH2Cl2disproportionation over alumina and oxidation over platinum [J]. Journal of Catalysis, 2012,291:104-109.
[30]Gannoun C, Delaigle R, Eloy P, et al. Sol-gel derived V2O5-TiO2mesoporous materials as catalysts for the total oxidation of chlorobenzene [J]. Catalysis Communications, 2011,15(1):1-5.
Catalytic combustion of chlorinated volatile organic compounds over V-M/TiO2(M=Cu、Cr、Ce、Mn、Mo) catalysts.
HUANG Hai-feng1, NING Xing-jie1, JIANG Xiao-jia1, GU Lei1, LU Han-feng2*(1.College of Biological and Environmental Engineering, Zhejiang University of Technology, Hangzhou 310014, China;2.Research Institute of Catalytic Reaction Engineering, College of Chemical Engineering and Materials Science, Zhejiang University of Technology, Hangzhou 310014, China). China Environmental Science, 2014,34(9):2179~2185
A series of V-M /TiO2(M= Cu、Cr、Ce、Mn、Mo)catalysts were prepared by impregnation method. The catalytic activity of chlorinated volatile organic compounds(CVOCs), such as chlorobenzene(CB)、dichloromethane(DCM) over V-M /TiO2were investigated. The physical-chemical properties of the catalysts were also investigated by XRD、BET、H2-TPR and NH3-TPD. It was found that the V-Mo/TiO2catalyst could completely combustion oxidation of chlorobenzene into CO2and HCl at 260℃, which was related to the biggest BET surface and highly dispersed of surface acidity; Moreover, the V-Mn/TiO2catalyst showed a high activity and good selectivity for catalytic combustion of dichloromethane (DCM), with a 100% conversion obtained at 380℃. This performance was attributed to a large amount of active surface oxygen, which could enhance the ability of deep oxidation of dichloromethane.
chlroinated organic compounds (CVOCs);V-M/TiO2bimetallic catalysts;catalytic combustion
X511
A
1000-6923(2014)09-2179-07
黄海凤(1954-),女,浙江诸暨人,教授,主要从事大气污染控制研究.发表论文50余篇.
2014-01-04
国家自然科学基金(21107096);浙江省重大科技专项(2013C03021)
* 责任作者, 教授, luhf@ziut.edu.cn

