离子对色谱-间接紫外检测法分析哌啶离子液体阳离子
王淼煜, 于 泓, 李 萍, 李 杰, 高玉凤
(哈尔滨师范大学化学化工学院,黑龙江 哈尔滨150025)
离子液体(ionic liquid)是一种在室温或近于室 温的情况下以离子为主体的熔融盐体系[1,2]。现在主要研究的离子液体是由含氮有机杂环阳离子(咪唑离子或吡啶离子等)和无机或有机阴离子构成的新型离子液体[3-5]。离子液体具有许多突出的特点,这使其在催化、有机合成、电化学等领域[6-9]的应用研究越来越受到人们的重视。因此离子液体的分离检测显得尤为重要。现有的分离分析方法主要有反相高效液相色谱法[10-13]、离子色谱法[14-16]、离子对色谱法[17-19]、亲水相互作用液相色谱法[20]等,其中所检测的离子液体大部分是具有紫外吸收的咪唑类和吡啶类离子液体阳离子[21,22]。而无紫外吸收的离子液体,如哌啶离子液体,其分离检测方法的报道很少。
本实验发展了无紫外光吸收的哌啶离子液体阳离子的整体柱离子对色谱-间接紫外检测法。研究了影响其保留的因素和保留规律,建立了离子对色谱-间接紫外检测法分离测定哌啶离子液体阳离子的方法,并应用于实验室合成的离子液体的分析。
1 实验部分
1.1 仪器与试剂
1200高效液相色谱仪(美国Agilent公司),配备G1311A型四元泵、Degasser-G1322A型在线脱气机、G1329A标准型自动进样器、G1316A型柱温箱、Revision B.04.01色谱工作站和G1315B DAD检测器;PHSF-3F型pH计(上海精密科学仪器有限公司);Simplicity纯水系统(美国 Millipore公司);0.22μm 滤 膜;DOA-P504-BN 型 无 油 真 空 泵(IDEX 公司)。
离子液体:溴化 N-甲基-N-乙基哌啶([MEPi]Br)(纯度99%);溴化 N-甲基-N-丙基哌啶([MPPi]Br)(纯度 99%);溴 化 N-甲基-N-丁基 哌 啶([MBPi]Br)(纯度99%)(上海成捷化学有限公司)。对氨基苯酚盐酸盐、5-磺基水杨酸、烟酰胺和邻苯二甲酸氢钾(分析纯,北京百灵威科技有限公司)。乙酸、氢氧化钠(分析纯,上海试剂一厂)。甲醇、乙腈(色谱纯,Dikma Technologies公司)。庚烷磺酸钠、戊烷磺酸钠(色谱纯,天津市光复精细化工研究所)。配制溶液均采用电阻率18.2 MΩ·cm的超纯水。
1.2 溶液配制
1.2.1 流动相的配制和处理
用超纯水配制一定浓度的对氨基苯酚盐酸盐-庚烷磺酸钠水溶液。实验所用对氨基苯酚盐酸盐-庚烷磺酸钠水溶液、甲醇、乙腈和去离子水经0.22 μm滤膜过滤后使用。
1.2.2 标准溶液的配制
用超纯水分别配制3种哌啶离子液体质量浓度为1 000 mg/L的标准储备液,取3种离子液体的标准储备液各5 mL定容于同一100 mL容量瓶中,配制成质量浓度为50 mg/L的混合标准溶液,置于样品瓶中备用。
1.3 色谱分析
色谱柱:Chromolith Speed ROD RP-18e(100 mm×4.6 mm,德国 Merck公司);流动相:0.5 mmol/L对氨基苯酚盐酸盐-0.1 mmol/L庚烷磺酸钠水溶液/甲醇(80∶20,v/v);间接紫外检测波长:210 nm;流速:1.0 mL/min;柱温:30℃;进样体积:20μL。
2 结果与讨论
2.1 色谱条件的优化
2.1.1 背景紫外吸收试剂的选择
由于哌啶离子液体阳离子无紫外吸收,因此在进行间接紫外检测时,流动相需要添加紫外吸收试剂。常用的紫外吸收试剂有对氨基苯酚盐酸盐、磺基水杨酸、邻苯二甲酸氢钾和烟酰胺等。实验考察了这4种紫外吸收试剂在各自最大吸收波长对哌啶类离子液体阳离子的检验。分别以0.5 mmol/L背景紫外吸收试剂水溶液(用乙酸或氢氧化钠调节pH 4.5)/甲醇(80∶20,v/v)为流动相,在其相应最大吸收波长处测定3种哌啶离子液体阳离子(MEPi、MPPi、MBPi),结果均无色谱峰出现。
考虑到在流动相中加入适当的离子对试剂对测定有一定的影响,实验又在流动相中加入离子对试剂进行考察。当以0.5 mmol/L背景紫外吸收试剂-0.1 mmol/L庚烷磺酸钠水溶液(pH4.5)/甲醇(80∶20,v/v)为流动相时,在各自最大吸收波长下进行测定,结果发现仅在对氨基苯酚盐酸盐-庚烷磺酸钠水溶液为流动相时,哌啶类离子液体阳离子有色谱峰出现,且色谱峰形较好。因此选定对氨基苯酚盐酸盐为背景紫外吸收试剂。
2.1.2 检测波长的选择
对氨基苯酚盐酸盐的最大吸收波长约为240 nm。实验分别测试波长(200、210、220、230、240、250 nm)的变化对测定的影响。结果发现,在210 nm时基线噪声值最小,峰形最好。故选择210 nm。
2.1.3 离子对试剂对哌啶阳离子保留的影响
较为常见的离子对试剂有庚烷磺酸钠和戊烷磺酸钠。实验分别以0.5 mmol/L对氨基苯酚盐酸盐-0.1 mmol/L戊烷磺酸钠水溶液/甲醇(80∶20,v/v)和 0.5 mmol/L 对 氨 基 苯 酚 盐 酸 盐-0.1 mmol/L庚烷磺酸钠水溶液/甲醇(80∶20,v/v)为流动相分离3种哌啶阳离子(见图1)。当使用戊烷磺酸钠为离子对试剂时,看不到3种哌啶阳离子的色谱峰。
在选定离子对试剂为庚烷磺酸钠后,又考察了庚烷 磺 酸 钠 浓 度 从 0.05 mmol/L 增 大 至 0.3 mmol/L时对分离测定哌啶阳离子的影响,结果见图2。可以看出,随着庚烷磺酸钠浓度的增大,3种哌啶阳离子的保留时间逐渐延长,这符合离子对色谱的保留规律。在浓度为0.05 mmol/L时,虽然保留时间较短,但是MEPi的色谱峰与系统峰有部分重叠。因此选择庚烷磺酸钠的浓度为0.1 mmol/L,此时哌啶阳离子的保留时间较短、峰形较好。
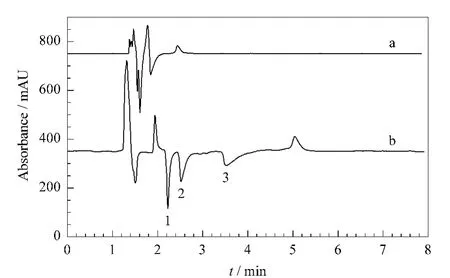
图1 分别使用离子对试剂(a)戊烷磺酸钠和(b)庚烷磺酸钠得到的色谱图Fig.1 Chromatograms obtained using ion-pair reagents of(a)1-pentanesulfonic acid sodium and(b)1-heptanesulfonic acid sodium
2.1.4 对氨基苯酚盐酸盐浓度对哌啶阳离子保留的影响
以对氨基苯酚盐酸盐-0.1 mmol/L庚烷磺酸钠水溶液/甲醇(80∶20,v/v)为流动相,考察了对氨基苯酚盐酸盐浓度分别为0.3、0.5、0.7、1.0 mmol/L时,对分离测定3种哌啶阳离子的影响,结果见表1。可以看出,随着对氨基苯酚盐酸盐浓度的增大,保留时间略有缩短,检出限增大。引起检出限增大的主要原因是:对氨基苯酚盐酸盐作为背景紫外吸收试剂,当其浓度增加时,背景吸收增加,导致基线噪声值增大。由于在对氨基苯酚盐酸盐浓度为0.3 mmol/L时,系统峰干扰 MBPi的测定,因此选择对氨基苯酚盐酸盐的浓度为0.5 mmol/L。

图2 用0.05~0.3 mmol/L庚烷磺酸钠作为流动相得到的色谱图Fig.2 Chromatograms obtained using0.05-0.3 mmol/L 1-heptanesulfonic acid sodium as mobile phases Other chromatographic conditions and peak marks as in Fig.1.

表1 流动相中对氨基苯酚盐酸盐浓度与保留时间、检出限的关系Table 1 Relationships between the mobile phases containing different concentrations of 4-aminophenol hydrochloride and retention times and detection limits of piperidinium cations
2.1.5 流动相水溶液pH值对哌啶阳离子保留的影响
以0.5 mmol/L对氨基苯酚盐酸盐-0.1 mmol/L庚烷磺酸钠水溶液/甲醇(80∶20,v/v)为流动相,考察流动相水溶液pH值(乙酸或氢氧化钠调节)分别为3、3.5、4.0、4.5(此流动相未调pH 时的自身值)和5.0时对分离测定3种哌啶阳离子的影响。结果表明,随着流动相水溶液的pH值增大,基线噪声值降低,保留时间在pH3到4.5时逐渐延长,在pH为5时缩短,但总体变化不大。因此,选择流动相水溶液pH值为4.5,即流动相不需调节pH值。
2.1.6 有机溶剂对哌啶阳离子保留的影响
甲醇和乙腈是反相液相色谱流动相中常用的有机溶剂,实验分别以0.5 mmol/L对氨基苯酚盐酸盐-0.1 mmol/L庚烷磺酸钠水溶液/甲醇(80∶20,v/v)和0.5 mmol/L对氨基苯酚盐酸盐-0.1 mmol/L庚烷磺酸钠水溶液/乙腈(80∶20,v/v)为流动相分离测定3种哌啶阳离子,色谱图见图3。可以看出,当选用乙腈作为有机溶剂时,看不到3种哌啶阳离子的色谱峰。可能原因是乙腈对哌啶阳离子的洗脱能力强,使哌啶阳离子的保留时间明显缩短,与系统峰重合,辨别不出。因此选择甲醇为流动相的有机组分。
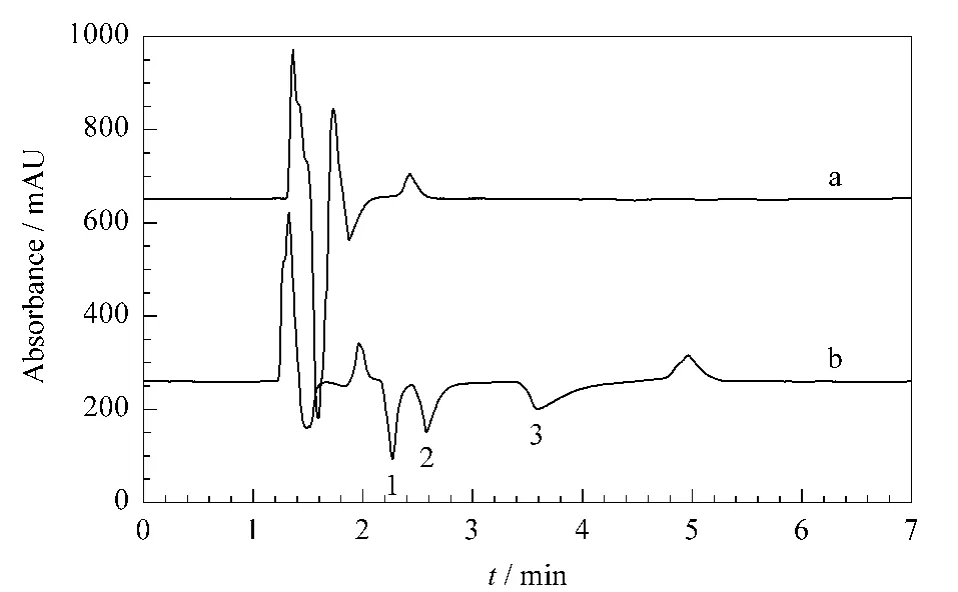
图3 分别使用含有有机溶剂(a)乙腈和(b)甲醇的流动相获得的色谱图Fig.3 Chromatograms obtained with mobile phases containing organic solvents of (a)acetonitrile and(b)methanol
选定甲醇作为有机溶剂后,以0.5 mmol/L对氨基苯酚盐酸盐-0.1 mmol/L庚烷磺酸钠水溶液/甲醇为流动相,考察流动相中甲醇体积分数变化(10%、15%、20%、25%)对哌啶阳离子分离测定的影响。结果表明,在甲醇体积分数为15%和20%时,3种哌啶阳离子的检出限最低,并且仅当甲醇体积分数为20%时,MEPi的色谱峰与系统峰分开,峰形最好。因此选择甲醇体积分数为20%。
在液相色谱中,分析物的保留因子与流动相中有机溶剂(乙腈或甲醇)含量之间有如下关系:lg k=cφ(MeOH)+d[9]。式中k 是分析物的保留因子,φ(MeOH)是流动相中甲醇的体积分数。将3种哌啶阳离子保留因子的对数值lg k与流动相中甲醇的体积分数值φ(MeOH)作图,所得曲线的线性回归数据见表2。由表2可知,lg k与φ(MeOH)之间呈现良好的线性关系,表明这3种哌啶阳离子的保留符合反相液相色谱模式。
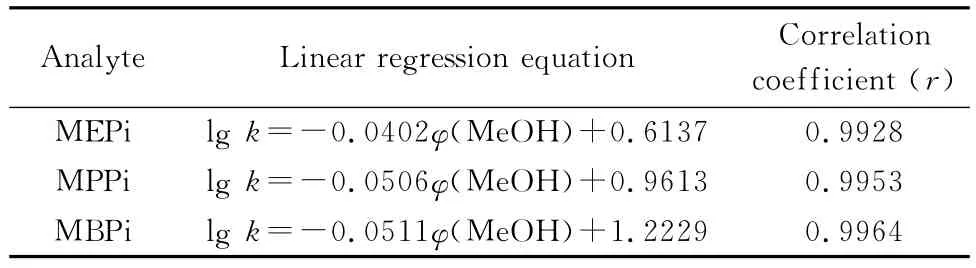
表2 哌啶阳离子的lg k与流动相中甲醇体积分数φ(MeOH)之间关系曲线的线性回归方程Table 2 Linear equations for the lg k vsφ(MeOH)obtained with the retention of piperidinium cations
2.1.7 流速对测定哌啶阳离子的影响
以0.5 mmol/L对氨基苯酚盐酸盐-0.1 mmol/L庚烷磺酸钠水溶液/甲醇(80∶20,v/v)为流动相,考察流速为1.0、2.0、3.0 mL/min时对3种哌啶阳离子保留时间、柱效和柱压的影响,结果见表3。结果表明,随着流速的增加,哌啶阳离子的保留时间缩短,柱压逐渐增大。由于在流速1.0 mL/min时,3种哌啶阳离子的保留时间已经比较短(最长的不到3.6 min),虽然提高流速会使保留时间进一步缩短,但亦使MEPi的色谱峰与系统峰靠得太近,产生干扰,而且当流速为3.0 mL/min时,柱压将接近色谱柱的极限压力20 MPa,所以本实验的适宜流速是1.0 mL/min。如只测定 MBPi组分,可以提高流速。

表3 流速对柱压、离子保留时间和柱效的影响Table 3 Effect of flow rate on column back-pressure,retention time of ions and column efficiency
2.1.8 色谱柱温度对哌啶阳离子保留的影响
流速为1.0 mL/min,以0.5 mmol/L对氨基苯酚盐酸盐-0.1 mmol/L庚烷磺酸钠水溶液/甲醇(80∶20,v/v)为流动相,考察柱温为20、25、30、35、40℃时对哌啶离子保留时间的影响。结果可知,随着柱温的逐渐升高,3种哌啶阳离子的保留时间均缩短;MEPi的保留时间从2.364 min逐渐缩短至2.134 min,MPPi的保留时间从2.707 min缩短至2.388 min,MBPi的保留时间从3.836 min缩短至3.224 min,总体影响不大。因此,实验选取接近室温的30℃为适宜的温度。
2.2 定量分析参数
通过以上实验,选择最佳色谱条件为:用Chromolith Speed ROD RP-18e反相硅胶整体柱,以0.5 mmol/L对氨基苯酚盐酸盐-0.1 mmol/L庚烷磺酸钠水溶液/甲醇(80∶20,v/v)为流动相,间接紫外检测波长210 nm,流速1.0 mL/min,柱温30℃。在此条件下,对3种哌啶阳离子系列标准溶液进行测定,色谱图见图1b。
采用峰面积定量,以峰面积(积分值)对离子质量浓度(mg/L)求得线性回归方程,以3倍信噪比计算检出限(噪声为0.310 6 mAU),连续5次重复测定 MEPi(30.81 mg/L)、MPPi(32.02 mg/L)和MBPi(33.09 mg/L)混合标准溶液,计算相对标准偏差(RSD),得到检出限、线性关系和重现性数据,结果见表4。
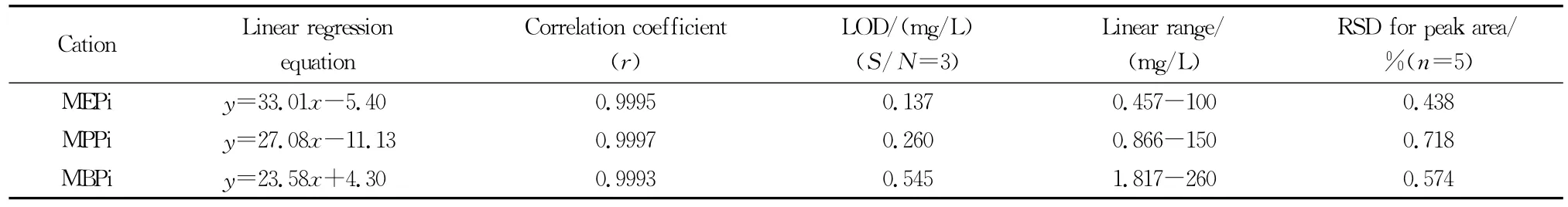
表4 3种哌啶阳离子的线性回归方程、检出限及精密度Table 4 Linear regression equations,limits of detection(LOD)and relative standard deviations(RSDs)of the three piperidinium cations
2.3 样品分析
采用本方法测定了3种化学实验室合成的离子液体溴化N-甲基-N-乙基哌啶、溴化N-甲基-N-丙基哌啶和溴化 N-甲基-N-丁基哌啶中的阳离子。分别准确称取0.101 1 g溴化 N-甲基-N-乙基哌啶、0.100 7 g溴化 N-甲基-N-丙基哌啶和0.101 4 g溴化N-甲基-N-丁基哌啶离子液体,配成100 mL溶液。分别取2.5 mL溴化N-甲基-N-乙基哌啶、2.5 mL溴化 N-甲基-N-丙基哌啶和2.5 mL溴化N-甲基-N-丁基哌啶浓溶液稀释至50 mL。稀释液经0.22μm滤膜过滤后进行色谱分析,色谱图见图4。采用标准加入法检验了方法的回收率,样品分析结果及回收率数据见表5。表中数据为5次测定平均值,其相对标准偏差小于0.5%。
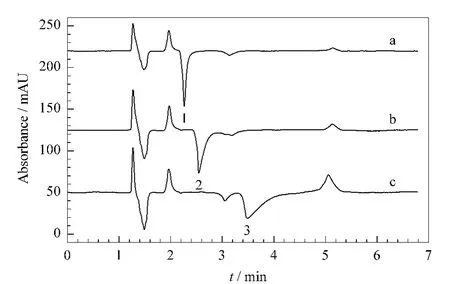
图4 离子液体样品的色谱图Fig.4 Chromatograms of ionic liquid samples
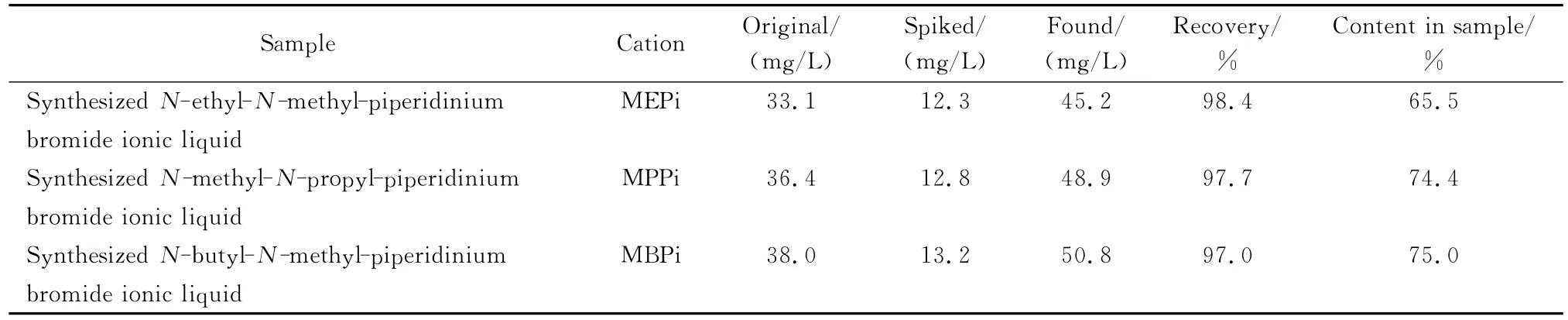
表5 样品分析结果及加标回收率(n=5)Table 5 Analytical results and spiked recoveries of piperidinium cations in samples(n=5)
3 结论
本工作建立了以对氨基苯酚盐酸盐为背景紫外吸收试剂的整体柱离子对色谱-间接紫外检测快速分析无紫外光吸收的哌啶类离子液体阳离子的方法。采用反相硅胶整体柱,以对氨基苯酚盐酸盐-庚烷磺酸钠水溶液/甲醇为流动相,N-甲基-N-乙基哌啶阳离子、N-甲基-N-丙基哌啶阳离子和 N-甲基-N-丁基哌啶阳离子在4 min之内达到基线分离;3种哌啶阳离子的检出限均低于0.1 mg/L。将该方法应用于化学实验室合成的哌啶离子液体的分析,结果准确、可靠。本方法简便、快速,重现性、线性关系等均能满足哌啶类离子液体阳离子的定量分析要求。
[1] Studzińska S,Molíková M,Kosobucki P,et al.Chromatographia,2011,73(Suppl 1):S35
[2] Sun X J,Xu J K,Zhao X J,et al.Chromatographia,2013,76(15/16):1013
[3] Orentiene A,Olsauskaite V,Vickackaite V,et al.Chromatographia,2011,73(1/2):17
[4] Ru S P,Wu J,Ying Y B,et al.Chinese Journal of Analytical Chemistry(茹柿平,吴坚,应义斌,等.分析化学),2012,40(6):835
[5] Qiu H D,Hu Y Y,Liu X,et al.Chinese Journal of Chromatography(邱洪灯,胡云雁,刘霞,等.色谱),2007,25(3):293
[6] Qi L,Zhang J,Zhang Z Q.Chinese Journal of Chromatography(亓亮,张婧,张志琪.色谱),2013,31(3):249
[7] Paszkiewicz M,Stepnowski P.Curr Org Chem,2011,15(12):1873
[8] Wang P,Guo X F,Jia L H,et al.Chinese Journal of Applied Chemistry(王平,郭祥峰,贾丽华,等.应用化学),2013,30(7):840
[9] Zhang S J,Liu X M,Yao X Q,et al.Scientia Sinica Chimica(张锁江,刘晓敏,姚晓倩,等.中国科学:化学),2009,39(10):1134
[10] Han B,Zhang L H,Liang Z,et al.Scientia Sinica Chimica(韩彬,张丽华,梁振,等.中国科学:化学),2010,40(10):1487
[11] Gao W,Yu H,Zhou S.Chinese Journal of Chromatography(高微,于泓,周爽.色谱),2010,28(1):14
[12] Stojanovic A,Lammerhofer M,Kogelnig D,et al.J Chromatogr A,2008,1209(1/2):179
[13] Ruiz-Angel M J,Berthod A.J Chromatogr A,2008,1189(1/2):476
[14] Meng L M,Yu H,Liu Y Z.Chromatographia,2011,73(3/4):367
[15] Meng L M,Yu H,Huang X,et al.Chinese Journal of Analytical Chemistry(孟令敏,于泓,黄旭,等.分析化学),2012,40(3):409
[16] Lamouroux C,Foglia G,Le Rouzo G.J Chromatogr A,2011,1218(20):3022
[17] Elkady E F,Mahrouse M A.Chromatographia,2011,73(3/4):297
[18] Mansour F R,Kirkpatrich C L,Danielson N D.Chromatographia,2013,76(11/12):603
[19] Buszewski B.Anal Bioanal Chem,2012,403(5):1199
[20] Huang X,Yu H,Dong Y J.Chinese Chem Lett,2012,23(7):843
[21] Gao W,Yu H.Anal Lett,2011,44(5):922
[22] Chen Q,Yu H,Meng L M,et al.Journal of Instrumental Analysis(陈倩,于泓,孟令敏,等.分析测试学报),2011,30(1):38

