若尔盖高原湿地地表水与大气湿沉降中有机氯农药和多氯联苯研究
盖 楠,潘 静*,陈大舟 ,杨永亮 (.国家地质实验测试中心,北京 00037;.中国计量科学研究院化学计量与分析科学研究所,北京 000)
某些持久性有机污染物具有半挥发性,因而可通过大气运移到世界各地,除了在运移过程中完全降解的部分以外,最终通过土-气交换或大气干、湿沉降进入地表,对生态环境和人类健康构成威胁.有机氯农药和多氯联苯是两大类对人类内分泌系统有危害的持久性有机污染物.残留在地表中的有机氯农药和多氯联苯可通过蒸发进入大气,通过大气远程迁移至边远地区和极地.在我国西部以畜牧业为主要人类活动的少数民族地区的大气、土壤、水体也观测到了这些物质,例如喜马拉雅山、青藏高原湖泊[1-7]、卧龙自然保护区等[8-10].水是牧草和牦牛必不可少的生命资源,也是对食物链中污染物富集规律研究中重要的参考背景介质.在高原牧场,水的唯一来源是大气降水.
研究表明,高原地区的降水(通常是雪)中POPs随海拔的增加产生富集现象[11].这种现象已被世界一些高山地区的观测所证实,如我国卧龙自然保护区、南岭、长白山、欧洲阿尔卑斯山、比利牛斯山、南美安第斯山、喜马拉雅山、北美落基山等[11-15].Tremolada[16]和 Wania等[17]的研究进一步表明,这些 POPs富集的地区均为湿润的高山地区.根据Wania 等[17]的高山冷凝效应理论,携带污染物的气流沿高山斜坡攀升,气温的逐步降低使其通过降雨和降雪进入高海拔地区,呈现 POPs的浓度与海拔高度正相关的现象.研究结论虽然较好地解释了具有较陡的海拔梯度高山的冷凝效应,却并不适用于主要来自高空的气流输入以及地势较为平坦的高原草甸地区.高原草甸地区海拔高度大多在3500m左右,受季风影响显著,降雪季节较长,其冷凝捕集作用与热带雨林高山的情况不同,是研究大气 POPs长距离传输与气候之间的关系的理想场所.
近年来,国内外学者对我国青藏高原地区POPs的地球化学行为也做了相应的研究[18],但是对若尔盖湿地,即西部高原过渡地区 POPs的研究甚少.该地区的地形变化呈阶梯状,跨度达数百至上千公里.本文选取若尔盖高原湿地及草甸牧场为研究区,以有机氯农药和多氯联苯残留量为研究对象,采集分析了地表水、雨水和雪样品,探讨大气湿沉降中OCPs和PCBs同系物残留状况及在冬、夏两季的分布特征以及大气沉降通量,以了解我国西部背景地区PCBs和OCPs的大气沉降通量和季节变化规律,探讨 POPs的区域地球化学行为,为研究 POPs的大气远程迁移和大气与地表之间的交换提供依据.
1 样品采集与实验方法
1.1 研究区概况
若尔盖高原地区西临巴颜喀拉山,东抵岷山,北起西倾山,南至邛崃山,是第四纪强烈隆起中一个相对沉降区,海拔高度在3200~3600m之间.若尔盖高原湿地地形十分独特,其特殊性在于与我国其他低海拔地区相比,它是典型的高原地区;而与周围将其环抱的群山相比,它又是一个盆地.独特的地理位置使其拥有特殊的自然环境.该地区气候寒冷,年平均气温约 2℃,年降水量约 600mm,且多为牧区,几乎没有农产品、蔬菜、园林等的发展.
1.2 样品采集
1.2.1 地表水样品 4组地表水分别为 2组黑河水样和 2组景区水样(花湖、黄河九曲第一湾)(图 1);每组 2L采集于聚乙烯塑料瓶中,加入13C标记内标,在室内经 C18固相萃取滤膜(Supelco, USA)萃取富集.回实验室于冰箱中4℃冷藏保存.
1.2.2 大气湿沉降样品 大气湿沉降样品采样地点设置于若尔盖县城湿地保护局内.采用自行设计的接收装置,接收面积为0.25m2.采样装置在样品采集前都用纯净水清洗 3遍,风干后再用丙酮清洗1~2遍.降雨或降雪样品收集完后,先转入清洗过的塑料量筒确定体积,之后转入干净的聚四氟乙烯瓶中冷藏,回实验室后立即分析.2011年7月、11月和2012年5月都采集到干湿沉降样品,由于采样时间有限,采集到的体积和数量有很大差异,尤其是 7月夏季时只采集到一个降雨样品.所有大气沉降样品均收集于若尔盖县城内,采集基本信息列于表1.
1.3 标准样品和主要试剂
分析 OCPs和 PCBs所用的有机试剂正己烷、丙酮、乙醚、二氯甲烷、乙酸乙酯均为HPLC级,购于美国 Fisher公司;弗罗里硅土,60~100目,CNW公司.
15种 OCPs标准样品(α-HCH、β-HCH、γ-HCH、HCB、p,p’-DDE、p,p’-DDD、o,p’-DDT、p, p’-DDT、七氯、环氧七氯、艾氏剂、狄氏剂、α-硫丹、β-硫丹、甲氧 D DT)、7种 P CBs标准品(PCB28、PCB52、PCB101、PCB118、PCB138、PCB153、PCB180)、TCMX)和PCB209购自百灵威公司.

图1 若尔盖采样点分布Fig.1 Sampling locations in Zoige alpine wetland

表1 若尔盖湿地大气干湿沉降沉样品采集Table 1 Description of atmospheric deposition samples in Zoige alpine wetland
层析用Florisil,在600℃下活化4h,置于干燥器中冷却后加入 2%的去离子水,震荡 10min,平衡2h,备用.无水硫酸钠(分析纯),于450℃马弗炉中焙烧6h,置于干燥器中冷却备用.
1.4 样品的前处理
将地表水湿沉降样品(雨水和融化后的雪水)置于分液漏斗中,加入 NaCl饱和溶液.用 10mL丙酮分 3次润洗样品瓶的内壁,并将丙酮洗液倒入分液漏斗中,加入 50mL正己烷,振摇 5min,静置 10~30min.将正己烷层转入 250mL 平底烧瓶中,再向水相中加入25mL正己烷进行第2次,第3次萃取,步骤同上,合并3次有机相.在35℃恒温水浴上旋转蒸发浓缩至 2~5mL,过无水硫酸钠-Florisil层析柱,接收到 KD瓶中,旋转蒸发浓缩至 2mL左右后,氮气浓缩并用正己烷定容至0.5mL.转移至样品瓶准备上机进行 HRGCHRMS测定分析.
1.5 HRGC-HRMS分析
仪器:Thermo Finnigan Trace GC 2000气相色谱仪和Thermo Finnigan MAT 900XL型高分辨质谱仪,均为美国热电公司产品,自动进样器AS2000.色谱柱为DB-1(30m×0.25mm×0.25 μm);载气为高纯氦气,流速 0.8mL/min;进样口温度:230℃,传输线:250℃;分流比为 10:1,进样量1μL.程序升温:初始温度 70℃,保持 1min,以 30℃/min升温至160℃,再以2.5℃/min升温至200℃,最后以5℃/min升温至250℃,保持15min.
1.6 质量保证与质量控制
质量保证与质量控制 (QA/QC)包括基质加标、基质加标平行样、样品重复分析以及流程空白分析.如果信噪比 S/N>3并且目标物/定性离子比值在标准值的 15%以内,则利用色谱峰的保留时间与标准物进行比较而被定性.任何回收率低于 40%的样品都被排除在本文讨论之外.氯代化合物的定量使用外标法和定量标准进行.
2 结果与讨论
2.1 若尔盖地区地表水中POPs的分布
由图2和表2可见,所有地表水样品中均检出 HCHs、HCB 和 DDE(下面讨论中,如无说明,DDE和DDD分别为p,p’-DDE和p,p’-DDD),但只在黄河水中检出所有 DDTs异构体,而花湖和黑河水中未检出 DDT.若尔盖地区地表水中HCHs、DDTs、HCBs、PCBs平均浓度分别为0.90,1.36, 0.95,1.35ng/L.与土壤中的情况相似(土壤数据另文发表),α-HCHs、β-HCH、γ-HCH、HCB、DDE的检出率最高(100%),其中 HCB和DDE 是 OCPs的主要成分.DDD、p,p’-DDT、o,p’-DDT 的检出率最低,硫丹未检出.由于该地区没有使用有机氯农药,因此所有化合物均为大气远程输送而来.地表水的平均α-HCH/γ-HCH比值为0.6,大气降水的平均比值为1.2,表明大气气团来自可能正在使用林丹的地区[19].总体来说,黄河第一湾河水水中 POPs含量最高,表现为黄河第一湾河水>黑河河水>花湖湖水.
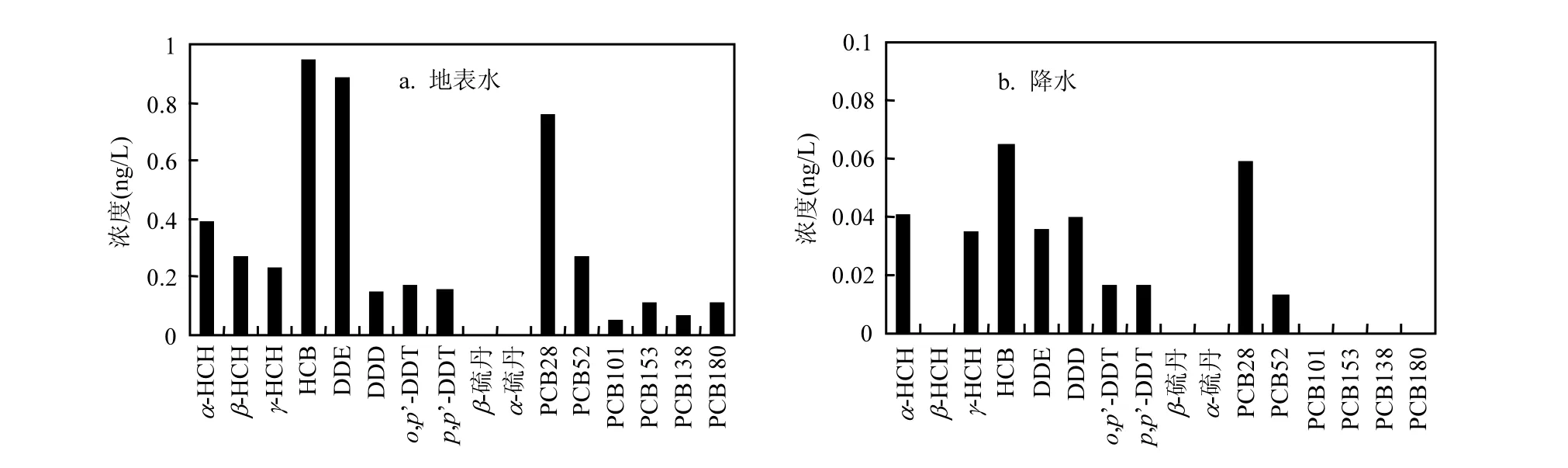
图2 若尔盖地区地表水和降水中POPs的平均浓度Fig.2 Averaged POP concentrations in surface waters and melt snow samples in Zoige alpine wetland

表2 若尔盖草原牧场地表水与降水中有机氯农药和多氯联苯含量水平(ng/L)Table 2 Concentrations of isomers of HCHs, DDTs, and PCBs in surface water and wet deposition in Zoige alpine wetland (ng/L)
若尔盖地区海拔高度大多在 3500m 左右,常年风向比较稳定.该地区年降水量约 600mm,年平均蒸发量 1232mm.蒸发量大于降水量.其高山冷凝作用与热带雨林高山的情况不同.若尔盖冬季受西风带环流影响,降水更加稀少.因此降水对于污染物在该地区的分配影响相对较小,而受大气环流和大气干沉降等因素影响的可能性更大.本文根据POPs大气沉降可能受到的影响,将高海拔地区分为“海拔梯度降水型”和“高原型”2类(表3)并与极地地区(“极地型”)进行比较[20-26]:与国内外其它高原/高山湖泊相比,若尔盖地区地表水样品中HCHs与西藏错鄂湖和羊卓雍湖、欧洲阿尔卑斯山、南美安第斯山湖泊处于同一水平,但显著高于喜马拉雅山尼泊尔侧的地表水和欧洲比利牛斯山脉Redon湖和Tatra山脉Ladove湖水.“海拔梯度降水型”高山海拔一般在2500m以下,具有在几十km至100km尺度内海拔高度显著上升以及气温也随之显著降低的特征,如我国南岭、长白山、欧洲阿尔卑斯山、哥斯达黎加热带雨林[17],而“高原型”的高原海拔一般在3500m以上,具有在数百km内海拔高度增加以及气温降低都不显著的特征,如我国喜马拉雅山和青海湖.“海拔梯度降水型”地区大气中挥发性较低的异构体(如PCB180和 PCB153)随海拔高度升高而富集,这种现象在我国长白山和南岭表层土壤中 PCBs异构体分布得到证实[12-13].而“高原型”地区挥发性较低的异构体随海拔高度升高则降低,而挥发性较高的(如PCB28、52、HCB)则相对富集[17].

表3 国内外高原湖泊地表水中POPs化合物的浓度比较Table 3 Comparison of concentrations of POPs in surface waters of high mountain/land lakes
2.2 降水中的POPs浓度的季节变化
由表2可见,若尔盖地区降雪中POPs的浓度远远低于其在地表水中的浓度.OCPs和PCBs湿沉降含量的最大值出现在 11月初冬的降雪样品中,分别达 0.363,0.118ng/L.该季节大气中的 OCPs和PCBs也为全年最高值(大气数据另文发表).与世界其他高海拔地区的比较(表 4),若尔盖地区降雪中HCHs浓度(0.011~0.19ng/L)要高于南极地区,但低于加拿大北极地区;DDTs浓度与欧洲高山地区基本相当,但低于珠穆朗玛峰东绒布新降雪和加拿大北极;PCBs浓度高于欧洲高山,但低于加拿大落基山、南美安第斯山、北极和南极地区.
主要有机氯农药在降水中检出率都达到100%,但是硫丹的检出率很低,且有 2个降水样品未检出 β-HCH.PCBs则仍是以低氯代化合物为主.半挥发性持久性有机污染物能否在高海拔地点被检出,除了与其物理化学性质,即其是否具有大气远程迁移潜势有关以外, 还与距污染源的距离以及风向、降水以及气温海拔梯度等因素有关.“海拔梯度降水型”地区大气湿沉降中挥发性较低的异构体(如 PCB138、PCB153、PCB180)随海拔高度升高而富集,是由于具备了降水以及气温海拔梯度的有利条件,如卧龙自然保护区、南岭、长白山,温度随海拔高度逐步降低,且后两者还有海洋气团的输入.而“高原型”地区远离海洋,海拔梯度变化平缓,气温变化不明显,因而有利于大气湿沉降中挥发性较高的异构 体(如PCB28和PCB52)的传输.

表4 若尔盖地区降水中POPs化合物的浓度及与世界其他高山及偏远地区比较(ng/L)Table 4 Concentrations of POPs in wet deposition samples in Zoige and other high mountain and remote areas in the world (ng/L)
2.3 沉降通量的季节变化

图3 若尔盖县城不同季节POPs大气湿沉降通量Fig.3 Wet deposition fluxes in different seasons in Zoige area
由于若尔盖地区海拔高且较为偏远,交通极不便利,因此,沉降样品只在采样期间进行了采集和观测.为了便于比较,将若尔盖湿地保护局提供的每月降水量的气象资料与所测数据结合,得到若尔盖地区夏、冬、春3个季节主要有机氯农药和多氯联苯的沉降通量值.由图3可见,若尔盖地区冬季大气沉降中 OCPs的含量明显高于其他季节.这与大气颗粒物和气态样品所检测到的数据一致(数据另文发表),也表明在季风的影响下,大气中POPs浓度的增高直接导致了降雪中浓度的提升.冬季采集的第 1d的降雪样品中出现了 γ-HCH/α-HCH >1 的情况,可能是由于受到大气传输的影响,林丹使用较频繁地区的大气经过迁移到达若尔盖地区.可见,湿沉降对 HCH在大气与地表之间的交换起着非常重要的作用.
2.4 清扫比
本研究的观测表明,若尔盖地区降雪中的POPs浓度远远高于降雨中的浓度.并且PCB101只在降雪中出现.Lei等[32]推断雪对有机化合物的清除比比雨对有机化合物的清除比要高,其主要原因是从气相到固相分配比具有强的温度依赖性.对于易溶于水的小分子极性化合物来说,雨的清除效率比雪的高.随着分子量的增大和极性的降低,雪表面能更有效调节有机蒸气和液态小雨滴,且在降雪中 PCBs以颗粒态为主导,而在降雨中颗粒态的百分比则有明显降低[32].
一个化合物是否可被降水有效地从大气中清扫出去可根据该化合物的清扫(WT)来判断.该比值被定义为

式中:CR,T为雨(雪)水中的某化合物的总浓度(溶解态+颗粒态)(pg/m3water),CA,T为在空气中的总浓度(气态+颗粒吸附态)(pg/m3空气).
由表 5可见,清扫比较大的化合物为 DDTs类化合物,其次为β-HCH,这是由于β-HCH具有较高的水溶解度.再其次为 γ-HCH、α-HCH、PCB52、28.由于若尔盖地区降雪中未发现PCB153、PCB138、PCB180,即这些化合物在未到达若尔盖地区之前就已沉降到迁移途中,因而在若尔盖地区未得到PCB153、138、180的清扫比数据.Lei等[30]提出,如果一个化合物的总清除比logWT在3.5~5.5范围内,将会产生湿沉降率随温度的变化.该模拟预测PCB180和PCB153会优先富集在高山高处,而较轻的PCBs和HCB则会随着大气环流远程迁移.这与我国卧龙、南岭、长白山以及阿尔卑斯山所观察到的结果一致[11-14].Wania等[17]比较了高山与极地冷凝捕集效应的区别,即在高山地区得以富集的化合物比在极地地区优先富集的化合物要趋向于较难挥发的物质,其差异程度大约是2个数量级.本研究结果表明,若尔盖地区的情况更类似于极地的冷凝效应.HCB、PCB28在若尔盖地区降水中得到了相对富集.
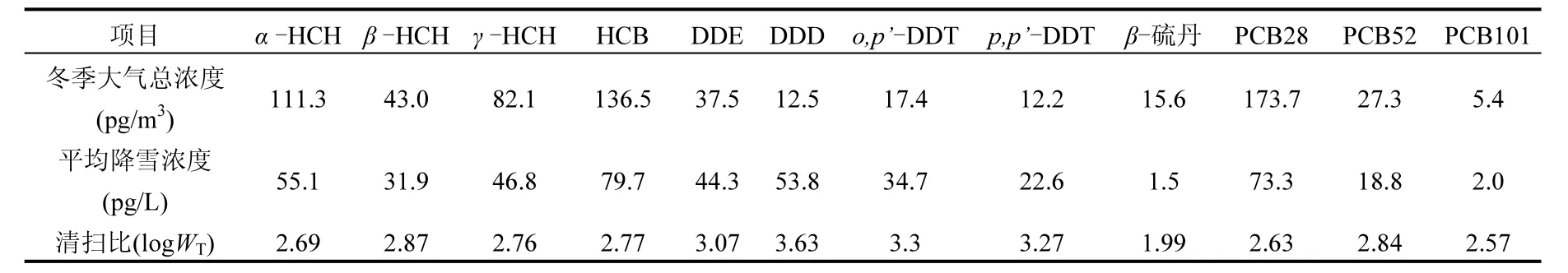
表5 若尔盖县城冬季大气降水的清扫比Table 5 Scavenging ratios in winter in Zoige alpine wetland
3 结论
3.1 若尔盖地区OCPs和PCBs湿沉降含量的最大值出现在 11月初冬的降雪样品中.总体上OCPs中按平均浓度排序为 HCB>PCB28>p,p’-DDD > p,p’-DDE > α-HCH > γ-HCH.PCBs以PCB28和PCB52为主,除少量的PCB101,其余高氯代多氯联苯都没有在该地区的沉降样品中检测到.PCB101主要在冬季和春季检出,这与其相对于 PCB28和 PCB52更具有持久性有关.HCHs、DDTs、PCB28和PCB52的大气沉降通量都是冬季>夏季>春季.这种季节变化特点与降水的洗刷率和降水量密切相关.
3.2 若尔盖地区降雪中的 POPs浓度远远高于降雨中的浓度.并且PCB101只在降雪中出现.证明对高山冷凝结效应的半挥发性有机污染物来说,雪比雨有更高的清除效率.PCB28在若尔盖地区降水中得到了相对富集.若尔盖冬季大气降水的清扫比较大的化合物为 DDTs类化合物,其次为 β-HCH,这是由于β-HCH具有较高的水溶解度的原因.再其次为 γ-HCH、α-HCH、PCB52、28.这一结果验证了高空大气远程迁移和局地的高山冷凝效应的区别.
[1]Wang X P, Yang H D, Gong P, et al.One century sedimentary records of polycyclic aromatic hydrocarbons, mercury and trace elements in the Qinghai Lake [J].Tibetan Plateau Environmental Pollution, 2010,158(10):3065-3070.
[2]张伟玲,张 干,祁士华,等.西藏错鄂湖和羊卓雍湖水体及沉积物中有机氯农药的初步研究 [J].地球化学, 2003,32(4):363-367.
[3]Wang X P, Yao T D, Cong Z Y, et a1.Gradient distribution of persistent organic contaminants along northern slope of Central-Himalayas, China [J].Science of the Total Environment,2006,372(1):193-202.
[4]王 峰,朱 彤,徐柏青,等.珠穆朗玛峰东绒布冰川新降雪中有机氯农药 [J].中国科学D辑(地球科学), 2007,37(5):670-675.
[5]Cheng H R, Zhang G, Jiang J X, et a1.Organochlorine pesticides,polybrominated biphenyl ethers and lead isotopes during the spring time at the Waliguan Baseline Observatory, northwest China: Implication for long-range atmospheric transport [J].Atmospheric Environment, 2007,41(22):4734-4747.
[6]Li J, Zhu T, Wang F, et a1.Observation of organochlorine pesticides in the air of the Mt.Everest region [J].Ecotoxicology and environmental safety, 2006,63(1):33-41.
[7]Yang R Q, Yao T D, Xu B Q, et a1.Distribution of organochlorine pesticides (OCPs) in conifer needles in the southeast Tibetan Plateau [J].Environmental Pollution, 2008,153(1):92-100.
[8]刘文杰,谢文明,陈大舟,等.卧龙自然保护区土壤中有机氯农药的来源分析 [J].环境科学研究, 2007,20(6):27-32.
[9]潘 静,杨永亮,陈大舟,等.HRGC-HRMS测定卧龙高海拔地区冰雪和水中OCPs和PCBs [J].环境化学, 2008,27(6):843-844.
[10]Zheng X Y, Liu X D, Liu W J, et a1.Concentrations and source identification of organochlorine pesticides (OCPs) in soils from Wolong Natural Reserve [J].Chinese Science Bulletin, 2009,54(5):743-751.
[11]杨永亮,潘 静,陈大舟,等.卧龙巴郎山地区夏、冬两季土壤中有机氯农药和低氯代多氯联苯的海拔高度分布 [J].环境化学,2009,28(5):728-733.
[12]朱晓华,杨永亮,路国慧,等.广东省部分高海拔地区表层土壤中有机氯药和多氯联苯的冷凝结效应 [J].环境科学研究,2012,25(7):778-784.
[13]万奎元,杨永亮,武振艳,等.长白山表层土壤中有机氯农药和多氯联苯的海拔高度分布特征 [J].岩矿测试, 2011,30(2):150-154.
[14]Vandrooge B L, Grimalt J O, Camarero L, et a1.Atmospheric Semivolatile Organochlorine Compounds in European High-Mountain Areas (Central Pyrenees and High Tatras) [J].Environmental Science and Technology, 2004,38(13):3525-3532.
[15]Grimalt J O, Barend L, Vandrooge B L.Polychlorinated Biphenyls in Mountain Pine (Pinus Uncinata) Needles from Central Pyrenean High Mountains (Catalonia, Spain) [J].Ecotoxicology and Environmental Safety, 2006,63(1):61-67.
[16]Tremolada P, Villa S, Bazzarin P, et a1.POPs in mountain soils from the Alps and Andes: suggestions for a ‘precipitation effect’on altitudinal gradients [J].Water, Air and Soil Pollution, 2008,188(1-4):93-109.
[17]Wania F, Westgate J N.On the mechanism of mountain cold-trapping of organic chemicals [J].Environmental Science and Technology, 2008,42(24):9092-9098.
[18]袁国礼,郎欣欣,孙天河.青藏高原持久性有机污染物的研究进展 [J].现代地质, 2012,26(5):910-916.
[19]付 允,孙玉川,毛海红,等,地下河流域土壤中有机氯农药分布及来源分析 [J].中国环境科学, 2012,32(3):517-522.
[20]Ricardo B, Peter P, Roberto Q, et a1.Persistent toxic substances in soils and waters along an altitudinal gradient in the Laja River Basin, Central Southern Chile [J].Chemosphere, 2005,58(7):905-915.
[21]Pilar F, Guillem C, Joan O, Persistent organic pollutants in remote freshwater ecosystems [J].Aquatic Sciences, 2005,67(3):263–273.
[22]Vilanova R M, Fernandez P, Martinez C, et a1.Organochlorine pollutants in remote mountain lake waters [J].Journal of Environmental Quality, 2001,30(4):1286-1295.
[23]Licia G, Giulia P, Adolfo D P, et a1.Organic persistent toxic substances in soils, waters and sediments along an altitudinal gradient at Mt.Sagarmatha, Himalayas, Nepal [J].Environmental Pollution, 2011,159(10):2552-2564.
[24]Helm P A, Diamond M L, Emkin R, et a1.A mass balance model describing multiyear fate of organochlorine compounds in a high Arctic lake [J].Environmental Science and Technology, 2002,36(5):996-1003.
[25]Rebecca M D, Alessandra C, Michele C, et a1.Atmospheric concentrations and air-water flux of organochlorine pesticides along the western Antarctic Peninsula [J].Environmental Science and Technology, 2005,39(2):465-470.
[26]Castro J J, Dueri S, Eisenreich S J, et a1.Polychlorinatedbiphenyls (PCBs) in the atmosphere of sub-alpine northern Italy [J].Environmental Pollution, 2009,157(3):1024-1032.
[27]Guillem C, Pilar F, Rosa M, et a1.Persistent organic pollutants in snow from European high mountain areas [J].Atmospheric Environment 2001,35(2):245-254.
[28]Blais J M, Schindler D W, Muir D C G, et a1.Accumulation of persistent organochlorine compounds in mountains of Western Canada [J].Nature, 1998,395(8):585-588.
[29]Roberto Q, Peter P, Ricardo B.Analysis of PCB levels in snow from the Aconcagua Mountain (Southern Andes) using the stir bar sorptive extraction [J].Environmental Chemistry Letters,2009,7(3):283-288.
[30]Hageman K J, Simonich S L, Campbell D H, et al.Atmospheric deposition of current-use and historic-use pesticides in snow at national parks in the western United States [J].Environmental Science and Technology, 2006,40(10):3174-3180.
[31]Gregor D J, Gummer W D.Evidence of atmospheric transport and deposition of organochlorine pesticides and polychlorinated biphenyls in Canadian Arctic snow [J].Environmental Science and Technology, 1989,23(5):561-565.
[32]Lei Y D, Wania F.Is rain or snow a more efficient scavenger of organic chemicals? [J].Atmospheric Environment, 2004,38(22):3557-3571.

