低硅/铝比X型分子筛(Li,Ca)-LSX的制备及其N2吸附性能
范明辉,任 博,白诗扬,孙继红
(北京工业大学 环境与能源工程学院,北京100124)
硅/铝比在1.0~1.1之间的X型分子筛通常被称为低硅/铝比X型分子筛(LSX)。因其晶体骨架具有较高的电荷密度和较大的孔径,表现出优越的选择吸附性能,尤其是经过Li+、Ca2+、Ag+等离子交换后的LSX,是变压吸附分离(PSA)和真空变压吸附分离(VSA)的优选吸附剂[1-3]。关 莉莉等[4]曾对Na-LSX分子筛进行Ca2+交换,结果表明,随着Ca2+交换度的增加,所制备的(Ca,Na)-LSX分子筛对N2的吸附量呈直线增长趋势,特别是当Ca2+交换度为97.1%时,该Ca-LSX分子筛对N2的吸附量达28.3mL/g,但是分子筛骨架中不同位置上的Ca2+对N2吸附性能的差别不明显。Kerry等[5]和John等[6]发现,只有当Li+交换度大于75%时,Li-LSX分子筛的N2吸附容量才会迅速增加,并且对N2吸附和解吸起关键作用的Li+主要位于FAU骨架结构中SⅢ位置。但由于这部分阳离子很难被交换,在制备高交换度的Li-LSX分子筛时难免浪费大量锂盐。笔者所在课题组曾利用LSX分子筛在高温焙烧时Na+容易发生迁移而重新分布的特点,提出水溶液交换法与高温固相焙烧法交替进行的离子交换新技术[7-8]。结果表明,该方法不仅可以保持较高的交换度(96%),而且大大提高了交换效率。但是该工艺复杂,而且容易造成环境污染。为克服Na-LSX分子筛骨架中个别位置上Na+较难交换以及锂盐价格持续上涨的问题,笔者提出在Na-LSX分子筛中同时引入Li+和Ca2+,制备出(Li,Ca)-LSX分子筛,希望藉此降低锂盐用量,并提高对N2的吸附效果。
1 实验部分
1.1 试剂与仪器
Na-LSX,工业级,洛阳建龙化工公司产品;氯化锂、盐酸、氯化钙、硝酸(68%),AR,国药集团化学试剂有限公司产品。
采用美国PE公司Optima 2000DV电感耦合等离子光谱仪(ICP-AES)测定样品的Li、Ca、Na含量。离子含量以摩尔分数表示,有利于比较,也便于反映晶格中的总离子位置数目。用Micromeritics公司ASAP2040静态吸附仪测定样品在8Pa、250℃下对N2的吸附量。测定前,样品真空脱水6h。采用Perkin-Elmer Pyris1TG热分析仪测定分子筛样品的吸水能力,N2气氛,流速20mL/min,升温速率10℃/min,最高温度800℃。
1.2 (Li,Ca,Na)-LSX分子筛的制备
将钠型低硅/铝摩尔比X型分子筛(Na-LSX)放入马福炉中,在100℃下干燥2h,550℃下焙烧1h后,置于干燥器中冷却。取5g活化后的Na-LSX分子筛与100mL 0.4mol/L的LiCl溶液或100mL 0.4mol/L的CaCl2溶液混合,置于90℃油浴中搅拌2h,抽滤、洗涤。将洗涤后的样品重新加到LiCl溶液中,重复上述步骤2~8次。将最终样品在100℃下干燥2h,在450℃下焙烧1h,得到具有一定 Li+和 Ca2+交换度的 (Na,Li,Ca)-LSX 分子筛[9]。由Li+交换 Na-LSX分子筛制备的 (Li,Na)-LSX分子筛按离子交换次数分别用L2、L4、L6、L8表示,其中,L8样品中Na+交换度小于5.0%时,命名为Li-LSX分子筛;由Ca2+交换Na-LSX分子筛制备的 (Ca,Na)-LSX分子筛按离子交换次数分别用C1、C2、C3、C4表示,其中,C4样品中Na+交换度小于5.0%,命名为Ca-LSX型分子筛;由Ca2+交换Li-LSX制备的 (Li,Ca)-LSX分子筛按离子交换次数分别用LC2、LC4、LC6、LC8表示;由Li+交换 Ca-LSX制备的 (Li,Ca)-LSX分子筛按离子交换次数分别用CL2、CL4、CL6、CL8表示。
2 结果与讨论
2.1 离子交换得到的各种(Li,Ca,Na)-LSX分子筛的离子交换度
表1为以Na-LSX为原料用不同阳离子交换得到的各种(Li,Ca,Na)-LSX 的离子交换度。由表1可知,当Na-LSX经4次Ca2+交换,得到的C4样品的Ca2+交换度可达96.1%,而Li+交换则至少需要8次,得到的L8样品的Li+交换度才达96.4%。另外,由Li-LSX分子筛经Ca2+交换8次,得到的LC8样品的Ca2+交换度可达90.5%,Li+交换度只剩7.5%;而Ca-LSX分子筛经Li+交换8次得到的CL8样品的Li+交换度仅为39.2%,Ca2+交换度仍为65.3%,说明离子的被交换由易到难顺序为Na+、Li+、Ca2+,与李志良等[10]所得结果一致。分子筛骨架中阳离子交换的难易程度主要是由电荷强度和阳离子半径共同决定[11],电荷强度越小越易交换,阳离子半径越小越易交换,且电荷强度起主要作用。Li+半径较小,相对于Na+更容易进入FAU骨架结构中,而Ca2+半径虽大于Li+,但1个Ca2+可以占据2个Li+或Na+位置,总电荷密度降低,相互之间斥力最小,所以Ca2+相对于Li+和Na+更容易充满整个FAU骨架中阳离子的位置。
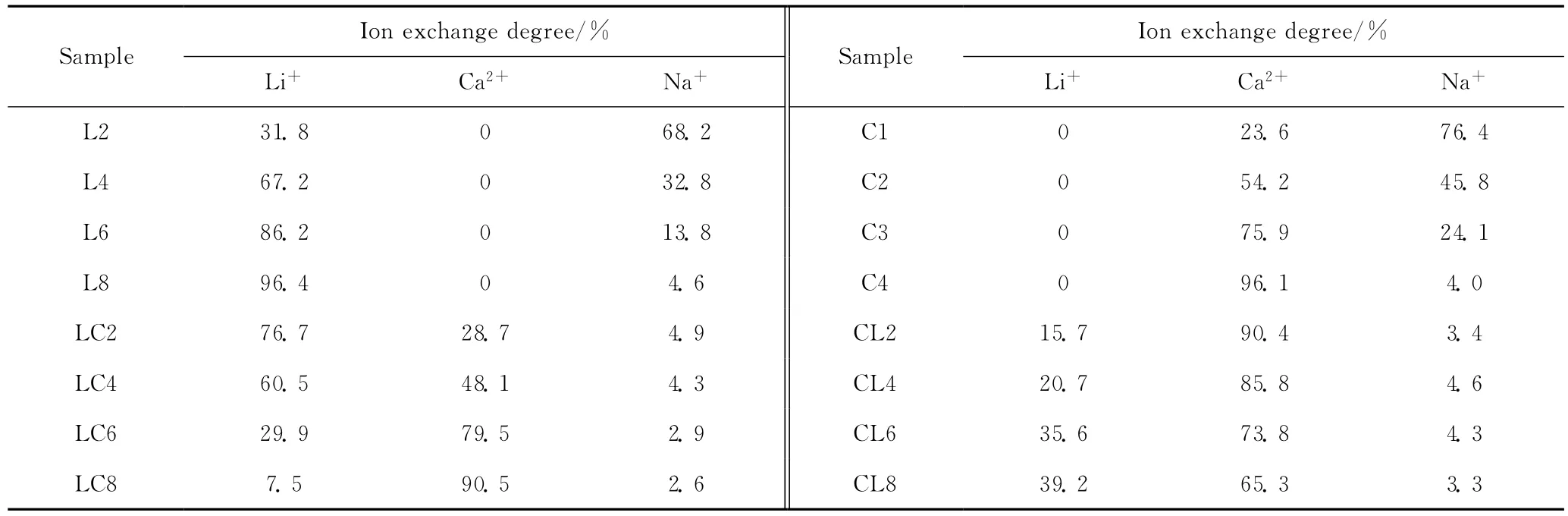
表1 以Na-LSX为原料用不同阳离子交换得到的(Li,Ca,Na)-LSX的离子交换度Table 1 Ion exchange degree of(Li,Ca,Na)-LSX prepared with Na-LSX as materials
2.2 不同离子交换度的(Na,Li,Ca)-LSX分子筛的吸水能力
图1为不同交换度(Na,Li,Ca)-LSX 分子筛的TG曲线。由图1可知,Na-LSX的失重率为17.7%,L8的失重率为27.9%,C4的失重率为24.1%,说明Na-LSX经过Li+的交换,其吸附水能力增强。LSX分子筛吸水能力由电场强度和孔体积大小共同决定,Li+半径最小,产生的电场强度较强,使离子的极化能力增强,有利于阳离子和骨架离子与水分子结合,增大吸水能力[12]。另外,在相同FAU(八面沸石)结构中,孔道体积由阳离子半径和个数共同决定[13],半径越小孔体积越大,个数越少孔体积越大;孔体积增大,便可吸附更多水分。气体分子(O2、N2、CO2等)可与分子筛骨架中阳离子键合,因此被吸附而实现分离[14];水分子和阳离子结合又与气体分子和阳离子的结合位置重叠,因而分子筛的吸水能力是影响其气体吸附量的重要因素。图1所示结果为研究(Na,Li,Ca)-LSX对 N2吸附能力提供了重要参数。

图1 不同交换度(Li,Ca,Na)-LSX分子筛的TG曲线Fig.1 TG curves of(Li,Ca,Na)-LSX with different cation exchange degrees
2.3 不同离子交换度的(Na,Li,Ca)-LSX分子筛的N2吸附性能

图2 77K时不同离子交换度的(Na,Li,Ca)-LSX分子筛的N2吸附-脱附等温线Fig.2 N2absorption-desorption isotherms of(Na,Li,Ca)-LSX samples with different cation exchange degrees at 77K
图2为不同离子交换度的(Na,Li,Ca)-LSX 分子筛在77K时的N2吸附-脱附等温线。从图2可以看出,在相对压力p/p0<0.1时,各分子筛样品对N2吸附量大幅度增加,其吸附-脱附曲线均为典型的I型等温线,表明样品中存在微孔。与Na-LSX相比较,在0.4<p/p0<1.0时,Li-LSX、Ca-LSX的N2吸附-脱附等温线存在明显的H4型滞后环,说明其中可能存在形状和尺寸均匀的狭缝状孔道[15-16],导致Li-LSX和Ca-LSX具有较高的N2吸附量。与此同时,在0<p/p0<0.1范围内,Li-LSX和Ca-LSX的比表面积 (772m2/g,806m2/g)和孔体积(0.48cm3/g,0.37cm3/g)均高于Na-LSX(623m2/g,0.33cm3/g),但 Ca-LSX 的比表面积大于Li-LSX,而Li-LSX的孔体积大于Ca-LSX,这是由于阳离子的大小差异所致,Li+的半径为0.076nm、Ca2+为0.099nm、Na+为0.102nm。Zanota等[17]报道,阳离子半径由 Li+(0.076nm)和 Na+(0.102nm)增加到 K+(0.138nm),分子筛的比表面积和孔体积下降,从而阻碍了N2分子进入分子筛FAU骨架内,与本实验结果类似。另外,从表2还可以看出,具有Li和Ca两种阳离子的样品LC4和CL4的孔体积介于Li-LSX和Ca-LSX之间。这些织构数据为降低锂盐用量而不影响N2吸附量提供了重要依据。

表2 在0<p/p0<0.1条件下不同离子交换度的(Na,Li,Ca)-LSX分子筛的比表面积和孔体积Table 2 The specific surface area and pore volume of(Na,Li,Ca)-LSX samples with different ion exchange degrees under the condition of 0<p/p0<0.1
图3为不同离子交换度的(Na,Li,Ca)-LSX 分子筛在298K时的N2吸附等温线。从图3可以看出,不同交换度的(Na,Li,Ca)-LSX分子筛对 N2的吸附量随Li+和Ca2+交换度的增加而增大,当Li+交换度为96.4%时(图3(a)中L8),N2的吸附量达19.8cm3/g,当Ca2+交换度为96.1%时(图3(b)中C4),N2的吸附量达25.4cm3/g。由于 N2分子具有较强的四极矩,且极化率较高,使得N2分子与FAU骨架中Li+或Ca2+及其极性表面存在较强的键合作用[18-19]。特别是LC4和CL4样品,对N2吸附能力分别达20.7和22.7cm3/g,均大于 Li-LSX的吸附量,这对于降低锂盐用量和减少环境污染起到积极作用,目前正在进一步评价和表征。298K下,Li-LSX和Ca-LSX对N2吸附量相比于Na-LSX分别提高了3.65倍和4.69倍,但比表面积和孔体积仅提高了1.24倍和1.31倍(见表2),充分说明分子筛织构参数并不是影响N2吸附性能的唯一因素,显然阳离子的大小和分布,以及阳离子与N2分子之间的结合力对N2的吸附性能起着关键作用。
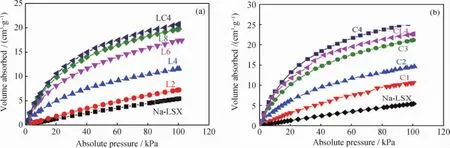
图3 298K时不同离子交换度的(Na,Li,Ca)-LSX分子筛的N2吸附等温线Fig.3 N2adsorption isotherms of(Na,Li,Ca)-LSX samples with different cation exchange degrees at 298K(a)Li+exchange;(b)Ca2+exchange
3 结 论
(1)以Na-LSX为原料,通过离子交换技术得到具有不同交换度的(Na,Li,Ca)-LSX分子筛;在3种阳离子中,离子交换由易到难的顺序为Ca2+、Li+、Na+。
(2)阳离子对LSX分子筛的吸水能力有明显影响,其吸水量由少到多的顺序为Na-LSX、Ca-LSX、Li-LSX,而不同离子交换度(Li,Ca)-LSX吸附水能力大于Ca-LSX、小于Li-LSX。经Li+和Ca2+交换后得到的LSX比表面积和孔体积均增大,有利于N2吸附,影响N2吸附的主要因素是阳离子大小及分布和阳离子与N2分子的结合力,并由此影响着水含量和织构性能,最终决定着对N2分子的吸附能力。
(3)(Li,Ca)-LSX 分子筛的制备,对于降低锂盐用量和减少环境污染以及改善其对N2分子的吸附性能具有重要作用。
[1]BULOW M, SHEN D M. Sorption kinetics of atmospheric gases on Li,RE (rare earth)-LSX zeolite beads as sorbents for oxygen PVSA processes[J].Microporous and Mesoporous Materials,2007,105(1-2):163-169.
[2]李宏愿,尹伟民,魏渝伟,等.高效空分制氧吸附剂Li-LSX的组成和性能评价[J].石油学报(石油加工),2009,25(3):1001-1019.(LI Hongyuan,YIN Weimin,WEI Yuwei,et al. Composition and performance evaluation of high efficient Li-LSX adsorbent for air separation and oxygen production[J].Acta Petrolei Sinica(Petroleum Processing Section),2009,25(3):1001-1019.)
[3]刘宗昉,曾懿,孙继红,等.Li+改性低硅铝X型沸石分子筛的研究进展[J].离子交换与吸附,2009,25(6):565-576.(LIU Zongfang,ZENG Yi,SUN Jihong,et al.The research progress on the LSX molecular sieve modified by Li+[J].Ion Exchange and Adsorption,2009,25(6):565-576.)
[4]关莉莉,段连运,谢有畅.Li+交换的几种分子筛的氮氩分离性能[J].物理化学学报,2004,20(7):684-689.(GUAN Lili,DUAN Lianyun,XIE Youchang.The adsorptive separation of N2and Ar by some zeolites highly exchanged with Li+[J].Acta Phys Chim Sin,2004,20(7):684-689.)
[5]KERRY W, DAVE J, ROBERT L C. Lithium exchanged zeolite X adsorbent blends:US,7300899[P].2005.
[6]JOHN F K,OREFIELD P.Nitrogen adsorption with highly Li exchanged X-zeolites with low Si/Al ratio:US,5268023[P].1993.
[7]孙继红,刘宗昉.一种制备锂型低硅铝X型沸石分子筛 (Li-LSX)的 离 子 交 换 方 法:CN,200710121786[P].2008.
[8]张丽,孙继红,任博,等.通过固相交换法制备的(Li,NH4)-LSX分子筛骨架中 Li+的分布[J].功能材料,2012,16(43):2166-2170.(ZHANG Li,SUN Jihong,REN Bo,et al.Li+distribution in the structure skeleton of the (Li,NH4)-LSX molecular sieves prepared by solid-state ion exchange method [J]. Functional Material,2012,16(43):2166-2170.)
[9]张丽,石迎亮,孙继红,等.水溶液交换法制备的(Li,Na)-LSX沸石骨架中Li+分布[J].离子交换与吸附,2012,28(3):240-248.(ZHANG Li,SHI Yingliang,SUN Jihong,et al.Li+distribution in the structure skeleton of the (Li,Na)-LSX molecular sieves framework prepared by aqueous solution exchange method[J].Ion Exchange and Adsorption,2012,28(3):240-248.)
[10]李志良,支建平,张玉林.起始物对Li+、Ca2+混合成型低硅铝X型分子筛(LSX)制备及吸附性能影响[J].无机材料学报,2008,23(5):975-980.(LI Zhiliang,ZHI Jianping,ZHANG Yulin.Effects of different starting materials on preparation and adsorption properties of the mixed Li+and Ca2+exchanged low silica X-type zeolites(LSX)[J].Journal of Inorganic Materials,2008,23(5):975-980.)
[11]ILIR A B,HERVE J,HEINZ B,et al.Inelastic neutron scattering and infrared spectroscopic study of furan adsorption on alkali-metal cation-exchanged faujasites[J].Spectrochimica Acta Part A,2001,57(7):1393-1403.
[12]WOZNIAK A,MARLER B,ANGERMUND K,et al.Water and cation distribution in fully and partially hydrated Li-LSX zeolite[J].Chemistry of Materials,2008,20(19):5968-5976.
[13]PLÉVERT J,RENZO D,FAJULA F.Structure of dehydrated zeolite Li-LSX by neutron diffraction:Evidence for a low-temperature orthorhombic faujasite[J].Journal of Chemical Physics B,1997,101(49):10340-10346.
[14]HUTSON N D,ZAJIC S C,YANG R T.Influence of residual water on the adsorption of atmospheric gases in Li-X zeolite:Experiment and simulation[J].Industrial& Engineering Chemistry Research,2000,39(6):1775-1780.
[15]ROJAD F,KORNHAUSER I,FELIPE C.Capillary condensation in heterogeneous mesoporous networks consisting of variable connectivity and pore-size correlation[J].Journal of Chemical Physics,2002,4(11):2346-2355.
[16]FLOQUET N,COULOMB J P,WEBER G.Structural signature of type IV isotherm steps:Sorption of trichloroethene,tetrachloroethene and benzene silicalite-I[J].Journal of Chemical Physics B,2003,107(3):685-693.
[17]ZANOTA M L,HEYMANS N,GILLES F,et al.Thermodynamic study of LiNaK-LSX zeolites with different Li exchange rate for N2/O2separation process[J].Microporous and Mesoporous Materials,2011,143(2-3):302-310.
[18]BAKSH M S A,KIKKINDES E S,YANG R T.Lithium type X zeolite as a superior sorbent for air separation[J].Separation Science and Technology,1992,27(3):277-294.
[19]MIKOSCH H, UZUNOVA E L, NIKOLOV G.Interaction of molecular nitrogen and oxygen with extraframework cations in zeolites with double sixmembered rings of oxygen-bridged silicon and aluminum atoms:A DFT study[J].Journal of Chemical Physics B,2005,109(22):11119-11125.

