肝门胆管癌三维适形放疗联合卡培他滨同步化疗效果评价
郑爱青,穆海玉,李 静,曲雅静,梁克明
肝门胆管癌三维适形放疗联合卡培他滨同步化疗效果评价
郑爱青,穆海玉,李 静,曲雅静,梁克明
目的 回顾性评价三维适形放疗联合卡培他滨同步化疗治疗非手术肝门部胆管癌的疗效和不良反应。方法 对19例不符合手术指征的肝门胆管癌患者行三维适形放疗联合卡培他滨同步化疗,放疗2Gy/次,5次/周,计划照射50 Gy/25次。放疗第1天开始口服卡培他滨,早1 g,晚2 g。结果 12例(63.2%)达部分缓解(partial remission,PR),7例(36.8%)达稳定(stable disease, SD)。中位生存期12.7个月(4.3~ 20.8个月),中位无病生存期9.3个月(3.6~18.6个月)。3例(15.8%)发生3级毒性反应,无4级毒性反应。结论 三维适形放疗联合卡培他滨同步化疗对肝门胆管癌非手术治疗有效,且安全。
胆管癌;化疗;放疗;同步化放疗
胆管癌是一种少见的恶性肿瘤,占消化道恶性肿瘤的2%~6%[1]。肝门胆管癌是指发生于左右肝管和肝总管的恶性胆管肿瘤,占胆管癌的50%~75%。外科切除是唯一的根治办法,但只有约20%患者可手术切除,且其中仍有50%局部复发[2]。非手术切除的胆管癌预后差,病情进展快,化疗、放疗或化放疗联合是主要治疗选择。本研究自2005-05至2012-03采用放疗联合卡培他滨同步化疗治疗不可切除的肝门胆管癌19例。
1 对象与方法
1.1 对象 19例不符合手术指征的肝门胆管癌患者行放疗联合卡培他滨同步化疗,男12例,女7例。年龄43~79岁,平均64岁。其中淋巴结转移6例,13例肿瘤直径 ≥ 3 cm,5例侵犯门静脉,放疗持续时间35~38 d。中位PTV 367.8(124.2~699.4)mm3。全部病例均合并黄疸,主要为皮肤、巩膜黄染,皮肤瘙痒,白陶土样便16例,伴肝区疼痛13例,伴恶心、呕吐11例,发热8例,乏力14例,食欲缺乏14例,体重下降8例。治疗前所有患者均行下列检查:胸片/胸部CT,腹部CT和盆腔CT/MRI,血常规,肝、肾功能,凝血功能、血清肿瘤标志物,EKG检查,4例行全身PET-CT检查。经皮肝穿刺胆道造影(percutaneous transhepatic cholangiogram,PTC)确定梗阻部位、形态和胆管狭窄程度。不可切除的肝门胆管癌由外科医师评估,符合以下标准被认为不可手术切除:(1)肿瘤直径>3 cm;(2)有肝脏、淋巴结转移或肿瘤侵及大血管。患者及家属同意并在治疗知情协议书上签字。
1.2 同步化放疗 因所有患者均有不同程度的阻塞性黄疸,所以在治疗前首先行PTC或内镜逆行胰胆管造影(endoscopic retrograde cholangio-pancreatography, ERCP) ,置入支架行胆汁引流减轻黄疸,然后再开始同步化放疗。
三维适形放射治疗在胆管支架置入2~3 d后进行。患者双手抱头仰卧位,负压真空垫固定体位,立体定位架下设置体表标记点。CT定位扫描前空腹4~6 h,在平静呼吸下进行增强螺旋CT扫描,扫描层厚0.5 cm(扫描前静脉注射优维显非离子型造影剂100 ml进行增强扫描);将CT扫描所得图像资料传入大恒STAR-2000三维放射治疗计划系统,在此基础上精确勾画大体靶区(gross tumor volume,GTV)及其邻近重要组织器官,靶区定义按照ICRU 50号和62号文件规定的标准定义,临床靶区(clinical target volume,CTV)是在GTV的基础上外放1~2 cm,计划靶区(planning target volume,PTV)是在CTV基础上左右外扩10~15 mm,上下外扩10~20 mm,控制重要器官如脊髓、肾脏等受量在可耐受范围内。90%等剂量曲线包括PTV,6MV X线,DT2 Gy/次,5次/周,计划照射50 Gy/25次。
从放疗第1天开始口服卡培他滨,早1 g,晚2 g,饭后1 h服用。治疗过程中每周监测血常规、肝肾功能,同时给予保肝、退黄及保护胃黏膜等对症支持治疗。
1.3 观察指标 评价指标包括局部控制率(治疗结束后3个月肿瘤无进展即为局部控制)、局部无进展生存期、总生存期(同步化放疗开始之日起到死亡或随访截止日)、症状改善情况(疼痛和/或阻塞性黄疸)和早期不良反应发生率,并于治疗结束后3个月进行评价。根据实体瘤疗效评价标准(response evaluation criteria in solid tumors,RECIST),分为完全缓解(complete remission,CR)、PR、SD和进展(progressive disease, PD)。客观缓解用CR+PR计算,无效用SD或PD计算。用CTC 3.0评价放化疗不良反应。如果出现中-重度不良反应(≥3级),卡培他滨暂停3~7 d,然后降低剂量10%~20%继续用药。
1.4 统计学处理 采用SPSS 19.0统计软件,用 Kaplan-Meier方法计算生存期。用自身配对法,对治疗前、治疗后胆红素水平进行t检验。P<0.05为差异有统计学意义。
2 结 果
2.1 随访 治疗期间每周评价2次,监测体重、不良反应、实验室检查(血常规、血生化、肝肾功能)。放化疗结束后4~8周行第1次随访,此后每2个月1次。随访内容包括症状、体征、血常规、肝肾功能,胸、腹部增强CT扫描和腹部B超。截止2013-03-31随访率为100%。
2.2 症状改善情况 19例治疗前平均总胆红素水平为(309.0 ±154.8) μmol /L,直接胆红素水平为(198.6±103.7) μmol /L,治疗后总胆红素平均值为(79.4±45.7) μmol /L,直接胆红素平均值为(50.3±37.2) μmol /L,较治疗前均有显著下降(P<0.01)。伴肝区疼痛13例,疼痛完全缓解10例,疼痛明显减轻3例。
2.3 肿瘤局部控制 19例非手术切除的肝门部胆管癌患者用放疗加卡培他滨同步化疗,12例(63.2%)达PR,7例(36.8%)达SD。虽然没有达CR,但随访过程中没有发现有照射野内复发者。
在随访过程中,有15例死亡,4例存活。全部患者中位生存期12.7个月(4.3~ 20.8个月),中位无病生存期9.3个月(3.6~18.6个月)。存活者5例中,肝转移2例,肺转移1例,肝和左肾上腺转移1例,无病生存1例。同步放化疗后5例出现反复发作的胆管炎,经重新置入支架和静滴抗生素后症状改善。
2.4 不良反应 患者对同步化放疗的耐受性较好(表1)。最常见的2级毒性反应是骨髓抑制、疲劳,恶心或呕吐,手足综合征,厌食和腹泻。3级毒性反应有恶心、呕吐和疲劳。19例中有3例(15.8%)发生3级毒性反应。无4级毒性反应出现。3例放疗暂停1 d,1例暂停3 d。4例(21.1%)患者因为急性毒性调整卡培他滨剂量,其中1例暂停卡培他滨3 d,1例卡培他滨减量后仍不耐受毒性而停止服用,2例卡培他滨减量。没有患者出现支架闭塞。
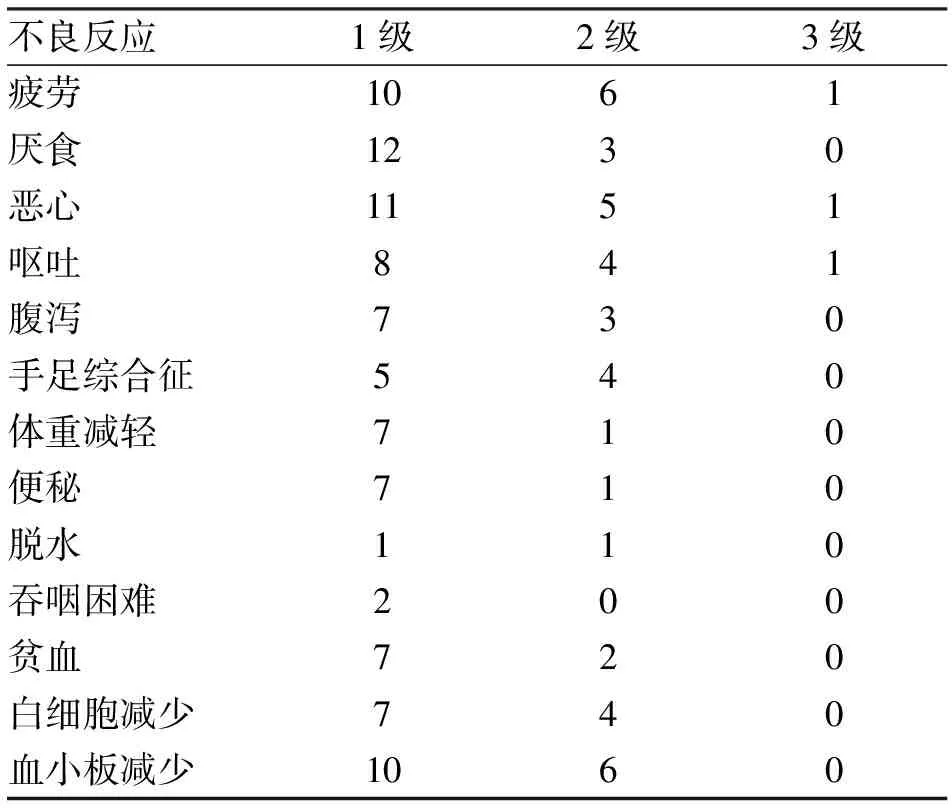
表1 肝门胆管癌19例同步放、化疗不良反应发生率(%)
3 讨 论
根据胆管癌发生部位,可分为肝内胆管癌和肝外胆管癌, 后者再分为肝门胆管癌和远端胆管癌。肝门胆管癌唯一可能长期生存的治疗方法是手术切除或肝移植,但这些方法仅适用于早期患者,即使根治性治疗后其中位生存期仍只有约2年[3,4]。由于肝门部胆管癌生长位置特殊,肿瘤体积不大时会阻塞胆管引流,引起阻塞性黄疸。胆管癌有一种沿胆管壁向胆管远端及近端浸润的倾向,绝大多数患者在诊断时已是进展期,失去手术机会,只能采取姑息性治疗方法。
不可切除的肝门胆管癌如果不予治疗, 平均生存期3个月。与单纯胆汁引流相比,姑息治疗对非手术切除的胆管癌可提高生活质量和延长生存期[5]。目前,对非手术切除的胆管癌还没有标准的姑息治疗方法。
放疗常用于治疗肝门胆管癌,以达到肿瘤局部控制,改善生存质量的目的,并将生存期延长10~16.8 个月。NCCN关于进展期胆管癌最新治疗指南认为,胆管癌属中度化疗敏感,推荐用吉西他滨或氟尿嘧啶治疗[6]。最常用的药物是氟尿嘧啶(5- FU),单独或与其他化疗药物联合应用,有效率10%~30%[7]。放疗和化疗联合应用可做到局部控制和全身治疗相结合;用氟尿嘧啶作为放疗增敏剂可提高胆管癌的放疗效果[8]。
卡培他滨是一种5-FU前体药物,口服给药作为一个完整的分子经胃肠道吸收,然后通过3个连续的酶促反应被转换成5-FU[9]。由于该途径中最后的酶——胸苷磷酸化酶(thymidine phosphorylase,TP)在肿瘤细胞中的含量较正常组织丰富,用卡培他滨治疗后致5-FU在肿瘤组织中浓度更高,即进一步提高了卡培他滨对靶向肿瘤的有效性。另外,放射可通过肿瘤细胞选择性上调TP放大卡培他滨对肿瘤的治疗作用[10],且通过卡培他滨可干扰肿瘤细胞DNA合成,成为放射增敏剂。另外,卡培他滨用药途径简单,治疗依从性好,因而被越来越多地用于胆管癌的治疗,如单药治疗,与铂类联合应用或与放疗同步应用。
一些回顾性和前瞻性研究报道,卡培他滨与放疗联合治疗腹部肿瘤耐受性好。Baisden等[11]回顾性分析调强放疗同时给予卡培他滨和光动力疗法治疗胆管癌10例,中位总生存期为13个月,中位无病生存期10~11个月,不良反应轻,主要为2级恶心和轻度疲劳。Das等[12]回顾性分析用卡培他滨同步放疗治疗上腹部恶性肿瘤88例,包括非手术切除的胆管癌18例,中位放疗剂量45 Gy(30~72 Gy),卡培他滨中位剂量为850 mg/m2,最常见的2级毒性反应是恶心、手足综合征、疲劳、呕吐和腹泻,3级毒性反应为恶心、呕吐和疲劳,没有患者出现 CTC 4级毒性反应,提示放疗与卡培他滨同步化疗治疗腹部肿瘤耐受性好。
本研究结果证实,同步放化疗治疗非手术切除的肝门胆管癌患者耐受性好,可显著改善预后。本组中位总生存期12.7个月,中位无进展生存期9.3个月。虽然没有患者达CR,但63.2%的患者达到PR,随访期内也没有患者出现照射野内复发。虽然本组患者中位年龄64岁,但对治疗耐受性好,相关毒性反应轻微且短暂,只有15.8%患者有3级急性毒性,没有出现4级急性毒性和治疗相关性死亡。经过对症治疗,没有患者中止放疗。治疗期间严密监测,及时对症处理可能发挥了重要作用,能降低急性毒性的发生,监测手段包括每周复查血常规1次和每周评价不良反应2次。
总之, 本研究结果表明,胆管癌对放化疗敏感,治疗急性毒性可耐受。由于肝门胆管癌发病率低, 多数研究为单中心、小样本的回顾性分析,需要进一步大规模的临床研究来验证卡培他滨同步放疗治疗的疗效及安全性。
[1] Ito F, Cho C S, Rikkers L F,etal. Hilar cholangiocarcinoma: current management [J]. Ann Surg,2009, 250(2):210-218.
[2] 刘召波,卢实春,李 宁,等. 肝门部胆管癌的外科治疗[J]. 中华消化外科杂志,2013,12(3):186-190.
[3] 王 林,耿智敏,宋晓刚, 等. 联合精准半肝切除治疗肝门部胆管癌[J]. 中华消化外科杂志,2013,12(3):204-209.
[4] 金昌国,张利刚,欧阳才国,等. 肝门部胆管癌49例手术并发症分析[J].武警医学,2012,23(3):210-213.
[5] Patel T, Singh P. Cholangiocarcinoma: emerging approaches to a challenging cancer[J]. Curr Opin Gastroenterol, 2007, 23(3):317-323.
[6] Benson A B, Abrams T A, Ben-Josef E,etal. NCCN clinical practice guidelines in oncology: hepatobiliary cancers[J]. J Natl Compr Canc Netw, 2009 , 7(4): 350-391.
[7] Ducreux M, Van Cutsem E, Van Laethem J L,etal. A randomized phase II trial of weekly high-dose 5-fluorouracil with and without folinic acid and cisplatin in patients with advanced biliary tract carcinoma: results of the 40955 EORTC trial[J]. Eur J Cancer, 2005, 41(3): 398-403.
[8] Oda A, Katayose Y, Rikiyama T,etal. Low-dose cisplatin plus 5- fluorouracil with radiotherapy for unresectable upper and hilar bile duct carcinoma[J]. Gan To Kagaku Ryoho, 2005 , 32(11): 1615-1617
[9] Gennatas C, Michalaki V, Gennatas S. The role of capecitabine in the management of tumors of the digestive system[J]. Rev Recent Clin Trials, 2009, 4(1):1-11.
[10] Sawada N, Ishikawa T, Sekiguchi F,etal. X-ray irradiation induces thymidine phosphorylase and enhances the efficacy of capecitabine (Xeloda) in human cancer xenografts[J]. Clin Cancer Res, 1999, 5(10): 2948-2953.
[11] Baisden J M, Kahaleh M, Weiss G R,etal. Multimodality treatment with helical tomotherapy intensity modulated radiotherapy, capecitabine, and photodynamic therapy is feasible and well tolerated in patients with hilar cholangiocarcinoma[J]. Gastrointest Cancer Res, 2008, 2(5): 219-224.
[12] Das P, Wolff R A, Abbruzzese J L,etal. Concurrent capecitabine and upper abdominal radiation therapy is well tolerated[J]. Radiat Oncol,2006, 24(1):41.
(2013-10-09收稿 2013-12-15修回)
(责任编辑 郭 青)
Efficacy of concurrent three-dimensional conformal radiation therapy and capecitabine in patients with unresectable hilar cholangiocarcinoma
ZHENG Aiqing, MU Haiyu, LI Jing, QU Yajing, LIANG Keming.
Department of Oncology, Affiliated Hostipal of Logistics University of CAPF, Tianjin 300162, China
Objective To retrospectively analyze the efficacy and toxicity of unresectable hilar cholangiocarcinoma treated with concurrent capecitabine and radiation therapy. Methods Nineteen patients with unresectable hilar cholangiocarcinoma underwent concurrent chemo-radiotherapy protocol from May 2005 through March 2012. All patients
three-dimensional conformal radiotherapy (3D-CRT), 5 times a week at 2 Gy per fraction per day to a total dose of 50 Gy. Concurrent chronomodulated capecitabine was administered on days of irradiation in a dosage of 1 g in the morning and 2 g in the evening. Results All patients completed the treatment course. Twelve patients(63.2%)achieved a PR, and seven (36.8%) achieved a SD at the first follow-up examination. The median survival time was 12.7 months (range 4.3 to 20.8 months) and the median disease-free survival time was 9.3 months (range 3.6 to 18.6 months). A cumulative grade 3 toxicity was observed in 3 out of the 19 patients (15.8%). No patient had any grade 4 toxicity. Conclusions Concurrent capecitabine and radiation therapy is effective and tolerable in patients with unresectable hilar cholangiocarcinoma.
biliary tract neoplasms;chemotherapy;radiotherapy;concurrent chemo-radiotherapy
郑爱青,博士,副主任医师,E-mail:aiqingzhengtj@gmail.com
300162天津,武警后勤学院附属医院肿瘤科
R735.8

