参附注射液联合化学治疗对非小细胞肺癌疗效的Meta分析
杨旭平 ,赖 丹 ,黄毅岚 ,钟小燕
(1.泸州医学院药学院,四川 泸州 646000; 2.泸州医学院附属医院,四川 泸州 646000)
肺癌是发病率较高的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)占肺癌的70% ~80%[1],晚期 NSCLC的治疗主要以化学治疗(简称化疗)为主[2],但化疗所产生的不良反应常常使患者难以忍受。减少化疗药物的不良反应是当前研究的热点,而复方中药配合化疗是提高恶性肿瘤治疗效果的重要途径[3]。参附注射液由红参、黑附片提取物组成,有效成分主要含人参皂苷、水溶性生物碱等。参附注射液能减轻化疗药物的不良反应,改善患者生存质量,联合化疗可用于治疗非小细胞肺癌[4-5],然而目前所进行的大多是小样本试验,缺乏一定的说服力。基于该类临床研究,本研究采用Cochrane系统评价的方法,客观评价参附注射液的安全性和有效性,以期为NSCLC的临床用药提供真实可靠的依据。
1 资料与方法
1.1 纳入标准
研究类型:纳入所有涉及参附注射液联合一线化疗方案治疗非小细胞肺癌的随机对照试验(RCT),纳入的文献均描述具体随机方法。
研究对象:均经过病理学或细胞学证实为中晚期NSCLC,性别、种族及国籍等均不限;近1个月内均未接受抗肿瘤治疗,化疗至少2周期以上;Karnof-sky(kPS)评分不小于50分或ECOG评分为 0~2分;预计生存期3个月以上;治疗前肝功、肾功、心电图、血常规均正常,有可测量临床或X线摄片观察指标,可以评价近期疗效。排除伴有严重内科疾病及感染;同时伴随其他恶性肿瘤;肺癌为其他肿瘤转移病灶;妊娠哺乳期妇女、精神病患者、过敏体质及多种药物过敏者;依从性差、不能坚持化疗者。
干预措施:治疗组静脉滴注参附注射液联合一线化疗方案治疗,对照组仅以一线化疗方案进行治疗。
结局指标:有效率,依据世界卫生组织实体瘤疗效四级标准进行评价,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD)4级。有效率为(CR+PR)/总例数 ×100% ;KPS评分,按KPS评分标准进行治疗前后评分;不良反应,包括血液学毒性、消化道毒性、肝肾毒性及对免疫功能的影响。
1.2 文献检索
RCT检索策略遵循 Cochrane系统评价手册 5.0版,采用主题词与自由词相结合的方式,并根据具体数据库调整,所有检索策略通过多次预检索后确定。国外数据库包括Cochrane Library,PubMed,EMbase;国内数据库主要有 CBM,VIP,CNKI,万方;另外,补充检索了中国 RCT数据库,并用 Google Scholar,Medical martix等搜索引擎在互联网上查找相关文献,追查已纳入文献的参考文献,与本领域的专家、通讯作者等联系,以获取以上检索未发现的相关信息。检索时间均截止到2013年7月。检索词为non-small cell lung cancer,non small cell lung carcinoma,non small cell lung carcinomas,non small cell lung,NSCLC,shenfu,shen-fu,非小细胞肺癌,参附注射液,参附注射剂等。
1.3 质量评价
由2位研究者交叉核对纳入研究的检索结果,对有分歧而难以确定其是否纳入的研究通过讨论或由第3位研究者决定是否纳入。按Cochrane系统评价员手册5.0版推荐的质量评价标准评价纳入研究的质量:是否描述了具体的随机分配方法;随机分配方案隐藏情况;是否采用盲法评价;是否描述了失访、退出发生的情况,如有退出或失访情况,是否进行了意向性治疗 (ITT)分析。将研究质量从高到低分为A,B,C 3级:A级低度偏倚,完全满足以上4条质量标准,发生各种偏倚的可能性最小;B级中度偏倚,其中1条或1条以上的标准为部分满足,有发生偏倚的中度可能性;C级高度偏倚,其中1条或1条以上的标准完全不满足,有发生偏倚的高度可能性。质量评价由2位研究者独立进行并交叉核对,如遇分歧通过讨论或请第3位研究者协助解决。
1.4 统计学处理
应用RevMan 5.2统计软件。计数资料用相对危险度(RR)为疗效分析统计量,并计算95%可信区间(CI);连续变量资料采用加权均数差(WMD),并计算其 95%CI。若合并研究间存在异质性(P < 0.1,I2>50%),寻找异质性原因如性别、年龄、不同病程和疾病严重程度、剂量、疗程等,并采用亚组分析;若未找到异质性的原因,则采用随机效应模型进行Meta分析;若合并研究间无异质性时,采用固定效应模型。若研究间存在明显的临床异质性,只对其进行描述性分析。必要时,采用敏感性分析检验结果的稳定性。
2 结果
2.1 纳入研究的基本情况
根据检索策略和资料收集方法,共检索到相关文献65篇,阅读文题及摘要后,排除43篇,利用Endnote X2软件去重及进一步阅读文献排除重复或不符合纳入标准的文献4篇,再经过阅读全文按纳入标准及数据完整性进行筛选,最终纳入6篇中文文献[6-9,11-12],1 篇英文文献[10]。评价有效率、KPS 评分提高率及不良反应。所纳入的7个研究均阐明了具体的随机分组方法、采用平行设计,试验地点均在中国,共涉及421例患者,均为NSCLC。纳入研究的基本特征见表1,纳入研究均未提及分配隐藏方法,依从性好,未进行ITT分析,基线相似性均为“相似”,其余见表2。

表1 纳入研究的基本特征

表2 纳入研究的质量评价
2.2 Meta分析
治疗有效率:共4项研究[6-7,9-10](198例)报道了有效率,且有详细的数据资料。结局指标为有效率时,纳入的研究无异质性(P =0.87),采用 固 定 效 应 模 型 ,其 合 并 RR=1.10,95%CI(0.75,1.63),合并效应量的检验,Z = 0.49,P =0.62。可认为参附注射液联合化疗组治疗NSCLC与单纯化疗在有效率方面比较,差异无统计学意义,见图1。
KPS评分:3项研究[8-10](141例)分别统计了参附注射液联合化疗组和单独化疗组KPS评分。结局指标为KPS评分时,纳入研究无异质性(P=0.14),采用固定效应模型,其合并WMD =8.27,95%CI(6.58,11.27)。 合 并 效 应 量 的 检 验 , Z =5.4,P <0.000 1,差异有统计学意义,可认为在提高 KPS评分方面,参附注射液联合化疗组治疗NSCLC比单纯化疗组更有效,见图 2。

图1 两组治疗有效率比较的Meta分析
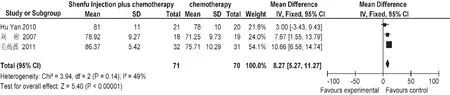
图2 两组KPS评分提高率比较的Meta分析
不良反应:Meta分析结果显示,与单纯化疗相比,参附注射液联合化疗治疗 NSCLC可减少白细胞下降[RR=0.59,95%CI(0.39, 0.90), P =0.01]和 血 小 板 下 降 [RR =0.63,95%CI(0.40,0.98), P = 0.04],降低恶心呕吐发生率[RR = 0.60,95%CI(0.42,0.85), P =0.004]及 腹泻发生率 [RR =0.54,95%CI(0.30,0.96), P = 0.03],而 在 肝 功 能损害 [RR =1.03,95%CI(0.47,2.24), P = 0.95]、肾功能损害[RR = 0.68,95%CI(0.21,2.19),P = 0.52]方面的差异无统计学意义,见图 3。

图3 两组不良反应比较的Meta分析
3 讨论
本系统评价结果显示,与单纯化疗方案相比,参附注射液联合化疗方案可以提高KPS评分、降低患者化疗后血小板减少和白细胞减少的发生率,同时减少胃肠道反应等。此外,姜孝新等[13]的研究报道,参附注射液可减轻肿瘤化疗药物对骨髓的抑制,有效改善机体的免疫功能;毛薇薇[8]、刘彬[9]的研究报道,参附注射液联合化疗可明显改善中医临床证候。综上所述,参附注射液对NSCLC化疗患者有一定的辅助治疗作用。
本研究纳入的7篇文献均描述了具体随机方法,均无正确实施分配隐藏和盲法。但由于肿瘤化疗的特殊性,往往难以采用随机方案的隐藏和盲法,故纳入的RCT具有发生偏倚的可能性。另外,本系统评价虽然全面收集了相关研究资料,但仍存在一些未能发表的阴性研究结果。数据的缺失可能存在一定的发表偏倚。但对于化疗药物治疗肿瘤的临床研究而言,仍可认为是较高质量的RCT。
本系统评价纳入研究存在局限性,从而影响结果的论证强度,如大多数研究均未提及样本量估算的依据,很多研究样本量较小,这会使检验效能低;所纳入的研究在药物的使用量及使用时间上不一致,这对最终的测量指标将会产生一定影响;本系统评价纳入的研究中无一项描述是否实施了隐蔽分组。据调查,不实施或不充分实施隐蔽分组会夸大疗效;由于在评价疗效时部分采用主观性指标,故盲法的使用在研究参附注射液联合化疗方案治疗NSCLC的研究中相当重要,未充分实施盲法会直接导致实施偏倚和测量偏倚的发生;所纳入的研究中仅有1篇[10]提到了随访,均未进行ITT分析,因此在一定程度上影响了系统评价的质量。纳入的研究对部分结果采用不同的统计量,致使有些试验不能合并,无法得出统一结论。
综上所述,通过本系统评价,初步证实了参附注射液联合化疗药物的一线化疗方案治疗NSCLC在提高KPS评分上优于单纯化疗,降低患者化疗后血小板减少和白细胞减少的发生率,减少胃肠道反应等方面差异有统计学意义。合并分析显示,参附注射液联合化疗方案对NSCLC患者有一定的辅助治疗作用。通过本系统评价提示,参附注射液联合化疗治疗NSCLC的试验方法学质量有待提高,仍需进行设计严谨、方法可靠的多中心临床研究,以便更好、更全面地对其疗效及不良反应做出正确的评价。
[1]陆再英,钟南山.内科学[M].第 7版 .北京:人民卫生出版社,2009:123.
[2]白春学,张 新.肺癌的治疗现状[J].中华结核和呼吸杂志,2006,29(3):146-148.
[3]杨国旺,石朝云.中药联合化疗的抗肿瘤增效作用[J].中国实验方剂学杂志,2000,6(3):59-62.
[4]Wu W,Long SQ,Zhang HB,et al.Improvement of quality of life with Shenfu Injection in Non Small Cell Lung Cancer Patients treated with Gemcitabine plus Cisplatin Regimen[J].Chin J Integr Med,2006,12(1):50-54.
[5]龙顺钦,廖桂雅,河文峰,等.生活质量量表评价参附注射液对肺癌化疗患者生活质量的影响[J].南方医科大学学报,2011,31(12):2 090-2 092.
[6]龚红卫,罗秀丽.参附注射液辅助化疗治疗老年晚期非小细胞肺癌临床观察[J].中国中医急症,2008,17(6):782-783.
[7]陆新岸,杨泽江,邓朝明.参附注射液配合化疗对晚期非小细胞肺癌患者免疫功能的影响[J].中医学报,2010,25(6):1 049-1 051.
[8]毛薇薇.参附注射液联合TP/GP方案治疗晚期非小细胞肺癌32例临床观察[J].中国现代医生,2011,49(15):61.
[9]刘 彬.参附注射液联合TP方案化疗对脾肾亏虚型晚期非小细胞肺癌患者生活质量影响的临床观察[D].南京中医药大学,2010.
[10]Hu Y,Hou AJ,Zhang HW,et al.Shenfu injection plus vinorelbine for elderly patients with Non-small Cell Lung Cancer in promoting the quality of life:a randomized controlled clinical trial[J].Chinese-German Journal of Clinical Oncology,2010,9(1):22-25.
[11]刘俊波,黄常江.参附注射液对晚期非小细胞肺癌化疗患者造血功能及生活质量的影响[J].中国医药导报,2001,8(20):119-120.
[12]何 朗,胡 欣,郭翠华,等.参附注射液对非小细胞肺癌化疗患者血小板及机体免疫功能的影响[J].中国中医急症,2012,21(9):1 389-1 390.
[13]姜孝新,伍小平,蒋 艳.参附注射液对中晚期非小细胞肺癌患者化疗后免疫功能的影响[J].苏州大学学报:医学版,2011,31(5):814-815.

