氧气在不同粒径Pt/C催化剂上的电催化还原
王彦恩 曹 爽*, 崔朋雷 唐亚文 陆天虹
(1河北农业大学理学院,河北农业大学现代科技学院,保定 071000)
(2南京师范大学化学与材料科学学院,南京 210097)
0 引 言
直接醇类燃料电池(DAFC)由于燃料来源丰富、价格低廉、便于储存和运输的优点,在小型化电源或可移动电源方面具有广阔的应用前景[1]。DAFC研究目前主要集中在两个方面:1、获得高效且价格低廉的阴阳极催化剂[2-4];2、醇渗透率低质子传导率高的新型电解质膜。Pt是DAFC最好的阴极氧还原催化剂[5-6]。已有研究表明[7-8],Pt金属的粒子大小明显影响着Pt/C催化剂对氧气的电催化还原性能[9]。Ross等[7]的研究表明,当Pt/C催化剂中Pt金属粒子大小为4 nm时,其对氧气的电催化还原质量比活性(Mass activity,MA)最佳。而Watanabe等[8]的研究结果却显示,Pt/C催化剂对氧气的电催化还原的MA随Pt粒子的粒径减小而增加。这些似乎矛盾的结论可能跟不同研究者、以及不同研究者制备不同粒径大小Pt/C催化剂的方法不同有关。因此研究氧气在高分散度、高均一性的Pt/C催化剂上的电催化还原非常有意义。
有机溶胶法能够制备得到具有良好分散度和高度均一性金属纳米粒子[10]。因此,本文利用甲醇作为溶剂,SnCl2作为还原剂制备了具有高度分散性和均一性、载有不同粒径Pt粒子的Pt/C催化剂。在上述制备方法基础上,本文研究了Pt/C催化剂中,Pt金属纳米粒子的大小对氧气电催化还原性能的影响。
1 实验部分
1.1 试剂和仪器
Vulcan XC-72活性碳为美国Cabot公司产品,Nafion溶液(质量分数为5%)为美国Aldrich化学公司产品),其余试剂均为分析纯级,所有溶液均用三次蒸馏水配制。
X-射线衍射(XRD)谱用D/max-rC型转靶X射线衍射仪 (日本理学公司)检测,电压40 kV,电流100 mA,Cu Kα 射线源为光源(λ=0.154 06 nm)。透射电镜(TEM)测量用JEM-2010仪(日本电子公司)进行,点分辨率0.14 nm。电化学测试用CHI600电化学分析仪(美国CHI仪器公司)和常规的三电极体系的电化学池进行。
1.2 不同粒径Pt/C催化的制备
室温下,将化学计量的0.038 6 mol·L-1H2PtCl6和 0.0310 mol·L-1SnCl2的甲醇溶液在超声波下混合均匀,由于H2PtCl6被SnCl2还原而形成浅黄色透明的Pt溶胶。缓缓加入Vulcan XC-72活性碳粉,N2保护下,分别控制干燥温度为30、40、50、65和70℃,磁力搅拌直至溶剂完全脱除。100℃下陈化12 h后,用6 mol·L-1NaOH洗涤Pt/C催化剂以除去SnCl2与SnCl4,蒸馏水洗涤至洗液中检测不到Cl-过滤,90℃真空干燥,即制得不同粒径大小的Pt/C催化剂,其中含Pt的质量百分比为20%。能量分散光谱分析并没有发现Sn的吸收峰,表明加入的SnCl2和生成的SnCl4已经完全除去。
1.3 电化学性能测试
旋转圆盘电极采用瑞士万通的Auto-Lab628型仪。对电极为铂片,参比电极为饱和甘汞电极(SCE)。工作电极制备用文献报道的方法[11],将直径3 mm的玻碳电极分别在 5# 金相砂纸、0.3 μm 和 0.05 μm的Al2O3粉上磨至镜面,淋洗干净后,在三次蒸馏水中超声清洗,再用三次蒸馏水淋洗干净。催化剂配成2 mg·mL-1的水相悬浮液。超声波分散10 min,移取6.6 μL悬浮液至电极表面,于60℃干燥。电极表面Pt载量为 28 μg·cm-2, 再移取 3.3 μL 的 5%Nafion溶液覆盖在电极催化剂表面,于60℃干燥。测量前,溶液通高纯N220 min以除去溶解氧,实验在30℃和N2保护下进行。文中所述电位均相对于SCE。
2 结果和讨论
有机溶胶法制备得到的不同粒径Pt/C催化剂XRD 图见图 1。图中,2θ为 24.7°左右出现的是Vulcan XC-72活性碳(002)晶面衍射峰,在 2θ为39.9°、46.5°、67.8°、81.2°处分别出现了 Pt的(111)、(200)、(220)、(311)晶面衍射峰,所得结果与文献报道值相同[12-13]。利用最强的Pt(111)晶面衍射峰的半峰宽,通过Scherrer公式可以计算出不同Pt/C催化剂中,Pt粒子的平均粒径分别为 2.10、3.18、3.73、4.17、4.80 nm。所得结果列于表1中。
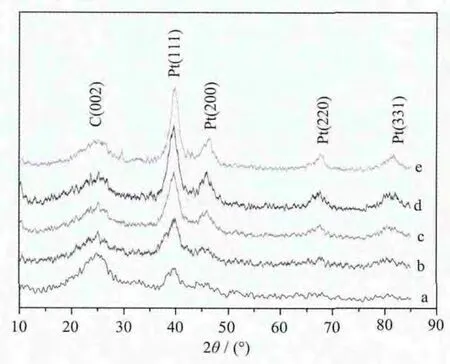
图1 不同粒径Pt/C催化剂的XRD图Fig.1 XRD patterns of Pt/C catalysts with the different Pt particles sizes
图2a为Pt粒子平均粒径为3.2 nm的Pt/C催化剂的TEM照片。图2b为经过统计200个Pt粒子后获得的粒子分布图,大约84%的Pt粒子粒径分布在 3.0~3.4 nm 的狭窄范围内,表明通过有机溶胶法制备得到的Pt/C催化剂中Pt粒子粒径非常均一。Pt/C催化剂中Pt粒子的表面平均分散度D(Surface averagedispersion)能够通过 Borodzinski和Bonarowska模型计算获得[14],所得结果也列在表1中。从表1中可以看出随着Pt粒子的粒径增加,Pt粒子的表面平均分散度逐渐减小,这与理论相符。然而,通过有机溶胶方法制备得到的Pt/C催化剂,即使Pt粒子的平均粒径达到4.3 nm,其表面平均分散度(D=28.4%)仍然略高于E-TEK公司Pt粒子平均粒径为2.8 nm的Pt/C催化剂(D=28.0%)[15]。这表明通过有机溶胶法制备得到的Pt/C催化剂中,Pt粒子的大小拥有良好的分散度和优异的均一性。
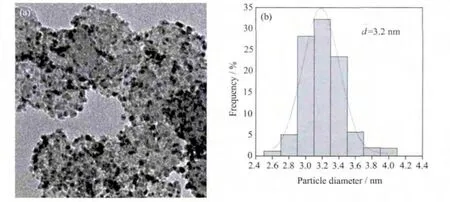
图2 (A)Pt粒子平均粒径为3.2 nm Pt/C催化剂的TEM图 和(B)Pt粒子粒径分布柱状图Fig.2 TEM image of the Pt/C catalysts with the average sizes of Pt particles 3.2 nm and the histogram of the Pt particle size distribution

表1 不同Pt/C催化剂的结构参数Tab 1 Structure parameters of the different Pt/C catalysts
2.2 电催化性能研究
图 3为不同粒径 Pt/C催化剂在 0.5 mol·L-1HClO4溶液中的CO溶出伏安图。由插图可见,随着Pt粒子粒径减小,CO的起始氧化电位逐渐正移。Takasu[16]等利用电化学方法研究Pt粒子大小对CO电催化氧化性能时也有类似的发现,其原因可能与较小的Pt粒子拥有更高的表面能有关。通过CO氧化 所 需 电 量 ,可 以 计 算 出 载 有 4.8、4.3、3.8、3.2、2.2 nm Pt粒子的Pt/C催化剂的电化学活性面积分别为 36.7、42.4、49.0、52.0、44.8 m2·g-1Pt。随着 Pt金属粒子的逐渐减小,催化剂的比表面积逐渐增大,催化剂的电化学活性面积亦逐渐增大,当Pt金属粒子减小到3.2 nm时,Pt/C催化剂的电化学活性面积增加到最大;但随着Pt金属粒子的粒径进一步减小到2.2 nm,催化剂的电化学活性面积反而下降。Takasu[17]等利用电化学方法研究Pt氧化物的电化学还原时,也发现当Pt粒子越小时,Pt粒子越容易被氧化。这些氧化物的生成抑制了CO在Pt金属粒子表面的解离吸附,造成了Pt/C催化剂的电化学活性面积下降。因此,片面追求降低Pt粒子的粒径,并不一定能提高Pt催化剂的催化活性。
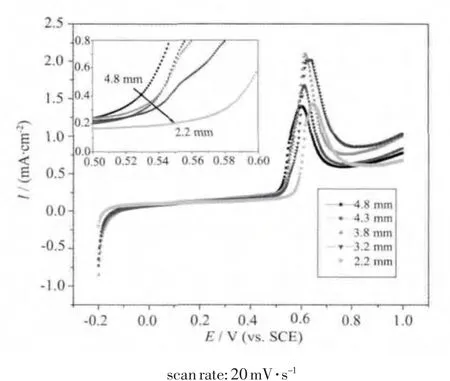
图3 不同的Pt/C催化剂在0.5 mol·L-1HClO4中吸附CO的线性扫描图谱Fig.3 CO-stripping voltammograms of the different Pt/C catalystsin0.5mol·L-1HClO4
图4为不同粒径Pt/C催化剂在氧气饱和的0.5 mol·L-1HClO4溶液中的线性扫描伏安图。在电势小于0.4 V时,氧气在所有的催化剂上电催化还原都显示出扩散控制过程;在0.3~0.7 V电势范围内,显示出混合扩散动力学控制过程。随着电位的负扫,不同粒径的Pt/C催化剂对氧气显示出不同的还原性能。图5为电位0.55 V时,Pt粒子对氧气电催化还原的质量比活性与粒径关系。从图5可以看出:当Pt/C催化剂中Pt粒子粒径为3.2 nm时,其对氧气的电催化还原的质量比活性最佳。
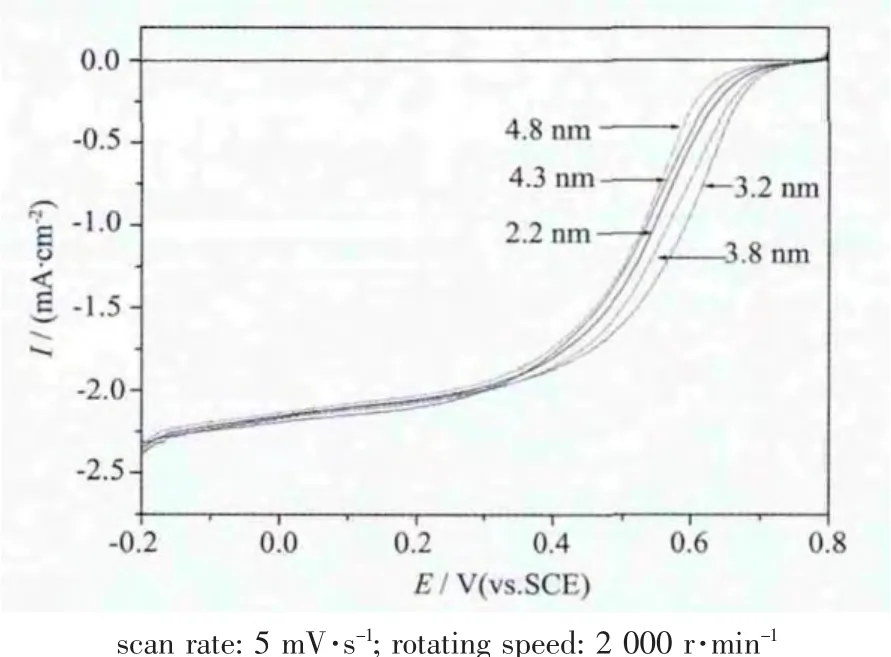
图4 不同Pt/C催化剂在O2饱和的0.5 mol·L-1HClO4中的线型扫描伏安图Fig.4 Linear scan voltammograms of the different Pt/C catalysts in O2-saturated 0.5 mol·L-1HClO4 solution
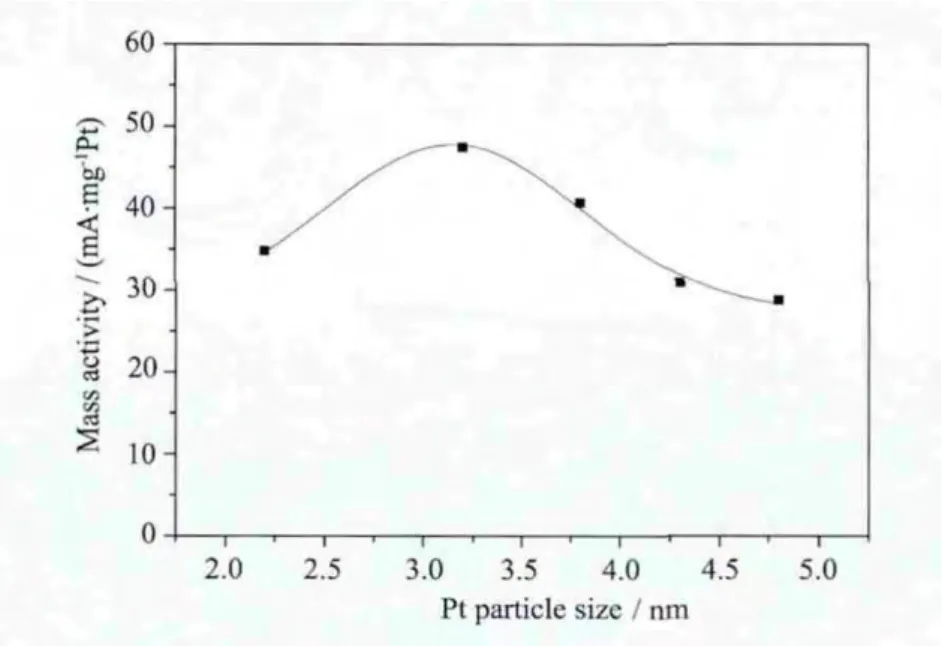
图5 Pt/C催化剂对氧气还原的质量比活性与Pt粒子粒径之间的关系图谱Fig.5 Relationship between the mass activity of the Pt/C catalysts for the oxygen reduction and the average sizes of the Pt particles in the Pt/C catalysts
上述结果表明,在氧气的电催化还原过程中,Pt粒子存在着明显的粒径效应。其原因可能与氧气在Pt金属的电催化还原机理有关。在发生电子转移前,氧气必然要在Pt金属表面发生吸附。当Pt粒子较小时,Pt粒子很容易被氧化,粒子表面含有丰富的OH基团,抑制了O2分子在Pt金属表面的解离吸附,从而降低了催化剂的催化活性。反之,由于较大的Pt粒子的比表面积较小,其活性中心数目相应也较少,从而导致总表面覆盖度降低,催化剂活性同样也降低。另一方面,Kinoshita等[18]的研究认为:当Pt金属粒子粒径位于3.5 nm附近时,Pt金属粒子中Pt(111)和(100)晶面含量较高,因此对氧气的电催化还原有利。
3 结 论
本文通过一种快速的有机溶胶方法制备了无保护剂的稳定性Pt溶胶,并将其负载在活性炭上,通过控制溶剂的挥发温度,从而有效控制Pt金属纳米粒子的大小。获得的Pt纳米粒子拥有良好的分散度和非常高的均一性。电化学的研究表明,对于氧气的电催化还原,Pt/C催化剂存在着明显的粒径效应。当Pt粒子粒径为3.2 nm时,Pt/C催化剂对氧气的电催化还原的质量比活性最佳。
[1]XIE Xiao-Feng(谢晓峰),FAN Xing-He(范星河).Fuel Cell Technique(燃 料 电 池 技 术 ).Beijing:Chemical Industry Press,2004:215-218
[2]Yang Z,Nie H,Chen X,et al.J.Power Sources,2013,236(15):238-249
[3]Tang Y W,Cao S,Chen Y,et al.Appl.Surf.Sci.2010,256(13):4196-4200
[4]Zhang L,Kim J,Dy E,et al.Electrochim.Acta,2013,108(1):480-485
[5]LIU Shi-Bin(刘世斌),YUAN Juan-Ning(员娟宁),ZHANG Zhong-Lin(张忠林),et al.Chinese J.Inorg.Chem.(无机化学学报),2010,26(7):1171-176
[6]JIA Yu-Jie(贾羽洁),CAO Shuang(曹爽),TANG Ya-Wen(唐亚文),et al.Chinese J.Inorg.Chem.(无机化学学报),2009,25(4):674-678
[7]Beard B C,Ross J P N.J.Electrochem.Soc.,1990,137(11):3368-3374
[8]Watanable M,Stonehart P.J.Electroanal.Chem.,1989,271(1/2):213-220
[9]Malheiro A R,Perez J,Villullas H M.J.Power Sources,2010,195(10):3111-3118
[10]Bnnemann H,Brijoux W,Brinkmann R,et al.Angew.Chem.Inter.Ed:Engl.,1991,30(10):1312-1314
[11]Schmidt T J,Noeske M,Gasteiger H A,et al.Langmuir,1997,13(10):2591
[12]White J H,Sammells A F.J.Electrochem.Soc.,1993,140(6):2167-2176
[13]Antolini E,Cardelini F.J.Alloys Compd.,2001,315(1/2):118-122
[14]Borodziński A,Bonarowska M.Langmuir,1997,13(21):5613-5620
[15]TANG Ya-Wen(唐亚文),YANG Hui(杨辉),XING Wei(邢巍),et al.Chin.Chem.Letts.(中国化学快报),2002,13(5):478-479
[16]Takasu Y,Iwazaki T,Sugimoto W,et al.Electrochem.Commun.,2000,2(9):671-674
[17]Takasu Y,Ohashi N,Zhang X G,et al.Electrochim.Acta,1996,41(16):2595-2600
[18]Kinoshita K.J.Electrochem.Soc.,1990,137(3):845-848

