基于FTIR的药桑主成分分析
宋峰峰, 倪雪雪, 魏 鸿, 谢 睆, 张 晖, 马晓丽
(新疆医科大学1药学院, 2分析测试中心, 乌鲁木齐 830011)
药桑属黑桑种( Morus nigra Linn) ,为天然22倍体半栽培类型野生桑树种质资源[1]。药桑原产于伊朗,自16世纪开始引入我国新疆地区栽培。药桑的桑椹不仅是营养丰富的果实,也是维吾尔族民间药材,仅分布于新疆阿克苏、和田和喀什地区,维吾尔族称其为“夏图土”,药桑作为独特而珍稀药材[2-4]。1988年药桑椹被国家卫生部列为首批药食同源植物,被医学界誉为“民间圣果”和“21世纪的最佳保健果品”[5]。
目前,药桑的鉴定方法主要有基源鉴别、形状鉴别、显微鉴别、理化鉴别等,理化鉴别主要采用色谱、质谱等技术,其耗时,耗试剂,操作繁琐;近年来傅立叶变换红外光谱法 (FTIR)在中药鉴别研究中的应用受到越来越多的关注,在药用植物的真伪与优势等无损快速鉴别方面得到广泛应用,已成功运用于鉴别不同品种菊花属药用植物等[6-10]。目前,国内外尚未有运用傅里叶变换红外光谱法对药桑药材进行鉴定评价的报道。本实验采用FTIR方法对10批药桑样品绘制FTIR红外指纹图谱,使用SIMCA主成分分析对不同产地药桑样品的FTIR 谱图进行分析,对其复杂化学组分进行全面综合地评价,确定药桑主要的指纹图谱特点,旨在为日后药桑药材的鉴别和研究方向提供理论依据。
1 材料与方法
1.1材料与仪器
1.1.1 样品 实验所用的10个产地药桑药材均由新疆医科大学药学院生药教研室帕丽达教授鉴定为药桑属黒桑种(Morus nigra Linn)植物药桑的干燥果实,见表1。
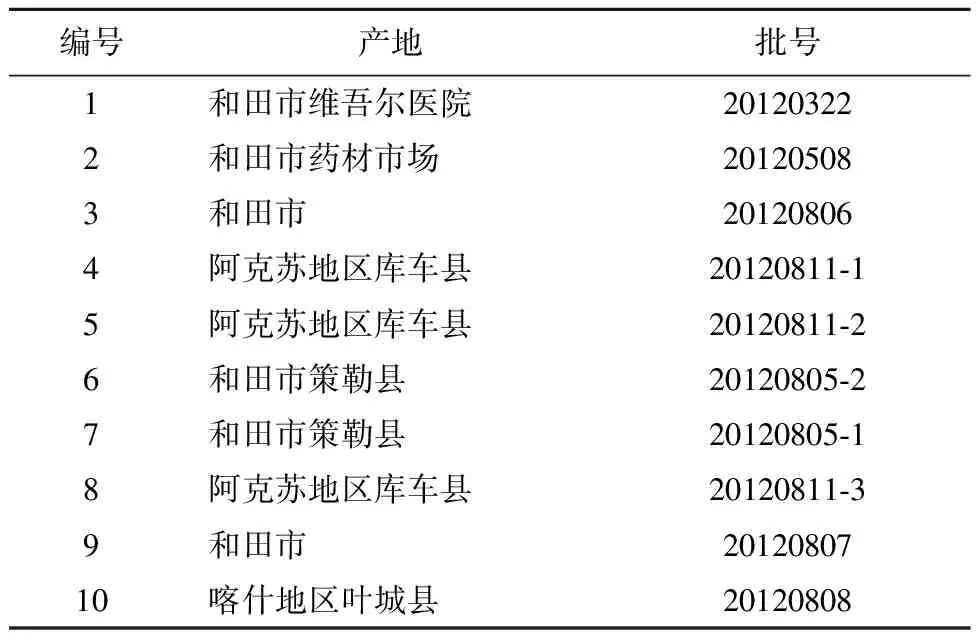
表1 不同产地药桑的采集情况
1.1.2 仪器与试剂 红外光谱仪(岛津IR-Prestege21,日本岛津),电子天平(AL204,梅特勒-托利仪器上海有限公司),KBr(光谱纯,国药集团化学试剂),红外快速干燥器(WS70-1型,上海索谱仪器有限公司),压片磨具(型号SSP-10A,日本岛津),玛瑙研钵。
1.2实验方法一维谱图:KBr压片法制样,将药桑原药材干燥、粉碎过200目筛,各取样品粉末约2 mg,分别与200 mg溴化钾混合研磨充分均匀,压片测定,获得一维红外光谱图。
1.3红外光谱条件的选择TGS检测器,扫描次数为20次,分辨率为4 cm-1,光谱范围600~4 000 cm-1。
2 结果与分析
2.1药桑果实、桑叶、桑枝的红外指纹图谱药桑作为新疆维药资源,地产丰富,成分复杂。从不同产地药桑、桑叶、桑枝样品红外光谱图(图 1)中可以看出,不同产地样品的红外光谱基本一致,但也有个别特征峰的相对吸收强度有所变化,指纹区小峰的微小差异,这可能与不同的环境条件差异有关。但其主要化学物质在红外光谱吸收峰中的峰强和出峰位置上都很相似,将其列表进行归属,结果见表2。
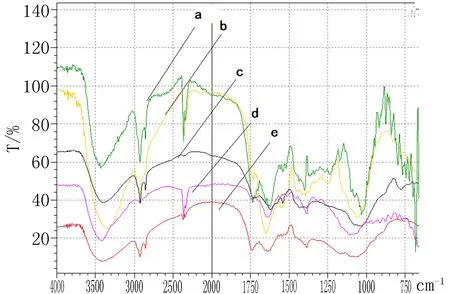
a:药桑(喀什地区);b:桑叶(乌鲁木齐市);c:药桑(和田市);d:桑枝(乌鲁木齐市);e:药桑(阿克苏地区)
图1不同地区及部位的药桑红外图谱
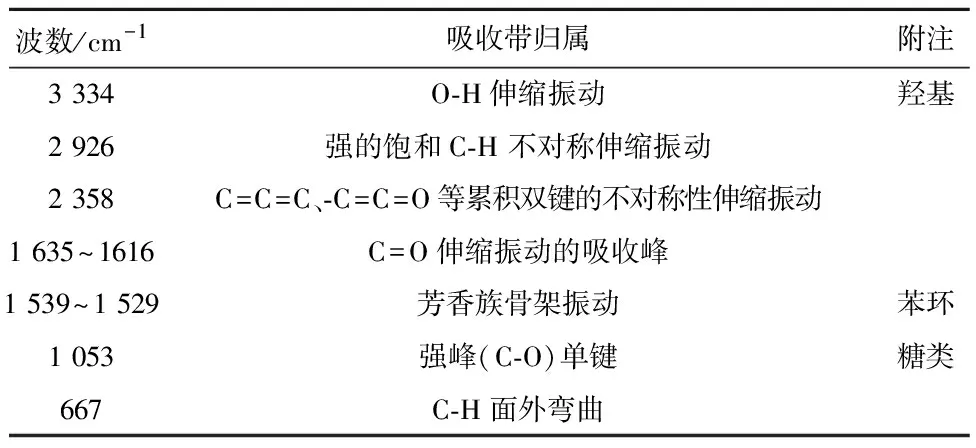
表2 药桑药材红外光谱中吸收带的归属
在3 334 cm-1处有强的羟基(O-H)伸缩振动和弯曲振动吸收峰,在2 926 cm-1处有强的饱和C-H 伸缩振动吸收峰,1 539~1 529 cm-1处主要为与芳香环相连的C=O的伸缩振动及酞胺化合物的特征收谱带和甾醇类中C=O伸缩振动的吸收峰。1 635~1 616 cm-1处的C=O伸缩振动峰。考虑到药桑中的化学成分,推断该区域应为黄酮的特征区。
2.2方法学考察
2.2.1 精密度试验 取同一药桑(和田市药材市场)原药材样品供试片连续测定5次,测量结果如图2所示,重复测定5次所得到的红外谱图非常相似,从其红外重叠的谱图看,5次测定得到的谱图基本一致。谱图样品中共有峰波数的RSD均<0.84%,见图2。

图2 药桑样品红外图谱比较
2.2.2 重复性试验 同一份药桑样品,分别取样5次进行压片测量, 所得红外光谱图比较一致, RSD
反映的是仪器的重复性,谱图样品中共有峰波数 RSD均<0.23%。
2.3主成分分析采集来自3 个不同地区的10个已知产地的药桑红外图谱,提取主要吸收峰共10个数据点(即对应的吸收峰及A值)进行主成分分析。前3个主成分的方差贡献率为70.416%,是最重要的成分;前4个主成分的累积方差贡献率为80.848%,特征值及累积可信度见表3,所以前4个主成分基本可以表示原红外光谱的主要信息,并能显示出各产地之间的相似性关系。

表3 特征值及贡献度表
3 结论
对不同产地药桑样品的主成分分析表明,分布地不同会造成药桑 在化学成分组成上存在着差异,同时也说明地理位置对药材质量是有影响的,只有采取对其复杂化学组分进行全面综合的评价方法,才能保障药桑产品质量的一致性。本实验采用FTIR方法测定了不同产地药桑的红外光谱图,使用SIMCA主成分分析对不同产地药桑样品的FTIR 谱图进行了分析,其结果能够很好地反映出药桑中的整体化学组分变化,同一产地药桑具有相似的化学组分,能够很好地归在同一类别中。从而形成可靠的数据库,以便于以后判断药桑的来源及对其进行分类。该方法具有客观全面的优点,是一种简便易行、快速准确且具有一定实用性的鉴别方法。
文献参考:
[1] 买买提依明.新疆药桑的研究[J].北方蚕业,2007,28(1):1-3.
[2] 买买提依明,卢红,木合达尔,等.新疆药桑的有效成分测定及药理作用的研究初报[J].北方蚕业,2006,27(4):16-18.
[3] 吴志平,周巧霞,顾振纶,等.桑树不同药用部位的降血糖效果比较[J].蚕业科学,2005,31(2):215-217.
[4] 宋大可,买买提依明·乃比江.新疆药桑果汁化学成份及药物价值探讨[J].蚕桑通报,1994,25(4):23-34.
[5] 国家药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2005:211-212.
[6] 赵明波,邓秀兰,王亚玲,等. 红花RP-HPLC指纹图谱的建立及其质量研究[J].药学学报, 2004, 39(3):212-216.
[7] 徐永群,孙素琴,袁子民, 等. 红外光谱结合主成分分析鉴别道地山药[J].分析化学, 2002, 30(10):1231-1233.
[8] 徐永群,黄吴,周群,等. 红外特征图谱和聚类分析法在赤芍产域分类鉴别种的应用[J].分析化学, 2003, 31(1):5-9.
[9] 程存归,郭水良,陈宗良. FTIR 直接测定法对川贝母和珠贝、小东贝的区别鉴定[J].中草药, 2002, 33(3):262-264.
[10] 张志祥,刘鹏,康华靖,等.基于主成分分析和聚类分析的FTIR不同地理居群香果树多样性分化研究[J].光谱学与光谱分析, 2008, 28(9):2081-2085.

