TiO2-Cu[HgI4]纳米复合材料的制备及其热致变色性能*
陈晓丽,林福华,文春燕,苏秋成,李新军
(中国科学院广州能源研究所,中国科学院可再生能源重点实验室,广州 510640)
TiO2-Cu[HgI4]纳米复合材料的制备及其热致变色性能*
陈晓丽,林福华,文春燕,苏秋成,李新军†
(中国科学院广州能源研究所,中国科学院可再生能源重点实验室,广州 510640)
以TiO2为载体制备了TiO2-Cu[HgI4]纳米复合材料,利用HRTEM、XRD、DSC、UV-Vis等方法对该材料的结构及其热致变色性能进行了研究。研究表明,TiO2-Cu[HgI4]纳米复合材料具有较好的热致变色性能,随着nTiO2/nCu[HgI4]摩尔比值的增大,其可见光吸收性能增强,相变温度也相应升高。
TiO2;Cu[HgI4];纳米复合材料;热致变色性能
0 前 言
热致变色是指一种材料受到温度变化时,其颜色发生明显改变的现象。热致变色材料一般可以分为可逆热致变色材料和不可逆热致变色材料[1]。1871年Houston第一次观察到CuI的热致变色现象,从20世纪80年代以来,热致变色材料的研究范围越来越广泛,其类型主要分为无机类和有机类,其中无机类主要为无机金属氧化物及其配合物,如:VO2、Ag2HgI4等;有机类主要包括:有机物、聚合物和生物大分子等[2,3]。目前研究较多的为荧烷类、三芳甲烷类[4]和席夫碱类[5]化合物,而关于无机类金属配合物研究的报道较少。
利用无机低温可逆热致变色材料具有颜色随温度变化改变的特性,用于商标、封签、票据的化学防伪。此外,在工业方面主要用于化工生产中热交换器、反应釜和其它加热装置等温度指示。有机类可逆热致变色材料制备的可逆示温涂料可用于建筑行业,建筑物颜色会随季节的变化而改变;将其微胶囊化后制作变色服装,可显示环境温度[6]。
无机金属配合物 Cu[HgI4]具有可逆热致变色特性,常温为红色,相变温度为71℃,晶型随温度变化时伴随颜色的变化[7]。由于其热稳定性和光学性能相对较差,主要用于一些中低温工业生产中的温度标示,在其他方面的研究和应用鲜有报道。因此,探寻提高可逆热致变色材料 Cu[HgI4]的热稳定性和光学性能是拓展其应用的关键。
纳米材料复合化是现代材料研究的发展趋势,不同材料的复合可以显著改变材料的结构和性能。TiO2的化学性质稳定、光电化学性能优良,且无毒无害[8,9]。由于纳米TiO2能与其担载的材料产生“材料-载体相互作用”,促进材料在其表面高度分散,改善材料的表面结构和性能,因此受到复合材料研究的追捧[10,11]。采用TiO2和不同的材料复合,可拓展其性能[1,12,13]。Fujishima和Tatsuma等[14-16]制备了TiO2-WO3复合薄膜,该材料表现出良好的储能性能。郑金玉等[17]将不同结构Ag掺杂的TiO2与VO2复合,可改变复合结构薄膜的热致变色性能。
本文以TiO2为载体,制备TiO2-Cu[HgI4]热致变色复合材料,并采用HRTEM、XRD、DSC、UV-Vis等手段研究了TiO2-Cu[HgI4]纳米复合材料的结构及其热致变色性能。
1 实验部分
1.1 Cu[HgI4] 的制备
取1.6680 g Hg(NO3)2·0.5H2O溶于50 mL的超纯水中,搅拌下滴加1 mol/L的HNO3溶液至完全溶解,然后滴加4wt% KI溶液至生成橙色沉淀,继续滴加KI溶液直至沉淀消失,溶液呈透明的淡黄色,在磁力搅拌下滴加5wt% Cu(NO3)2溶液,直至生成最大量的沉淀,静置后倾去上层清液,沉淀用去离子水洗2~3次,再用无水乙醇洗2次,在70℃下干燥12 h。
1.2 TiO2-Cu[HgI4] 纳米复合材料制备:
取1.6680 g Hg(NO3)2·0.5H2O溶于50 mL的超纯水中,滴加1 mol/L的HNO3溶液,搅拌至完全溶解,滴加4wt% KI溶液至生成橙色沉淀,继续滴加KI溶液直至沉淀消失,溶液呈透明的淡黄色,在此溶液中加入P25型TiO2搅拌2 h,使其充分混合,得淡黄色TiO2悬浊液。将制备好的TiO2悬浊液在磁力搅拌下滴加5wt%Cu(NO3)2溶液,直至溶液完全变为桔红色,静置分离,得到的桔红色沉淀用去离子水洗2~3次,再用无水乙醇洗2次,抽滤,在70℃下干燥12 h后,即得TiO2-Cu[HgI4]纳米复合材料,通过添加不同量的TiO2得到TiO2-Cu[HgI4]纳米复合材料(nTiO2/nCu[HgI4]=1、2.5)。
1.3 纳米复合材料的表征
1.3.1 HRTEM
采用日本电子公司生产的JEM-2100F型高分辨透射电子显微镜(High-resolution transmission electron microscopy, HRTEM)观察纳米复合材料的结构。加速电压为200 kV。
1.3.2 XRD分析
采用X'Pert Pro MPD型多晶粉末X射线衍射仪(荷兰帕纳科公司)进行物相分析。K=0.154 06 nm铜靶,工作电压和电流分别为40 kV和200 mA,采用5℃/min的升温条件进行物相扫描。
1.3.3 DSC分析
采用德国耐驰 STA449F3型同步热分析进行热力学性能分析。称取25 mg样品,以100 mL/min干燥空气为动态载气,以10 K/s的速率升温,在室温至150℃条件下进行测试。
1.3.4 UV-Vis分析
采用美国 PERKINELMER公司的 Lambda750紫外/可见/近红外分光光度计进行光吸收特性分析。称取适量样品,与KBr混合后压制成片,在室温至90℃、波长200~800 nm(波长精度± 0.15 nm)条件下进行测试。
2 结果与讨论
2.1 HRTEM
图1为nTiO2/nCu[HgI4]=2.5样品的高分辨透射电子显微镜照片。由图1 A可以看出,Cu[HgI4]纳米颗粒(深色颗粒)均匀地分散在TiO2纳米颗粒(浅色颗粒)表面上,TiO2颗粒的粒径为11~33 nm,Cu[HgI4]颗粒的粒径为2~6 nm。在其高分辨照片图1B中,浅色区域TiO2的晶面间距为0.32 nm,对应金红石相TiO2的(110)晶面;而深色区域Cu[HgI4]的晶面间距为 0.22 nm,对应四方晶相 Cu[HgI4]的(205)晶面。由此可见,TiO2与Cu[HgI4]的晶面紧密接触,形成了较好的复合结构。
2.2 物相分析
图2为室温下不同比例样品的XRD谱图。由XRD图可以看出,Cu[HgI4]的特征吸收峰为 2θ=14.4°、16.4°、21.7°、29.4°、33.9°、40°、60°和67.2°,TiO2中锐钛矿相(anatase)的特征吸收峰为 2θ=24.9°、37.5°、48.1°、53.7°、54.8°和62.7°,金红石相(rutile)的特征吸收峰为2θ=27.2°、35.9°、41.1°和53.7°。谱图a~c表明,随着TiO2添加比例的不同,复合样品的特征吸收峰相较于 Cu[HgI4]有所偏移,这说明TiO2与Cu[HgI4] 二者不是单纯的混合,而是形成一种紧密的复合结构。
图3为nTiO2/nCu[HgI4]=1时热致变色复合物的XRD变温谱图。从图中可以看出,在30℃~70℃范围内热致变色复合物的吸收峰随着温度的升高无明显变化,当温度高于70℃时,XRD吸收峰发生明显变化,2θ=16.2°、26.2°、33.75°、40°和45.3°的吸收峰完全消失,以上结果表明热致变色复合物在低于 70℃时,结构无明显改变,当温度大于70℃,热致变色复合物发生了相变,结构发生了显著改变,这也与热致变色单体Cu[HgI4] 在温度大于70℃时发生相变的结论一致。
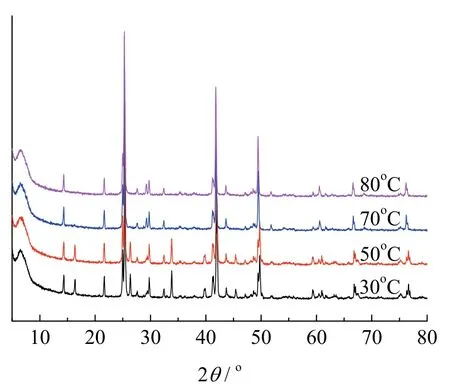
图3 nTiO2/nCu[HgI4]=1时的XRD变温谱图Fig. 3 XRD temperature spectra of nTiO2/nCu[HgI4]=1
图4为不同比例nTiO2/nCu[HgI4]样品的DSC曲线。由图可以看出程序升温过程中,热致变色单体Cu[HgI4] 在71.9℃时,晶形发生改变,由四方晶系转变为立方晶系,有一个明显的热量吸收峰,与理论值基本一致;复合物的相转变温度均高于单体Cu[HgI4] 的相转变温度 71.9℃,说明 TiO2和Cu[HgI4] 形成了较为稳定的复合结构,使得Cu[HgI4] 发生晶形转变的难度加大,需在较高的温度下发生晶型转变;样品 nTiO2/nCu[HgI4]=1的相转变温度为73.3℃,样品nTiO2/nCu[HgI4]=2.5的相转变温度为 74.6℃,该结果表明热致变色复合物随着TiO2与Cu[HgI4] 摩尔比值增大,TiO2-Cu[HgI4]纳米复合材料的结构更加紧密,热稳定性增强。随着TiO2的增加,Cu[HgI4] 相转变过程受到阻碍,从而使得相转变温度升高。

图4 不同比例样品的DSC曲线Fig. 4 DSC Curves of samples in different proportions
2.3 热致变色性能
图5为不同样品的紫外-可见吸收光谱,从图中可以看出,TiO2在紫外光区(200~400 nm)具有较强的吸收峰,在可见光区(400~800 nm)无明显的吸收峰;而 Cu[HgI4]在紫外和可见光区的吸光性能较弱。相对 TiO2和 Cu[HgI4]单体,复合后的TiO2-Cu[HgI4] 纳米材料可见光吸收性能增强,且随着nTiO2/nCu[HgI4]比例的增大,可见光吸收性能明显增强。以上说明,TiO2和Cu[HgI4]形成了良好的复合结构,该结构扩大了对可见光的响应范围,且随着nTiO2/nCu[HgI4]比例的增大,二者形成更紧密复合结构,在可见光区的吸收性能也相应增强。

图5 不同比例样品的UV-Vis吸收光谱Fig. 5 UV-Vis absorption spectra of samples in different proportions
图6为nTiO2/nCu[HgI4]=2.5样品的变温紫外-可见吸收光谱,如图所示,随着温度的升高,热致变色复合材料在紫外光区(200~400 nm)吸收性能略有增强,在570~750 nm范围内有明显的特征吸收峰,随着温度的升高其吸收峰位置发生红移,颜色由红色转变为棕黑色。当温度为80℃时,其吸收峰从570 nm红移至617 nm,这说明了Cu[HgI4] 在温度升高后(> 71℃)发生了晶形转变,由四方晶系向立方晶系转变,与理论相符[7]。温度降至室温后,材料的紫外光区吸收曲线与相变前的曲线吻合,颜色由棕黑色变为红色,说明 Cu[HgI4]相变过程具有可逆性,温度降低,Cu[HgI4]由立方晶系转变为四方晶系。

图6 nTiO2/nCu[HgI4]=2.5变温UV-Vis吸收光谱Fig. 6 UV-Vis absorption spectra of nTiO2/nCu[HgI4]=2.5 at different temperature
由表1可知,样品加热至80℃后,随着复合材料中TiO2和Cu[HgI4] 二者摩尔比例的增大,相变特征吸收峰位置发生蓝移,以上现象说明复合后TiO2和Cu[HgI4]之间产生较好的复合结构,热稳定性增强,随着 TiO2比例的增大,TiO2颗粒的表面能及表面结合能增大,更易于和Cu[HgI4] 相结合而稳定下来。

表1 纳米复合材料及单体的UV-Vis吸收光谱Table 1 UV-Vis absorption spectra of nanocomposites and monomer
图7为不同温度下样品Cu[HgI4]和nTiO2/nCu[HgI4]=2.5的实物照片,由图中可以看到,当温度从 25℃升至 80℃后,Cu[HgI4]和nTiO2/nCu[HgI4]=2.5的样品均出现热致变色现象,颜色由红色变为棕黑色;同时,通过在相同温度下两个样品的实物对照还发现,虽然热致变色前后Cu[HgI4]和nTiO2/nCu[HgI4]=2.5两个样品的颜色均为红色和棕黑色,但是复合后nTiO2/nCu[HgI4]=2.5样品的颜色有了改变,相对较深。该现象也说明TiO2和Cu[HgI4]分子之间产生结合价键,形成了复合结构。

图7 不同温度下样品Cu[HgI4]和nTiO2/nCu[HgI4]=2.5的照片Fig. 7 Pictures of Cu[HgI4] and nTiO2/nCu[HgI4]=2.5 under different temperature
2.4 讨 论
可逆热致变色单体 Cu[HgI4] 室温下属四方晶系,呈红色;当温度高于71℃ 时,其结构向立方晶系转变,呈棕黑色,其晶型转化过程如图8所示。

图8 Cu[HgI4]晶型转化示意图Fig. 8 Crystal transformation diagram of Cu[HgI4]
当 TiO2和 Cu[HgI4]形成TiO2-Cu[HgI4]纳米复合材料后,表现出较好的热稳定性,相变温度升高。这可能是Cu[HgI4]单体以[Cu2+-I--Hg2+]结构存在,而在TiO2和Cu[HgI4] 两者的复合界面上,TiO2颗粒具有较高的比表面积,Cu[HgI4]单体和TiO2在分子水平上结合,即[O2--Ti4+]与[Cu2+-I--Hg2+]之间形成分子键,如图 9,从而使单体结构更加稳定,而且随着TiO2比例的增大,这种分子键的数量也增多,Cu[HgI4]单体结构的稳定性进一步增大。
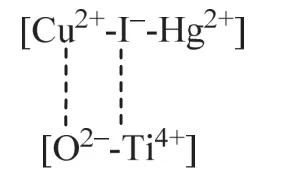
图9 TiO2-Cu[HgI4]纳米复合材料分子键Fig. 9 Molecular bond of TiO2-Cu[HgI4] nanocomposite
3 结 论
以 TiO2为载体制备了 TiO2-Cu[HgI4]纳米复合材料,纳米复合材料具有较好的热致变色性能,随着nTiO2/nCu[HgI4] 摩尔比值的增大,其可见光吸收性能增强,相变温度也相应升高。
[1] Chen S, Paulose M. Ruan C, et al. Electrochemically synthesized CdS nanoparticle-modified TiO2nanotubearray photoele-ctrodes: Preparation characterization and application to photoelectrochemical cells[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2006, 177(2): 177-184.
[2] Ahmed M D, El-Zeiny M E. Thermochromism in Ni (Ⅱ) complexes with Schiff base derivatives of 4-aminoantipyrine[J]. Thermochimica Acta., 1988, 131: 1-6.
[3] Tamotsu I, Naomi H. Structure and optical properties of a thermochromic Schiff base. Low temperature structurestudies of the N, N-disalicylidene-p-phenyl endiamine and N, N-disalicylidene-1,6-pyrendiamine crystals[J]. Bull. Chem. Soc. Jpn., 1989, 62: 2245-2251.
[4] Zhu C F, WU A B. Studies on the synthesis and thermochromic properties of crystal violet lactone and its reversible thermochromic complexes[J]. Thermochimica Acta., 2005, 425(1-2): 7-12.
[5] 朱少萍, 冯玉英, 乐传俊, 等. 2-羟基-1-萘醛缩2-氨基-4-甲基吡啶的合成及其热色性研究[J]. 化工新型材料, 2010, 38(11): 81-82.
[6] 梁小蕊, 张勇, 张立春. 可逆热致变色材料的变色机理及应用[J]. 化学工程师, 2009, 164(5): 56-58.
[7] 张慧萍, 李正宇, 李永明, 等. 无机低温热变色材料的研究及应用[J]. 云南师范大学学报, 2000, 20(5):59-61.
[8] Zhu K, Neale N R, Miedaner A, et al. Enhanced charge-collection efficiencies and light scattering in dye-sensitized solar cells using oriented TiO2nanotubes arrays[J]. Nano Letters, 2007, 7(1): 69-74.
[9] Senadeera G, Kitamura T, Wada Y, et al. Enhanced photoresponses of polypyrrole on surface modified TiO2with self-assembled monolayers[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2006, 184(1): 234-239.
[10] Xie T F, Wang D J, Zhu L J, et al. Application of surface photovoltage technique in photocatalysis studies on modified TiO2photo-catalysts for photo-reduction of CO2[J]. Materials chemistry and physics, 2001, 70(1): 103-106.
[11] Surnev S, Ramsey M, Netzer F. Vanadium oxide surface studies[J]. Progress in surface science, 2003, 73(4): 117-165.
[12] Sun W T, Yu Y, Pan H Y, et al. CdS quantum dots sensitized TiO2nanotube-array photoelectrodes[J]. Journal of the American Chemical Society, 2008, 130(4): 1124-1125.
[13] Gao X F, Li H B, Sun W T, et al. CdTe quantum dots-sensitized TiO2nanotube array photoelectrodes[J]. The Journal of Physical Chemistry C, 2009, 113(18): 7531-7535.
[14] Ngaotrakanwiwat P, Tatsuma T. Optimization of energy storage TiO2-WO3photocatalysts and further modification with phosphotungstic acid[J]. Journal of Electroanalytical Chemistry, 2004, 573(2): 263-269.
[15] Takahashi Y, Ngaotrakanwiwat P, Tatsuma T. Energy storage TiO2-MoO3photocatalysts[J]. Electrochimica acta, 2004, 49(12): 2025-2029.
[16] Tatsuma T, Saitoh S, Ngaotrakanwiwat P, et al. Energy storage of TiO2-WO3photocatalysis systems in the gas phase[J]. Langmuir, 2002, 18(21): 7777-7779.
[17] 郑金玉, 吴梁鹏, 王学伟, 等. 紫外光下Ag掺杂TiO2薄膜基底对 VO2相转变温度的影响[J]. 新能源进展, 2014, 2(1): 59-62.
Preparation of TiO2-Cu[HgI4] Nanocomposite and Its Thermochromic Performance
CHEN Xiao-li, LIN Fu-hua, WEN Chun-yan, SU Qiu-cheng, LI Xin-jun
(CAS Key Laboratory of Renewable Energy, Guangzhou Institute of Energy Conversion, Chinese Academy of Sciences, Guangzhou 510640, China)
TiO2-Cu[HgI4] nanocomposite was synthesized by using TiO2as carrier. HRTEM, XRD, DSC and UV-Vis were employed to characterize the structure and investigate the thermochromic performance of the nanocomposite. Results indicate that TiO2-Cu[HgI4] nanocomposite has good thermochromic performance. The visible light absorption is strengthened with the increase of nTiO2/nCu[HgI4] mole ratio, and the phase transition temperature rises accordingly.
TiO2; Cu[HgI4]; nanocomposites; thermochromic performance
TK01
A
10.3969/j.issn.2095-560X.2014.04.011
2095-560X(2014)04-0310-05
陈晓丽(1978-),女,博士,高级工程师,主要从事分析测试技术研究。
2014-05-05
2014-07-07
国家自然科学基金(51172233)
† 通信作者:李新军,E-mail:lixj@ms.giec.ac.cn
李新军(1967-),男,博士,研究员,主要从事能量转换材料、环境功能材料研究。

