复配型席夫碱缓蚀剂对碳钢在海水中缓蚀性能研究
刘 进,刘 峥,谢思维,刘宝玉
(桂林理工大学 化学与生物工程学院,广西 桂林 541004)
海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源[1]。加强对海水资源的开发利用,是解决沿海地区淡水危机和资源短缺问题的重要措施[2],是实现国民经济可持续发展战略的重要保证。然而,海水是一种含有多种盐类的电解质溶液,以3%~3.5%的氯化钠为主盐,pH为8左右,并溶有一定量的氧气。除了标准电极电位很低的镁及其合金外,大部分金属材料在海水中都存在氧去极化腐蚀。缓蚀剂(Corrosion inhibitor)是具有抑制金属腐蚀功能的一类无机物质和有机物质的总称[3]。在腐蚀环境中投入少量的这种化学物质就能有效地阻止或减缓金属的腐蚀速度。缓蚀剂的优点在于使用方便、投加量少、见效快、成本较低,目前已广泛应用于石油化工、化肥、钢铁机械运输、动力等部门。海水缓蚀剂的发展经历了从无机到有机,从单一到复配,从单一抑制型到混合抑制型以及与其他电化学方法的联用的历程,并且突出低毒无害、环保绿色、高效持久的理念[4-7]。本课题组在前期研究中制备了水杨醛类吡啶甲酰腙席夫碱缓蚀剂、水杨醛类脱氢枞胺席夫碱缓蚀剂,结果表明这两类席夫碱缓蚀剂对在海水介质中的碳钢有明显的缓蚀作用[1]。本文根据低毒环保高效的复配缓蚀剂设计思路,结合课题组前期的研究成果和相关的文献[8-12],选择邻氧乙酸苯甲醛-4-吡啶甲酰腙席夫碱、脱氢枞胺邻香草醛席夫碱、ZnSO4、Tween-80进行复配,通过研究确定了缓蚀剂使用的临界浓度,同时探讨了复配型席夫碱缓蚀剂在不同盐度、不同温度、不同流速海水中对碳钢的的缓蚀性能以及对有锈试样和间浸试样在海水中的缓蚀性能,重点考察了复配型席夫碱缓蚀剂实际应用的可能性。
1 实验方法
1.1 主要材料、试剂
实验试样材料为低碳钢。实验中所用试样的尺寸为2.0 cm×2.0 cm×0.2 cm,使用前用120目、600目和1200目水砂纸逐级打磨至光亮,然后用去离子水充分洗涤,再用丙酮除油后干燥备用。失重实验时用环氧树脂密封非工作面,使钢板的工作面积均为2.0 cm×2.0 cm;电化学测试时,试样保留1.0 cm×1.0 cm的工作面,其余用环氧树脂密封。
腐蚀介质为人工海水按文献[13-14]配制。
复配缓蚀剂配方组成为: 邻氧乙酸苯甲醛-4-吡啶甲酰腙席夫碱(记为L3)80 mg/L,邻香草醛脱氢枞胺席夫碱(记为M3)6 mg/L,ZnSO450 mg/L,Tween-80 100 mg/L。
1.2 失重法
失重实验参照国家标准GB10124-88执行[15]。选取干燥备用的 3组实验碳试样在分析天平上准确称量,将碳钢试样分别浸入到含有不同浓度缓蚀剂的海水和空白海水的100 mL的烧杯中,浸泡240 h(期间要用用去离子水定期补充损失掉的水分,保持海水盐度不变)后取出,去离子水洗涤、无水乙醇脱水、去除环氧树脂、丙酮洗涤、干燥8 h后称重。计算三组平行实验的平均失重量,所研究的复配型席夫碱缓蚀剂在海水介质中对碳钢的缓蚀率IE按下面的公式进行计算[15]:
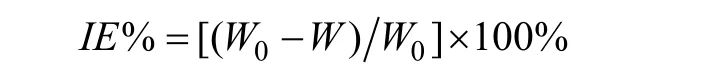
W0为空白海水碳钢失重量(g);W为添加有不同浓度缓蚀剂的海水碳钢失重量(g)。
利用失重法测定有锈碳钢试样在添加不同浓度复配缓蚀剂,在海水中的缓蚀性能评价方法: 三组平行的碳钢试样(每组有 6个碳钢试样)浸入空白海水中腐蚀 216 h后,将其中一组平行样取出,除锈并称重,计算出腐蚀 216 h的失重量。然后将其余的平行试样(现在已经是有锈试样)分别浸入到空白海水和5个添加有不同浓度复配缓蚀剂海水中继续腐蚀288 h,然后取出,除锈并称重,有锈试样的失重量等于试样总的失重量减去前 216 h的失重量,以此计算出两组试样的平均失重量和各浓度下的缓蚀率。
利用失重法测定间浸碳钢试样在添加不同浓度缓蚀剂在海水中的缓蚀性能评价方法: 三组平行的碳钢试样分别被浸泡到空白海水和添加有不同浓度缓蚀剂的海水中腐蚀20 h后,取出暴露在空气中4 h。然后再浸泡20 h后,取出暴露4 h,如此往复。实验中浸泡时间︰暴露时间为5︰1。腐蚀循环周期为24 h,总循环时间为192 h,最后计算三组试样的平均失重量和各缓蚀率。
1.3 电化学方法
电化学测试在上海辰华仪器有限公司生产的CHI660c型电化学工作站上进行,实验采用三电极体系,铂电极为辅助电极,饱和甘汞电极为参比电极,所有实验都在室温下进行。
Tafel 极化曲线测试前,将工作电极浸入到海水介质中 30 min,直至自腐电位稳定,然后设定电位扫描范围为: Ecorr±300 mV,扫描速度是1 mV/s。极化曲线数据由系统自动收集,并用系统自带的软件进行拟合和计算。缓蚀率IE用如下公式进行计算[15]:
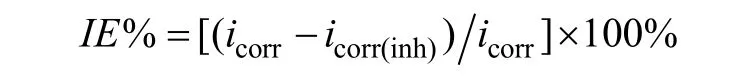
icorr为空白海水中的腐蚀电流密度 (μA/cm2);icorr(inh)为加入缓蚀剂后海水中的腐蚀电流密度 (μA/cm2)。
交流阻抗测试前,将工作电极浸入到海水介质中 30 min,直至开路电位稳定,然后设定扰动电位为5 mV,频率范围为0.01~100 000 Hz。实验所收集的数据用 ZSimpWin 3.21软件进行拟合和计算,缓蚀率IE用如下公式进行计算[16]:
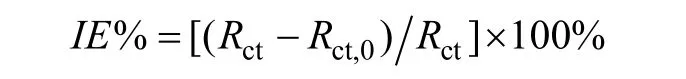
Rct,0为空白海水中的极化电阻(Ω·cm2);Rct为加入缓蚀剂后海水中的极化电阻(Ω·cm2)。
2 结果与讨论
2.1 复配缓蚀剂临界浓度的确定
图1为碳钢在添加不同浓度的复配缓蚀剂海水中的缓蚀效果,从图中可以看出,当浓度低于143 mg/L时,缓蚀率随浓度的增加直线上升趋势,但是,当缓蚀剂的添加浓度大于143 mg/L时,缓蚀率随浓度的变化并不明显,据此,可以确定缓蚀剂的临界浓度为 143 mg/L,此时,复配缓蚀剂对碳钢在海水中的缓蚀率为96.20%。
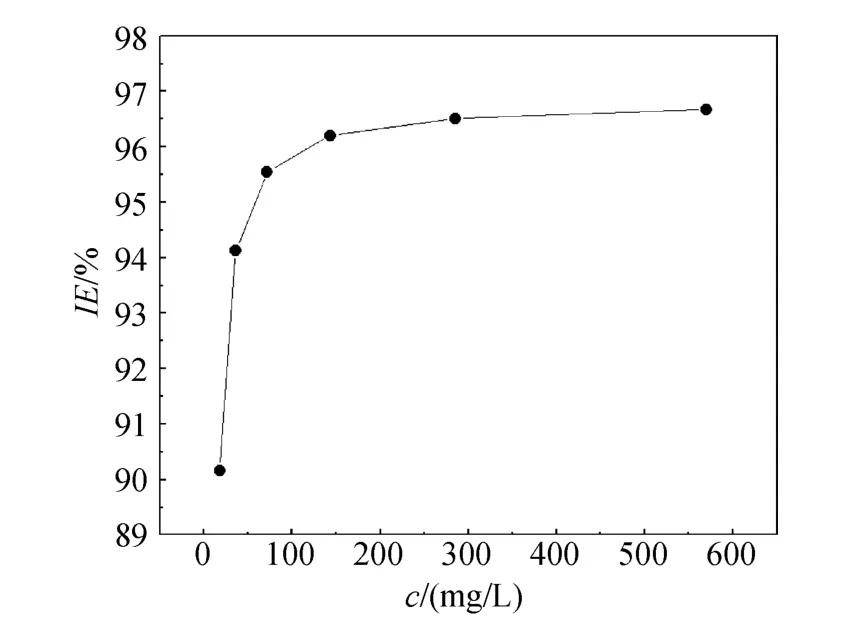
图1 碳钢在添加不同浓度复配缓蚀剂海水中的缓蚀效果Fig.1 Inhibition efficiency of mild carbon steel in seawater in the presence of various concentrations of compound inhibitor
2.2 复配型缓蚀剂在不同盐度海水中对碳钢的缓蚀效果
碳钢试样在添加不同浓度复配缓蚀剂的不同盐度的海水中的缓蚀性能被测试,结果见图2。图2中当缓蚀剂在低浓度时,对不同盐度海水中碳钢的腐蚀均有良好的抑制作用,复配型缓蚀剂在自来水中的浓度为18 mg/L时,对碳钢的缓蚀率为88.06%,而对盐度为15的稀释海水中碳钢的缓蚀率为90.51%。这是因为盐度的不同引起了海水中溶解氧的变化,自来水中盐度很低,溶解氧比较大,阴极的去极化反应速率大,所以腐蚀速率较大。
一般情况下,盐度的变化会引起的腐蚀介质中有害离子(如 Cl-)的变化和溶解氧的变化,这将会影响碳钢在海水中的腐蚀反应速率,观察图2,腐蚀介质的盐度从自来水(S=0)变化到浓缩海水(S=52),复配缓蚀剂的添加浓度由18 mg/L升高到285 mg/L,缓蚀率的变化却不大。这说明该复配缓蚀剂在低浓度就可以有效抑制碳钢的腐蚀反应,它受海水盐度的影响较小。
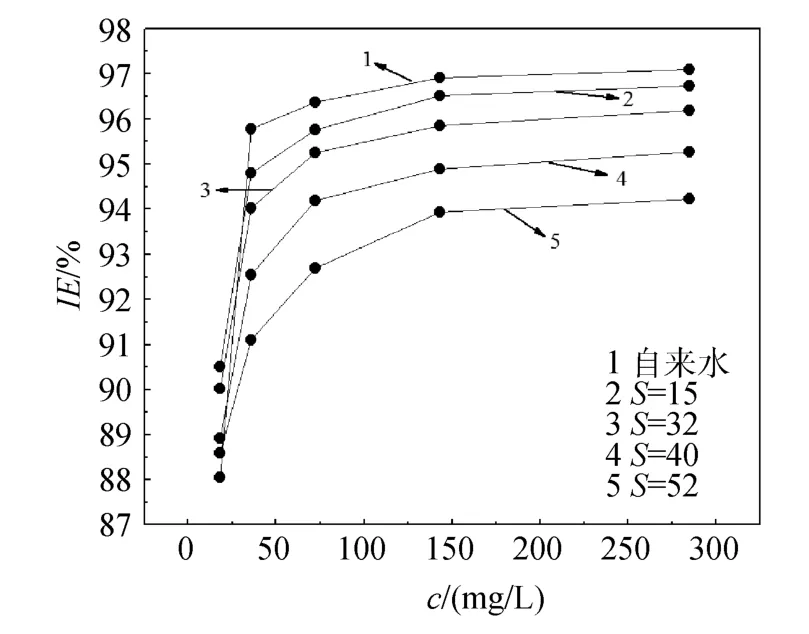
图2 复配缓蚀剂对碳钢在不同盐度海水中的缓蚀效果Fig.2 The inhibition effect of mild carbon steel in seawater with different salinity in the presence of compound inhibitor
2.3 复配缓蚀剂在不同温度海水中对碳钢的缓蚀效果
在不同温度下,用电化学交流阻抗技术测试了碳钢在添加143 mg/L复配缓蚀剂的海水中的缓蚀效果,用图5所示等效电路来拟合数据,拟合后的电化学参数: Rct(电荷转移电阻),Rs(参比电极到工作电极的溶液电阻),A(CPE常相位角元件常数),n(弥散指数),Cdl(双电层电容),τ(控制电流测量时间常数)见表1,相应空白海水和添加有缓蚀剂海水的奈奎斯特图见图3和图4。从表1可以看出,缓蚀剂添加浓度一定时,海水的温度不同,缓蚀剂对碳钢的缓蚀效果不同,随着海水温度的升高,缓蚀率降低。在温度一定时,与空白海水相比,加入缓蚀剂的海水,电荷转移电阻 Rct显著增大,这表明复配缓蚀剂抑制了碳钢在海水中的腐蚀反应。
图3表明空白海水中,电荷转移电阻 Rct较小,说明腐蚀比较严重,随着海水温度的升高,Rct逐渐减小,这说明温度的升高,加速了溶液中离子的运动速度,增强了有害离子的活性,使腐蚀反应进一步加剧,但是,当温度达到 60℃时,Rct又增大了,这说明温度的升高使的海水中溶解氧的量减小,并且当温度达到60℃时,阴极氧的去极化反应减弱,在一定程度上抑制了腐蚀反应的进行,使的Rct再度升高。
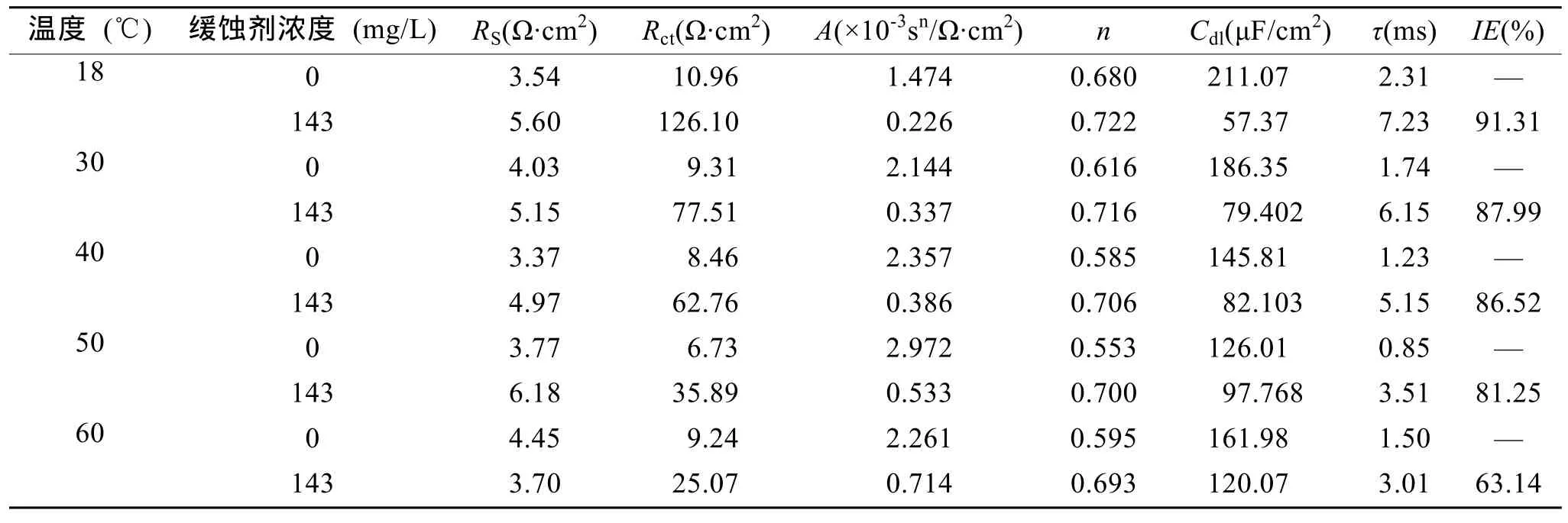
表1 碳钢在不同温度海水中的电化学交流阻抗数据Tab.1 The electrochemical parameters of EIS for mild carbon steel in seawater with different temperatures
图4中在添加 143 mg/L复配缓蚀剂的海水中,Rct随着温度的升高而减小,这说明温度的升高,使水中有害离子活性增大的同时,也使已在碳钢表面形成的保护膜变得不牢固。当温度达到 60℃时,Rct减低到 25.97Ω·cm2,这说明温度升高阻止了缓蚀剂分子在碳钢表面的吸附,当能量超过吸附能后,缓蚀剂便开始脱落,使得Rct急速降低。
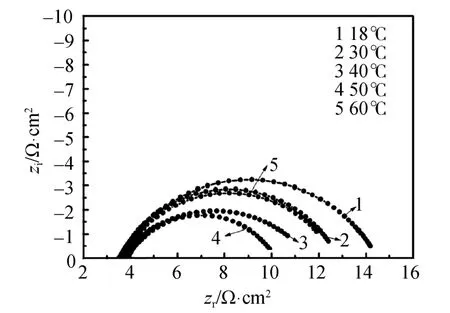
图3 碳钢在不加缓蚀剂的不同温度海水中的奈奎斯特图Fig.3 Nyquist plots of mild carbon steel in seawater with different temperatures in the absence of inhibitor
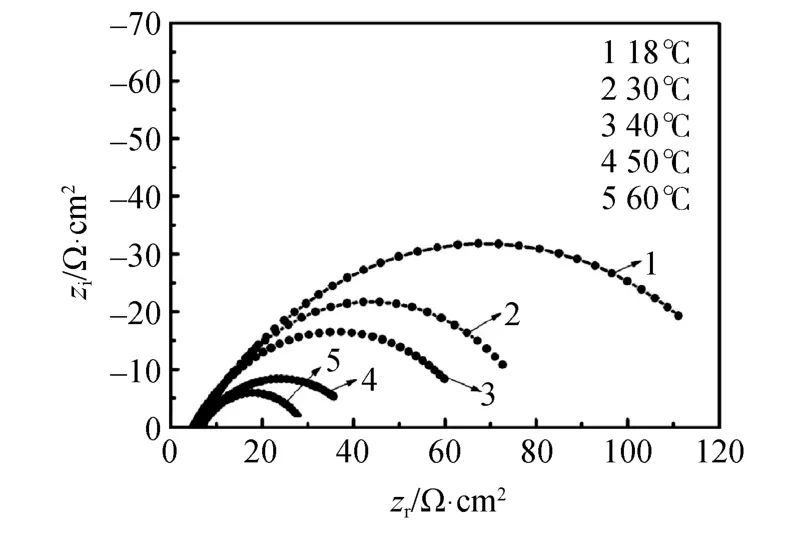
图4 碳钢在添加 143 mg/L复配缓蚀的不同温度海水中的奈奎斯特图Fig.4 Nyquist plots of mild carbon steel in seawater with different temperatures in the presence of 143 mg/L compound inhibitor
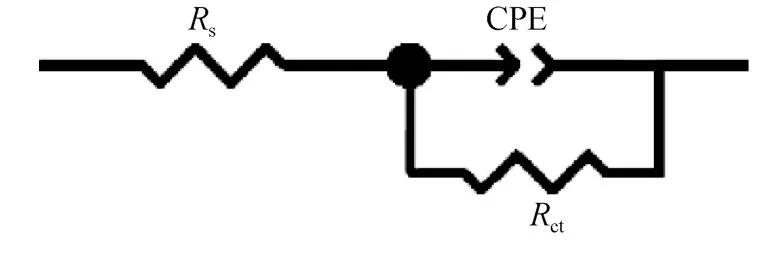
图5 阻抗拟合的等效电路图Fig.5 The equivalent circuit model for impedance fitting
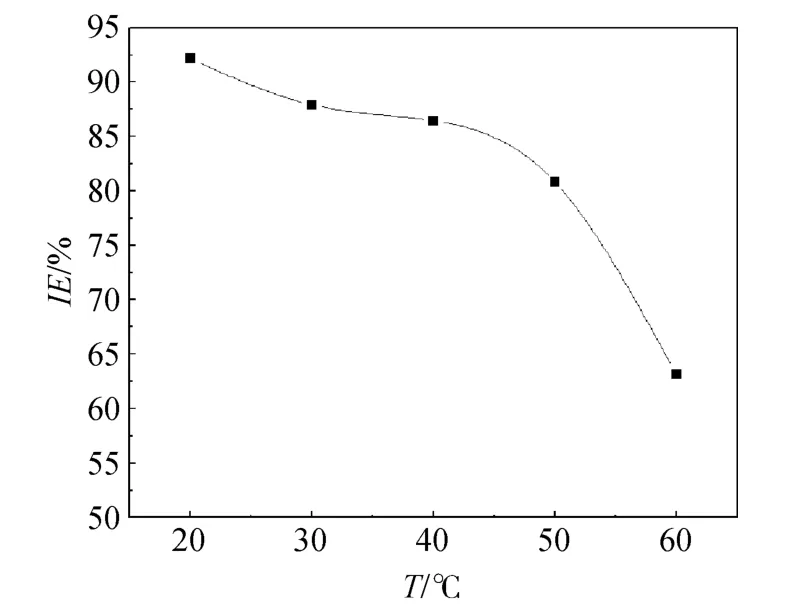
图6 碳钢在添加143 mg/L复配缓蚀剂的不同温度海水中的缓蚀效果Fig.6 The inhibition effect of mild carbon steel in seawater with different temperatures in the presence of 143 mg/L compound inhbitor
碳钢在添加临界缓蚀剂浓度 143 mg/L的海水中,缓蚀率随海水温度变化的关系见图6。从图6可以看出,当海水温度低于 50℃时,缓蚀剂对碳钢有很好的保护作用,缓蚀率都在 80%以上,且缓蚀率在温度达到30℃后出现一个平台,温度超过40℃后缓蚀率继续减小,当海水温度超过 50℃后,缓蚀率呈急剧下降趋势,在海水温度达到 60℃时,缓蚀剂的缓蚀率仅为 63.14%。这是由于温度升高,抑制了缓蚀剂在碳钢表面吸附。当温度低于 50℃时,缓蚀剂分子可在碳钢表面牢固吸附,这时缓蚀率下降并不明显。当温度再升高时,吸附过程的吸附能增大,这时缓蚀剂分子的吸附变的较为困难。所以,当温度超过50℃时,该复配缓蚀剂对碳钢腐蚀的抑制效果并不好。
2.4 复配缓蚀剂在不同流速海水中对碳钢的缓蚀效果
在不同流速海水中,用电化学极化曲线研究了复配缓蚀剂对碳钢的缓蚀效果(复配缓蚀剂的添加浓度为临界浓度 143 mg/L),实验结果见表2。空白海水中的极化曲线和添加 143 mg/L 复配缓蚀剂的海水中的极化曲线分别见图7和图8。从表2可以看出,与空白海水相比,在相同流速的海水中,加入缓蚀剂后腐蚀电流Icorr显著减小,这说明复配缓蚀剂在临界浓度时能有效抑制碳钢的腐蚀反应。但对于不同流速的海水,这种抑制作用并不相同,在静止的海水中Icorr(inh)为45.81 μA/ cm2,在控制海水流动的转速为1 125 r/min的海水中 Icorr(inh)为400.65 μA/cm2,这说明流动的海水削弱了缓蚀剂对碳钢腐蚀的抑制作用,使腐蚀电流密度增加。
图7表明在空白海水中腐蚀电位随着海水流速的增加逐渐的向负方向移动,这说明海水流速的变化,引起了阳极金属溶解反应和阴极去极化反应速率的变化,随着流速增大海水中阳极溶解反应的速率大于阴极去极化反应速率,从而使得腐蚀电位负移。同样的结果可以在图8中被观察到,图中腐蚀电位也随着海水流速的增加,向负方向移动,但是移动的幅度并没有空白海水中那么大,这说明缓蚀剂在流动的海水中仍能抑制阳极的溶解反应。
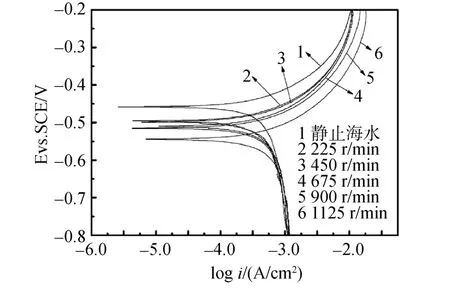
图7 碳钢在不加缓蚀剂的不同流速海水中的极化曲线Fig.7 Polarization curves of mild carbon steel in seawater with different velocity in the absence of inhibitor
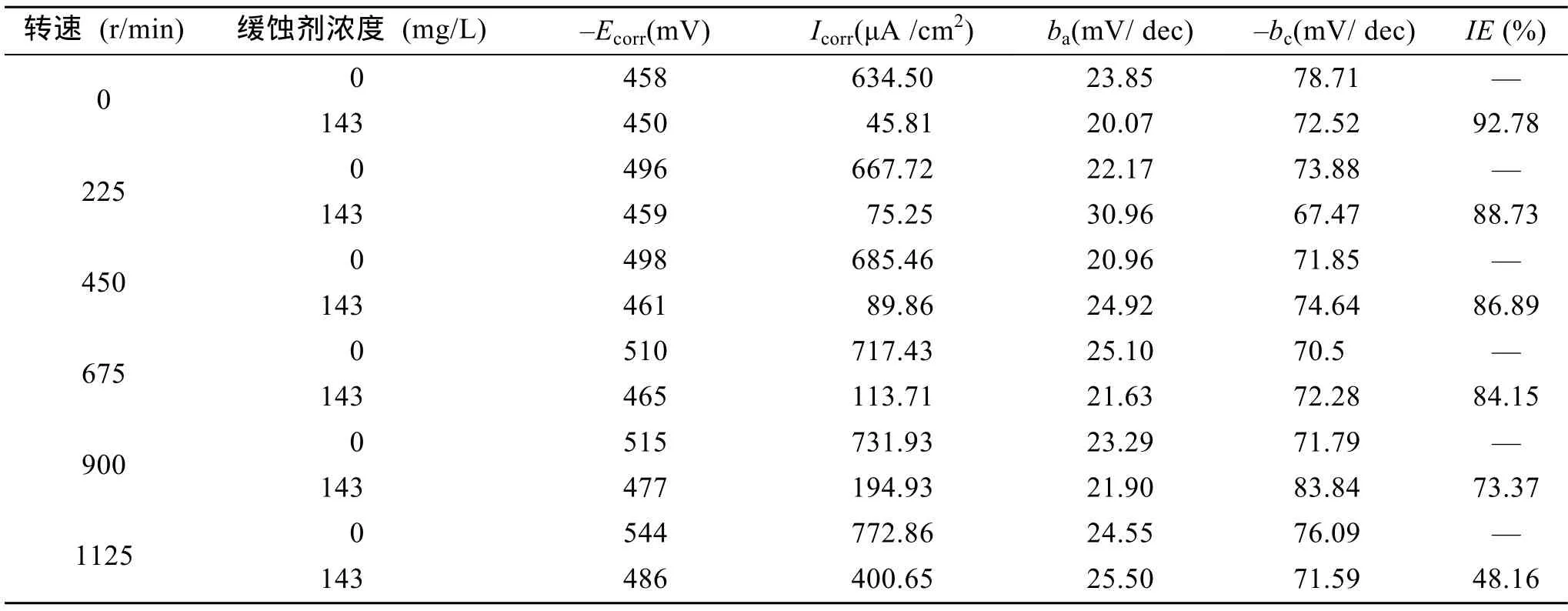
表2 碳钢在不同流速海水中的极化曲线数据Tab.2 Polarization data of mild carbon steel in seawater with different velocity
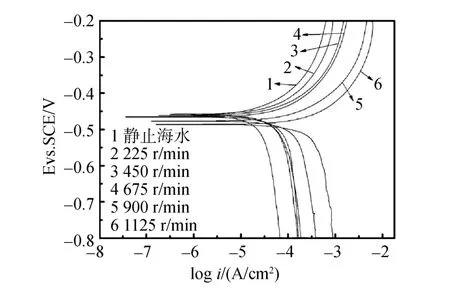
图8 碳钢在添加 143 mg/L 复配缓蚀的不同流速海水中的极化曲线Fig.8 Polarization curves of mild carbon steel in seawater with different velocity in the presence of 143 mg/L compound inhibitor
碳钢在添加临界缓蚀剂浓度143 mg/L的海水中,缓蚀率随海水流速变化的关系见图9。从图中可以看出,缓蚀率随着海水流速的增加而减小,当海水流速较小时,复配缓蚀剂对碳钢有很好的保护作用,缓蚀率都在 80%以上,当海水流速较大时,缓蚀率呈急剧下降趋势。这是因为海水流速的增加,一个方面使得海水中离子的运动速率增大,也就是使得海水中离子的活性增大,最终使得腐蚀反应加剧,另一方面,快速流动的海水能够对碳钢表面形成很大的冲刷力,使得吸附在碳钢表面的缓蚀剂分子脱落,最终使得缓蚀剂对碳钢的腐蚀抑制作用减小。总的来说,该复配缓蚀剂在低流速海水中对碳钢有很好的抑制作用,当流速较大时,缓蚀效果并不好。
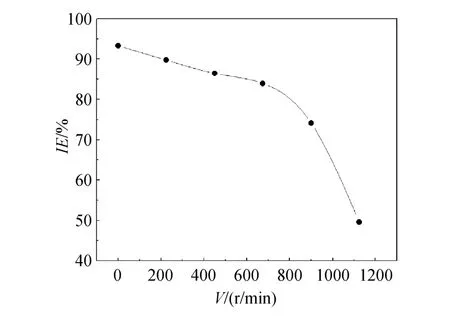
图9 碳钢在添加 143 mg/L复配缓蚀剂的不同流速海水中的缓蚀效果Fig.9 The inhibition effect of mild carbon steel in seawater with different velocity in the presence of 143 mg/L compound inhbitor
2.5 复配缓蚀剂对有锈试样在海水中的缓蚀效果
通过失重法研究了有锈碳钢试样在添加不同浓度复配缓蚀剂海水中的缓蚀效果,实验结果见表 3和图 10。表中数据显示缓蚀率随着缓蚀剂添加浓度的增加而增加,这说明缓蚀剂是通过在碳钢表面吸附,从而抑制了腐蚀反应的活性点来抑制腐蚀的。但缓蚀率与除锈碳钢相比整体下降,尤其是当复配缓蚀剂的添加浓度为18 mg/L时,缓蚀率仅为43.72%,而相同浓度下,除锈碳钢缓蚀率达 90.08%,这说明碳钢表面的铁锈阻止了缓蚀剂在碳钢基体上的成膜过程,缓蚀剂不能像在表面洁净的试样上那样很好的吸附、成膜。这也说明该复配缓蚀剂的渗透能力不强,不能很好的通过表面的锈层在碳钢表面吸附,缓蚀剂先与碳钢表面的铁锈一起混合,然后只有少部分透过锈层吸附在碳钢基体上,所以缓蚀率偏低。
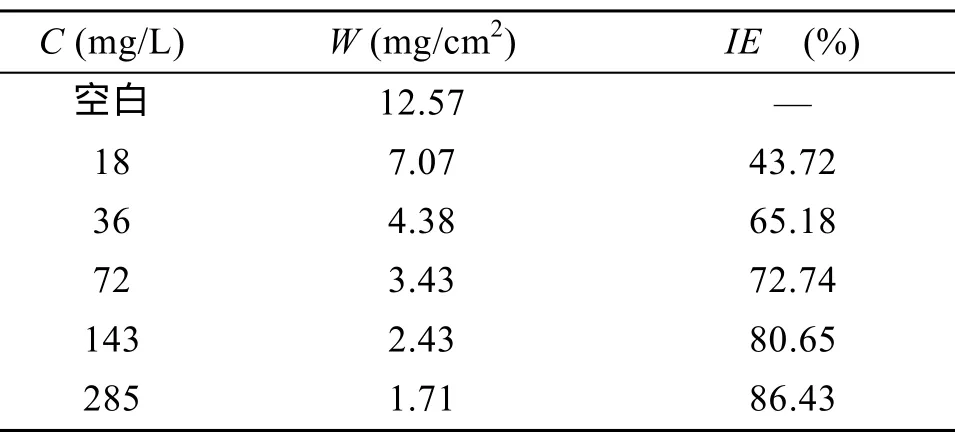
表3 有锈碳钢试样在添加不同浓度复配缓蚀剂海水中的失重实验数据Tab.3 The weight lost experimental data of rusty carbon mild steel samples in seawater withdifferent concentrations of compound inhibitor
从图 10来看,在缓蚀剂低浓度时,缓蚀效果并不好,当缓蚀剂浓度达到 72 mg/L时,缓蚀率才为72.74 %。随着缓蚀剂浓度的增加,缓蚀率逐渐上升,当缓蚀剂浓度达到143 mg/L时,缓蚀率为80.65,这说明缓蚀剂浓度增大时,能够透过锈层进入碳钢基体的缓蚀剂分子数目增大,缓蚀率会相对升高。因此,本复配缓蚀剂在使用时应将被保护材料的表面除锈或增大其使用浓度或与其他防腐手段一起联用才能达到较理想的防腐蚀目的。
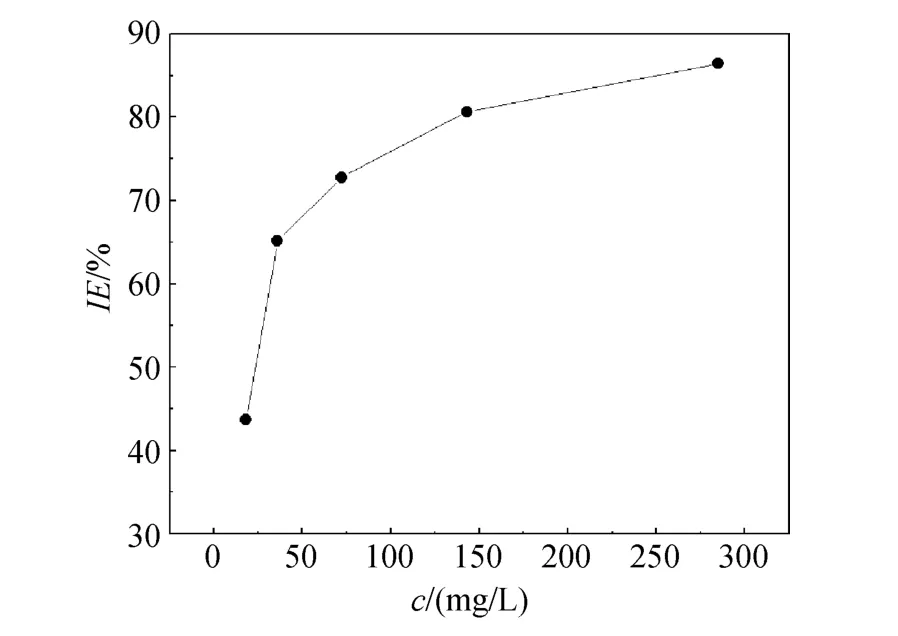
图10 有锈碳钢试样在添加不同浓度复配缓蚀剂海水中的缓蚀效果Fig.10 The inhibition effect of rusty carbon mild steel samples in seawater with various concentrations of compound inhibitor
2.6 复配缓蚀剂对间浸试样在海水中的缓蚀效果
有时候被保护的材料不是一直浸泡在腐蚀介质中,比如潜艇的压水舱,当潜艇上浮时,压舱水被排出,这时压水舱的一部分将会暴露在空气中,当潜艇下沉时,压舱水又被吸入,如此往复使得材料不断处于浸入和暴露的循环过程。又如海上石油转井平台的立柱不断遭受海浪的拍打,使它时而在海水中浸泡,时而又暴露空气中,所以研究碳钢在海水中的间浸缓蚀作用是很有现实意义的。
碳钢试样在添加不同浓度复配缓蚀剂海水中的间浸实验通过失重法被研究,失重实验数据见表 4,相应的缓蚀率随缓蚀剂添加浓度的变化趋势见图11。从表 4可以看出缓蚀率随着缓蚀剂添加浓度的增加而升高,与非浸实验相比,缓蚀率整体下降。这主要是在间浸实验中,碳钢试样经历了干湿交替的环境变化,改变了碳钢表面的盐度和接触氧含量。当碳钢从海水介质中移至空气中暴露时,碳钢表面的水分减少,盐度增加,而且碳钢表面的接触氧含量增大,使得碳钢的腐蚀加剧,缓蚀率下降。
观察图 11可以发现,在缓蚀剂添加浓度低时,碳钢的腐蚀比较厉害,当缓蚀剂添加浓度为72 mg/L时,缓蚀率仅为 78.54,但当缓蚀率添加浓度达到143 mg/L时,缓蚀率变化较为平缓,且缓蚀率都在80%以上,这说明当缓蚀剂浓度增大时,缓蚀剂分子在碳钢表面形成的膜更致密、更厚实,当碳钢试样移出海水暴露在空气中时,吸附在碳钢表面的缓蚀剂就会起到保湿作用,使碳钢表面的盐度不至过高,同时也减少了碳钢表面与空气中氧的接触面积,能够对碳钢的腐蚀起到良好的抑制作用。
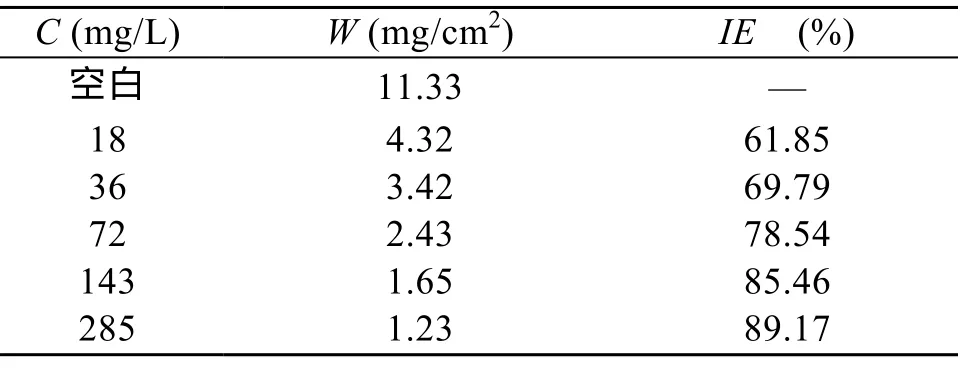
表4 碳钢在添加不同浓度复配缓蚀剂海水中的间浸失重实验数据Tab.4 The interval soak weight lost experimental data of carbon mild steel in seawater with various concentrations of compound inhibitor
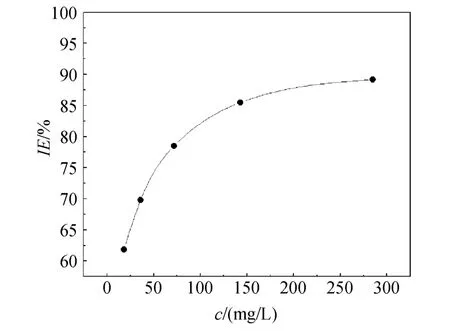
图11 碳钢在添加不同浓度复配缓蚀剂海水中的间浸实验缓蚀效果Fig.11 The inhibition effect of interval soak experiment for carbon mild steel in seawater with various concentrations of compound inhibitor
3 结论
1)控制复配型席夫碱缓蚀剂配方组成为邻氧乙酸苯甲醛-4-吡啶甲酰腙席夫碱 80 mg/L,邻香草醛脱氢枞胺席夫碱6 mg/L,ZnSO450 mg/L,Tween-80 100 mg/L,通过失重法研究了碳钢在添加不同浓度复配缓蚀剂海水中的缓蚀率,最终确定了该复配缓蚀剂的临界浓度为 143 mg/L。
2)复配型席夫碱缓蚀剂受海水盐度影响较小,即使在盐度为 52的海水仍能对碳钢有很好的保护作用。
3)复配型缓蚀剂受海水流速和温度的影响较大,在低流速和低温度海水中,缓蚀效果良好,但是当海水流速较大或海水温度超过 50℃时,缓蚀效果并不好。
4)在有锈实验和间浸实验中,低浓度的缓蚀剂对碳钢腐蚀的抑制作用不佳,但是当复配型缓蚀剂添加浓度达到143 mg/L时,缓蚀率都在80%以上。
[1]李雅芙,陈向峰.浅谈海水化学资源综合利用生产工艺[J].无机盐业,2008,38(4): 11-12.
[2]黄昌硕,徐澎波.我国海水资源的利用模式与发展趋势[J].中国资源综合利用,2008,126(5): 3-5.
[3]皇甫健,侯纯扬,高翔,等.海水中一种曼尼希碱对20#钢缓蚀行为的电化学特征[J].水处理技术,2012,38(10): 54-56,69.
[4]李凌杰,于生海,雷惊雷,等.AZ40镁合金在模拟海水介质中的腐蚀行为[J].重庆大学学报,2008,31(6):701-706.
[5]杨圣和,田惠文,侯保荣,等.海洋环境友好型阻锈剂的筛选和快速评价[J].海洋科学,2012,36(8): 1-8.
[6]李凌杰,于生海,雷惊雷,等.AZ31和AZ61镁合金在模拟海水中的腐蚀电化学行为[J].电化学,2008,14(1): 95-99.
[7]Gopi D,Manimozhi S,Govindaraju K M,et al.Surface and electrochemical characterization of pitting corrosion behaviour of 304 stainless steel in ground water media[J].Jappl Electrochem,2007,37(4): 439-449.
[8]刘峥,刘洁,刘进,等.水杨醛类吡啶甲酰腙席夫碱对碳钢在海水中缓蚀行为的研究[J].中国腐蚀与防护学报,2013,33(2): 109-116.
[9]Amar H,Benzakour J,Derja A,et al.Synergistic corrosion inhibition study of Armco iron in sodium chloride by piperidin-1-yl-phosphonic acid–Zn2+system[J].Corrosion Science,2008,50(7): 124-130.
[10]Li Xianghong,Mu Guannan.Tween-40 as corrosion inhibitor for cold rolled steel in sulphuric acid: Weight loss study,electrochemical characterization,and AFM[J].Applied Surface Science,2005,252(7):1254-1265.
[11]Karpagavalli R,Cairns D R,Rajeswari S.Synergistic inhibition effect of 2-mercaptobenzothiazole and Tween-80 on the corrosion of brass in NaCl solution[J].Applied Surface Science,2008.254(12): 4483-4493.
[12]周建奇,王宏智,马青华,等.海水管路黄铜焊接接头在人工海水中的电化学阻抗谱[J].腐蚀与防护,2007,28(8): 403-406.
[13]王冀恒,谢春生,刘占超,等.高阻尼螺旋桨材料CuAlBe合金在人工海水中耐蚀性能的研究[J].华东船舶学院学报,2004,18(4): 75-77.
[14]Yan Ying,Li Weihua,Cai Lankun,et al.Electrochemical and quantum chemical study of purines as corrosion inhibitors for mild steel in 1M HCl solution[J].Electrochimica Acta,2008,53(7): 5953-5960.
[15]Bentiss F,Gassama F,Barbry D,et al.Enhanced corrosion resistance of mild steel in molar hydrochloric acid solution by 1,4-bis(2-pyridyl)-5H-pyridazino[4,5-b]indole: Electrochemical,theoretical and XPS studies [J].Applied Surface Science,2006,252(8):2684-2691.
[16]Finšgar M,Lesar A,Kokalj A ,et al.comparative electrochemical and quantum chemical calculation study of BTAH and BTAOH as copper corrosion inhibitors in near neutral chloride solution[J].Electrochimica Acta,2008,53(6): 8287-8297.

