莱州湾河流表层沉积物中六溴环十二烷的含量水平、分布及组成特征
刘艺凯, 王景芝, 唐建辉, 于志强, 张 干
莱州湾河流表层沉积物中六溴环十二烷的含量水平、分布及组成特征
刘艺凯1,3, 王景芝2,3, 唐建辉1*, 于志强2, 张 干2
(1. 中国科学院 海岸带环境过程与生态修复重点实验室(烟台海岸带研究所), 山东省海岸带环境过程重点实验室, 中国科学院 烟台海岸带研究所, 山东 烟台 264003; 2. 中国科学院 广州地球化学研究所, 广东 广州 510640; 3. 中国科学院大学, 北京 100049)
从莱州湾附近河流采集了36个表层沉积物样品, 采用高效液相色谱耦合三重四极杆串联质谱的分析方法对沉积物中的六溴环十二烷(HBCDs) 3种异构体进行了测定, 目的是表征研究区域内HBCDs的污染水平和组成特征, 并探讨其分布、来源及影响因素。结果表明, 莱州湾河流沉积物中åHBCDs的含量范围为0.03~20.17 ng/g dw (均值是2.14 ng/g dw);较国内外其他河流, 该研究区域HBCDs含量水平较低。HBCDs异构体组成各不相同, 除1个站位外, 其他站位样品中-HBCD占主导地位(52.3%~97.3%, 均值72.4%), 但是在农业区-HBCD相对丰度较高。对HBCDs的分布特征及来源分析得出, 含量较高的站点多集中在工业区, 呈现出明显的点源特征;而远离工业区的采样点, HBCDs可能主要来自大气的传输和沉降, 且HBCDs的含量与TOC含量呈现出较好的相关性, 表明TOC是非工业区分布的一个控制因素。
六溴环十二烷; 表层沉积物; 含量; 分布; 组成; 莱州湾河流
0 引 言
六溴环十二烷(hexabromocyclododecanes, HBCDs)作为一种溴系阻燃剂(brominated flame reterdants, BFRs)在世界范围内广泛使用, 是继多溴联苯醚(PBCDs)、四溴双酚A(TBBPA)之外的世界第三大阻燃剂产品, 主要应用于聚苯乙烯泡沫等建筑材料、室内装潢纺织品, 在电子电器领域也有较少的应用[1‒2]。作为一种添加型的阻燃剂, HBCDs易通过产品的生产、使用和处理等多种方式和途径释放到环境中去。自1998年在瑞典Viskan河的底泥和鱼类样品中首次检出HBCDs[3], 随后其他国家学者对其在生物和非生物体(如大气、沉积物和土壤等)环境介质及食物链方面开展了广泛的研究[4‒6]。由于HBCDs具有持久性有机污染物(persistent organic pollutants, POPs)的特征, 即长距离迁移性、生物累积性及毒性[7], 它对环境和人体健康造成的不利影响是不容忽视的。目前, 有些国家(如英国和日本等)已对HBCDs采用了相应的控制措施, 相关专家也在进行HBCDs的评估以决定是否将其列入《斯德哥尔摩公约》受控名单的物质[8]。
目前, 我国HBCDs的生产厂家主要集中在渤海莱州湾、江苏连云港和苏州等近海地区[8]。作为世界主要的阻燃剂市场, 其生产和使用量正在逐年增长。特别是五溴联苯醚和八溴联苯醚阻燃剂产品在欧洲和北美禁用以来, HBCDs作为一种替代品, 其需求量将继续保持增长的趋势, 预计我国HBCDs每年的生产能力约为7500万t[9], 但是国内关于HBCDs向环境的排放量、在环境介质中的存在状况及对人群健康等的研究数据有限。本研究拟开展对莱州湾周边河流沉积物样品中HBCDs的含量、异构体组成及分布特征的分析, 为更好地了解HBCDs的来源、分布及环境行为积累原始性和基础性数据。此外, 通过对莱州湾地区不同功能区河流沉积物中HBCDs污染水平的综合研究, 可以更好地评估不同的人类活动对该地区水生环境产生的影响, 从而对当地的产业结构调整和环境保护具有重要的借鉴意义。
1 材料与方法
1.1 样品采集
2009年9月14日至10月17日, 用不锈钢抓斗式采泥器在莱州湾附近河流及河口采集了表层(0~10 cm)沉积物样品, 共采集表层样品36个, 采样点如图1所示。样品采集后立即用干净的聚乙烯袋密封并于实验室低温冰箱中冷冻(–20 ℃)保存至分析。
河流沉积物来自12条河流, 包括溢洪河(YHH)、广利河(GLH)、淄脉沟(ZMG)、小清河(XQH)、弥河(MH)、白浪河(BLH)、虞河(YH)、堤河(DH)、潍河(WH)、胶莱河(JLH)和大家洼污水渠(DJW)。根据采样点的信息, 可以大致将站点分为4类: (1)位于工业区附近, 明显受到工业排放影响; (2)位于城区(或人口密集区), 采样时没有发现明显的工业输入, 但是可能受到非点源的工业排放或者市政污水的影响; (3)农业站点; (4)未分类区, 这些采样信息不全面, 或者受到人为活动的干扰就不被纳入其他任何分组内。
1.2 实验材料
实验过程所用到的溶剂均为HPLC级, 购自德国默克公司(Merck Darmstadt, Germany);13C标记和未标记的-HBCD、-HBCD和-HBCD购自Cambridge Isotope Laboratories (Andover, MA, USA);硅胶(80-100目)、氧化铝(100-200目)分别用分析纯甲醇、二氯甲烷索氏抽提48h, 通风橱干燥后, 分别在180 ℃和250 ℃的温度下活化12 h, 再用3%的蒸馏水去活化;无水硫酸钠在450 ℃条件下焙烧5 h。所用填料置于干燥器中备用。
1.3 样品处理
采集的沉积物样品经过冷冻干燥、研磨和过筛(80目)后, 贮存在棕色磨口玻璃瓶中于冰箱(–20 ℃)保存至分析。
样品的提取与净化过程已有文献详细描述[10‒11]。称取沉积物样品约20 g, 用预先抽提过的滤纸包好, 用200 mL体积比为1﹕1的丙酮/正己烷索氏抽提48 h。抽提前用微量进样针在样品中加入回收率指示物13C--HBCD和13C--HBCD (30 μL×1 μg/mL), 并在底瓶中加入适量活化的铜片用于脱硫。抽提液经过旋转蒸发后, 浓缩液加入多级硅胶氧化铝层析柱净化, 采用正己烷湿法装柱, 由下至上分别为6 cm氧化铝, 2 cm中性硅胶, 5 cm碱性硅胶(去活化硅胶和1 mol/L NaOH溶液质量比为3﹕1), 2 cm中性硅胶, 8 cm酸性硅胶(去活化硅胶和分析纯浓硫酸质量比为1﹕1)和1 cm无水硫酸钠。用体积比为1﹕1的二氯甲烷/正己烷混合溶液70 mL淋洗。淋洗液再经旋转蒸发至约1 mL, 在柔和的高纯氮气下吹干, 用甲醇定容至400 μL。
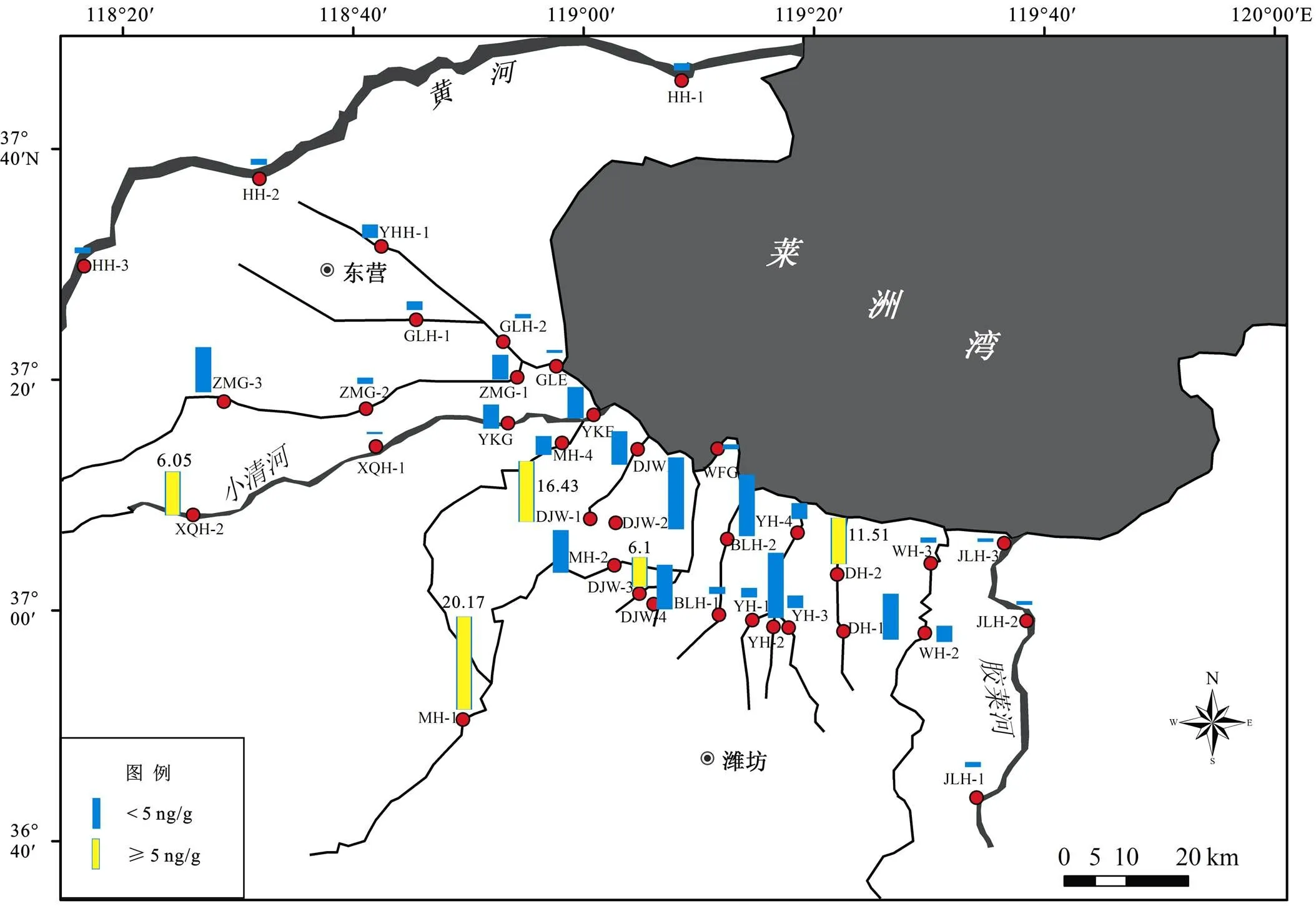
图1 莱州湾河流采样点及沉积物中HBCD的含量分布
1.4 仪器分析
分析仪器采用美国安捷伦1100液相色谱(Agilent Technologies, Palo Alto, CA)耦合应用生物系统API 4000三重四极杆串联质谱系统(API 4000 LC/MS/MS, Applied Biosystems, Foster City, CA)。质谱分析采用负离子电喷雾(electrospray ionization negative ion mode, ESI)和多重离子裂解检测模式(multiple reaction monitoring, MRM)。仪器分析扫描离子:-HBCD、-HBCD和-HBCD为(荷质比)= 640.7/78.8,13C-HBCD为(荷质比)= 652.7/78.8。碰撞气为高纯氮气, 进样量为10 μL。
HBCD异构体采用Zorbax SB-C18反相色谱柱(4.6 mm×250 mm×5 µm, Agilent)进行分离。梯度流动相组成为甲醇(B)/乙腈(C)/水(D), 流速为0.5 mL/min。初始流动相体积比B﹕C﹕D = 80﹕10﹕10, 在18 min内缓慢调整为B﹕C﹕D = 50﹕40﹕10, 23 min后调整为B﹕C = 30﹕70, 并保持7 min, 然后再5 min内再调整为B﹕C﹕D = 80﹕10﹕10, 色谱柱平衡10 min。
1.5 质量保证和质量控制(QA/QC)
每分析一批样品(12个左右)同时分析QA/QC样品, 包括方法空白、空白加标、基质加标和样品平行样。空白样品中均没有HBCDs检出或低于检出限。基质加标-HBCD、-HBCD和-HBCD的回收率分别为(100.78±4.55)%, (87.94±15.01)%和 (73.74±20.85)%;13C--HBCD和13C--HBCD的回收率分别为(100.38±5.27)%和(71.54±19.52)%;空白加标-HBCD、-HBCD和-HBCD的回收率分别为(101.10±3.03)%, (98.97±2.11)%和(52.9±14.57)%,13C--HBCD和13C--HBCD的回收率分别为(106.66±5.49)%和(54.18±12.82)%。平行样品所有目标化合物的重现性符合美国EPA规定的QA/QC要求, 平行样的相对标准偏差小于25%。
样品回收率指示物13C--HBCD和13C--HBCD的回收率控制范围分别为(88.75±11.00)%和 (80.16±12.78)%, 本研究数据没有用回收率校正。仪器检出限定义为3倍信噪比, 即S/N=3,-HBCD、-HBCD和-HBCD的检出限分别为0.005、0.003和0.003 ng。对HBCD异构体的定量采用了5个浓度系列(浓度范围是0.5~10 μL/L)针对每个目标化合物用外标法建立标准曲线(其中-HBCD,-HBCD和-HBCD标准曲线的相关系数2>0.9999)。
2 结果与讨论
2.1 沉积物中六溴环十二烷的含量水平及污染现状
莱州湾河流表层沉积物中HBCDs的含量水平如表1所示。所有沉积物样品中均有HBCDs的检出, 说明HBCDs在研究区域已经成为一种普遍存在的污染物质。åHBCDs在研究区域河流沉积物中的含量为0.03~20.17 ng/g dw (均值是2.14 ng/g dw), 其中-HBCD、-HBCD和-HBCD的含量分别为0.01~5.94 ng/g dw (均值是0.47 ng/g dw)、0.00~3.00 ng/g dw (0.22 ng/g dw)和0.01~11.32 ng/g dw (1.72 ng/g dw)。沉积物中åHBCDs的含量水平因采样区域的不同而异。从研究区域的功能分区内åHBCDs的含量对比得出, 河流沉积物中浓度最低的样品来自农业区的黄河、胶莱河和潍河, 而浓度较高的样点集中在工业区内, 工业区(均值3.57 ng/g dw) > 城市区(除MH-1, 均值为0.80 ng/g dw) > 未分类区(均值为0.70 ng/g dw) > 农业区(均值为0.17 ng/g dw), 这表明沉积物中HBCDs污染可能主要来自当地的工业释放源。其中,åHBCDs浓度从高到低依次为MH-1 (均值为20.17 ng/g dw), DJW-1 (16.43 ng/g dw), DH-2 (11.51 ng/g dw), DJW-3 (6.10 ng/g dw)和XQH-2(6.05 ng/g dw)。浓度最高点出现在城市区MH-1, 出现这一结果并不奇怪, 因为MH-1样品采自寿光市区建筑土, 而HBCDs作为添加型的阻燃剂广泛应用于聚苯乙烯泡沫等建筑材料中[12], 可能在建筑材料的使用和废弃的过程中向周边环境介质中释放。其他高浓度点均集中在工业区内, 如溴系阻燃剂工厂及化工厂比较集中的大家洼(DJW)采样点、上游有炼油厂和化工区的小清河(XQH)采样点和上游有印染业、纺织业的堤河(DH)采样点。通常河口、港口地区人类活动较为频繁, 污染物的浓度一般较高。但是位于河口、港口采样点(WFG、YH-4、YKG、YKE、DJWE)的浓度较低, 浓度范围为0.16~1.42 ng/g dw (均值0.91 ng/g dw), 主要原因是其与莱州湾相接, 受潮汐和海水的影响, 浓度受到稀释。特别的, 样点DJW-4距离DJW-3较近, 但是含量比DJW-3低3倍, 显示出强烈的点源特征, 一些文献也指出了HBCDs的浓度随着距离点污染源的增加而显著降低[13‒14]。在远离污染源的农业区(如黄河和胶莱河), HBCDs的浓度较低;与此相反, 在没有明显污染源的地区ZMG-3却有相对较高的浓度(达到1.95 ng/g)。这可能来自工业区大气中HBCDs的迁移和沉降, 因为HBCDs具有较低的蒸汽压(6.3×10‒5Pa, 21 ℃)[7], 有文献报告大气的传输和沉降是其由污染点源向远距离地区迁移的重要方式[15]。
由于HBCDs具有较高的辛醇-水分配系数 (lgow = 5.4~5.8)和较低的水溶性(-HBCD、-HBCD和-HBCD在水中的溶解度分别为48.8、14.7和2.1 μg/L)[7], 因此它可以较强地吸附在固体颗粒物上, 如沉积物、土壤和污泥。到目前为止, 关于环境介质中HBCDs含量水平的报告多集中于欧洲地区, 特别是明显的点源污染区和工业区。随着各国学者对HBCDs研究的关注, 已经开展了世界范围内有关HBCDs的调查和报道。
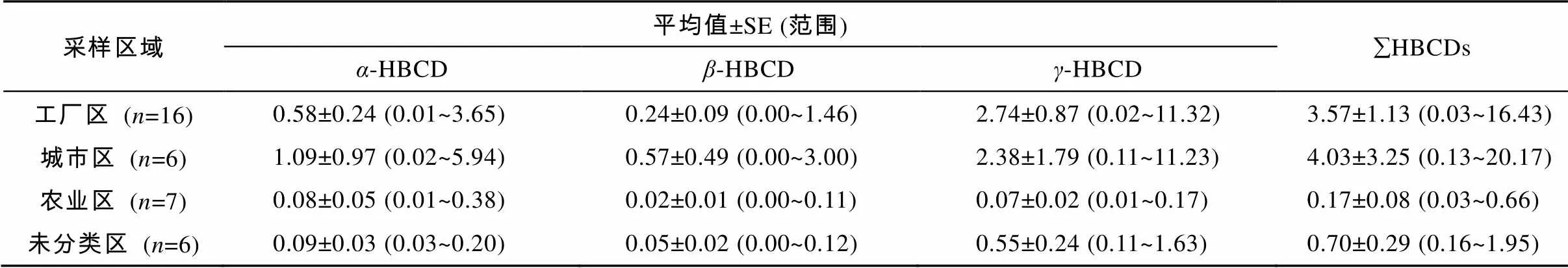
表1 莱州湾河流表层沉积物样品中六溴环十二烷的含量(ng/g dw)
为了清晰地描述本研究区域沉积物中HBCDs的污染水平, 我们对比了莱州湾河流和国内外其他地区河流表层沉积物中åHBCDs的含量, 发现除了少数几个站位含量较高(MH-1、DJW-1和DH-2), 本研究区域沉积物中åHBCDs浓度与其他欧洲国家相比处于较低的水平, 而与国内河流[15‒16]和美国五大湖[17]沉积物中åHBCDs含量水平相当(表2)。Feng.[15]关于珠江三角洲的研究结果与我们的研究类似:即HBCDs具有明显的点源特征;在远离污染源的地区HBCDs的浓度较低;莱州湾河流沉积物中HBCDs的浓度略低于珠江三角洲地区。总的来说, 在靠近生产区或者工业区附近沉积物中HBCDs的含量水平显著高于其他地区。如靠近溴系阻燃剂制造区英格兰东北Skerne河的淡水沉积物样品中HBCDs的浓度高达1700 ng/g[18];在纺织厂附近的瑞士Viskan河的表层沉积物中HBCDs的浓度表现为下游明显高于上游, 浓度分别为1~25 ng/g和小于0.1~0.2 ng/g, 说明点源污染显著影响HBCDs的分布[19]。而在没有明显HBCDs释放源的地区, 其浓度较低(小于10 ng/g), 如美国与加拿大的边界河Detroit河(0.075~3.7 ng/g)[23]、英国湖泊(0.88~4.8 ng/g)[5]、北美五大湖(0.04~3.1 ng/g)[17]沉积物中均检测到低含量的HBCDs。研究报告显示了欧洲地区的环境介质、生物及人体样品中检测到相对较高含量的HBCDs[18–20], 这些可能表明了由于五溴联苯醚(Penta-PBDE)和八溴联苯醚(Octa-PBDE)阻燃剂产品在欧洲和北美的禁用, HBCDs作为替代品, 其需求量不断增长(2001年欧洲地区HBCDs的市场需求量大约占全球需求量的60%)[24]。本研究中, 莱州湾河流沉积物中相对较低含量的HBCDs反映了中国的HBCDs使用量相对较少;与该地区相同采样点样品中PBDEs的含量相比较低, 且某些样品浓度比BDE-209低1~2个数量级[25], 可能说明在这些地区HBCDs并不是主要的BFRs污染物。
2.2 沉积物中六溴环十二烷的分布特征及影响因素
莱州湾河流沉积物中六溴环十二烷的分布如图1所示, 其中85%的沉积物样品中HBCDs小于5 ng/g dw, 高浓度点主要集中在工业区附近(如DJW-1、DH-2和XQH-2)。其中, 城市区(除MH-1)和农业区采样点HBCDs含量分布较为均匀, 而工业区及未分类区附近的采样点沉积物中HBCDs的含量变化趋势并不一致。在小清河(XQH)和广利河(GLH), 上游åHBCDs含量比下游高; 而在堤河(DH)和白浪河(BLH), 趋势正好相反;在淄脉沟, 则是两头比中间的高(ZMG-3 > ZMG-2 < ZMG-1)。将研究区域分为工业区和非工业区(包括城市区、未分类区和农业区), 如图2所示。工业区采样点沉积物中HBCDs的浓度高于非工业区, 而其他划分的3个功能分区(城市区、无明显污染源区和农业区)的浓度水平并没有呈现出显著性差异; 并且工业区沉积物中HBCDs的浓度差异变化较大, 城市区和农业区沉积物中HBCDs浓度差异几乎不变, 而未分类区沉积物中HBCDs浓度介于两者之间。从以上分析来看, HBCDs的空间分布具有明显的点源特征, 化工厂和溴系阻燃剂工厂很可能是莱州湾区域河流中HBCDs的主要来源。
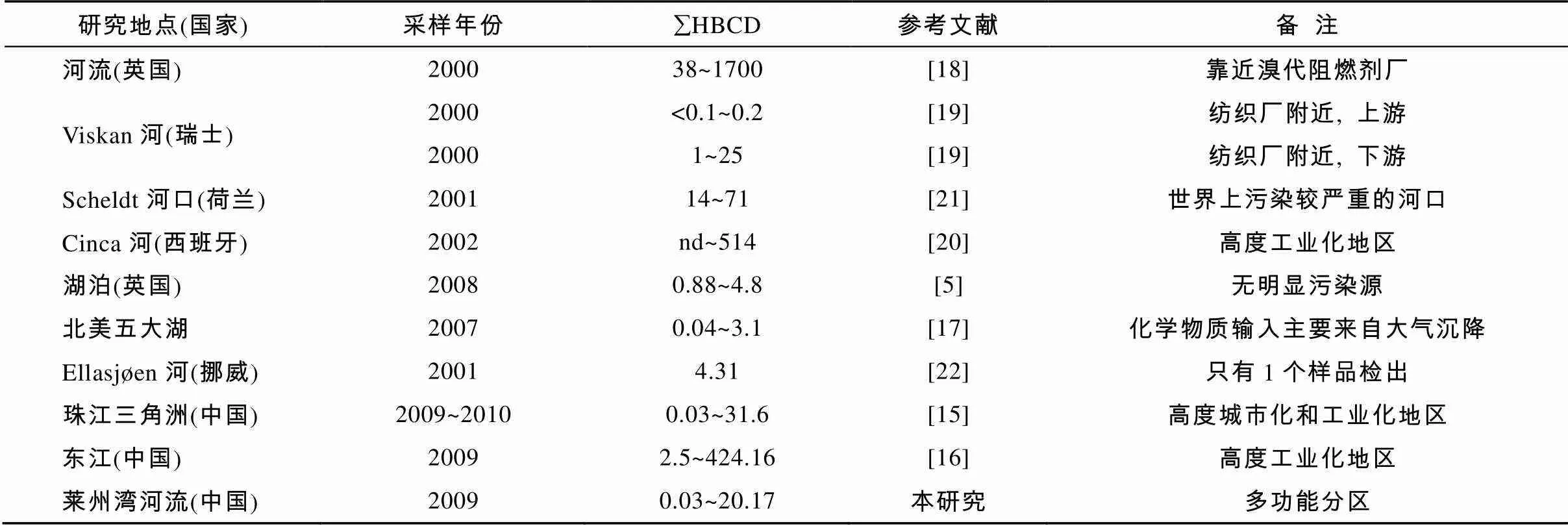
表2 莱州湾河流表层沉积物中六溴环十二烷的含量与国内外其他河流比较(ng/g)
由于低水溶性、高辛醇-水分配系数有机物能够分配到沉积物的有机质颗粒中, 且颗粒物颗粒越小, 比表面积越大, 越有利于其吸附[26]。将研究区域沉积物中HBCDs的含量与粒度(分为黏土(<4 µm)、粉砂(4~63 µm)和砂(>63 µm))进行相关性分析, 如图3所示。研究区域河流沉积物中HBCD的含量与粒度的相关性很低, 可能受到该地区复杂环境的影响, 导致污染物在颗粒物上的吸附很难达到平衡状态。

图2 不同功能分区河流沉积物中六溴环十二烷的含量箱式图
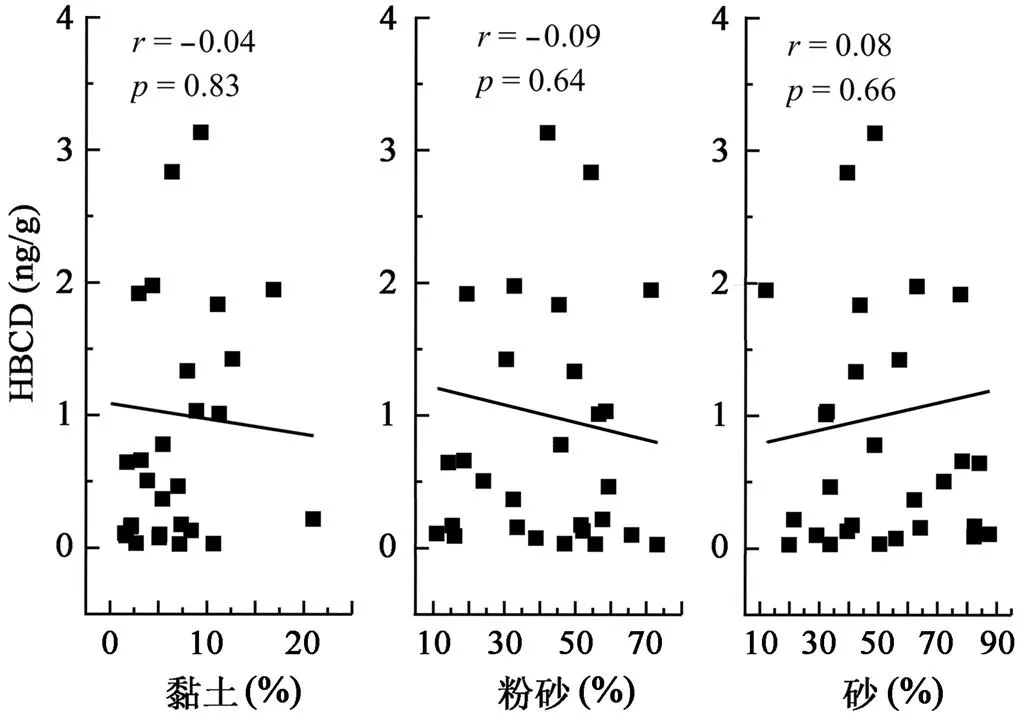
图3 研究区域沉积物中HBCDs含量与颗粒物粒度的相关分析
沉积物中的总有机碳(total organic carbon, TOC)的含量常常作为控制有机污染物在水体环境中分布的重要因素。HBCDs的理化性质决定了它们能够被强烈地吸附在土壤、沉积物和污泥等固体颗粒上[27]。因此, 我们对沉积物中HBCDs的含量和TOC含量做了相关性分析, 如图4所示。在所有样品中, HBCDs与TOC呈现出正相关性, 相关系数为= 0.57(=0.004), 总的来说, 沉积物HBCDs的含量分布受到TOC的支配。为了进一步探讨TOC对不同功能分区的影响, 又分别做了非工业区与工业区沉积物中HBCD与TOC的相关性分析。结果表明, 非工业区沉积物中HBCDs与TOC呈现较好的相关性(=0.63,=0.011), 可见TOC是HBCD在非工业区分布的一个控制因素。但是在工业区沉积物中的HBCDs含量与TOC的相关性差一些(=0.46,= 0.208), 这表明工业区沉积物中的HBCDs主要受到当地的点源污染的影响。
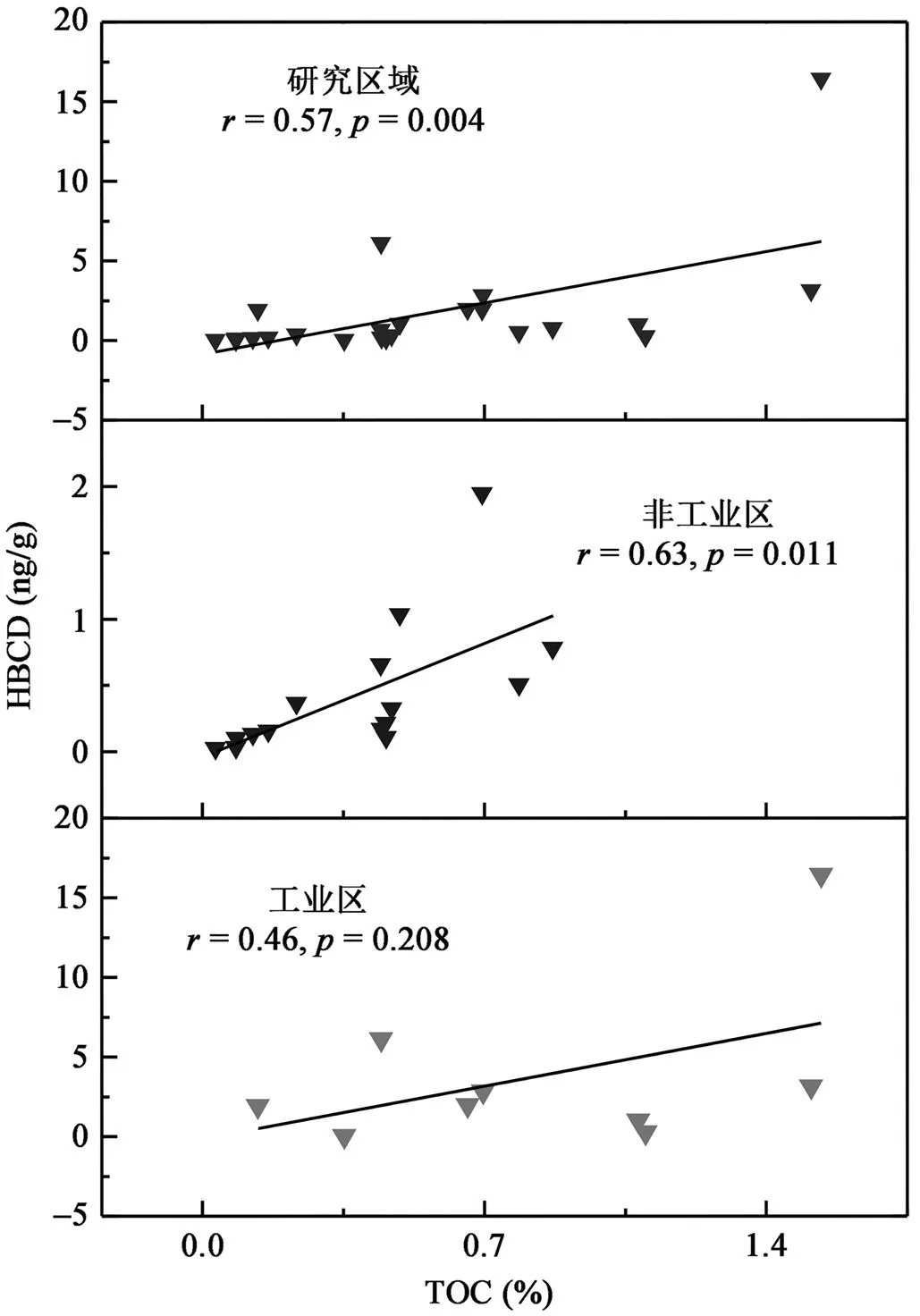
图4 研究区域沉积物中HBCDs含量与TOC的相关性分析
2.3 沉积物中六溴环十二烷异构体的组成分析
莱州湾河流沉积物样品中HBCD异构体的组成模式如图5。通常来说, HBCDs的技术品主要是由-HBCD、-HBCD和-HBCD 3种异构体组成, 其相对丰度分别为10%~13%、1%~12%和75%~89%, 另外还有极少量的-HBCD(0.5%)和-HBCD(0.3%)[2]。在不同的环境介质中3种HBCD异构体的组成、分布和环境行为存在不同。一般地, 在大部分非生物样品(如沉积物和土壤等)中HBCD的组成与HBCD技术品组成类似, 以-HBCD为主要异构体。与之相反, 在生物样品(如鱼类、鸟类和哺乳动物等)中通常则以-HBCD为主[27], 这种异构体组成的变化可能是多种因素造成的, 如HBCDs的物理化学性质、环境行为及环境条件等。

图5 研究区域表层沉积物中HBCD异构体分布模式
莱州湾河流沉积物中HBCDs异构体的组成各不相同。在所有样品中,-HBCD的相对丰度最小, 范围是0.2%~16%(均值为8.2%), 除1件样品外, 所有沉积物样品中-HBCD占主导地位, 其次是-HBCD, 相对丰度平均值分别为71.6%和21.5%, 与珠江三角洲沉积物和莱州湾工厂附近沉积物中HBCD异构体组成类似[14‒15]。其中15个沉积物样品中-HBCD(73.8~87.6%)与技术品组成相似, 而大部分样品则呈现出了多变的异构体分布模式。值得注意的是, 不同功能分区HBCD的组成变化有明显不同。城市区沉积物(18.5%-HBCD, 8.9%-HBCD和72.6%-HBCD)和工业区沉积物(17.9%-HBCD, 7.7%-HBCD和74.4%-HBCD)中-HBCD和-HBCD与农业区沉积物(37.1%-HBCD, 9.5%-HBCD和53.4%-HBCD)的异构体组成呈现出明显的不同(<0.002, T-test)。工业区沉积物中-HBCD的相对丰度的范围是55.7%~87.0%, 远大于农业区-HBCD的相对丰度(25.7%~66.7%), 且工业区沉积物中-HBCD相对丰度(1.5%~44.3%)的变化程度高于农业区(22.8%~58.3%)。这些不同点可能来自于这两个地区具有不同的HBCDs来源。工业区沉积物中的HBCDs主要来自处理以及未处理的工业废水的排入, 使得该地区HBCD异构体组成更接近于技术品, 而农业区远离工业污染源, 该地区的HBCDs来自污染源地区HBCDs的挥发及一系列的大气传输和沉降, 加之农业区特殊的环境条件, 可能导致HBCD异构体在这种环境介质中发生了异构体的转化。有学者发现在沉积物和土壤样品中会发生HBCDs异构体的生物转化和降解行为[28], 且-HBCD的半衰期明显长于-HBCD和-HBCD[29‒30]。特别的, 在城市区MH-1采样点HBCD的组成(29.4%-HBCD, 14.9%-HBCD和55.7%-HBCD)与其他地区(除农业区)HBCD组成具有明显的不同, 主要原因可能是由于沉积物样品来自当地的建筑土, 因为HBCD具有热不稳定性, 在温度高于160 ℃时常会发生热重组, 而在温度高于240 ℃时会发生热降解[31], 因此, 含有HBCDs材料的产品(如建筑材料)与HBCDs的技术产品在异构体组成的差异可能来源于在生产、处理、废弃等过程中由于异构体的转化和降解造成。如Heeb.[32]研究防火聚苯乙烯材料中的膨胀聚苯乙烯(expanded polystyrenes, EPS)和挤塑聚苯乙烯(extruded polystyrenes, XPS)暴露于140~160 ℃高温前后HBCDs异构体组成的变化情况, 结果表明热暴露前以-HBCD最为丰富, 而在热暴露后-HBCD得到明显富集, 且不同的EPS和XPS中-HBCD/-HBCD变化范围为1/13 ~ 3/1, 其推测认为HBCDs异构体的相互转化造成了其组成发生了改变。即使在同一功能分区内的某些样品HBCDs的异构体组成也有所不同, 可能是由于HBCD的3种异构体的物理化学性质的不同(如热稳定性和光降解性等), 使得在不同的环境介质中导致了异构体选择性地转化、分配、降解和生物代谢等[14]。目前为止, 导致HBCD异构体组成发生改变的原因还不是很清楚, 需要进一步探究。
3 结 论
(1)HBCDs在莱州湾附近河流沉积物中均有检出, 说明HBCDs在该地区已经成为一种普遍存在的污染物质, 含量范围是0.03~20.17 ng/g dw (均值是2.14 ng/g dw), 其浓度与欧洲国家相比处于较低的水平, 与珠江三角洲及美国五大湖沉积物中HBCDs含量水平相当。
(2)HBCDs在研究区域不同功能分区内的分布特征不同, 城市区和农业区HBCDs分布较为均匀, 其来源可能是污染源区HBCDs的大气传输和沉降。而工业区附近HBCDs含量变化趋势有一定差异, 具有明显的点源特征, 化工厂和溴系阻燃剂工厂很可能是莱州湾区域河流中HBCDs的主要来源。
(3)研究区域沉积物中HBCDs的含量与粒度的相关性很差, 可能受到复杂的环境影响, 导致污染物很难在颗粒物上达到平衡状态。非工业区沉积物中HBCDs与TOC呈现较好的相关性, 可见TOC是其分布的一个控制因素, 但是工业区沉积物中HBCDs含量与TOC相关性差。
(4)研究区域沉积物样品中HBCDs呈现出多变的异构体分布模式, 且不同功能区表现出显著的不同, 可能由于HBCDs的热转化、降解和生物代谢等因素影响。
由于HBCDs具有持久性、毒理作用和富集放大作用, 对水生生物及人类健康的影响不容忽视。目前, 对环境介质中HBCDs的含量和分布状况的认识不断深入, 有利于对其环境及生态风险进行更好的评估。
[1] Bromine Science and Environmental Forum(BSEF). About hexabromocyclododecane(HBCD)[Z]. http://wwwbsefcom/our-substances/hbcd/about-hbcd [2011-06-01].
[2] Heeb N V, Schweizer W B, Kohler M, Gerecke A C. Structure elucidation of hexabromocyclododecanes — A class of compounds with a complex stereochemistry [J]. Chemosphere, 2005, 61(1): 65–73.
[3] Sellstrom U, Kierkegaard A, de Wit C, Jansson B. Polybrominated diphenyl ethers and hexabromocyclododecane in sediment and fish from a Swedish river[J]. Environ Toxicol Chem, 1998, 17(6): 1065–1072.
[4] Meng X Z, Duan Y P, Yang C, Pan Z Y, Wen Z H, Chen L. Occurrence, sources, and inventory of hexabromocyclododecanes (HBCDs) in soils from Chongming Island, the Yangtze River Delta (YRD)[J]. Chemosphere, 2011, 82(5): 725–731.
[5] Harrad S, Abdallah M A E, Rose N L, Turner S D, Davidson T A. Current-Use Brominated Flame Betardants in Water, Sediment, and Fish from English Lakes[J]. Environ Sci Technol, 2009, 43(24): 9077–9083.
[6] Li H R, Mo L G, Yu Z Q, Sheng G Y, Fu J M. Levels, isomer profiles and chiral signatures of particle-bound hexabromocyclododecanes in ambient air around Shanghai, China[J]. Environ Pollut, 2012, 165: 140–146.
[7] Marvin C H, Tomy G T, Armitage J M, Arnot J A, McCarty L, Covaci A, Palace V. Hexabromocyclododecane: Current understanding of chemistry, environmental fate and toxicology and implications for global management[J]. Environ Sci Technol, 2011, 45(20): 8613–8623.
[8] 王亚韡, 蔡亚岐, 江桂斌. 斯德哥尔摩公约新增持久性有机污染物的一些研究进展[J]. 中国科学: 化学, 2010, 40(2): 99–123.
Wang Yawei, Cai Yaqi, Jiang Guibin. Research processes of persistent organic pollutants (POPs) newly listed and candidate POPs in Stockholm Convention[J]. Scientia Sinica Chimica, 2010, 40(2): 99–123 (in Chinese with English abstract).
[9] 姜玉起. 溴系阻燃剂的现状及其发展趋势[J]. 化工技术经济, 2006, 24(9): 14–18, 24.
Jiang Yu-qi. Current situation and development of bromine retardant world wide[J]. Chem Tech Econ, 2006, 24(9): 14–18, 24 (in Chinese with English abstract).
[10] Yu Z Q, Chen L G, Maw B X, Wu M H, Sheng G Y, Fu J M, Peng P A. Diastereoisomer- and enantiomer-specific profiles of hexabromocyclododecane in the atmosphere of an urban city in South China [J]. Environ Sci Technol, 2008, 42(11): 3996–4001.
[11] Yu Z Q, Peng P A, Sheng G Y, Fu J M. Determination of hexabromocyclododecane diastereoisomers in air and soil by liquid chromatography-electrospray tandem mass spectrometry[J]. J Chromatogr A, 2008, 1190(1/2): 74–79.
[12] Bromine Science and Environmental Forum(BSEF)[Z]. http://wwwbsefcom/ (last accessed Dec 2005).
[13] Gao S T, Wang J Z, Yu Z Q, Guo Q R, Sheng G Y, Fu J M. Hexabromocyclododecanes in surface soils from E-waste recycling areas and industrial areas in South China: Concentrations, diastereoisomer- and enantiomer-specific profiles, and inventory[J]. Environ Sci Technol, 2011, 45(6): 2093–2099.
[14] Li H H, Zhang Q H, Wang P, Li Y M, Lv J X, Chen W H, Geng D W, Wang Y W, Wang T, Jiang G B. Levels and distribution of Hexabromocyclododecane (HBCD) in environmental samples near manufacturing facilities in Laizhou Bay area, East China[J]. J Environ Monit, 2012, 14(10): 2591–2597.
[15] Feng A-H, Chen S-J, Chen M-Y, Chen M-Y, He M-J, Luo X-J, Mai B-X. Hexabromocyclododecane (HBCD) and tetrabromobisphenol A (TBBPA) in riverine and estuarine sediments of the Pearl River Delta in southern China, with emphasis on spatial variability in diastereoisomer- and enantiomer-specific distribution of HBCD [J]. Mar Pollut Bull, 2012, 64(5): 919–925.
[16] Zhang X, Zhang D D, Luo Z X, Lin L F, Yan C Z. Diastereoisomer- and enantiomer-specific profiles of hexabromocyclododecane in the sediment of Dongjiang River, South China[J]. Environ Chem, 2011, 8(6): 561–568.
[17] Yang R Q, Wei H, Guo J H, Li A. Emerging brominated flame retardants in the sediment of the Great Lakes [J]. Environ Sci Technol, 2012, 46(6): 3119–3126.
[18] Morris S, Allchin C R, Zegers B N, Haftka J J H, Boon J P. Distribution and fate of HBCD and TBBPA brominated flame retardants in North Sea estuaries and aquatic food webs[J]. Environ Sci Technol, 2004, 38(21): 5497–5504.
[19] Remberger M, Sternbeck J, Palm A, Kaj L, Stromberg K, Brorstrom-Lunden E. The environmental occurrence of hexabromocyclododecane in Sweden[J]. Chemosphere, 2004, 54(1): 9–21.
[20] Eljarrat E, De La Cal A, Raldua D, Duran C, Barcelo D. Occurrence and bioavailability of polybrominated diphenyl ethers and hexabromocyclododecane in sediment and fish from the Cinca River, a tributary of the Ebro River (Spain)[J]. Environ Sci Technol, 2004, 38(9): 2603–2608.
[21] Verslycke T A, Vethaak A D, Arijs K, Janssen C R. Flame retardants, surfactants and organotins in sediment and mysid shrimp of the Scheldt estuary (The Netherlands)[J]. Environ Pollut, 2005, 136(1): 19–31.
[22] Evenset A, Christensen G N, Carroll J, Zaborska A, Berger U, Herzke D, Gregor D. Historical trends in persistent organic pollutants and metals recorded in sediment from Lake Ellasjoen, Bjornoya, Norwegian Arctic[J]. Environ Pollut, 2007, 146(1): 196–205.
[23] Marvin C H, Tomy G T, Alaee M, MacInnis G. Distribution of hexabromocyclododecane in Detroit River suspended sediments[J]. Chemosphere, 2006, 64(2): 268–275.
[24] Alaee M, Arias P, Sjodin A, Bergman A. An overview of commercially used brominated flame retardants, their applications, their use patterns in different countries/regions and possible modes of release[J]. Environ Int, 2003, 29(6): 683–689.
[25] Pan X H, Tang J H, Li J, Zhong G C, Chen Y J, Zhang G. Polybrominated diphenyl ethers (PBDEs) in the riverine and marine sediments of the Laizhou Bay area, North China[J]. J Environ Mon, 2011, 13(4): 886–893.
[26] 杨毅, 刘敏, 侯立军. 长江口潮滩含氯有机物的分布及与TOC、粒度的相关性[J]. 上海环境科学, 2002 (9): 530–532, 553–580.
Yang Yi, Liu Min, Hou Li-jun. Distribution of polychlorinated organic compound in Yangtze estuary and its correlation with TOC and particle size[J]. Shanghai Environ Sci, 2002 (9): 530–532, 553–580 (in Chinese with English abstract).
[27] Covaci A, Gerecke A C, Law R J, Voorspoels S, Kohler M, Heeb N, Leslie H, Allchin C R, De Boer J. Hexabromocyclododecanes (HBCDs) in the environment and humans: A review[J]. Environ Sci Technol, 2006, 40(12): 3679–3688.
[28] de Wit C A. An overview of brominated flame retardants in the environment[J]. Chemosphere, 2002, 46(5): 583–624.
[29] Davis J W, Gonsior S, Marty G, Ariano J. The transformation of hexabromocyclododecane in aerobic and anaerobic soils and aquatic sediments[J]. Water Res, 2005, 39(6): 1075–1084.
[30] Davis J W, Gonsior S J, Markham D A, Friederich U, Hunziker R W, Ariano J M. Biodegradation and product identification of [14C] hexabromocyclododecane in wastewater sludge and freshwater aquatic sediment[J]. Environ Sci Technol, 2006, 40(17): 5395–5401.
[31] Barontini F, Cozzani V, Petarca L. Thermal stability and decomposition products of hexabromocyclododecane[J]. Ind Eng Chem Res, 2001, 40(15): 3270–3280.
[32] Heeb N V, Graf H, Bernd Schweizer W, Lienemann P. Thermally-induced transformation of hexabromocyclo dodecanes and isobutoxypenta bromocyclododecanes in flame-proofed polystyrene materials[J]. Chemosphere, 2010, 80(7): 701–708.
Levels, distributions and isomer profiles of hexabromocyclododecanes in the riverine sediments of the Laizhou Bay area, North China
LIU Yi-kai1,3, WANG Jing-zhi2,3, TANG Jian-hui1*, YU Zhi-qiang2and ZHANG Gan2
1. Key Laboratory of Coastal Environmental Processes and Ecological Remediation, Yantai Institute of Coastal Zone Research, Chinese Academy of Sciences, Shandong Provincial Key Laboratory of Coastal Zone Environmental Processes,Yantai 264003, China; 2. Guangzhou Institute of Geochemistry, Chinese Academy of Sciences, Guangzhou 510640, China; 3. University of Chinese Academy of Sciences,Beijing 100049,China
Thirty-six surface sediment samples were collected from nearly ten rivers or distributaries in the Laizhou Bay area. Three diastereoisomers of hexabromocyclododecanes (HBCDs) were analyzed by high performance liquid chromatograph, coupled to a triple quadrupole mass spectrometer (HPLC-MS/MS). The concentrations of HBCDs ranged from 0.03 to 20.17 ng/g dw, with a mean vale of 2.14 ng/g dw. The study area is less contaminated by HBCDs in comparison with other riverine regions around the world. HBCD diastereoisomer profiles differed among the sediment samples, and-HBCD (52.3%–97.3%, mean 72.4%) was the dominant isomer (except one sample), whereas-HBCD contributions were relatively high in sediments from the rural areas. Higher concentrations occurred mostly at industry areas, indicating the sources of HBCD was direct discharge from local factories; however, in the less industrial areas, including urban areas and rural areas, sources of HBCDs were from atmospheric transport and deposition. Moreover, relatively strong correlation between TOC and HBCD concentrations suggested that TOC is the control factor for HBCD distribution in the less industrial areas.
hexabromocyclododecanes (HBCDs); surface sediments; concentration; distribution; isomer profiles; Laizhou Bay rivers
P593
A
0379-1726(2014)01-0055-09
2012-10-31;
2013-02-26;
2013-07-04
中国科学院知识创新工程项目(KZCX2-YW-Q07-04, KZCX2-EW-QN210)
刘艺凯(1987–), 女, 硕士研究生, 主要研究方向为海洋化学。E-mail: ykliu@yic.ac.cn
TANG Jian-hui, E-mail: jhtang@yic.ac.cn; Tel: +86-535-2109151

