超声诊断分泌性中耳炎的研究进展
闵美平 综述 张志远 审校
分泌性中耳炎(SOM)是以中耳积液及听力下降为主要特征的中耳非化脓性炎性疾病,是引起小儿听力下降的常见原因之一[1]。如不能准确诊断和及时治疗,可导致儿童听力损失并延误幼儿语言能力的发展;在成年人,可能引起粘连性中耳炎、胆脂瘤型中耳炎乃至耳聋。
诊断分泌性中耳炎的两个关键因素是中耳积液是否存在和积液类型(浆液性、黏液性或化脓性)。常规诊断方法包括耳镜检查、声导抗测试及诊断性鼓膜穿刺。鼓膜穿刺术可确切诊断,是诊断中耳积液的“金标准”[2]。通过细针穿刺鼓膜直接抽吸来确定中耳腔内有无液体,并对所抽出的液体进行观察或生化分析确定其性质。因其需在麻醉状态下进行,是侵入性操作,且有发生并发症的风险,不易被儿童及部分成人患者所接受。声导抗测试是最常用的诊断方法,根据鼓室导抗图的类型推测中耳腔是否存在积液。声导抗测试和耳内镜检查对诊断中耳积液的准确率分别为83%和76%,甚至更低[3]。最近的一项研究显示,大约只有74%的耳鼻喉科医生、51%的儿科医生以及46%的普通医生在耳镜检查时可准确识别出分泌性中耳炎[4]。这两种方法中没有一种可与鼓膜穿刺术的结果100%一致,而且各种非侵入性测试方法仅能推测中耳积液存在与否,不能提供中耳积液类型的相关信息。因此,寻找一种更加可靠而精确的非侵入性方法诊断中耳积液是必要的。超声具有无创简便的特点,近年来在诊断中耳积液方面取得了不少新进展,现综述如下。
1 超声应用于诊断SOM的历史及发展
在诊断SOM的研究过程中,最早由Abramson等[5]于1972年尝试在A型超声模式下应用10 MHz的非聚焦换能器插入外耳道分析中耳的回声,检测中耳积液存在与否,并证明了此方法可行,但当时还无法区分积液的类型;Alvord等[6]使用眼科超声扇形扫描器(10 MHz,B型超声)放置在外耳道,也证明了超声可用于分泌性中耳炎的诊断;吴志修等[7]应用腔内超声换能器(20 MHz)显示小儿分泌性中耳炎的中耳超声图像,验证了超声对诊断中耳积液的实用性;Discolo等[8]研究团队应用A型超声诊断分泌性中耳炎时,不仅可准确诊断中耳腔内积液的存在(准确率94%),而且可以100%准确区分浆液性和粘液性积液,但当时的探头及超声装置在临床实践中缺乏实用性。为进一步推进这一技术的临床使用,克里斯托弗教授通过对探头的进一步改进和完善,设计出一种含有9个独立的超声波发射元素并以3×3格式排列在探头针尖凸面的新型超声探头,最大可能地使发射的超声波垂直于鼓膜的反射表面并充分地反射回探头[9];Rahul Seth等[9]应用这种新型探头对56例患儿进行检测,证明对中耳积液特性(浆液性、粘液性及化脓性)检测的灵敏度及特异度至少为94%。因此,探头设计的进一步完善,将可使这一技术在临床应用中更加精确而实用,具有可观的发展前景。
2 中耳积液的超声成像原理
超声(图1)采用高频声波使组织成像,是一种安全而准确的成像方式,广泛应用于各学科的临床诊疗,不同组织声阻抗的差异决定了朝向探头(回声)反射回来的声波能量的不同。正常中耳腔充气,空气中的声阻抗显著低于鼓膜的声阻抗,鼓膜-空气界面的反射系数很高,声波能量全部从鼓膜折回,此时将产生一个强回声,通过换能器可检测到只有一个脉冲波形。当中耳腔内有液体存在时会显著降低鼓膜内侧面和中耳腔之间界面的反射系数,使声波穿透中耳腔直达鼓岬。因骨质的声阻抗比空气高约4倍,积液-鼓岬界面也会产生回波信号,故可检测出两个脉冲波形(图2)。此外,回波的振幅可以反映出各种积液的粘度及其特性(浆液性、粘液或脓性)[8]。
基于上述工作原理,这种超声装置由超声波脉冲发生器/接收器(即超声探头装置)和图像数据采集系统组成。在测试过程中,超声波扫描监视器上可实时观察脉冲形态并以数字格式保存。

图1 超声探头 R指球形凸面半径,D指外直径

图2 超声工作原理
3 中耳超声检查方法
在行中耳超声检查之前,应尽量清除外耳道内的所有耵聍并使鼓膜清晰可见。患者去枕侧卧位,患耳朝上,在室温下用滴管将0.5~1.0 ml无菌水作为一种超声传感介质滴入外耳道内,使之覆盖鼓膜。然后将超声探头在直视下垂直地插入外耳道内,并放置在距离鼓膜大约5 mm的位置[10],必要时可将耳廓向后上方提拉,使外耳道生理弯曲消失,稍微变换探头角度以便检测。开启超声换能器使其通过探头发射高频声波(20 MHz)至鼓膜表面,检测中耳腔内是否有回声出现,在显示器上观察所测得的相关脉冲波形。检测结束后,嘱患者患耳向下侧卧或用吸引器将水从外耳道中清除。
4 中耳超声检测结果评估
超声换能器在检测过程中根据中耳腔内有无积液表现出相应的超声波回波形态(图3)。中耳无积液时,回波表现为只有1个脉冲;当中耳内有积液存在时,在第一个脉冲波形之后可观察到一个振幅衰减的波形。利用这种脉冲显示模型,超声探头正确检测中耳积液存在与否的准确率为96%(P=0.04)。第二个回波的振幅会因中耳内积液的粘度不同而表现不同(图4),当积液稠厚时其粘度越大(如粘液性),超声回波衰减的越多,显示的第二脉冲波形的振幅就越小;同理,积液越稀薄时(如浆液性或化脓性)其振幅衰减就越少,表现为第一脉冲之后较大振幅的波形。在积液存在时,利用第一脉冲振幅与第二脉冲振幅的二元逻辑回归模型区分液体状态,当A2+0.306A1-1.04>0时,积液为非黏液性,当A2+0.306A1-1.04<0时,积液为黏液性,(A1为第一脉冲波形振幅,A2为第二脉冲波形振幅),可有效区分粘液和非粘液之间(浆液性或化脓性)的积液状态,其准确率达100%(P=0.04)(图5)[8]。
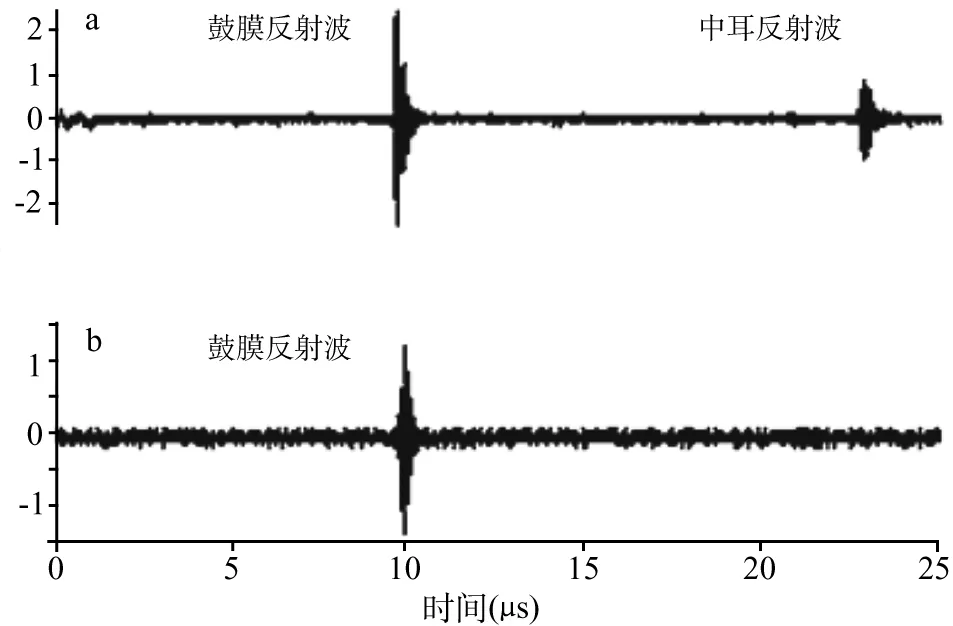
图3 超声扫描中耳系统
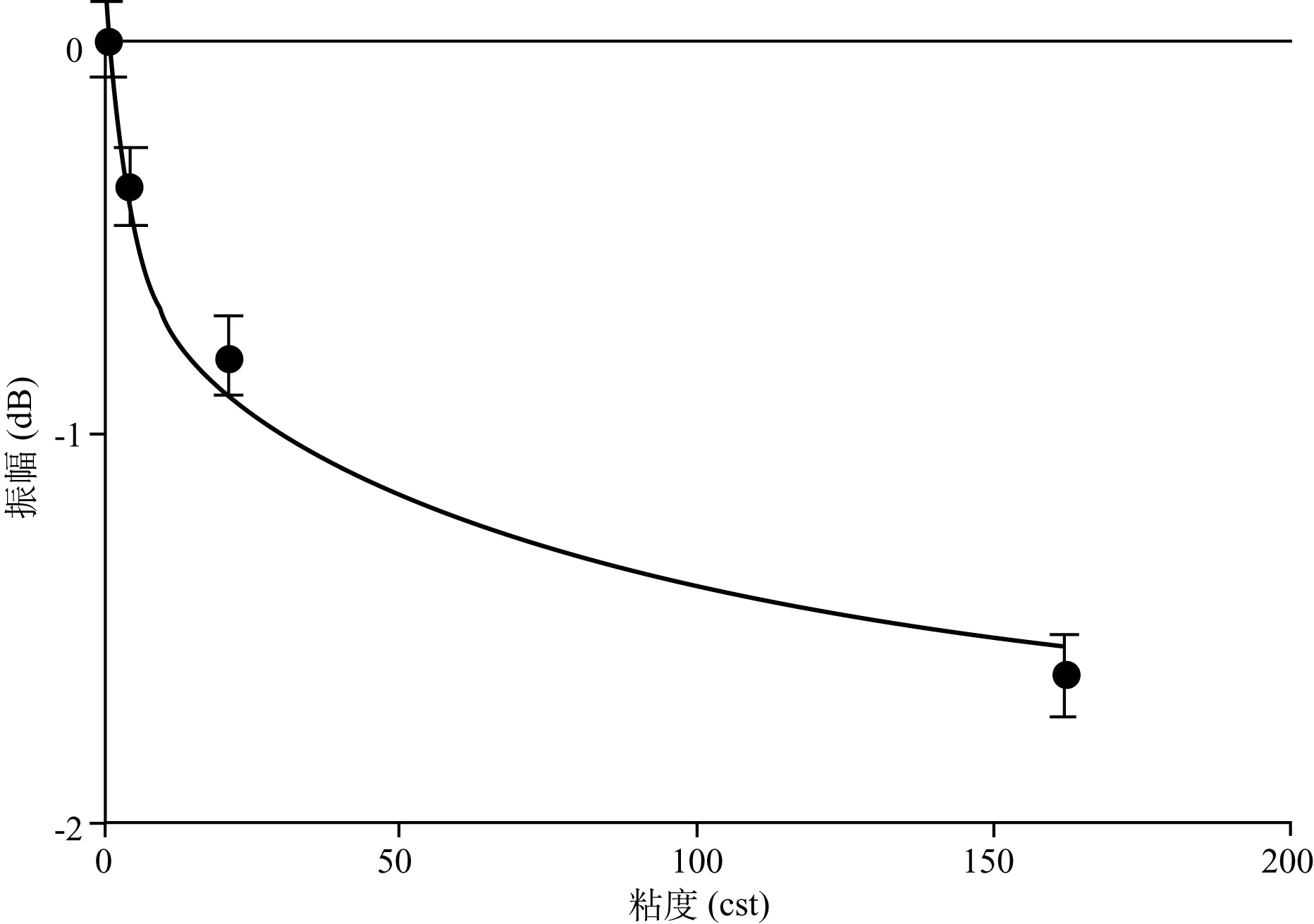
图4 中耳腔的回波幅度反映积液的粘度(CST表示厘沲)
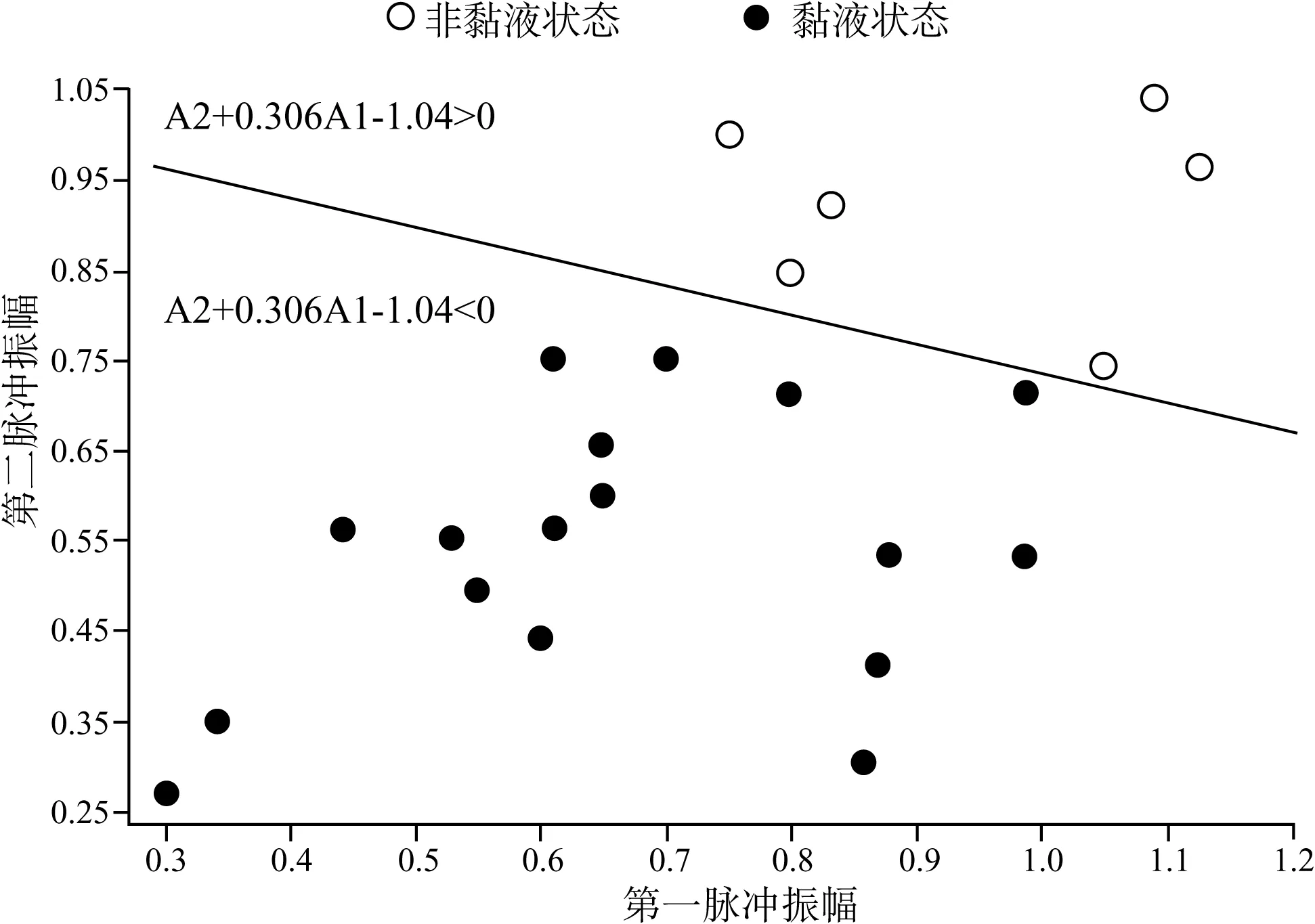
图5 第一个脉冲的振幅(A1)比第二脉冲幅度(A2)的二元逻辑回归分析图形 可用于区分粘液状态和非粘液状态
5 问题与展望
中耳腔的超声成像有可能成为一种高度精确的诊断方法用于诊断分泌性中耳炎,目前越来越多的国内外研究结果证明了这一点[11]。鼓室导抗图仅反映鼓膜随耳道气压变化的顺应性[12],间接推断积液是否存在;而超声可直接给出中耳腔的图像情况,从而准确检测中耳腔内积液与否,进一步指导正确的诊疗方案,避免不必要的鼓膜穿刺及抗生素应用,有效防止患者持续性听力下降及中耳炎反复发作[13]。
目前的超声探头是一种手持式超声换能器,约5号弗雷泽吸引装置大小,配有自动化波形采集翻译系统和计算机分析程序,探头针尖凸面9个小型发射波元素的设计,解决了之前Discolo等[8]应用单发射波的A型超声仪时必须人工翻译波形及探头需不停调整以使探头尽量与鼓膜表面垂直的问题。其超声波的产生和接收都是瞬间的,对强度过高的外界杂音的反应很差,如:哭闹声或谈话声,故其对周围环境及儿童患者的检查配合要求不高[14]。
虽然目前的这种设计实现了波形读取自动化及最大范围采集鼓膜反射波,但它仍面临着一些挑战,首先,用水作为传感介质滴入清醒患者的外耳道内可能使患者难以忍受,儿童患者更不易配合,因此临床适用性降低;其次,水注入外耳道内会稍微改变鼓膜的外观,影响探头的准确放置;此外,由于患者外耳道的整体大小和几何形状不同,微型探头对轻微的手部动作也非常敏感,手动插入探头到外耳道内难以维持探头的稳定,可能会使探头的正确放置变得困难,影响波形的充分采集;最后,目前的研究是在使用显微镜达到微观可视的情况下应用超声探头进行的,而临床应用中这种微观可视化没有必要。这些问题均在一定程度上制约了超声诊断分泌性中耳炎的广泛性研究与临床应用。
尽管如此,国内外的耳鼻喉科专家如克里斯托弗教授等一直致力于将这种无创诊断技术应用于临床实践,不断改善探头的设计,使检测更加简便、快速和准确;夏仲涛等[15]对中耳积液的超声诊断方法做了简要介绍,阐明超声鼓室检查的客观性、无损伤性及简便快速性;周凯书[16]、温武[17]及张亚梅[18]等也肯定了超声诊断中耳积液的可行性。目前,国内越来越多的耳鼻喉医师对中耳疾病的超声诊断方法有一定认识。
超声应用较普遍,操作技巧简单易学,若能将其应用于中耳积液的常规检测,将进一步提高SOM的确诊率,从而及时治疗。这一技术有望广泛应用于临床,预期超声将进一步应用于中耳腔其他疾病的诊断[19],如胆脂瘤型中耳炎[20]、婴儿隐匿性鼓窦炎[21]及听小骨破坏[22]等。
6 参考文献
1 Ravicz ME, Rosowski JJ, Merchant SN. Mechanisms of hearing loss resulting from middle-ear fluid[J].Hearing Research, 2004,195:103.
2 罗仁忠,王小亚. 儿童分泌性中耳炎的诊疗进展[J]. 中国医学文摘耳鼻咽喉科学,2013,28:19.
3 Pichichero ME.Diagnostic aaccuracy, tympanocentesis ttraining performance, and antibiotic selection by pediatric residents in management of otitis media[J].Pediatrics, 2002,110:61064.
4 Pichichero ME,Poole MD.Comparison of performance by otolaryngologists,pediatricians, and general practioners on an otoendoscopic diagnostic video examination[J]. International Journal of Pediatric Otorhinolaryngology,2005,69:361.
5 Abramson DH,Ahuamson AL,Coleman D.Ultrasonics in otolaryngology. An aid in the diagnostics of middle ear fluid[J].Archives of Otolaryngology,1972,96:146.
6 Alvord LS, Fine PG. Real-time B-scan ultrasound in mid-dle ear assessment[J]. J Ultrasound Med,1990,9:91.
7 Wu CH, Hsu CJ, Hsieh FJ.Preliminary use of endoluminal ultrasonography in assessment of middle ear with effusion[J].JUM,1998,17:427.
8 Discloo CM, Byrd MC, Bates T, et al. Ultrasonic detection of middle ear effusion: a preliminary study[J]. Arch Otolaryngol Head Neck Surg,2004,130:1407.
9 Seth R, Discolo CM, Palczewska GM,et al. Ultrasound characterization of middle ear effusion[J].American Journal of Otolaryngology,2013,34:44.
10 Clade O,Palczewska G, Lewandowski JJ,et al.P3Q-2 development and evaluation of a 20 MHz array for ultrasonic detection of middle ear effusion[J]. Ultrasonics Symposium, 2006,3:2357.
11 Seth R, Discolo C, Krakovitz PR.Ultrasound characterization of middle ear effusion[J].Otolaryngology Head and Neck Surgery,2008,139:70.
12 黄孝文,王春芳,曹平平,等. 鼓室导抗图与颞骨CT对分泌性中耳炎的诊断价值比较[J]. 听力学及言语疾病杂志,2013,21:483.
13 Rosenfeld RM, Culpepper L, Doyle KJ, et al. Clinical practice guideline: otitis media with effusion[J]. Otolaryngol Head Neck Surg,2004,130:S95.
14 Song J, Hynynen, K.Accurate assessment of middle ear effusion by monitoring ultrasound reflections from a tympanic membrane[J]. IEEE International, Ultrasonics Symposium, 2009,2:193.
15 夏仲涛. 鼓室超声检查对中耳疾病的客观诊断[J]. 国外医学耳鼻咽喉科学分册,1984,1:46.
16 周凯书. 超声诊断在耳鼻科的应用[J]. 中国超声医学杂志,1985,1:19.
17 温武,萧轼之,李兆基. 耳鼻咽喉科超声诊断现状与展望[J]. 国外医学耳鼻咽喉科学分册,1992,2:93.
18 张亚梅.分泌性中耳炎临床诊疗进展[J].继续医学教育,2006,20:56.
19 肖跃明,戴径捷,孟雅君,等,超声诊断中耳疾病的探讨及临床应用研究[J].中国超声医学杂志,2000,16:14.
20 张锦,肖跃明,戴经捷,等. 超声诊断胆脂瘤型中耳炎的临床应用[J]. 中华超声影像学杂志,2000,12:45.
21 陆明雄. 超声扫描术对于诊断婴儿隐匿性鼓窦炎的意义[J]. 国外医学耳鼻咽喉科学分册,1986,4:222.
22 孟雅君,肖跃明,戴径捷,等. 超声诊断中耳听小骨破坏[J]. 中国医学影像学杂志,2001,01:63.
——外耳道成形技术进展

