白杨素-羟丙基-β-环糊精包合物的制备与表征
曾倩,纪晖,唐慧慧,谢学渊(.海军总医院药剂科,北京 00048;.海军保健委员会办公室,北京 0048)
·研究报告·
白杨素-羟丙基-β-环糊精包合物的制备与表征
曾倩1,纪晖2,唐慧慧1,谢学渊1(1.海军总医院药剂科,北京 100048;2.海军保健委员会办公室,北京 100481)
目的为提高白杨素的水溶性和生物利用度,用羟丙基-β-环糊精对其进行包合,拓宽白杨素的药用途径。方法利用研磨法制备白杨素-羟丙基-β-环糊精包合物,通过粉末X射线衍射分析、差示扫描量热分析和红外光谱分析等方法对制备的白杨素-羟丙基-β-环糊精包合物进行鉴定和表征;应用紫外分光光度法对包合物的溶解度进行测定。结果白杨素与羟丙基-β-环糊精形成包合物,包合前后溶解度考察表明,形成包合物后白杨素的溶解度增加了120.7倍。结论羟丙基-β-环糊精对白杨素具有良好的增溶作用,白杨素环糊精包合物的制备方法简捷实用,达到了增加药物溶解度的目的,有助于白杨素的进一步开发利用。
白杨素;羟丙基-β-环糊精;包合物;表征
黄酮类化合物是自然界中常见的生物活性成分,研究发现它们具有许多潜在的药用价值。白杨素又名白杨黄素,主要来源于紫葳科植物木蝴蝶的干燥种子。它是一类植物界中广泛存在的黄酮类化合物,现代药理研究发现白杨素具有抗氧化[1]、抗炎[2-4]、改善脑损伤[5]、抗糖尿病等作用,特别是近年来发现白杨素能够抑制肿瘤细胞增殖,诱导肿瘤细胞凋亡,抑制肿瘤新生血管形成、逆转肿瘤细胞多药耐药,具有抗基因突变等方面的药理作用[6-8],有一定开发价值。但是由于白杨素不溶于水,极大地影响了该药物在制剂上的应用和人体内的吸收利用,限制了其临床应用。
羟丙基-β-环糊精(hydroxypropyl-β-cyclodextrins, HP-β-CD)是一类亲水性物质,是β-环糊精的羟烷基化衍生物,对碱、热和光稳定,安全性高。与β-环糊精相比,具有肾毒性低、几乎不参与生物体内代谢、不蓄积、溶血性与刺激性低等优点,被认为是极有潜力的增溶剂、稳定剂和促渗剂等药用辅料[9,10]。
本实验采用包合技术,制备羟丙基-β-环糊精与白杨素的包合物,以提高白杨素的水溶性,并对包合物进行了鉴定分析和溶解度考察,为白杨素新药开发和临床应用研究提供实验依据。
1 仪器与试药
1.1 仪器Bruker D8 ADVANCE X-Ray粉末衍射仪(德国),NETZSCH DSC 204 F1差示扫描量热仪(德国),Nicolet 5700型傅里叶变换红外光谱仪(美国热电公司Thermo),TU1901双光束紫外分光光度仪(北京普析通用仪器有限公司),Pulverisette 6型球磨机(德国FRITSCH公司)。
1.2 试药白杨素(C15H10O4,陕西慧科植物开发有限公司,SI20120718,纯度>98.5%)(图1),羟丙基-β-环糊精(北京西美杰科技有限公司),白杨素对照品(中国食品药品检定研究院,批号:111701-200501),其他试剂均为分析纯。
图1 白杨素结构图
2 方法与结果
2.1 包合物的制备采用研磨法[11,12]制备白杨素包合物。白杨素-羟丙基-β-环糊精包合物的制备:按照摩尔比1∶1精密称取羟丙基-β-环糊精1 541.54mg,白杨素254.25 mg,放入球磨机中进行研磨。研磨条件:转速4 000 r/min,时间15min,暂停2min。4 h后即得白杨素-羟丙基-β-环糊精包合物。
白杨素-羟丙基-β-环糊精物理混合物的制备:以摩尔比1∶1精密称取羟丙基-β-环糊精1 541.58 mg,白杨素254.31mg,放入研钵中轻轻研磨30 s,即得白杨素-羟丙基-β-环糊精物理混合物。
2.2 包合物的鉴定与表征分析
2.2.1 粉末X射线衍射(PXRD)实验X射线衍射图谱的摄取采用D8 ADVANCE vertical goniometer,Ni-filter单色器,Theta/Theta连续扫描,电压40 kV,电流40mA,扫描速度8°/min,LynxEye检测器,扫描范围3°~80°。结果见图2。
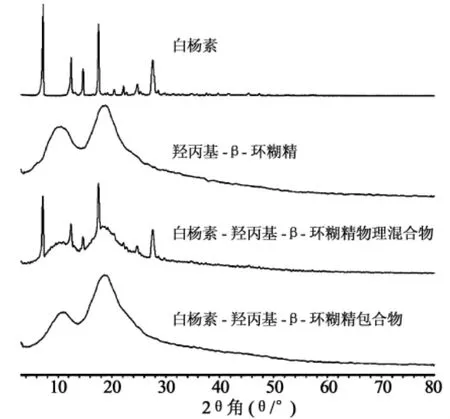
图2 粉末X射线衍射图谱
由图谱可见白杨素为晶态化合物,表现为尖锐的特征衍射峰,羟丙基-β-环糊精为非晶态化合物,表现为弥散衍射峰;白杨素-羟丙基-β-环糊精物理混合物的主要衍射峰为两种成分的叠加,白杨素-羟丙基-β-环糊精包合物为非晶态化合物,表现为弥散衍射峰。从包合物的图谱中未见白杨素的衍射峰,这说明通过包合制备过程,白杨素与羟丙基-β-环糊精均形成新的物相。
2.2.2 差示扫描量热分析(DSC)测定样品的DSC采用NETZSCH DSC 204 F1型差热分析仪测定,N2气流保护,空铝坩埚作为参比物,扫描范围30~330℃,升温速率10℃/min。测定结果见图3。
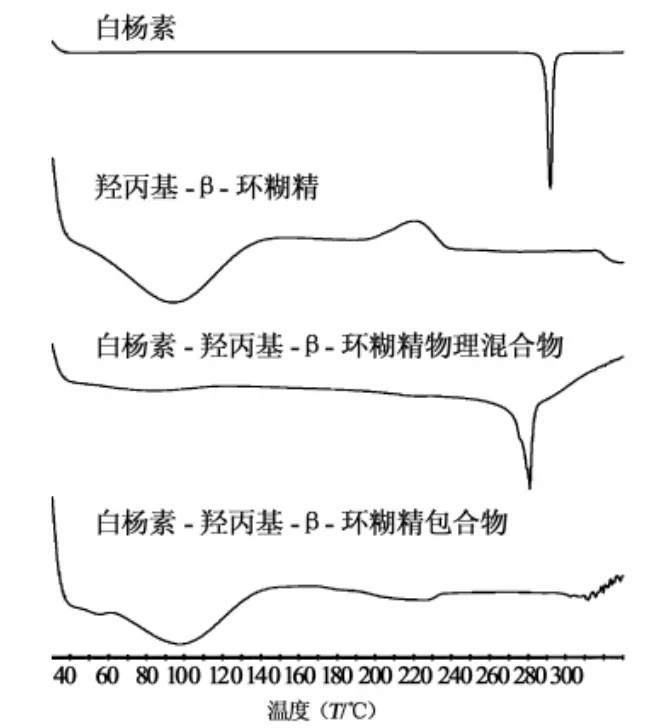
图3 DSC测定图谱
DSC测定结果表明,羟丙基-β-环糊精在98.17℃有一宽化的吸热峰,表明羟丙基-β-环糊精为非晶态,白杨素在289.75℃有尖锐的吸热峰,表明白杨素为晶态化合物,白杨素-羟丙基-β-环糊精物理混合物在280.28℃仍可见白杨素的吸热峰,而白杨素-羟丙基-β-环糊精包合物在测定范围中未见明显白杨素的熔点吸热峰,表明有新的物质生成,通过包合作用提高了白杨素的热稳定性。
2.2.3 红外光谱分析(IR)样品的红外光谱测定采用傅里叶变换红外光谱仪Nicolet5700型,美国热电公司(Thermo),光谱范围4 000~650 cm-1,分辨率4.000 cm-1,扫描次数16次。测定结果见图4。
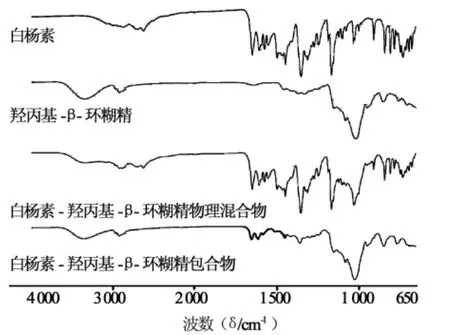
红外光谱分析表明,通过研磨获得白杨素-羟丙基-β-环糊精包合物,包合物中主要体现环糊精的CO伸缩振动,白杨素的骨架C=C、C=O的伸缩振动特征峰发生变化,表明白杨素与羟丙基-β-环糊精产生了包合作用。
2.3 包合物的溶解度测定
2.3.1 测定波长的选择分别将羟丙基-β-环糊精、白杨素-羟丙基-β-环糊精包合物的水溶液和白杨素的甲醇溶液在190~400 nm波长范围进行紫外扫描,白杨素溶液在268 nm与212 nm波长处有强烈而稳定的吸收峰(图5),白杨素-羟丙基-β-环糊精包合物水溶液与白杨素的最大吸收波长一致,而羟丙基-β-环糊精的最大吸收波长为205 nm。故最终选择268 nm为检测波长。
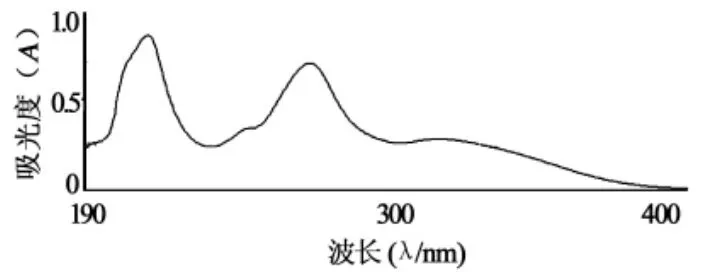
图5 UV测定图谱
2.3.2 标准曲线的制备精密称取白杨素对照品12.50 mg,移至250 ml容量瓶中,用甲醇定容,配制成浓度为51.8μg/ml的储备液。分别精密吸取0.1、0.2、0.5、1.0、2.0、5.0 ml置50 ml容量瓶中,用甲醇稀释至刻度,获得6种梯度浓度样品。取不同浓度的溶液3 ml在268 nm处记录吸光度,以吸光度对质量浓度进行线性回归,得标准曲线方程Y=0.127 9X+0.084 5(r=0.999 9,n=6),在0.104~5.184 μg/ml浓度范围内线性关系良好。
2.3.3 回收率实验精密称取一定含量的白杨素6份,置于50 ml量瓶中,加入适量的HP-β-CD(与白杨素的物质的量之比为1∶1),用甲醇稀释至刻度,摇匀,在268 nm处测其吸收度,计算白杨素在HP-β-CD中的平均回收率及RSD,分别为98.9%和0. 87%(n=6)。
2.3.4 精密度实验精密称取白杨素10.0 mg,加甲醇溶解,并定容至250ml容量瓶中,精密吸取1 ml,置10 ml容量瓶中,配制成浓度为4μg/ml的溶液,摇匀,在268 nm处重复进样6次测其吸光度,实验结果表明:重复进样6次,样品平均吸光度的RSD值为0.21%,表明利用紫外分光光度法测定白杨素含量的检测分析方法精密度良好。
2.3.5 重复性实验精密称取6份白杨素各10.0 mg,甲醇溶解并转移至250 ml容量瓶中,甲醇定容,精密吸取1 ml,置10 ml容量瓶中,配制成浓度为4 μg/ml的溶液,摇匀,在268 nm处测其吸光度,实验结果表明:计算获得6份样品平均吸光度RSD值为1.05%,表明利用紫外分光光度法测定白杨素含量的检测分析方法具有良好的重复性。
2.3.6 溶解度测定利用建立的标准曲线,采用紫外分光光度法,分别测定白杨素、白杨素-羟丙基-β-环糊精包合物在水中的溶解度,结果发现,白杨素在水中的溶解度为0.30μg/ml,白杨素-羟丙基-β-环糊精包合物的溶解度为36.22μg/ml,包合物在水中的溶解度增加了119.7倍。表明通过包合作用,白杨素的水溶性得到明显提高。
3 结论
白杨素的药用价值十分广泛,临床上已被用于心血管疾病、痛症及免疫系统疾病的治疗。近年来随着对其抗肿瘤活性的深入研究,又发现了很多新的极有价值的药用线索,但是其应用却受到水溶性低的局限。本实验利用羟丙基-β-环糊精具有环形中空筒状结构的特点,可以作为主体与其他化合物分子形成超分子结构,从而改变客体的理化性质,在一定程度上增加了白杨素在水中的溶解度。
常用的包合物制备方法有:饱和水溶液法、研磨法、超声法、冷冻干燥法、喷雾干燥法,液-液法和气-液法,本实验通过研磨法制备获得白杨素-羟丙基-β-环糊精包合物。该方法操作简单,条件易控,免去了溶解、搅拌、洗涤、干燥等复杂过程,样品在研磨机中充分包合,避免了原料的损失,包合率与包合的产率均较高。
从PXRD、DSC、IR对包合物的鉴定与表征分析可知,通过研磨法改变了白杨素药物的存在状态,获得的白杨素-羟丙基-β-环糊精包合物为无定型态。无定型态物质具有较大的分散度,由于无晶格束缚,自由能大,因此溶解度和溶解速度均较大。
本实验采用紫外分光光度法考察了白杨素-羟丙基-β-环糊精包合物的增溶效果,发现制备的白杨素-羟丙基-β-环糊精包合物的溶解度是白杨素溶解度的120.7倍,这表明通过包合作用可提高白杨素在水中的溶解度,提高了白杨素药物的生物利用度和适用范围,为白杨素的开发利用拓宽了思路。
[1]Woodman OL,Chan Ech.Vascular and anti-oxidant actions of flavonols and flavones[J].Clin Exp Pharmacol Physiol,2004,31(11):786-790.
[2]Mantawy EM,El-BaklyWM,Esmat A,etal.Chrysin alleviatesacute doxorubicin cardiotoxicity in rats via suppression of oxidativestress,inflammation and apoptosis[J].Eur JPharmacol,2014,728:107-118.
[3]Xiao J,Zhai H,Yao Y,et al.Chrysin attenuates experimental autoimmune neuritis by suppressing immuno-inflammatory responses[J].Neuroscience,2014,262:156-164.
[4]Cho H,Yun CW,Park WK,et al.Modulation of the activity of pro-inflammatory enzymes,COX-2 and iNOS,by chrysin derivatives[J].Pharmacol Res,2004,49(1):3743.
[5]He XL,Wang YH,BiMG,etal.Chrysin improves cognitive deficits and brain damage induced by chronic cerebralhypoperfusion in rats[J].Eur JPharmacol,2012,680(1-3):41-48.
[6]赵翔,陈希,李常虹,等.白杨素对人肝癌BEL-7402细胞表面超微结构和蛋白质磷酸化及相关通路的影响[J].中国组织工程研究与临床康复,2011,15(6):1050-1055.
[7]Parajuli P,Joshee N,Rimando AM,et al.In vitro anti-tumor mechanisms of various Scutellaria extractsand constituent flavonoids[J].Planta Med,2009,75(1):41-48.
[8]Woo KJ,Jeong YJ,Park JW,et al.Chrysin-induced apoptosis is mediated through caspase activation and Akt inactivation in U937 leukemia cells[J].Biochem Biophys Res Commun,2004,325 (4):1215-1222.
[9]缪菊连,黄照昌.羟丙基-β-环糊精对人参皂苷Rg1溶解度的影响[J].中国实验方剂学杂志,2011,17(21):17-19.
[10]白秀秀,夏广萍,赵娜,等.羟丙基-β-环糊精对二氢杨梅素的增溶作用[J].中国实验方剂学杂志,2013,19(9):12-14.
[11]毛利娟,王永禄,李学明,等.共研磨法提高兰索拉唑的溶出度[J].中国医药工业杂志,2011,42(8):595-599.
[12]张聪.共研磨技术在提高难溶性药物溶出度中的应用[J].中国医药指南,2013,11(4):384-385.
Preparation and characterization of chrysin-hydroxypropyl-β-cyclodextrins inclusion com pound
ZENG Qian1,JIHui2,TANG Huihui1,XIE Xueyuan1(1.Department of Pharmacy,Navy General Hospital,Beijing 100048,China;2. The Chinese Navy Healthcare Committee Office,Beijing 100841,China)
Objective Toprepare the water soluble chrysin-hydroxypropyl-β-cyclodextrins inclusion compound and widen the administration path of chrysin.MethodsThe cogrindingmethod had been used to prepare chrysin-hydroxypropyl-β-cyclodextrins inclusion compound.The PXRD,DSC and IR techniques had been used to characterize the inclusion compound.ResultsChrysin and hydroxypropyl-β-cyclodextrins had formed the inclusion compound,and the formation of the inclusion compound could increase solubility by 120.7 times.ConclusionThe inclusion compound preparationmethod was simple and available,which was suitable to improve the bioavailability.
chrysin;hydroxypropyl-β-cyclodextrins;preparation;characterization
R932 [文献标志码]A [文章编号]1006-0111(2014)06-0456-04
10.3969/j.issn.1006-0111.2014.06.014
2014-04-08
2014-09-09[本文编辑]顾文华
曾倩,本科,主管药师.Tel:(010)66958415,E-mail: zeqhrl@sina.com.
唐慧慧,副主任药师.Tel:(010)66957617,E-mail:tanghui106@aliyun.com.

