基于生物燃料电池智能逻辑生物传感器的研究进展
赵灵芝,张小清,苗延青,邓文婷,胡颢
(西安医学院药学院,陕西西安 710021)
逻辑生物传感器(LB)是以蛋白质、DNA、酶以及整个活细胞为分子识别单元,通过生化反应方式进行信息输入,通过布尔逻辑运算对信息进行处理和加工,然后输出信息的装置。与传统生物传感器不同,智能化的逻辑生物传感器不是通过输入信号和输出信号一对一的定量响应模式来实现检测和分析的目的[1-3],它可以在复杂体系中,通过布尔逻辑运算向生物计算系统编程,从而同时反映多种目标物的存在以及相互间的关系。生物燃料电池(BFC)是指以酶或微生物作为催化剂,通过生物电化学途径将生物物质的化学能转化为电能的装置,其可作为自供电能源发展为植入式微型人工电子器件[4-7]。基于生物燃料电池发展的智能逻辑生物传感器将两者的优点相结合,可发展为智能化、微型化、不需外接电源的分析装置,已初步应用于医学检测、诊断以及药物的控释研究中[8-11]。本文重点综述近5年基于BFC发展的逻辑生物传感器的工作原理和研究进展[12-19]。
1 基于封闭效应的自供电逻辑生物传感器
基于封闭效应发展的自供电逻辑生物传感器,往往在BFC两极修饰适配子或脱氧核酶等具有识别能力的生物大分子,在多种目标物处于某种存在状态时,它们在电极表面可自由伸展,不阻碍电极表面的电子传递;一旦目标物达到特定的存在状态时,适配子或脱氧核酶与相应的目标物结合,形成复合物,吸附于电极表面,从而使两极电子传递受到不同程度的抑制,表现出BFC各电化学参数的变化。这种逻辑传感器以几种目标物的存在状态(如无目标物存在、单一目标物存在、目标物均存在等)为输入信号Input,以电池的电化学参数达到某一定值作为输出信号Output,基于电极表面的封闭效应来设计逻辑关系,从而构建不同逻辑关系的自供电传感器。2010年,董绍俊等[12]报道了首个基于封闭效应适配子逻辑体系控制的生物燃料电池,并以此发展了自供电逻辑生物传感器(见图1)。电池两极均以氧化铟锡为基底电极,阳极通过自组装膜将葡萄糖氧化酶(GOD)和凝血酶适配子(TBA)修饰于电极表面;阴极以同样的方式,将胆红素氧化酶(BOD)和溶解酵素适配子(LBA)修饰于电极表面;整个电池是以葡萄糖为燃料,以羧酸二茂铁(FMCA)为两极的电子介体,通过阳极GOD催化葡萄糖氧化和阴极BOD催化O2还原产生输出电流。当凝血酶存在、溶解酵素不存在于体系中时,即输入信号Input(1,0),阳极TBA可特异性结合凝血酶,形成蛋白复合物,封闭了电极表面,从而阻碍电极表面电子传递,使GOD催化葡萄糖氧化产生过电位,降低电池的开路电位;凝血酶的存在并没有影响阴极的电化学反应,从而没有造成电池开路电位大幅度下降,即输出信号 Output 1(开路电位 >0.05 V为 Output 1,<0.05 V为Output 0);同样当体系中存在目标物溶解酵素而不存在凝血酶时,即Input(0,1),也不会使电池开路电位的大幅度下降;只有当目标物凝血酶和溶解酵素均存在于体系中时,即Input(1,1),由于蛋白复合物封闭了两极造成电池开路电位的大幅度下降,即Output 0;也就是当体系处于Input(0,0)、Input(1,0)和 Input(0,1)3 种状态下,Output均为1;只有体系处于 Input(1,1),Output为0。董绍俊组首次提出适配子与生物燃料电池之间的“互惠”概念,即基于适配子的逻辑生物信号作为控制生物燃料电池能量的输出及生物燃料电池作为适配子的传感器。相对于传统传感器,这个体系的特征对应于“与非”逻辑门,可用于分析在单一体系中两种目标物是否同时存在,并可智能化检测复杂样品中各种物质间的关系。随后,他们组[13]基于封闭效应发展了适配子具有重置功能的自供电式传感器,整个装置通过生物物质作为输入信号,通过简单的处理方式可使体系重置来达到多次使用的目的,并成功应用于智能化检测人血清中凝血酶和ATP。但这个装置的不足之处在于BFC较低的输出电压和功率,限制了装置的实际应用,或可通过电池两极电子介体的选择和改进来完善这一装置。
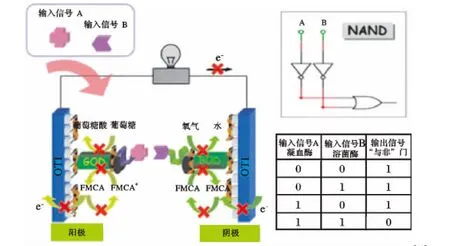
图1 模仿布尔“与非”逻辑门的适配子逻辑体系控制的生物燃料电池示意图[12]Fig.1 Schematic illustration of the assembled aptamer-based BFC logically controlled by biochemical signals that mimicks a boolean NAND logic gate
Katz等[14]基于封闭效应,发展了自供电生物分 子键盘锁安全系统(见图2),电池阳极设计了3个连锁的酶催化反应,最终将燃料葡萄糖氧化为葡萄糖酸,从而使整个体系pH从最初6.7降至4.2,电池阴极表面修饰了聚-4-乙烯基吡啶(P4VP),当体系pH>5.5时,聚合物P4VP呈现疏水收缩状态封闭电极表面,阻碍电子介体铁氰化钾[Fe(CN)6]3-在电极表面的电子传递,即Output 0;当体系pH<4.5时,聚合物P4VP的吡啶基发生质子化呈现带正电的亲水溶胀状态,不再阻碍电子介体在电极表面的电子传递,从而使BFC两极构成回路,有最大输出功率即Output 1;这个逻辑体系的输入信号设计在电池阳极,以3个连锁化学反应的催化剂酶为Input A、Input B和Input C,体系只有当3种酶依次出现A-B-C,并逐个完成催化反应,才能使体系pH降至4.5以下;其他5种输入信号C-B-A、A-C-B、B-CA、B-A-C、C-A-B,因阴极没有电子传递,无功率输出,即Output 0。这个多酶控制的键盘锁安全系统以生物分子酶的正确排列为输入密码,以电池有最大功率输出为正确通过状态,可用于构建生物计算机的密码验证安全系统;另一方面,也可作为自供电逻辑传感器用于智能化分析体内多种酶及其相互间的关系研究。
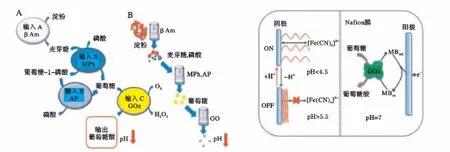
图2 基于pH控制的生物燃料电池发展的键盘锁安全系统原理示意图[14]Fig.2 The pH-switchable biofuel cell for“reading”the output signals generated by the keypad lock system
2 基于底物效应的自供电逻辑生物传感器
由于酶型BFC以酶的底物作为电池两极的生物燃料,所以电池的电化学参数均与多种底物的存在状态呈现某种逻辑关系,而自供电逻辑生物传感器大都通过输出电流,或开路电位以及输出功率等这些电化学参数达到某一定值作为输出信号Output,基于此,研究者可设计多种底物关系控制的逻辑体系,并以此发展基于BFC的自供电式逻辑传感器。董绍俊组[15]基于底物O2控制的BFC,发展了酶逻辑体系控制的传感系统(见图3),电池阳极通过GOD催化葡萄糖氧化,阴极通过BOD催化O2还原来构成回路输出电流,分别以羧酸二茂铁FMCA和 2,2-连氮-双-(3-乙基苯并噻吡咯啉-6-磺酸)(ABTS)为电子介体;O2作为阴极BOD的底物即阴极的燃料,其浓度的增加可促使电池阴极还原电流增大,而O2作为阳极GOD催化葡萄糖氧化的电子受体,其与电子介体FMCA属于竞争关系,随着O2浓度的增加,电池阳极氧化电流减小;所以当体系中O2浓度达到适中值,即空气饱和状态(O2达21%)时,电池有最大功率输出,O2浓度达到极高值或极低值均能影响电池功率的输出。整个逻辑体系以通入O2和通入N2作为Input A和 Input B,构建了“与”门和“非”门逻辑体系控制的BFC,并成功应用于体液中溶解O2的检测。随后,董绍俊组[16]以底物O2作为逻辑体系输入信号,为模拟体内血液流动的动态过程,将搅拌溶液作为另一个输入信号,建立了能同时检测血液中含氧量以及判断血流是否通畅的自供电逻辑传感装置。此类气体控制的逻辑传感器具有以下优势:其一,以气体作为输入信号控制整个体系,操作更方便;其二,利用通入不同气体来改变体系的初始态,从而快速简易地实现两种逻辑门体系间的转换;其三,基于无隔膜单极室的BFC,将两极催化剂酶固定在电极上,反应所需酶的量很少,并可发展作为一体化的装置应用于在医学诊断中。

图3 空气、氧气、氮气影响生物燃料电池输出功率的作用机制[15]Fig.3 Effect of air,O2,or N2on the power output of the BFC based on GOD/OMCs-FMCA-bioanode and BOD/OMCs-ABTS-biocathode
Zhou等[17]基于底物效应,将BFC技术与生物逻辑体系结合,发展了集病理性生物标志物检测、病情诊断、药物控释为一体的自供电智能应答体系,将其应用于腹外伤病理模型中药物的控释研究。电池阳极通过乳酸脱氢酶(LDH)催化乳酸(LA)氧化,阴极通过O2的还原输出电流,将LDH和LA作为Input A和Input B。研究者巧妙地在电池阴极固定包载药物乙酰胺酚的导电聚合物,当体系处于以下3种状态 Input(0,0)、Input(0,1)、Input(1,0)时,即LDH和LA都不存在或仅存在一种,这代表正常的生理状态,整个电池体系均无输出电流,即Output 0,从而药物依然包载于导电聚合物中;只有当体系处于Input(1,1),即LDH和LA都存在,这代表缺血缺氧等病理状态,电池电路才有电流的输出Output 1,从而导致导电聚合物将包载药物释放到体系中。这个体系通过阳极内置的逻辑体系控制BFC的功率输出,可进一步应用于医疗保健和临床诊断相关的智能化药物释放体系中,但体系仍存在一些需要改进的地方,如增强逻辑体系的诊断能力、减少复杂体系的干扰、增大BFC输出功率等。
Wang等[18]基于底物效应发展了脱氧核酶逻辑体系控制的生物燃料电池,并以此发展了自供电逻辑生物传感器,体系特征对应于“抑制”门,可用于反映病理环境中多种目标物间的抑制关系。此项研究的创新之处在于将DNAzymes活性用于逻辑关系的构建,伴随着现代生物技术的高速发展,多种底物的DNAzymes均很容易得到,所以可进一步发展为反映生理环境中多种具有DNAzymes的目标物(如凝血酶、溶解酵素、K+等)之间关系的逻辑生物传感体系。
3 基于基因调控的自供电逻辑生物传感器
Angenent等[19]报道了基因调控逻辑体系控制的微生物燃料电池(MFC),以此发展了自供电“与”门生物传感器。是以绿脓杆菌lasI/rhlI基因片段调控的两种高丝氨酸内酯作为Input A和Input B,当两者同时存在于体系,即Input(1,1),启动菌群密度感应系统调控体系产生电活性吩嗪,从而使MFC有最大电流的输出Output 1。细菌代谢反应涉及到复杂的基因调控和蛋白质调控网络,研究者利用其中一种信号转导关系发展的逻辑生物传感器,可用于实时监控致病菌群的变异和感染情况。此外,相信基于MFC发展的逻辑传感器,可通过菌群种类和菌群涉及的多种信号转导关系的选择,进一步应用于智能化控制污水处理和发酵等工作。
4 结束语
自2010年首个适配子逻辑体系控制的生物燃料电池构建以来,研究者们将生物逻辑体系与生物燃料电池的优势相结合,基于不同效应构建了多种功能性的逻辑生物传感器,普遍具有智能化、微型化、装置一体化、不需要外接电源等优点,已初步应用于反映多种目标物的存在以及智能化检测复杂样品中各物质间的关系。这种智能化的传感器属于生物计算领域,是以生物分子作为输入信号,所以可以基于多种生化反应来构建不同的逻辑体系。但同时也存在着一些局限,此类智能传感器研究的生理活性物质往往不是临床医学中关键的生物标志物,也尚不能适用于反映特殊环境下(如生理、病理等)的多种目标物,仍需进一步合理设计传感器的逻辑体系,寻找适宜的生化反应,并以此构建重要生物标志物的逻辑智能体系,或许生物体复杂的信号网络是解决这一问题的可靠途径。此外,生物燃料电池较低的输出电压和功率,也限制了这种自供电装置的实际应用,研究者或可通过改进电池两极电子介体和两极物质的固定方式来完善这一问题。最终将这种基于生物燃料电池发展的智能逻辑生物传感器广泛用于临床医学检测和诊断以及多种病理环境下药物的控释中。
[1]Wang J.Electrochemical glucose biosensors[J].Chem Rev,2007,108(2):814-825.
[2]Zhou M,Dong S.Bioelectrochemical interface engineering:Toward the fabrication of electrochemical biosensors,biofuel cells,and self-powered logic biosensors[J].Acc Chem Res,2011,44(11):1232-1243.
[3]Campuzano S,Wang J.Nanobioelectroanalysis based on carbon/inorganic hybrid nanoarchitectures[J].Electroanalysis,2011,23(6):1289-1300.
[4]Barton S C,Gallaway J,Atanassov P.Enzymatic biofuel cells for implantable and microscale devices[J].Chem Rev,2004,104(10):4867-4886.
[5]Heller A.Miniature biofuel cells[J].Phys Chem Chem Phys,2004,6(2):209-216.
[6]Kim J,Jia H,Wang P.Challenges in biocatalysis for enzyme-based biofuel cells[J].Biotechnology Advances,2006,24(3):296-308.
[7]Arnaud A,Montoro G,Analog C.Fully integrated signal conditioning of an accelerometer for implantable pacemakers[J].Analog Integrated Circuits and Signal Processing,2006,49(3):313-321.
[8]Wang J,Katz E.Digital biosensors with built-in logic for biomedical applications——biosensors based on a biocomputing concept[J].Anal Bioanal Chem,2010,398(4):1591-1603.
[9]Szacilowski K.Digital information processing in molecular systems[J].Chem Rev,2008,108(9):3481-3548.
[10]Katz E,Privman V.Enzyme-based logic systems for information processing[J].Chem Soc Rev,2010,39(5):1835-1857.
[11]Wang J,Katz E.Digital biosensors with built-in logic for biomedical applications[J].Isr J Chem,2011,51(1):141-150.
[12]Zhou M,Dong S,Wang E,et al.Aptamer-controlled biofuel cells in logic systems and used as self-powered and intelligent logic aptasensors[J].J Am Chem Soc,2010,132(7):2172-2174.
[13]Zhou M,Dong S,Wang E,et al.An IMP-Reset gate-based reusable and self-powered“smart”logic aptasensor on a microfluidic biofuel cell[J].Lab Chip,2010,10(21):2932-2936.
[14]Halamek J,Tam T K,Katz E,et al.Self-powered biomolecular keypad lock security system based on a biofuel cell[J].Chem Commun,2010,46(14):2405-2407.
[15]Zhou M,Wang F,Dong S,et al.Boolean logic gates based on oxygen-controlled biofuel cell in“one pot”[J].Electrochimica Acta,2011,56(11):4112-4118.
[16]Zhou M,Zheng X,Dong S,et al.‘Non-destructive’biocomputing security system based on gas-controlled biofuel cell and potentially used for intelligent medical diagnostics[J].Bioinformatics,2011,27(3):399-404.
[17]Zhou M,Zhou N,Wang J,et al.A self-powered“Sense-Act-Treat”system that is based on a biofuel cell and controlled by boolean logic[J].Angew Chem Int Ed,2012,51(11):2686-2689.
[18]Zhou M,Kuralay F,Wang J,et al.DNAzyme logic-controlled biofuel cells for self-powered biosensors[J].Chem Commun,2012,48(32):3815-3817.
[19]Li Z,Katz E,Angenent L T,et al.Bacteria-based AND logic gate:A decision-making and self-powered biosensor[J].Chem Commun,2011,47(11):3060-3062.

