尼龙-6的合成工艺研究
周诗彪, 肖安国, 鲁 鹏, 杨 静, 黄小兵, 庄永兵
尼龙-6的合成工艺研究
周诗彪*, 肖安国, 鲁 鹏, 杨 静, 黄小兵, 庄永兵
(湖南文理学院 化学化工学院, 湖南 常德, 415000)
以己内酰胺为原料, 无机酸为催化剂, 水为开环引发剂, 己二酸为稳定剂, 合成了聚己内酰胺(PA6). 探讨了不同聚合条件对尼龙-6聚合转化率的影响, 及不同聚合条件对尼龙-6的软化温度的影响, 并对产物进行了产率测算、软化温度测试和红外表征. 研究表明, 在反应温度240 ℃、反应时间3.5 h、己内酰胺和浓磷酸质量比为100: 2、己内酰胺和己二酸质量比为100: 3的聚合条件下, 己内酰胺转化率可高达92.0%, 所合成的聚合物粘均分子量为6.9×104g/mol.
己内酰胺; 聚己内酰胺; 聚合工艺; 开环剂
聚酰胺(PA)俗称尼龙, 主要包括PA6、PA66、PA11、PA610、PA1010等系列产品, 其中PA6和PA66为主导产品, 占聚酰胺的90%以上. 而尼龙-6由于突出的易染色性和柔软耐磨性, 不仅在工程上广泛使用, 还非常适合做印花织物和生活用品. 己内酰胺聚合方法有水解聚合[1]、阴离子聚合[2—8]、阳离子聚合[9]等, 生产工艺有间歇聚合与连续聚合工艺, 不论哪种聚合方法与合成工艺都存在着己内酰胺的转化率不够高的问题[10—14]. 因此, 探索聚合新方法、优化合成工艺以提高己内酰胺的转化率有较大的实际意义. 本研究旨在优化尼龙-6合成工艺条件, 期望在保证尼龙-6产品质量的前提下最大限度地提高己内酰胺的转化率.
1 实验部分
1.1 主要实验材料与仪器
己内酰胺, 化学纯, 国药集团化学试剂有限公司; 浓硫酸, 分析纯, 株洲石英化玻有限公司; 浓磷酸, 分析纯, 长沙分路口塑料化工厂; 氢氧化钠, 分析纯, 天津市风船化学试剂科技有限公司; 己二酸, 分析纯, 天津市化学试剂公司; 无水乙醇, 分析纯, 长沙安泰精细化工公司; 甲酸, 分析纯, 天津韦斯实验用品有限公司.
CL-4A型磁力加热搅拌器, 郑州长城科工贸有限公司;傅立叶变换红外光谱仪Nicolet 370型,美国尼高力仪器公司; BS3005-O电子天平, 北京赛多利斯天平有限公司; YKKYFM70型雪花制冰机, 北京长流科学仪器公司; YW-1型远红外电热干燥箱, 江苏省东台市电器厂; KQ5200B超声波清洗机, 昆山市超声仪器有限公司; 循环水式真空泵, 河南巩义市英峪豫华仪器厂.
1.2 实验方法
1.2.1 己内酰胺开环聚合
在三口瓶中加入一定量的己内酰胺, 在减压下加热除去原有的水, 以浓磷酸为催化剂、水为开环聚合引发剂、己二酸为分子量稳定剂按一定的比例依次加入到三口瓶中. 通氮气隔氧保护, 用油浴锅加热至160 ℃左右, 预聚反应持续1 h, 使己内酰胺开环成直链状态. 然后升温至250 ℃左右继续进行聚合反应, 反应持续一段时间后, 以减压或氮气流的方式带走原体系中及反应生成的水和小分子低聚物. 待聚合产物变得粘稠, 缓慢冷却制得尼龙-6, 反应时间约为4~5 h.
1.2.2 产品纯化
以浓硫酸作为尼龙-6的良溶剂, 稀硫酸作为不良溶剂[15], 将所得的尼龙产品定量溶解于95%浓硫酸中, 过滤除去不溶性杂质, 然后用水稀释使得浓硫酸变为稀硫酸, 溶解的尼龙-6将发生沉降, 形成白色絮状沉淀. 待基本沉淀完成, 用蒸馏水和NaOH稀溶液将过滤后的尼龙-6洗涤至PH约为7左右, 真空干燥48 h即可得到纯化产物.
1.2.3 转化率的计算

1.3 测试与分析
1.3.1 软化温度的测定
将经纯化处理的尼龙-6于真空干燥箱中干燥至恒重后, 然后, 取部分试样置于X-5(控温型)显微熔点测定仪上进行软化温度的测定. 测定过程中, 先将温度升至80 ℃, 然后以10 ℃/min的速度缓慢升温, 在显微镜中观察尼龙-6粉末的软化情况, 并记录其软化温度.
1.3.2 红外光谱分析
将干燥的KBr和干燥处理的尼龙-6产品按质量比100:1于红外灯下进行混合研磨, 并进行压片, 用傅立叶红外光谱仪进行红外光谱分析.
1.3.3 粘度及分子量的测定
用粘度法测定尼龙-6的粘均相对分子质量, 以40%的浓硫酸作溶剂, 在25 ℃的恒温条件下测定, 取3次测定的平均值[16]. 粘度与分子量关系式如下:

其中为特性粘度, K = 5.92×10-2 cm3·g-1, α = 0.69[17], 为粘均分子量.
2 结果与讨论
2.1 不同聚合条件对转化率的影响
2.1.1 压力与反应温度对转化率的影响
向反应容器中加入20 g己内酰胺, 加入己内酰胺质量3%的浓磷酸为催化剂, 并加入己内酰胺质量1%的水, 在聚合温度分别为220、230、240、250 ℃下聚合, 反应持续一段时间后, 通过减压或氮气流的方式, 带走水及低分子物. 测定其转化率, 结果如图1所示.
由图1可知, 无论是在减压下聚合还是充氮气常压聚合, 转化率随反应温度的增加而增加, 且反应温度在240 ℃时转化率达最大值, 然后, 再升高反应温度, 转化率随之下降; 在减压下聚合的转化率均高于相同温度的常压聚合的转化率. 己内酰胺聚合反应分链引发、链增长和链平衡3个步骤. 根据吕·查德原理, 若不断地排出反应体系中生成及未参加开环反应的水, 则有利于反应向相对分子质量增高的方向移动, 并减轻了高聚物的水解程度; 水解反应是吸热反应, 若降低其反应的温度, 则高聚物的水解速度将大大低于其逆反应的速度, 这样最终反应体系中低聚物含量将降低, 而聚合温度影响聚合反应的速度, 同时也影响小分子排出速度, 这样存在着最佳反应温度. 采用减压聚合有利于排出反应体系中生成及未参加开环反应的水, 因此, 可得到较高的转化率[18].
2.1.2 催化剂种类对转化率的影响
己内酰胺聚合的催化剂种类很多, 且各有优点[19]. 本研究采用的催化剂为无机酸即浓硫酸和浓磷酸. 向反应容器中加入20 g己内酰胺, 催化剂加入量为己内酰胺质量的3%, 并加入己内酰胺质量1%的水, 在聚合温度分别为220、230、240、250 ℃下聚合, 反应持续一段时间后, 通过减压方式带走小分子物, 测定转化率, 结果如图2所示.

图2 催化剂种类对转化率的影响
由图2可以看出, 随着反应温度的升高, 己内酰胺的转化率一般先升高后降低. 其原因可能是在较高温下, 浓硫酸能较快的水解尼龙-6; 浓磷酸本身含水, 反应过程中也有水生成, 聚合生成的尼龙-6会和水反应而降解. 结果表明: 不论选用何种催化剂, 温度过高都会促进水解反应的进行; 在相同的条件下浓磷酸的催化效果比浓硫酸的好.
2.1.3 催化剂用量对转化率的影响
己内酰胺是不能自动进行聚合反应的, 必须存在少量的水和催化剂才行[20]. 向反应容器中加入20 g己内酰胺, 以浓硫酸或浓磷酸, 催化剂的用量分别为己内酰胺质量的0.5%, 1%, 2%, 3%, 5%, 并分别加入己内酰胺质量1%的水, 在240 ℃下聚合3.5 h得转化率, 分别对产物转化率进行对比, 结果如图3所示.
由图3可以看出, 随着催化量的加大, 己内酰胺的转化率一般先升高后降低. 其原因可能是在较高的反应温度下, 浓硫酸能水解聚己内酰胺; 浓磷酸本身含水, 反应过程也生成水, 聚合生成的尼龙会和水反应而降解. 结果表明: 浓硫酸催化下, 己内酰胺与浓硫酸最佳质量比为100: 1, 浓磷酸催化下, 己内酰胺与浓磷酸最佳质量比为100: 2, 且以浓磷酸催化效果更好.

图3 催化剂用量对转化率的影响
2.1.4 聚合时间对转化率的影响
聚合时间的长短直接影响着聚合度的高低. 向反应容器中加入20 g己内酰胺, 0.4 g浓磷酸, 在氮气保护下, 聚合温度240 ℃, 聚合时间分别为2.5、3、3.5、4.5 h, 将测得的转化率对反应时间作图, 其结果如图4所示.
在聚合过程中, 反应速度随时间变化. 它起初有一个诱导期, 反应速度随时间增加而增加, 当单体转化率达到40%~42%时, 反应速度最快, 随后反应速度随时间的延长而降低, 直至平衡. 诱导期的存在主要是因为己内酰胺在水的作用下开环需要一定的时间. 自动加速作用是因为己内酰胺水解以及反应过程中生成的氨基和羧基都有开环作用, 因此, 反应速度随体系中氨基和羧基的增加而增加. 到达最大反应速度后, 由于短链的缩聚占优势, 氨基和羧基的数目减少, 反应速度也逐渐减慢. 然后, 随着时间的增加而降低, 直到平衡. 聚合时间越长, 单体转化率和聚合物平均分子量都随着增加, 直至平衡. 在聚合反应后期, 聚合时间越长, 聚合物分子量分布越均匀. 从图4可以看出, 在相同反应条件下, 随着反应时间增加, 己内酰胺的转化率先上升后下降, 其原因可能是持续时间越长, 反应产生的单体小分子和水难以排出而使得产物的水解越严重所致, 但采用减压聚合会使这一现象有所改善.

图4 聚合时间对尼龙-6聚合转化率的影响
2.2 不同聚合条件对尼龙-6的软化温度的影响
尼龙-6聚合物没有标准熔点, 以软化温度表示. 聚合物的聚合度不同其分子量不同, 聚合物的软化温度也会不同.
2.2.1 压力与反应温度对尼龙-6的软化温度的影响
向反应容器中加入20 g己内酰胺, 以浓磷酸为催化剂, 加入的质量比为3%, 并加入己内酰胺质量1%的水, 在聚合温度分别为220、230、240、250 ℃下聚合, 反应持续一段时间后, 通过减压或氮气流的方式带走小分子, 将聚合物的软化温度进行对比, 结果如图5所示.

图5 压力与反应温度对尼龙-6的软化温度的影响
由图5可以看出, 通过减压聚合处理后所得产物的软化温度较没有进行减压聚合的要高; 随着反应温度的升高, 聚合物的软化温度逐步增高, 达到最大值后, 又随反应温度的升高而聚合物的软化温度下降.
2.2.2 催化剂种类对尼龙-6的软化温度的影响
向反应容器中加入20 g己内酰胺, 催化剂加入量为己内酰胺质量的3%, 并加入己内酰胺质量1%的水, 在聚合温度分别为220、230、240、250 ℃下聚合, 反应持续一段时间后, 通过减压或氮气流的方式带走小分子. 分别对产物软化温度进行对比, 结果如图6所示:
由图6可以看出, 随着反应温度的升高, 所得尼龙-6产品的熔化温度呈先升高后降低的趋势. 且浓磷酸催化所得的尼龙-6产品软化温度均高于浓硫酸催化所得的尼龙-6产品. 其原因可能是: 随着温度的升高, 尼龙-6由于酸的存在受到的水解反应越来越明显, 导致聚合的尼龙-6又发生降解, 而使得软化温度降低, 而硫酸的水解催化作用要强于磷酸.
2.2.3 催化剂用量对尼龙-6的软化温度的影响
向反应容器中加入20 g己内酰胺, 催化剂的用量分别为己内酰胺质量的0.5%, 1%, 2%, 3%, 5%, 并分别加入己内酰胺质量1%的水, 在240 ℃下聚合3.5 h得转化率, 分别对产物软化温度进行测试对比, 结果如图7所示.
由图7可以看出, 随着催化量的加大, 尼龙-6产品的软化温度一般先升高后降低. 其原因可能是在较高的反应温下, 酸催化水解聚己内酰胺速度加快所致; 浓磷酸本身含水, 反应过程也生成水, 聚合生成的尼龙会由于酸的存在和水反应而发生降解. 结果表明, 浓硫酸催化下, 己内酰胺与浓硫酸最佳质量比为100: 1, 浓磷酸催化下, 己内酰胺与浓磷酸最佳质量比为100: 2, 且以浓磷酸催化效果更好.
2.2.4 聚合时间对尼龙-6的软化温度的影响
在氮气保护下, 聚合温度240 ℃, 向反应容器中加入20 g己内酰胺, 0.4 g浓磷酸, 聚合时间分别为2.5、3、3.5、4.5 h, 其聚合物的软化温度如图8所示.
由图8可以看出, 在其他实验条件一定的情况下, 随着反应时间的增加, 尼龙-6的软化温度先迅速升高, 然后逐渐趋于平稳; 在聚合反应后期, 随着聚合时间越长, 聚合物软化温度增加不明显. 其原因是随着聚合时间延长, 单体转化率和聚合物平均分子量都随之增加, 直至反应达到平衡.

图6 催化剂种类对尼龙-6 的软化温度的影响

图7 催化剂用量对尼龙-6 的软化温度的影响
2.3 样品的红外光谱分析
图9是样品的红外光谱图. 从图9可看出, 在3 299.1 cm-1、2 930.0 cm-1、1 635.9 cm-1、1 540.6 cm-1均有较强的吸收峰, 其中3 299.1 cm-1是分子间氢键及自身羟基振动吸收峰, 2 930.0 cm-1是烷烃—CH2—CH2—的伸缩振动吸收峰, 1 635.9 cm-1是C=O的伸缩振动吸收峰, 1 540.6 cm-1是N—H的伸缩振动吸收峰. 这些振动吸收峰表明该产物具有典型的高分子聚酰胺结构特征峰[18].

图8 聚合时间对尼龙-6 的软化温度的影响
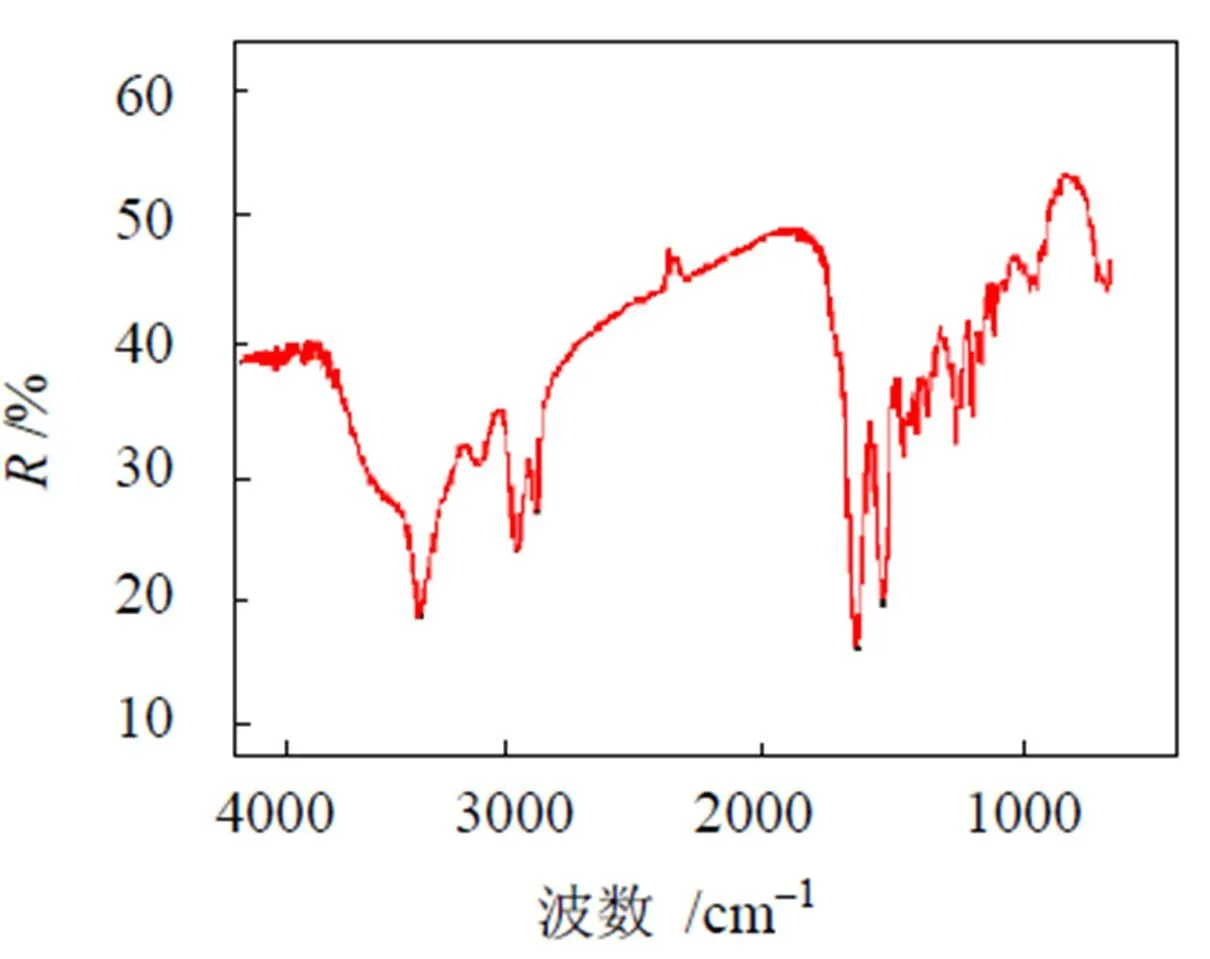
图9 尼龙6 的红外光谱图
2.4 分子量稳定剂对产品性能的影响
理论上讲可以用改变尼龙-6聚合物中残余水量的方法来控制它的分子量, 但实际上很难做到, 因为在高温下熔融状态的尼龙-6极易氧化, 而且这样得到的聚合物平均分子量很不稳定. 因此, 在实际生产中, 一般都在聚合时加入一些能封闭这些大分子端基的物质来控制分子量, 这些物质称之为分子量稳定剂.
常用的分子量稳定剂有己二酸、醋酸等有机酸, 它们的端羧基与聚合体大分子的端氨基作用后, 使大分子的两端均为羧基、羧基或乙酰基, 这样就能阻止大分子链的进一步增长, 使聚合体的分子量稳定下来. 本研究采用的分子量稳定剂为己二酸, 通过己二酸添加量的不同进行对照实验, 实验条件采用前面所得到的较优工艺条件. 对反应所得产品进行软化温度测定, 结果如图10所示.

图10 不同己二酸作用所得尼龙-6 软化温度
由图10可知, 加入己二酸对己内酰胺聚合度的提高有一定的促进作用, 使尼龙-6的软化温度有所升高, 分子量更加均匀稳定. 然而己二酸加入过多则抑制尼龙-6的持续扩链, 尼龙-6的分子量将达不到预期标准. 故己内酰胺和己二酸最佳质量比例为100: 3.
3 结论
通过对浓磷酸和浓硫酸催化己内酰胺聚合工艺的探讨, 考察了催化剂种类和用量、聚合时间、聚合温度对聚合反应转化率和软化温度的影响, 得出较优的反应条件为: 以浓磷酸为催化体系, 反应温度为240 ℃, 聚合时间为3.5 h, 己内酰胺和浓磷酸的质量比为100: 2, 己内酰胺和己二酸质量比例为100: 3, 在该条件下, 己内酰胺的转化率达到92.0%, 用粘度法测得粘均分子量为6.9×104g/mol.
[1] 布伊斯W,霍恩恩R J H. ε-己内酰胺聚合生成聚酰胺-6的方法[P]. CN: 99814711, 2002-01-16.
[2] Daniel Crespy, Katharina Landfester. Anionic polymerization of ε-Caprolactam in miniemulsion: synthesis and characterization of polyamide-6 nanoparticles[J]. Macromolecules, 2005, 38: 6882—6887.
[3] Demicheli A, Russo S, Marianib A. Synthesis and characterization of ε-caprolactam-L-phenylalanine copolymers[J]. Polymer, 2000, 41: 1481—1486.
[4] Laura Ricco, Orietta Monticelli, Saverio Russo, et al. Fast-Activated Anionic Polymerization of-caprolactam in suspension. Macromol[J]. Chem Phys, 2002, 203: 1436—1444.
[5] Mateva R, Petrov P, Rousseva S, et al. On the structure of poly-ε-caprolactams, obtained with bifunctional N-carbamyl derivatives of lactams[J]. European Polymer Journal, 2000, 36: 813—821.
[6] Laura Ricco, Saverio Russo. Caprolactam-laurolactam copolymers: fast activated anionic synthesis, thermal properties and structural investigations[J]. Macromol Chem Phys, 2001, 202: 2114—2121.
[7] Laura Ricco, Saverio Russo, Orietta Monticelli, et al.-Caprolactam polymerization in presence of polyhedral oligomeric silsesquisoxanes(POSS)[J]. Polymer, 2005, 46: 6810—6819.
[8] 杨军. PA6聚合生产技术[J]. 合成纤维工业, 1996, 19(2): 35—42.
[9] 王玉萍, 王辉. PA6民用丝推广前景及纺丝设备的关键[J]. 纺织信息周刊, 2000,(34),19.
[10] 赵丽英. 我国聚己内酰胺工业的发展及展望[J]. 河北化工, 2004(2): 16—18.
[11] 王文波, 余跨纲, 李练武. 浓缩液直接回用的聚己内酰胺聚合工艺开发[J]. 合成纤维工业, 2003, 26(4): 22—23.
[12] 周吕. 聚己内酰胺生产中的三废回收[J]. 成纤维工业, 1999, 13(4): 21—27.
[13] 李智范. 用废旧聚己内酰胺生产己内酰胺的方法[P]. CN: 1374333A, 2002-10-16.
[14] 葛立柱, 王鸿儒. 低温下己内酰胺低聚物的合成[J]. 陕西科技大学学报, 2007, 25(2): 20—23.
[15] [西德]沃尔默特B. 著. 孙以实, 译. 聚合物化学(上)[M]. 北京: 化学工业出版社, 1980: 77—79.
[16] 张风才. PA6减压后聚合生产工艺[J]. 合成纤维工业, 1999, 22(5): 50—52.
[17] 王积涛, 张宝申, 王永梅, 等. 有机化学[M]. 2版. 天津: 南开大学出版社, 2009: 431—446.
[18] 邓芹英, 刘岚, 邓慧敏, 等. 波谱分析教程[M]. 北京: 科学出版社, 2003: 20—28.
[19] 赵华山, 姜胶东, 吴大成, 等. 高分子物理学[M]. 北京: 中国纺织工业出版社, 1982: 92—93.
[20] 谢崇禹. 影响聚己内酰胺质量的主要因素[J]. 纤维复合材料, 2006(2): 33—34.
Study on the synthetic process of Nylon-6
ZHOU ShiBiao, XIAO AnGuo, LU Peng, YANG Jin, HUANG XiaoBing, ZHUANG YongBing
(Department of Chemistry and Chemical Engineering, Hunan University of Arts and Science, Changde 415000, China)
Polycaprolactam was synthesized via ring-opening polymerization using water as initiator. In the polymerization process, oxalic acid was adopted for stabilizer. The influences of polymerization condition on the conversion rate and softening temperature of resultant polymer were investigated. The optimal polymerization conditions were determined with the results of the conversion rate, softening temperature and infrared spectra of resultant polycaprolactam. Caprolactam conversion rate was up to 92% under the reaction temperature of 240 ℃ when the ratios of the phosphoric acid and oxalic acid to caprolactam was 0.02 and 0.03, respectively, viscosity average molecular weight of resultant polymer was about 6.9 × 104g/mol.
caprolactam; polycaprolactam; polymerization process; ring opening agent
TQ 323.6
1672-6146(2014)01-0016-06
10.3969/j.issn.1672-6146.2014.01.005
通讯作者email: zhsb1961@163.com.
2014-01-06
湖南省自然科学基金项目(14JJ2123); 2013年常德市科技计划重点项目.
(责任编校:刘晓霞)

