无表面活性剂 快速沉淀法制备盐酸吡格列酮微粉
于世华,陈 萍,程振玉,连丽丽
(吉林化工学院化学与制药工程学院,吉林 吉林 132022)
无表面活性剂 快速沉淀法制备盐酸吡格列酮微粉
于世华,陈 萍,程振玉,连丽丽
(吉林化工学院化学与制药工程学院,吉林 吉林 132022)
本研究在不加入表面活性剂条件下采用快速沉淀法制备盐酸吡格列微粉,分别利用扫描电镜( SEM )、X射线衍射( XRD)、红外光谱分析( FT-IR)等分析方法对原药及产品的性质进行了表征。SEM分析表明,使用快速沉淀法制备的盐酸吡格列酮超微粉尺寸降低,粒度分布均匀,FT-IR、X RD分 析表明,微粉化 前后药物的化学结构并未发生改变,粒度明显减小,结晶度明显降低。
盐酸吡格列酮;快速沉淀法;微粉
盐酸吡格列酮[(±)5-{4-[2-(5-乙基-2-吡啶基)乙氧基]苯甲基}-2,4-噻唑二酮盐酸盐]属于噻唑烷二酮类抗糖尿病药物,对治疗Ⅱ型糖尿病有明显的疗效,且副作用较少[1-4],它的研制和开发对糖尿病以及与胰岛素抵抗的相关疾 病的治疗产生重大的积极作用。由于盐酸吡格列酮药物水溶性差[5],所以导致其溶解度和溶出速率较差,影响其生物利用度。根据Noyese-Whitney方程,减小药物粒径是 提高药物饱和溶解度和溶出率的有效手段[6]。
传统的减小药物颗粒的方法主要包括气流粉碎法[7]、高压均质、喷雾干燥、冷冻干燥、超临界流体技术[8],然而这些技术具有能耗较高,药物粒度较大,产品粒度分布不均匀,药品回收率低等缺点。相比较而言,液相沉淀法(主要包括反应沉淀法和抗溶剂沉淀法)具有成本低、易操作、易工业化,形貌、粒径大小可控等优点。
抗溶剂沉淀法主要基于溶剂-抗溶剂在快速混合过程中改变药物的过饱和度,将含有药物的有机溶剂加入到快速搅拌的抗溶剂中,由于药物在抗溶剂中几乎是不溶的,所以药物在混合溶液中快速达到超饱和,使得成核率大于晶体生长的速率,增加了成核率,有助于形成微小的药物颗粒。近几年来,有大量关于抗溶剂沉淀法[9-10]制备药物微粉的研究,并取得了很好的效果。
1 材料、方法与表征
1.1 材料与仪器
盐酸吡格列酮(PH,纯度99.9%),甲醇(分析纯),蒸馏水(实验室自制),乙醇(分析纯),氢氧化钠(分析纯)。
D8 FOCUSX-射线衍射仪,Nicolet-6700型傅立叶红外光谱仪,JSM-6490LV扫描电镜,UV-2550紫外可见分光光度计,AUX-320分析天平。
1.2 实验方法
一定质量的盐酸吡格列酮溶解在甲醇中配置成一定浓度的药物溶液,0.45μm的微孔滤膜过滤除去不溶物,蒸馏水为反溶剂,在一定的实验条件下,将盐酸吡格列酮的甲醇溶液在磁力搅拌下快速倒入反溶剂中,搅拌一定时间得到混悬液,经减压过滤、干燥得到微粉化产品。采用SEM、FT-IR、XRD对微粉化产品的性质进行表征。
1.3 盐酸吡格列酮 微粉的表征
1.3.1 形貌及粒径尺寸分析(SEM)
采用JSM-6490LV型SEM观察PH形貌和粒径尺寸。把样本固定在扫描电镜专用双面 导电胶上,使用溅射镀膜机在氩气氛 围下对样品镀金(50mA,3 min),观察粒子形貌。
1.3.2 傅里叶红外光谱分析(FT-IR)
样品的红外光谱采用Nicolet-6700型傅里叶红外光谱仪进行测定,采用KBr压片(KBr,样品=150∶1),光谱分辨率4 cm-1,测量范围4000~400 cm-1。
1.3.3 粉末X射线衍射分析(XRD)
晶体结构测定采用德国布鲁克粉末X射线衍射仪对样品进行扫描分析,测试条件:Cu靶(Kα=0.15418 nm),管电流:40 mA,管电压:40 kV。
2 结果与讨论
为了进一步证明抗溶剂沉淀过程对粒径分布及理化性质的影响,在上述优化的条件下分别采用SEM 、XRD、FT- IR和DSC进行了表征,优化的实验条件为:药物溶液浓度为25 mg·mL-1,反溶剂/溶剂体积比为20,体系温度为10 ℃。
2.1 形貌分析
图1为PH原药与微粉化产品的电镜图,PH原料的粒径较大,大约在几十微米,且分布不均匀,优化的抗溶剂法制备的微粉化产品的粒径明显比原药的粒径小,且大小分布均匀。
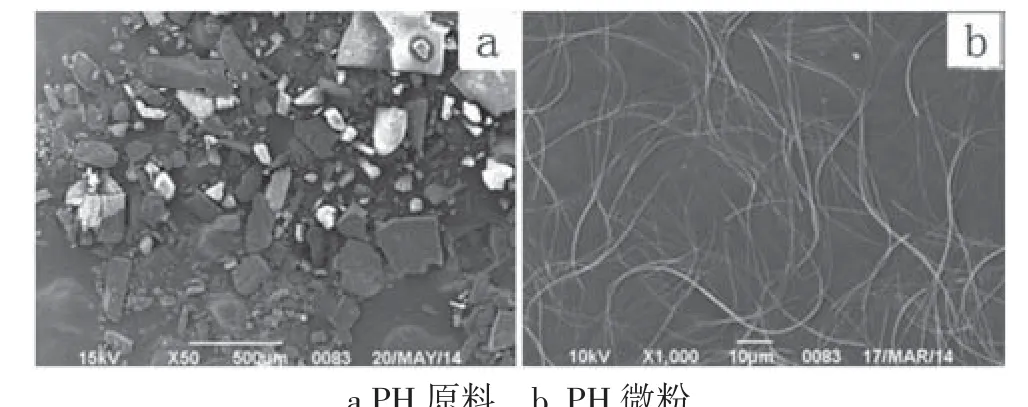
图1 PH的扫描电镜图
2.2 FT-IR分析
PH原药与微粉化产品的红外光谱图如图2所示。通过对比可知,原药与微粉化产品的吸收峰位置和强度基本一致,即物质的化学结构在微粉化前后未发生变化,说明抗溶剂制备PH过程属于物理变化。
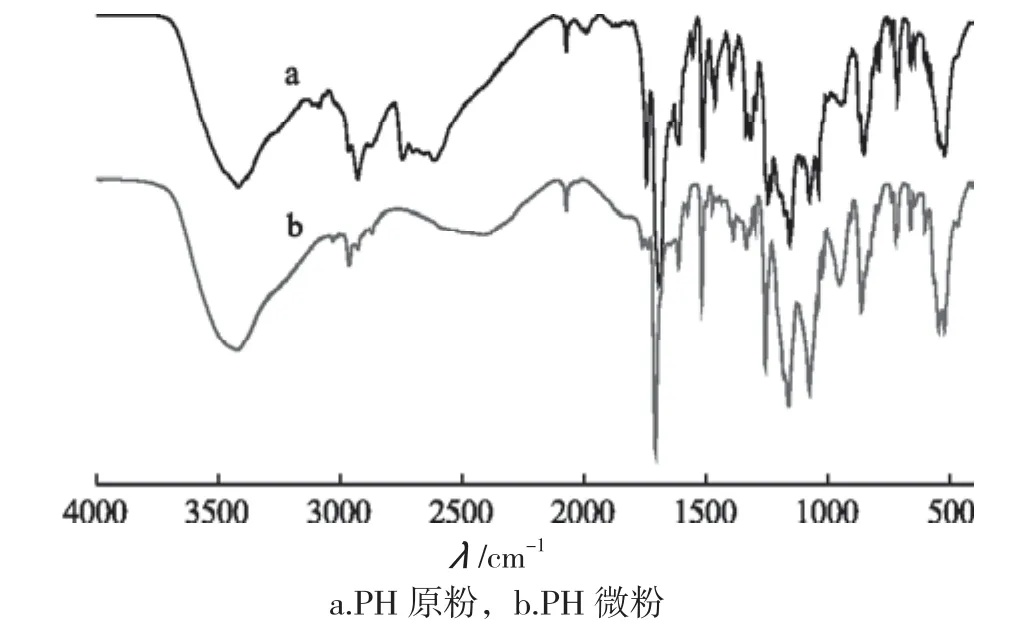
图2 PH的红外光谱图
2.3 晶体结构分析
图3为PH原粉和微粉的XRD谱图,微粉化前后衍射峰的位置完全改变,说明微粉化前后药物的晶体结构发生了改变,原粉的衍射峰强度明显高于微粉,说明微粉化以后结晶度明显降低,分别计算了微粉化前后主衍射峰的半高宽(FWHM)及晶粒尺寸,其中晶粒尺寸按照谢乐公式计算:

其中:dXRD为晶粒尺寸;K为常数,0.89;λ为衍射线波长,0.154184 nm;β为试样宽化,rad;θ为衍射角,rad。FWHM和dXRD计算结果见表1。
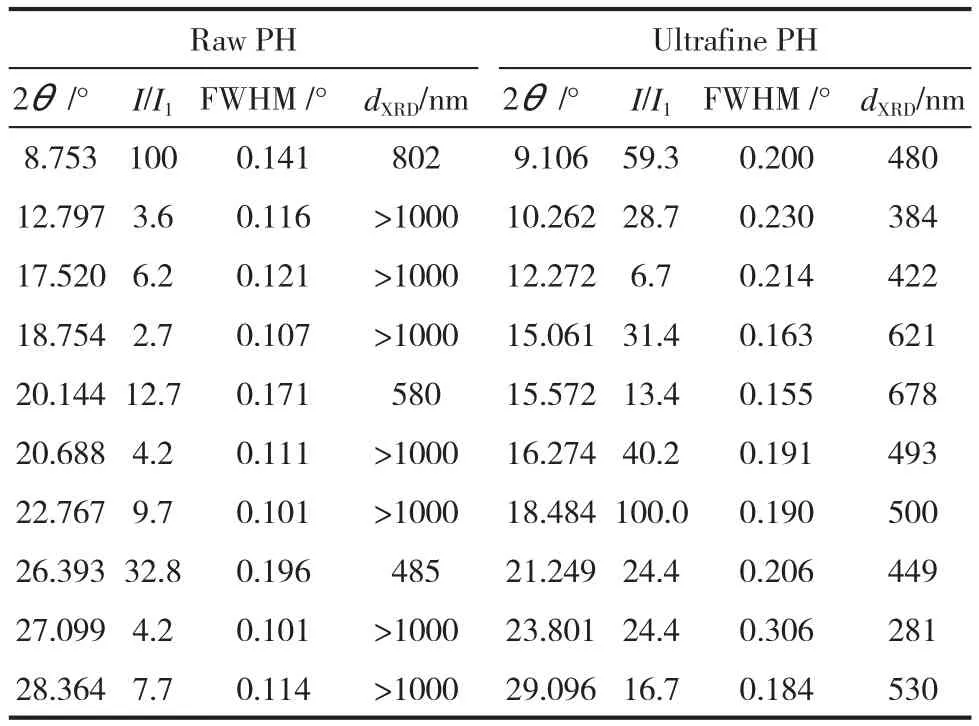
表1 Raw PH与Ultrafine PH半高宽的比较
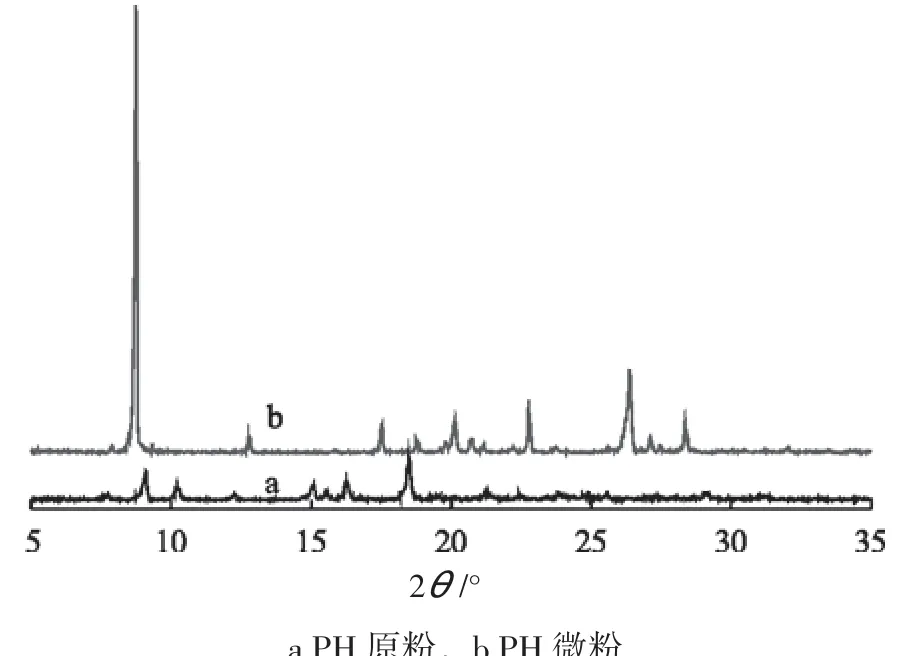
图3 PH的XRD图
根据式(1)能推断出FWHM与物质的粒径成反比,半高宽越大,粒径越小。从表1可以看出,PH原粉与微粉的平均半高宽分别为0.12°和0.20°,说明微粉化以后半高宽宽化比较严重,晶粒细化是造成微粉化的主要原因,这与SEM分析结果一致。
3 结论
本研究在加入表面活性剂的条件下,使用反溶剂沉淀法成功地制备了盐酸吡格列酮药物超微粉体。实验以甲醇和水分别作为溶剂、反溶剂,药物溶液浓度为25mg·mL-1,反溶剂/溶剂体积比为20,体系温度为10℃,混合强度(磁力搅拌速率)为1000r·min-1。此外,SEM分析表明,使用反溶剂沉淀法制备的盐酸吡格列酮超微粉体在粒度和形貌方面都优于原药,FT-IR分析表明,微粉化前后药物的化学结构并未发生改变,XRD结果表明,微粉化后药物的结晶度明显降低。
[1] Einhorn D, Rendell M, Rosenzweig J. Pioglitazone hydrochloride in combination with metformin in the treatmentof type 2 diabetes mellitus:A randomized, placebo-controlled study[J]. Clinical Therapeutics, 2000, 22(12):1395-1409.
[2] Wang Y F, YeS D, HuY Y. The effect of hydrochloride pioglitazone on urinary 8-hydroxy-deoxyguanosine excret ion in type 2 diabetics[J].Journal of Diabetes and Its Complications, 2013(27):75-77.
[3] SatoK, AwasakiY, KandoriH. Suppressive effects of acidforming diet against the tumorigenic potential of pioglitazone hydrochloride in the urinary bladder of male rats[J].Toxicology and Applied Pharmacology, 2011(251):234-244.
[4] ChilcottJ, PaulT, Jones M L.A Systematic Review of the Clinical Effectiveness of Pioglitazone in the Treatment of Type 2 Diabetes Meilitus[J].Clinical Therapeutics, 2011, 23(11):1792-1823.
[5] Tao M Y, Wang Z, Gong J B. Determination of the Solubility,Dissolution Enthalpy,and Entropy of Pioglitazone Hydrochloride (Form II) in Different Pure Solvents[J].Industrial & Engineering Chemistry Research.2013(52):3036-3041.
[6] Kesisoglou F, Panmai S, Wu Y. Nanosizing-oral formulation development and biopharmaceutical evaluation [J]. Advanced Drug Delivery Review, 2007(59):631-644.
[7] Rasenack N, Steckel H, Mu¨ller BW. Micronization of anti-Inflammatory drugs for pulmonary delivery by a controlled crystallization process[J]. Pharm. Sci., 2003, 92(1):35-38.
[8] Ste ckel H, Thies J, Mu¨ller BW. Micronizing of steroids for pulmonary delivery by supercritical carbon dioxide.Int[J]. Pharm, 1997(152): 99.
[9] Kim S, Kiong W, Dong Y C, et al. Preparation and physicochemical characterization of trans-resveratrol nanoparticles by temperature-controlled antisolvent precipitation[J].Journal of Food Engineering, 2012(108):37-42.
[10] Meng X X, Chen Y H, Cubhendu R, et al. Stabilizing dispersions of hydrophobic drug molecules using cellulose ethers during anti-solvent synthesis of micro-particulates[J]. Colloids and Surfaces B:Biointerfaces, 2009(70):7-14.
Preparation of Micro-scale Particulates of Pioglitazone Hydrochloride by Rapid Precipitation without Surfactants
YU Shi-hua, CHEN Ping, CHENG Zhen-yu, LIAN Li-li
(College of Chemical&Pharmaceutical Engineering, Jilin Institute of Chemical Technology, Jilin 132002, China)
Th e microsized pioglitazone hydrochloride(PH) was prepare d via the rapid precipitation proces without surfa ctant. The microsize d pioglitazone hydrochloride and the raw drug were well characterized by scanning electron microscopy (SEM), powder X-ray diffraction (XRD), fourier transfo rm infrared spectrometry (FT-IR). The study indicated that after microniza tion, the particle size decreased, the range of particle size distribution became well through SEM. FT-IR and XRD analysis indicated the particle size decreased and ccrystallinity decreased during the process and no change in chemical group structure.
PH; rapid precipitation; micro-scale particulates
O 626
A
1671-9905(2014)10-0014-03
于世华(1984-),助教,硕士研究生,研究方向为药物微粉制备及水溶性研究。E-mail:ysh@jlict.edu.cn
2014-08-28

