生物质催化转化制备呋喃基化学品和酚类化合物
仝新利,燕勇涛,王艳华
(天津理工大学 化学化工学院 天津市有机太阳能电池和光化学转化重点实验室,天津 300384)
随着化石资源的逐渐枯竭和CO2排放导致的“温室效应”日益加剧,以生物质为原料生产化工产品和液体燃料已成为当前能源化工领域的研究热点[1-4]。
为了满足社会经济发展的需求,使生物液体燃料和生物基化学品逐步替代由化石资源(石油、煤、天然气等)衍生的燃料和精细化学品,科学家已详细列出了基于化石路线和生物质路线可生产的各种液体燃料和化学中间体,并以相应物质的价值链进行了排序(图1)。由图1可知:2种能源价值链中的化工产品在工业应用中具有异曲同工的效应,且它们均可通过催化和化学合成法制取;特别的,生物质能源价值链中的2,5-二甲基呋喃(简称 DMF,高密度液体燃料)、2,5-呋喃二甲酸(简称FDCA,高分子单体)和苯酚(芳香类大宗化学品),可分别对应于化石能源价值链中最具代表性的汽油(液体燃料)、对苯二甲酸(高分子单体)和苯(大宗化学品),说明利用生物质资源替代化石资源是一条切实可行的、有广阔前景的资源转化路线[5]。

图1 化石能源价值链和生物质能源价值链的对比Fig.1 Comparison of value chains between fossil and biomass energy
1 生物质组成及转化利用
1.1 植物生物质原料的组成
一般来说,常用的植物生物质主要包括纤维素、半纤维素和木质素[6-7]。其中,纤维素是由许多D-吡喃式葡萄糖基通过β-1,4-苷键连接起来的具有线性结构的高分子化合物,通常含数千个葡萄糖基,内部存在大量的晶区、非晶区和氢键。半纤维素则由于来源不同而具有不同的结构和组成,最常见的结构是D-木糖基以β-1,4-糖苷键连接形成主链,L-呋喃式阿拉伯糖基和4-O-甲基-D-吡喃式葡萄糖醛酸基分别连接在主链的C2或C3上成为支链,通常半纤维素聚合度比较低,约含有60~200个糖单元数。木质素则是一种由类苯基丙烷结构单元组成的、非结晶性的三维网状酚类高分子聚合物。通常认为,木质素的基本结构单元是以苯丙烷为主体的3种基本结构:即愈创木基丙烷、紫丁香基丙烷和对羟苯基丙烷;它们由苯丙烷基单元经 C == C和C==H相互连接耦合而成,是具有三维空间结构的复杂无定型高聚物(图2)。
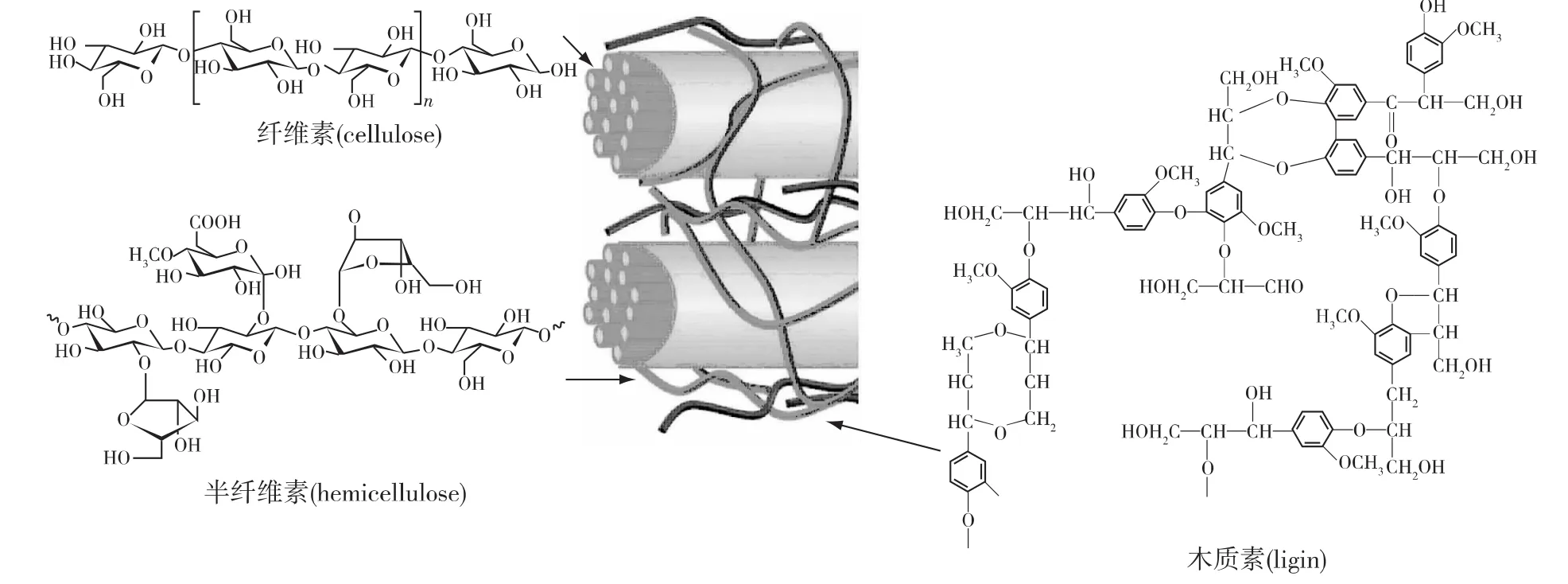
图2 植物生物质中纤维素、半纤维素和木质素的对应结构Fig.2 Molecular structures of cellulose,hemicellulose and lignin in the plant biomass feedstock
1.2 纤维素、半纤维素和木质素的转化路线及主要产物
研究发现,纤维素和半纤维素性质比较接近,只不过它们经催化脱聚可生成不同结构的糖化合物,而糖分子经催化脱水、环合等过程可制得各种呋喃醛(图3)。其中,纤维素转化得到的5-羟甲基糠醛(HMF)进一步转化可合成DMF和FDCA;木质素经催化脱聚、脱氧及脱烷基等反应过程可以制备苯酚。
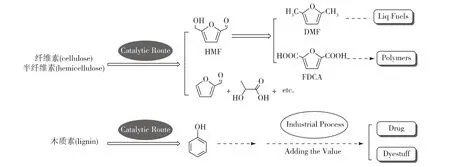
图3 纤维素和木质素催化降解的基本路线Fig.3 General route of degradation of cellulose and lignin
在科学研究中,鉴于对生物质原料直接降解而面临的工艺复杂、产物繁多、条件苛刻以及分离困难等原因,目前开发的催化体系主要用于纤维素和半纤维素以及木质素的催化降解过程,以下分别进行论述。
2 纤维素和半纤维素的催化转化
在纤维素和半纤维素催化转化过程中,起关键作用的是反应媒介和催化剂的效率高低。
2.1 反应媒介
由于纤维素是聚合度较大的高分子化合物,且分子内或分子间存在大量的氢键作用力,因此,选用合适的具有强溶解能力的溶剂为反应媒介是进行纤维素转化研究的前提。目前,对于纤维素溶剂体系应用较多的是四氧化二氮/二甲基甲酰胺体系、LiCl/二甲基乙酰胺(DMA)体系、多聚甲醛/二甲基亚砜体系、N-氧化甲基吗啉和一些水合熔盐等[8];近几年,离子液体和超临界水作为一种可替代的绿色溶剂,对生物质原料也具有良好的溶解性[9-10]。已报道的能够溶解纤维素的离子液体:在阳离子基团中含有咪唑、吡啶和三乙基季铵离子等;在阴离子基团中含有卤素、甲酸、乙酸、酰胺、亚酰胺、硫氰酸酯、磷酸和磺酸等官能团[11]。由于半纤维素和纤维素结构接近,因此,可以溶解纤维素的反应媒介基本上都可以实现对半纤维素的溶解。
2.2 催化剂体系
综合目前的研究进展,在纤维素催化转化合成呋喃化学品的研究中,催化体系主要包括金属盐、复合杂多酸和固体氧化物。
1)在以金属盐作催化剂的研究中,用CrCl3或CrCl3/LiCl体系进行催化反应时,微波条件下在离子液体[BMIM]Cl中可以实现对纤维素的高效降解,其主要产物 HMF的收率可达 61.0% ~62.3%[12-13];若用 CrCl2-CuCl2组合作为催化体系在离子液体[EMIM]Cl中进行纤维素降解反应时,产物 HMF 的收率为 57.5%[14];使用 CrCl2-HCl催化体系在DMA-LiCl-[EMIM]Cl复合溶剂中催化纤维素降解时,产物HMF的收率可达54%[15];进而,若使用Zr(O)Cl2-CrCl3为催化剂时,在DMA-LiCl溶剂中催化纤维素选择性转化时,产物HMF收率可达57%[16]。此外,使用 MnCl2作催化剂,在 1-(4-磺酸基)叔丁基-3-咪唑硫氢酸盐离子液和甲基异丁酮混合溶剂中反应时,纤维素转化为 HMF的收率可达 37.5%[17]。
2)在150℃热水中,用胶束杂多酸为催化剂Cr[(DS)H2PW12O40]3催化纤维素降解反应时,产物HMF 的收率可达 52.7%[18]。在热水中用 ZrO2-TiO2催化纤维素降解反应时,产物中的HMF收率可达9.1%[19]。如果将生成的HMF转移至含催化剂的还原体系中,即可实现液体燃料DMF的催化合成。当使用甲酸为氢源、Pd/C为催化剂时,该过程中DMF的产率为51%[20];而使用H2进行还原HMF时,在Cu-Ru/C催化体系加速下产物DMF的收率为49%[15]。另一方面,如果将生成的HMF转至含催化剂的氧化体系中,即可实现高分子单体FDCA的催化合成。以O2为氧源催化HMF直接氧化制备FDCA的过程中,若用匀相催化剂Co/Mn/Br时,在125℃和7 MPa氧气压力下,反应3 h后,生成FDCA的收率为60%左右[21];若使用含稀有金属的固相催化剂Pt/Al2O3或Pt-Pb时,在60℃和大气压力下,反应4~6 h后,90%以上的HMF可以转变为FDCA类化合物[22-23]。这些催化体系的氧化效率均比较高,但其缺点是需要用到溴或者稀有金属。
3)在半纤维素催化转化合成呋喃化学品研究中,催化体系主要包括有机酸、分子筛和金属氯化物。Kim等[24]发现,用马来酸酐为催化剂直接催化半纤维素或木糖转化合成糠醛反应时,具有很高的选择性。Dhepe等[25]和 Sahu 等[26]报道了使用分子筛HBeta(Si/Al=19)和HUSY(Si/Al=15)催化半纤维素转化的反应,结果发现,在纯水中使用HUSY作为催化剂时,糠醛收率为18%,若采用水-二甲苯两相反应体系,在170℃反应6 h后,糠醛的收率可达56%左右。研究人员还发现,在微波条件下使用AlCl3·6H2O和NaCl作为催化剂,在两相体系中可以将玉米秸秆、树木等生物质原料直接转化为糠醛;当温度为160℃时,产物收率在38% ~64%之间[27]。
3 木质素的催化转化研究
由于木质素催化转化过程生成的产物往往比较复杂,除了生成苯酚以外,还可能得到单酚或二酚衍生物、烷基苯酚和苯等,所以有针对性的催化体系报道相对较少,该过程通常所采用的反应途径是加氢还原降解法。对于溶剂体系,应用较多的是无机酸碱体系和有机溶剂体系[28];至于催化体系方面,主要包括如下:①当使用FeS为催化剂时,在250~450 ℃、15~45.6 MPa条件下,主要生成苯酚和苯[29],而当压力为5~15 MPa时,主要产物则为C6-C9的苯酚衍生物[30];②使用 Co-Mo/Al2O3为催化剂时,在400~500℃、7 MPa条件下,主要的产物是苯酚和可溶性残渣[31];③当采用A型分子筛时,在375℃ 、10 MPa条件下,主要产物为苯酚、甲苯酚、愈创木酚和二甲苯酚[32];④另外,使用硫化的Ni-W/SiO2-Al2O3-PO4催化剂时,在300~500℃、3.5~24 MPa条件下,主要产物为苯酚衍生物[33];⑤当用Pt/C作为催化剂时,在温度200℃、4 MPa条件下,主要产物则为单酚和二酚聚合物[34];并且,使用Pd/C和Nafion@SAC-13组合为催化剂、水和甲酸溶液为溶剂时,在300℃时,主要产物为邻苯二酚和愈创木酚[35]。而在使用Ni/C催化剂时,在多醇溶剂中200℃、5MPa条件下,木质磺酸盐转化率可达91%,主要产物为愈创木酚和乙基愈创木酚[36]。
表1中列出了近年来文献报道的酚类收率数据,由表1可知,若以Pt/Al2O3[37]或 Pt/C[38]为催化剂时,产物中只有1.2%(质量分数)愈创木酚或7.8%4-乙基愈创木酚;而以 Ru/C为催化剂时,产物主要为4-乙基苯酚,且其收率只有3.1%左右[39];另外,在高温水中,Raney Ni催化剂催化木质素降解主要生成苯酚、愈创木酚和邻苯二酚,这3种酚类总收率为1.6%左右[40]。由上述不同催化体系的结果可以看出,木质素催化转化的反应要在高温高压下进行,并且产物中酚类化合物的选择性和收率普遍较低,这主要是由于木质素分子结构稳定及含支链较多所致;因此,该方向仍是今后需集中研究的焦点,催化体系仍需进行不断的完善和改进。

表1 近年来木质素催化转化制酚类化合物的典型反应Table 1 Typical reaction results in the catalytic conversion of lignin to phenols
4 结论和展望
综上所述,在纤维素和半纤维素转化制备呋喃基化学品及木质素转化制酚类化合物的过程中,已报道的催化体系仍存在各自的缺点和局限性,因此,开发合适的催化剂实现纤维素和木质素的高效、高选择性转化制取呋喃衍生物与苯酚仍面临着巨大挑战。其中,研究和开发高活性、多功能的催化新体系是实现高收率、高选择性的关键。
反应溶剂方面,选用离子液体和超临界体系是需突破的研究方向;近年来,功能化离子液体也越来越受到研究者的重视,这是由于功能化离子液体可以根据特殊需要合成不同结构的离子液体。通常,可引入的官能团包括羟基、醚基、琉基、羧酸基、磺酸基、酯基及酰胺等基团,进而可以调节其化学性质,不同官能团的引入可以实现离子液体特定的功能化需求,例如含质子酸的离子液体和含有—OH的离子液体都已得到实现;进而,通过设计特定离子液体使生物质原料得到较好溶解。
对于生物质原料的催化转化过程,比较有前景的催化材料包括:①以固体酸为载体的金属氧化物催化剂;②酸性离子液为媒介的反应体系;③多功能纳米杂化材料开发及其催化应用。
针对木质素转化较有前景的催化体系:①超临界流体和纳米金属离子结合进行催化脱聚研究;②使用金属碳化物和双金属材料进行催化加氢降解研究;③使用金属配位化合物选择性氧化裂解。
[1] CormaA,Iborra S,Velty A. Chemicalroutes forthe transformation of biomass into chemicals[J].chem Rev,2007,107(6):2411-2502.
[2] Chheda J N,Huber G W,Dumesic J A.Liquid-phase catalytic processing of biomass-derived oxygenated hydrocarbons to fuels and chemicals[J].Angew Chem Int Ed,2007,46(38):7164-7183.
[3] Christensen C H,Rass-Hansen J,Marsden C C,et al.The renewable chemicals industry[J].Chem Sus Chem,2008,1(4):283-289.
[4] FitzPatrick M,Champagne P,Cunningham M F,etal.A biorefinery processing perspective:treatment of lignocellulosic materials for the production of value-added products[J].Bioresour Technol,2010,101(23):8915-8922.
[5] Melero J A,Iglesias J,Garcia A.Biomass as renewable feedstock in standard refinery units:feasibility,opportunities and challenges[J].Energy Environ Sci,2012,5(6):7393-7420.
[6] Hendriks A T W M,Zeeman G.Pretreatments to enhance the digestibility of lignocellulosic biomass[J].Bioresour Technol,2009,100(1):10-18.
[7] Alonso D M,Wettstein S G,Dumesic J A.Bimetallic catalysts for upgrading of biomass to fuels and chemicals[J].Chem Soc Rev,2012,41(24):8075-8098.
[8] 李琳,赵帅,胡红旗,纤维素溶解体系的研究进展[J].纤维素科学与技术,2009,17(2):69-75.
[9] Mora-Pale M,Meli L,Doherty T V,et al.Room temperature ionic liquids as emerging solvents for the pretreatment of lignocellulosic biomass[J].Biotech Bioeng,2011,108(6):1229-1245.
[10] Kim K H,Hong J. SupercriticalCO2pretreatmentof lignocellulose enhances enzymatic cellulose hydrolysis[J].Bioresour Technol,2001,77(2):139-144.
[11] Zhao H,Jones C L,Baker G A,et al.Regenerating cellulose from ionic liquids for an accelerated enzymatic hydrolysis[J].J Biotechnol,2009,139(1):47-54.
[12] Li C Z,Zhang Z H,Zhao Z B K.Direct conversion of glucose and cellulose to 5-hydroxymethylfurfuralin ionic liquid under microwave irradiation[J].Tetrahedron Lett,2009,50(38):5403-5405.
[13] Wang P,Yu H,Zhan S,etal.Catalytic hydrolysisof lignocellulosic biomass into 5-hydroxymethylfurfuralin ionic liquid[J].Bioresour Technol,2011,102(5):4179-4183.
[14] Yu S,Brown H M,Huang X W,et al.Single-step conversion of cellulose to 5-hydroxymethylfurfural(HMF),a versatile platform chemical[J].Appl Catal A:General,2009,361(1/2):117-122.
[15] Binder J B,Raines R T.Simple chemical transformation of lignocellulosic biomass into furans for fuels and chemicals[J].J Am Chem Soc,2009,131(5):1979-1985.
[16] Dutta S,De S,Alam M I,et al.Direct conversion of cellulose and lignocellulosic biomass into chemicals and biofuel with metal chloride catalysts[J].J Catal,2012,288:8-15.
[17] Tao F,Song H,Chou L.Efficient conversion of cellulose into furans catalyzed by metal ions in ionic liquids[J].J Mol Catal A:Chemical,2012,357:11-18.
[18] Zhao S,Cheng M,Li J,et al.One pot production of 5-hydroxymethylfurfural with high yield from cellulose by a brønsted-lewis-surfactant-combined heteropolyacid catalyst[J].Chem Commun,2011,47(7):2176-2178.
[19] Chareonlimkun A,Champreda V,Shotipruk A,et al.Catalytic conversion of sugarcane bagasse,rice husk and corncob in the presence of TiO2,ZrO2and mixed-oxide TiO2-ZrO2under hot compressed water(HCW)condition[J].Bioresour Technol,2010,101(11):4179-4186.
[20] Román-Leshkov Y,Barrett C J,Liu Z Y,et al.Production of dimethylfuran for liquid fuels from biomass-derived carbohydrates[J].Nature,2007,447(7147):982-986.
[21] Partenheimer W,Grushin V V.Synthesis of 2,5-diformylfuran and duran-2,5-dicarboxylic acid by catalytic air-oxidation of 5-hydroxymethylfurfural.unexpectedly selective aerobic oxidation of benzyl alcohol to benzaldehyde with metal=bromide catalysts[J].Adv Synth Catal,2001,343(1):102-111.
[22] Vinke P,van Dam H H,van Bekkum H.Platinum catalyzed oxidation of 5-Hydroxymethylfurfural[J].Stud Surf Sci Catal,1990,55:147-158.
[23] Merat N,Verdeguer P,Rigal L,et al.Process for the manufacture of furan-2,5-dicarboxylic acid:FR,2669634[P].1992-05-29.
[24] Kim E S,Liu S,Abu-Omar M M.et al.Selective conversion of biomasshemicellulose to furfuralusing maleic acid with microwave heating[J].Energy Fuels,2012,26(2):1298-1304.
[25] Dhepe P L,Sahu R.A solid-acid-based process for the conversion of hemicellulose[J].Green Chem,2010,12(12):2153-2156.
[26] Sahu R,Dhepe P L.A one-pot method for the selective conversion of hemicellulose from crop waste into C5 sugars and furfural by using solid acid catalysts[J].Chem Sus Chem,2012,5(4):751-761.
[27] Yang Y,Hu C,Abu-Omar M M.Synthesis of furfural from xylose,xylan,and biomass using AlCl3·6 H2O in biphasic media via xylose isomerization to xylulose[J].Chem Sus Chem,2012,5(2):405-410.
[28] 廖俊和,罗学刚.有机溶剂法提取木质素最新进展[J].林产化工通讯,2004,38(3):20-24.
[29] Oshima M,Maeda Y,Kashima K.Method for liquefying lignin:CA,700210[P].1964-12-22.
[30] Urban P,Engel D J.Process for liquefaction of lignin:US,4731491[P].1988-03-15.
[31] Ratcliff M A,Johnson D K,Posey F L,et al.Hydrodeoxygenation of lignins and model compounds[J].Appl Biochem Biotechnol,1988,17(1/2/3):151-160.
[32] Meier D,Berns J,Faix O,et al.Baldauf W,hydrocracking of organocell lignin for phenol production[J].Biomass Bioenergy,1994,7(1/2/3/4/5/6):99-105.
[33] Romero Y,Richard F,Renème Y,et al.Hydrodeoxygenation of benzofuran and its oxygenated derivatives(2,3-dihydrobenzofuran and 2-ethylphenol)over NiMoP/Al2O3catalyst[J].Appl Catal A:General,2009,353(1):46-53.
[34] Yan N,Zhao C,Dyson P J,et al.Selective degradation of wood lignin over noble-metal catalysts in a two-step process[J].Chem Sus Chem,2008,1(7):626-629.
[35] Liguori L, Barth T. Palladium-nafion SAC13 catalysed depolymerisation of lignin to phenols in formic acid and water[J].J Anal Appl Pyrolysis,2011,92(2):477-484.
[36] Song Q,Wang F,Xu J.Hydrogenolysis of lignosulfonate into phenols over heterogeneous nickel catalysts[J].Chem Commun,2012,48(56):7019-7021.
[37] Zakzeski J,Weckhuysen B.Lignin solubilization and aqueous phase reforming for the production of aromatic chemicals and hydrogen[J].Chem Sus Chem,2011,4(3):369-378.
[38] Xu W,Miller S J,Agrawal P K,et al.Depolymerization and hydrodeoxygenation of switchgrass lignin with formic acid[J].Chem Sus Chem,2012,5(4):667-675.
[39] Forchheim D,Hornung U,Kempe P,et al.Influence of RANEY Nickel on the formation of intermediates in the degradation of lignin[J].Inter J Chem Eng,2012,doi:10.1155/2012/589749.
[40] Ye Y,Zhang Y,Fan J,et al.Selective production of 4-ethylphenolics from lignin via mild hydrogenolysis[J].Bioresour Technol,2012,118:648-651.

