近红外光谱分析技术在制药领域中的应用研究进展
臧恒昌,臧立轩,张 惠,王金凤,杨海龙,姜 玮,柳东明,王 斐,胡 甜
(1.山东大学药学院,山东 济南 250012;2.北京凯元盛世科技发展有限责任公司,山东 济南 250012)
近红外光谱(Near-infrared spectroscopy,NIRS)是介于可见光和中红外之间的电磁辐射波,其波谱范围为780~2526 nm[1]。NIRS主要反映了有机分子中含氢基团(O-H,N-H,C-H)振动的基频与合频吸收,具备无损、快速、高效、可在线分析等优点,近年来被广泛用于农业、化工、制药等行业中,其中在制药领域中的应用非常广泛,包括原辅料鉴别、制剂过程控制、成品药分析、假药劣药快速识别等环节,NIRS的使用在节约生产成本的基础上大大减少了工作量,并提升了经济效益。
1 原辅料鉴别
《药品生产质量管理规范》(2010年修订版)(Good Manufacturing Practice,GMP)第一百二十条规定“应当制定相应的操作规程,采取核对或检验等适当措施,确认每一包装内的原辅料正确无误[2]”。新版GMP的推行使得制药企业在原辅料入库检查环节中耗费大量的时间和费用,而NIRS结合化学计量学可建立定性判别模型,从而对原辅料的性质进行鉴别,因此基于NIRS的原辅料快速鉴别成为应用热点。Candolfi等[3]将近红外光谱分析技术结合SIMCA方法建立了10种药用辅料的定性鉴别模型,光谱经过SNV或微分处理后,模型在95%和99%两种置信度下均可达到无错判别。孟昱等[4]采用近红外漫反射光谱法对41种常用药用辅料进行快速、准确、无损的鉴别,光谱经过预处理之后,“主库”模型可准确鉴别胶态二氧化硅、200目乳糖、二水磷酸氢钙等30种辅料,对于相似度高的11种辅料,则建立“子库”模型进一步鉴定。将NIRS分析技术应用于药用辅料的快速鉴别,样品无需预处理,推广至制药企业用于原辅料入库、出库的快速放行将具有很大使用价值。
2 制剂过程
目前国内制剂过程的生产过程控制多依靠经验,因此产品多出现稳定性、均一性较差的问题,从而影响最终产品安全性,而NIRS在线控制制剂过程则能实现生产过程的实时监测,从而对关键质量属性与关键过程参数进行掌握,进一步达到生产过程控制与工艺优化的目的。制剂过程中应用最为广泛的关键环节包括混合、干燥、制粒、包衣等。
2.1 混合过程监测 混合是制药工艺中的关键环节,物料混合的均匀程度直接决定了最终成品的质量是否均一,FDA指导原则用于“均匀度分析”的步骤繁琐而且复杂,建议10个取样点,且每个点至少需重复取样3次,如图1所示。
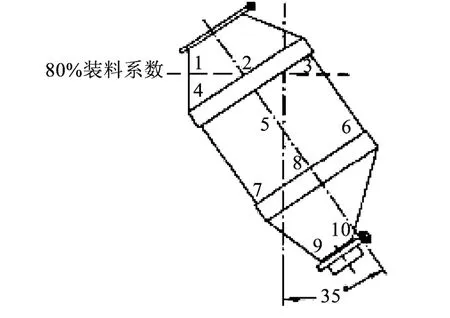
图1 混合桶取样点[5]
NIRS技术用于混合过程在线监测的应用是具有很大发展空间,监测的实施方式主要包括采用光纤探头插入物料中采集光谱或通过蓝宝石窗口采集样品光谱。
NIRS技术用于混合过程在线监测的方式首先是以光纤探头作为开发模式的,由Sekulic等[6]采用10%苯甲酸钠作为模型活性药物,39%微晶纤维素、50%乳糖和1%硬脂酸镁作为辅料模拟实际制药混合过程,将漫反射光纤探头水平插入至双V混合器中,然后通过近红外光谱仪采集光谱,随着混合过程的进行,光谱逐渐趋于稳定与一致,因此,通过计算混合过程中光谱标准偏差即可准确判断混合均匀终点。以光纤作为光谱采集工具在很长一段时间内都是混合过程监测的主要模式,Shi等[7]将对乙酰氨基酚、乳糖和微晶纤维素三元混合物作为实验体系,实验将采集光纤同时安装于二维混合机的顶部和水平位置,结果表明在两个取样点的光谱更能代表混合状态,最后通过计算混合过程中API浓度的相对标准偏差,当偏差小于5%即认为混合均匀。
但是以光纤作为采样工具的方式存在一定不足,即混合过程中混合器的转动容易导致光纤的弯曲,进而影响光路的传递,所采集的光谱也受到一定影响,为克服此缺点,以无线通讯技术的信号传递方式应运而生,代表产品为Antaris Target混合均匀度分析仪。Marzena等[8]采用此款仪器用于混合过程中API含量的检测。Rosas等[9]采用非接触样品方法采集混合过程中固体的近红外光谱,基于原理即为无线传输,通过考察不同定性方法(MBSD、PCSDA、M指数),结果显示M指数是用于混合过程混合均匀度检查的准确、精密的化学计量学方法。
2.2 干燥过程监测 干燥过程是制药领域尤其是固体制剂生产过程中的重要操作单元,干燥环节中的残留水分是最主要的检测指标。由于O-H键的吸收很容易在近红外光谱区域获得,即在1940 nm(组合频)和1440 nm(O-H伸缩振动的一级倍频)有一些特征性很强的吸收带[1],而其它各种分子的合频和倍频吸收相对较弱,这是NIRS用于干燥过程监测的重要理论基础,因此NIRS被用于流化床干燥、冷冻干燥等各种干燥方式中。Demers等[10]将NIRS用于流化床干燥过程中的在线水分检测。Kauppinen等[11]结合NIRS用于冷冻干燥过程中水分含量的定量分析,采用多点监测,光谱代表不同位置的样品状态,所建立模型可成功用于干燥过程的终点监测。
2.3 制粒过程监测 制粒过程能增加药物的可压性和流动性,以确保药物含量均匀,在制粒过程中,颗粒大小和含水量是评价所制得颗粒是否合格的两个关键指标。将NIRS用于制粒过程监测,可连续采集过程中的光谱,提供制粒过程中粒度、含水量变化的可靠数据,从而对制粒环节进行过程控制以及错误诊断。在制粒工艺中,流化床喷雾制粒将混合、制粒和干燥三个单元操作过程集成在一个密闭的设备中完成,是一种较先进的制粒方法。Mark等[12]针对流化床干燥环节安装在线自动监测系统,通过连续采集近红外光谱,在线判定水分含量及溶剂残留量以优化最佳产品性能。Kona等[13]采用NIR分析技术在线监测流化床干燥过程,结合(partial least square,PLS)算法预测干燥过程中的水分含量变化,同时结合主成分分析(principal component analysis,PCA)用于建立多元统计控制图以实现实时错误诊断的目的。
2.4 包衣过程监测 包衣的目的除避免片剂与外界环境接触,掩蔽不良气味之外,还可控制药物释放速率,因此薄膜包衣厚度对药物崩解及溶出的时间有很大关系,而片剂样品的近红外光谱变化与包衣厚度之间存在相关性,因此采用NIRS对片剂包衣层检测,可快速测定包衣厚度。Lee等[14]采用基于NIR技术的光纤探头在线监测包衣过程,通过激光共聚焦显微镜和激光衍射粒度分析两种方法测定包衣过程中薄膜厚度,两种方法所建立校正模型均可以给出很好的预测结果(R2>0.995)。包衣厚度与药物释放度之间存在一定关系,通过近红外光谱的变化可预测药物释放度是否符合要求,从而判断包衣终点。Gendre等[15]安装NIR探头于包衣机中,包衣材料为乙基纤维素混合PVA-PEG高聚物,建立包衣厚度所对应药物释放度的PLS模型,从而实现通过对包衣片剂释放度实时预测以判断包衣终点。
3 成品药分析
药品制备为成品后,仍需要质量检验,NIRS可实现快速无损检测药品质量。Broad等[16]采用透射NIRS模式对片剂中类固醇激素的含量进行快速检测,实验结果表明NIRS可在20min内完成30片药品的无损测试,而传统方法HPLC则需要6 h才可完成,因此大大节省了时间,减少了工作量。Blanco等[17]利用NIRS建立了片剂的含量均匀度以及硬度的PLS模型,因而可以采用NIRS替代UV分析方法对片剂的合格性进行快速鉴别与分析。Cogdill等[18]也对比了脉冲太赫兹波成像与NIRS对于片剂包衣厚度与均一性的快速检测结果,结果更能证明NIRS的无损、快速的优点。
4 假药劣药识别
假药是目前世界各国,尤其是发展中国家共同面临的问题之一。在第六十七届世界药学大会上,世界卫生组织(WHO)指出目前全球范围的假药比例达5%~10%。目前药检部门快速打假的技术则采用近红外光谱分析技术,中国药品生物制品检定所将近红外识别系统与化学快速鉴别系统结合建立快速检测平台,研发了集药品快速检测技术、信息技术于一体的流动实验室,也即药品检测车,以实现“掌握信息,快速筛查,靶向抽样,目标检验”的目的[19],药品检测车用于基层现场快速鉴别假药具有很大使用价值。
5 中药生产
中药是我国的民族瑰宝,在医药行业中占据重要的地位,但是目前中药领域中存在药材一致性差、中间过程不可控、产品质量均一性差等问题[20],而近红外光谱分析技术的快速、多参数测定、无污染等优点,成为目前解决中药领域关键问题的有力工具。胡咏川等[21]综述了NIRS鉴定中药的进展,从中药真伪鉴定、中药优劣鉴定、中药添加西药的监测三个方面进行了总结与展望,NIRS可成为解决药材一致性问题的重要手段。在中药生产过程控制方面,Huang等[22]将NIRS结合多元统计过程控制方法用于中药丹参注射液醇沉过程的在线控制,所建立控制模型可用于生产过程异常批次快速诊断。由于中药成分的天然复杂性,在使用NIRS应用在中药生产的过程中,如何扣除复杂背景,提取有效信息仍是需要克服的问题。
6 问题与展望
目前NIRS已经成为当今国际上研究的热门课题,但是NIRS在制药领域应用存在一定弱点,首先是模型建立的过程需要耗费一定人力、财力和物力,模型的稳健性是在应用过程中需要考虑的问题,因此需要对模型进行定期维护。此外,是由于物质在近红外区的吸收系数较小,对于制药过程中有些含量较低的物质无法实现准确检测。
本文综述了NIRS在制药领域中的应用,基于其优点,NIRS已成功应用至制药领域中原辅料鉴别、制剂过程、成品药分析以及中药生产等各个环节中。NIRS实现了过程分析与控制,为制药生产环节提供过程理解,从而能更好地控制最终产品质量,提高药品品质,随着研究的进一步深入,NIRS在制药领域将有更为广泛的应用。
[1]陆婉珍.现代近红外光谱分析技术[M].北京:中国石化出版社,2006.
[2]中华人民共和国卫生部.药品生产质量管理规范(2010年修订)[S].卫生部令第79号,2010.
[3]Candolfi A,De Maesschalck R,Massart DL,et al.Identification of pharmaceutical excipients using NIR spectroscopy and SIMCA[J].J Pharm Biomed Anal,1999,19(6):923-935.
[4]孟昱,李悦青,蔡蕊,等.近红外漫反射光谱法快速鉴别药用辅料[J].精细化工,2013,10:69-74.
[5]国家发展和改革委员会.中华人民共和国制药机械行业标准[S].北京:中国计划出版社,2004.
[6]Sekulic SS,Ward HW,Brannegan DR,et al.On-line monitoring of powder blend homogeneity by near-infrared spectroscopy[J].Anal Chem,1996,68(3):509-513.
[7]Shi Z,Cogdill RP,Short SM,et al.Process characterization of powder blending by near-infrared spectroscopy:blend end-points and beyond[J].J Pharm Biomed A-nal,2008,47(4-5):738-745.
[8]Jamrógiewicz M,Cal K,Gruszecka M,et al.Determination of API content in a pilot-scale blending by near-infrared spectroscopy as a first step method to process line implementation[J].Acta Pol Pharm,2013,70(3):419-429.
[9]Rosas J,Blanco M,Santamar AF,et al.Assessment of chemometric methods for the non-invasive monitoring of solid blending processes using wireless near infrared spectroscopy[J].Journal of Near Infrared Spectroscopy,2013,21(2):97.
[10]Demers AM,Gosselin R,Simard JS,et al.In-line near infrared spectroscopy monitoring of pharmaceutical powder moisture in a fluidised bed dryer:An efficient methodology for chemometric model development[J].The Canadian Journal of Chemical Engineering,2012,90(2):299-303.
[11]Kauppinen A,Toiviainen M,Korhonen O,et al.In-line multipoint near-infrared spectroscopy for moisture content quantification during freeze-drying[J].Anal Chem,2013,85(4):2377-2384.
[12]Maärk J,Karner M,Andre M,et al.Online process control of a pharmaceutical intermediate in a fluidized-bed drier environment using near-infrared spectroscopy[J].Anal Chem,2010,82(10):4209-4215.
[13]Kona R,Qu H,Mattes R,et al.Application of in-line near infrared spectroscopy and multivariate batch modeling for process monitoring in fluid bed granulation[J].Int J Pharm,2013,452(1-2):63-72.
[14]Lee MJ,Seo DY,Lee HE,et al.In line NIR quantification of film thickness on pharmaceutical pellets during a fluid bed coating process[J].Int J Pharm,2011,403(1-2):66-72.
[15]Gendre C,Boiret M,Genty M,et al.Real-time predictions of drug release and end point detection of a coating operation by in-line near infrared measurements[J].Int J Pharm,2011,421(2):237-243.
[16]Broad NW,Jee RD,Moffat AC,et al.Application of transmission near-infrared spectroscopy to uniformity of content testing of intact steroid tablets[J].Analyst,2001,126(12):2207-2211.
[17]Blanco M,Alcalá M.Content uniformity and tablet hardness testing of intact pharmaceutical tablets by near infrared spectroscopy:a contribution to process analytical technologies[J].Anal Chim Acta,2006,557(1-2):353-359.
[18]Cogdill RP,Forcht RN,Shen Y,et al.Comparison of terahertz pulse imaging and near-infrared spectroscopy for rapid,non-destructive analysis of tablet coating thickness and uniformity[J].J Pharm Innov,2007,2(1-2):29-36.
[19]胡昌勤,成双红,冯艳春,等.药品检测车运行模式的探讨[J].中国药事,2008,22(8):641-644.
[20]聂黎行,王钢力,李志猛,等.近红外光谱法在中药生产过程分析中的应用[J].光学学报,2009,29(2):541-547.
[21]胡咏川,田晓鑫,刘蕾,等.近红外光谱技术鉴定中药的进展[J].中国中药杂志,2012,37(8):1066-1071.
[22]Huang H,Qu H.In-line monitoring of alcohol precipitation by near-infrared spectroscopy in conjunction with multivariate batch modeling[J].Anal Chim Acta,2011,707(1-2):47-56.

