高效液相色谱法测定宫炎康颗粒中芍药苷含量
杨 玲,杨 浩
(陕西省肿瘤医院,陕西 西安 710061)
宫炎康颗粒是由当归、赤芍、川芎、北败酱、香附、柴胡、泽兰、红花等12味药材经加工制成的颗粒剂,具有活血化瘀、解毒消肿之功效,临床上主要用于慢性盆腔炎[1]。目前该药品的质量标准中只有鉴别项,未建立有效成分的含量测定,其主要有效成分是芍药苷,经参考相关文献报道[2-8],笔者采用高效液相色谱法对芍药苷的含量进行测定,该法操作简便、分离良好、重现性好、结果准确,可用于该制剂的质量控制。
1 仪器和试药
Agilent 1260型高效液相色谱仪;Sartorius BS224S型电子天平;KQ3200DE型数控型超声波清洗器。芍药苷对照品(中国药品生物制品检定所,批号为110736-200833);宫炎康颗粒(市售品,批号为 20120506,20121130,20110921,规格为 8.30 mg /袋);乙腈、甲醇均为色谱纯,水为哇哈哈纯净水,其余试剂均为分析纯。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:Agilent TC C18柱(250 mm ×4.6 mm,5 μm);检测波长:230nm;流动相:乙腈-0.1%磷酸溶液(15∶85):流速:0.8mL/min;进样量:10 μL;柱温:30℃。在此色谱条件下,参照 2010年版《中国药典(一部)》赤芍含量测定项下将理论板数,按芍药苷峰计算应不低于3 000[9]。色谱图见图1。
2.2 溶液制备
精密称取经五氧化二磷减压干燥器中干燥36 h的芍药苷对照品[7]0.005 2 g,置50 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀,精密量取3 mL,置10 mL容量瓶中,加甲醇至刻度,摇匀,即得对照品溶液(每1 mL溶液中约含芍药苷30 μg)。取装量差异项下本品,研细,精密称定0.5 g,置50 mL具塞三角瓶中,精密加入甲醇20 mL,称定质量,超声处理(功率150 W,频率40 kHz)20 min,取出放冷,再称定质量,用甲醇补足减失的质量,摇匀,以0.45 μm的微孔滤膜滤过,取续滤液,即得供试品溶液。按处方另取除赤芍药材外的其他药味,照供试品溶液处理方法制备成不含赤芍的阴性对照品溶液。
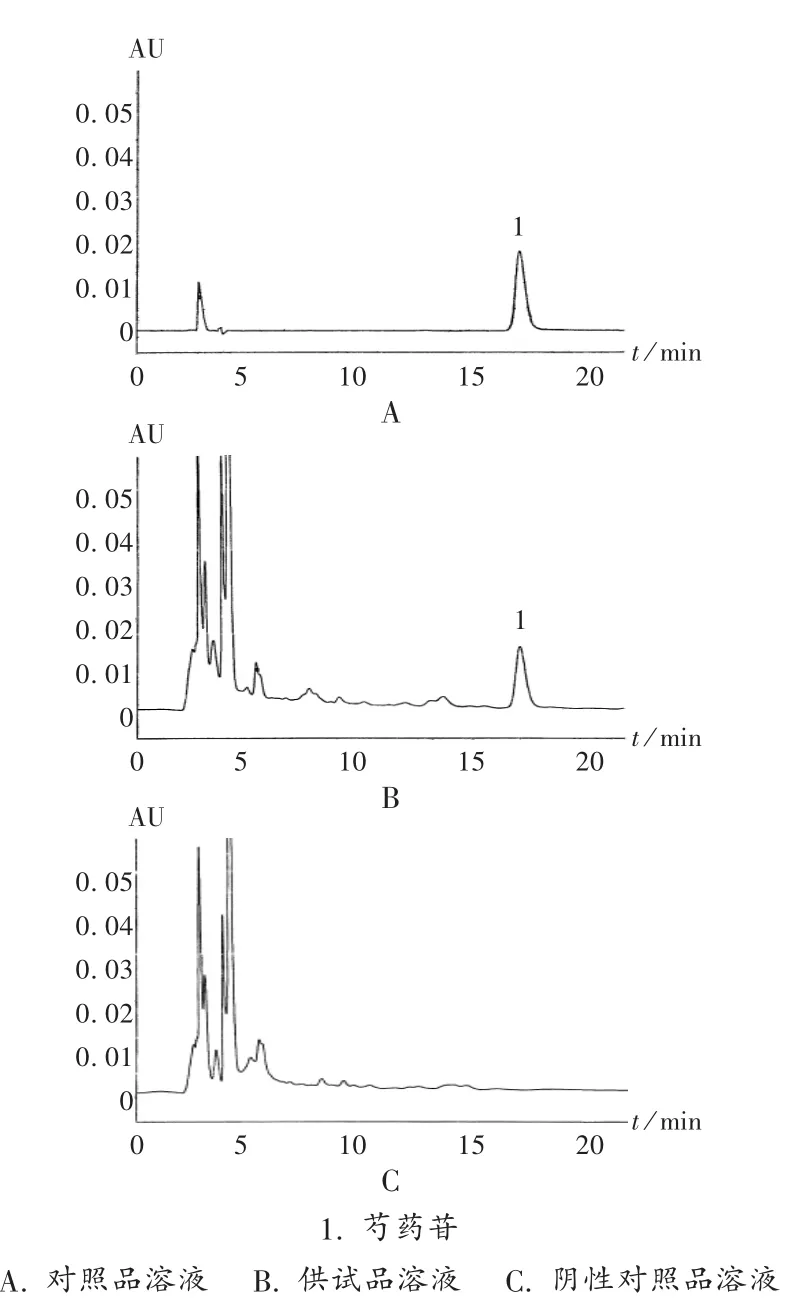
图1 高效液相色谱图
2.3 方法学考察
阴性干扰试验:分别取2.2项下3种溶液,注入高效液相色谱仪,进样量10 μL,记录色谱图。结果供试品溶液色谱中,在与对照品溶液色谱主峰相同位置上有保留时间一致的峰出现,而阴性对照品溶液色谱在相应位置没有峰出现,(见图1),表明该法专属性强。
线性关系考察:精密称取芍药苷对照品,加甲醇配制成质量浓度依次为 7.6,15.2,30.4,60.8,121.6 μg /mL 的溶液,各吸取10μL,依次进样,记录色谱图,以对照品溶液质量浓度(X)为横坐标、峰面积(Y)为纵坐标绘制标准曲线,得回归方程 Y=1.4×106X-6 070,r=0.999 6(n=5)。结果表明,芍药苷进样量在 0.08~1.21 μg范围内与峰面积呈良好线性关系。
精密度试验:取同一对照溶液,依法连续进样5次,记录色谱图。结果峰面积的 RSD为0.8%(n=5),表明仪器精密度良好。
稳定性试验:取新制备的供试品溶液(批号为20120506),分别在 0,2,4,6,8 h 时进样。结果进样量为 10 μL,记录色谱图。结果峰面积的 RSD为0.9%(n=5),表明供试品溶液在8 h内稳定。
重复性试验:分别精密称取样品(批号为20120506)5份,依法制备供试品溶液并测定含量。结果的 RSD为0.4%,表明方法重复性良好。
加样回收试验:分别取已知芍药苷含量(批号为20120506)的供试品内容物,研细,取细粉适量(约为含量测定的1/2量)精密称定,共5份,分别置具塞三角瓶中,精密加入相当于含量1/2量的芍药苷对照品溶液(0.152 g /L,1.5 mL),按含量测定方法测定,计算回收率。结果见表1。

表1 芍药苷加样回收试验结果(n=5)
2.4 样品含量测定
取对照品及3批样品,依法制备对照品溶液及供试品溶液,分别进样10 μL,记录色谱图,按外标法以峰面积计算含量。结果批号为20120506,20121130,20110921的3批样品中,芍药苷平均含量为 8.29,7.87,8.00 mg/袋。
3 讨论
赤芍为宫炎康颗粒方中的主要药味,本试验制订的赤芍含量测定方法简单、重复性好、精密度高。
取芍药苷对照品溶液,在200~400 nm波长处扫描,结果芍药苷在230,266,349 nm波长处处均有最大吸收,为与药典规定一致。故确定以230 nm为测定波长。
比较了多种流动相,流动相A为甲醇-0.05 mol/L磷酸二氢钾(33 ∶67),流动相 B 为乙腈 -0.1% 磷酸溶液(15 ∶85),流动相C为乙腈-0.1%磷酸溶液(10∶90),最终选择了流动相B,其分离好,柱温低,理论板数高,供试品主峰与杂质峰达到基线分离,保留时间适中。
本试验中还比较了样品超声处理时间,分别取10,20,30 min,结果超声20 min与超声30 min芍药苷的含量无明显差异,即超声20 min可提取完全,故超声处理时间定为20 min。
参考文献:
[1]WS3-B-3921-98,中华人民共和国卫生部药品标准·中药成方制剂(第二十册)[S].
[2]韩 平,胡 敏,曹 阳,等.高效液相色谱法测定芍黄通便汤中芍药苷含量[J].中国药业,2011,20(24):51 -52.
[3]王 芳,胡雪莲,陈 琳,等.高效液相色谱法测定胃灵胶囊中芍药苷含量[J].中国药业,2011,20(1):17 -18.
[4]程新萍,孙文基,李新生.赤芍药材中芍药甙的含量考察[J].西北药学杂志,1998,13(1):41.
[5]谢晓梅,余长柱,徐衡,等.赤芍饮片质量标准研究——芍药苷的含量测定[J].中国中药杂志,2004,29(8):759 -761.
[6]周海玲,许舜军,杨 柳.HPLC法测定赤芍中芍药苷的含量[J].临床医学工程,2011,18(4):487 - 488.
[7]周红涛,骆亦奇,胡世林,等.赤芍与白芍的化学成分含量比较研究[J].中国药学杂志,2003,38(9):654 -657.
[8]林 海,胡 黎.不同产地赤芍中芍药苷的含量测定[J].中国医药指南,2009,7(16):91 -92.
[9]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:147 -148.

