尼莫地平纳米混悬剂在大鼠体内药代动力学研究
曾泷彪,张军东,唐文燕,吴君莲
(1.中国药科大学 药剂学教研室,江苏 南京 210009;2.上海信谊药厂有限公司 药物研究所,上海 201206;3.安徽职业技术学院 化工系分析教研室,安徽 合肥 230011)
尼莫地平纳米混悬剂在大鼠体内药代动力学研究
曾泷彪1,2,张军东2*,唐文燕2,吴君莲3
(1.中国药科大学 药剂学教研室,江苏 南京 210009;2.上海信谊药厂有限公司 药物研究所,上海 201206;3.安徽职业技术学院 化工系分析教研室,安徽 合肥 230011)
目的:研究尼莫地平纳米混悬剂在大鼠体内的药代动力学情况。方法:以尼膜同为参比,研究自制尼莫地平纳米混悬剂在SD大鼠体内的生物利用度。结果:尼莫地平纳米混悬剂在口服灌胃后禁食与进食大鼠体内的Cmax分别为(242.96±47.50)μg/mL 和(236.33±7.80)μg/mL,AUC(0-t)分别为(409.01±89.34)μg·h/mL和(415.42±42.76)μg·h/mL;以尼膜同为参比,尼莫地平纳米混悬剂在禁食与进食条件下大鼠体内的相对生物利用度分别为657%和522%。结论:在比较食物效应对口服尼莫地平制剂的影响时,尼膜同在进食状态下大鼠体内的生物利用度是禁食组的1.28倍,而纳米结晶进食组大鼠的生物利用度仅为禁食组的1.02倍。
尼莫地平;纳米混悬剂;生物利用度
尼莫地平(Nimodipine)是第二代钙离子拮抗剂,其可选择性地作用于脑血管平滑肌,扩张脑血管,增加脑血流量,临床用于治疗急性高血压、脑出血后脑血管痉挛引起的缺血性神经损伤[1]。尼莫地平是一种溶于乙醇、乙醚等有机溶媒但不溶于水的药物,且其存在严重的肝脏首过效应,口服绝对生物利用度仅为3%~28%[2]。
纳米混悬剂是以表面活性剂或聚合物为稳定剂,将纳米尺度的药物粒子分散在水中形成的稳定胶体分散体系[3]。因其粒径极小,能显著提高药物的饱和溶解度,增加药物溶出速率,提高其生物利用度。
1 仪器与材料
1.1 仪器
液相色谱仪(美国Waters公司, Empower系统和2487检测器);TGL-16G高速离心机 (上海安亭科学仪器厂)。
1.2 材料
尼莫地平纳米冻干粉(自制); 尼膜同(尼莫地平片,拜尔医药保健有限公司,批号: BJ08192);甲醇(merck公司, 色谱纯 );乙腈(merck公司,色谱纯);健康SD大鼠,体重 230~270g (合格证号:2007000559729 )。
2 方法
2.1 尼莫地平体内分析方法建立
2.1.1 色谱条件 色谱柱:Phenomenex C18柱(250mm×4.6mm,5μm);流动相为乙腈∶水=70∶30(v/v);检测波长:358nm;流速:1.2mL/min;柱温:35℃;内标:尼群地平;进样体积:20μL。
2.1.2 血浆处理 取大鼠空白血浆0.2mL,加入10μg/mL尼莫地平标准液20μL,其中内标浓度均为5.0μg/mL,加乙醚∶正己烷(1∶1,v/v)1mL,涡旋2min后,4 000rpm离心5min,取上清液0.7mL于离心管中,常温避光,氮气吹干,避光保存。2.1.3 血浆干扰试验 分别取大鼠空白血浆、尼莫地平对照品(含内标)溶液、空白血浆加尼莫地平对照品(含内标)溶液和给药后大鼠血浆样品,按“2.1.2”项方法处理、进样。
2.1.4 标准曲线建立 吸取6份大鼠空白血浆各0.2mL,分别加入0.5、1.0、2.0、4.0、8.0、16μg/mL尼莫地平标准溶液20μL(其中内标浓度均为5.0μg/mL),加入乙醚∶正己烷(1∶1,v/v)1mL,涡旋2min,4 000rpm离心5min,取上清液0.7mL于离心管中,常温避光,氮气吹干,试管中的残留物加入甲醇60μL,涡旋振荡2min,取20μL注入高效液相色谱仪,分别记录色谱图中尼莫地平的峰面积(Anim)与尼群地平的峰面积(Anit),并以峰面积比值A(Anim/Anit)对尼莫地平浓度C(μg/mL)进行线性回归,得回归方程 Y =0.183 7X+0.017 3,R2=0.999 8(n=6),表明尼莫地平在0.508~16.256μg·mL-1浓度范围内与其峰面积积分线性关系良好。
2.1.5 回收率试验 在大鼠空白血浆中加入尼莫地平标准液适量,使其浓度分别为0.5μg/mL、2μg/mL、8μg/mL,其中内标浓度均为5.0μg/mL。按“2.1.2”项方法处理并进样分析,按“2.1.4”项标准曲线计算测定值,测定值与实际加入值的比值即为回收率。低、中、高三个浓度的回收率分别为(102.14±0.11)%、(102.68±1.91)%、(102.32±1.93)%,表明方法准确度较好。
2.1.6 精密度试验 在大鼠空白血浆中加入尼莫地平标准液适量,使其浓度分别为0.5μg/mL、2μg/mL、8μg/mL,其中内标浓度均为5.0μg/mL,按大鼠血浆中尼莫地平工作曲线制备法测定,1天内进样3次,记录峰面积,计算得日内RSD为1.47%;每日测定峰面积,连续测定3天,计算得日间RSD为2.43%。
2.2 大鼠体内药动学研究
2.2.1 给药方法与血样处理 取SD大鼠12只,于实验前禁食12h,自由饮水,分成两组,分别灌胃给予尼莫同混悬液和尼莫地平纳米结晶片混悬液,给药剂量为40.0mg/kg[4]。
取进食的SD大鼠12只,分成两组,分别灌胃给予尼莫同混悬液和尼莫地平纳米结晶片混悬液,给药剂量为40.0mg/kg。
2.2.2 血样采集与测定 上述动物给药后,分别于给药前(0h)和给药后0.25h、0.5h、1.0h、1.5h、2.0h、3.0h、4.0h、8.0h、12.0h、24.0h于大鼠眼底静脉丛毛细管取血0.4mL于肝素化的离心管中,10 000rpm离心5min,取上层血浆-20℃保存备用。
按照“2.1.2”项方法提取药物,采用高效液相色谱法测定,计算各时间点尼莫地平的血药浓度。
2.2.3 大鼠体内尼莫地平血药浓度 禁食组大鼠口服给药后平均血药浓度和进食组大鼠口服给药后平均血药浓度分别见表1和表2。
2.2.4 数据处理 采用非房室模型法计算SD大鼠口服给药后的各项药动学参数,其中Cmax和Tmax为实测值,AUC(0-t)为通过梯形法计算所得,结果见表3。
以尼膜同为参比制剂,根据血药浓度-时间曲线下面积AUC(0-t)分别计算禁食与进食组纳米结晶的相对生物利用度F,计算公式如下:
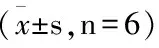
表1 禁食组大鼠口服给药后平均血药浓度
注:- 表示未检出

表2 进食组大鼠口服给药后平均血药浓度
3 结论
在相同状态下,以尼膜同为参比制剂,经计算,禁食组大鼠尼莫地平纳米结晶的相对生物利用度为657%;进食组大鼠尼莫地平纳米结晶的相对生物利用度为522%。
在比较食物效应对口服尼莫地平制剂的影响时,尼膜同在进食状态下大鼠体内的生物利用度是禁食组的1.28倍;而纳米结晶进食组大鼠的生物利用度仅为禁食组的1.02倍,这也说明纳米结晶可消除食物效应对口服制剂吸收的影响。
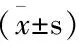
表3 口服给药后大鼠药代动力学参数
[1] 杨力,赵德化.尼莫地平的药理和临床应用[J].陕西医学杂志,1993,22(2):98-101.
[2] 李帅,王伟姣,李昌亮,等.国产尼莫地平及其制剂质量的研究进展[J].中南药学,2012,10(9):689-691.
[3] RABINOW BE. Nanosuspensions in drug delivery[J].Nat Rev Drug Discov,2004,3(9):785-796.
[4] 贺浪冲,王嗣岑.非手性与手性色谱法研究尼莫地平及其对映体在大鼠体内的药代动力学及组织分布[J].药学学报,2003,38(8):603-608.
(责任编辑:尹晨茹)
2014-03-12
曾泷彪(1988-),男,中国药科大学药剂学教研室硕士研究生,研究方向为药物新剂型与新技术。
张军东(1974-),男,上海信谊药厂有限公司药物研究所高级工程师,研究方向为药物新剂型与新技术。
R945
A
1673-2197(2014)16-0009-02

