波替单抗治疗伴或不伴有肾功能不全的老年多发性骨髓瘤探讨
王志红,曹志刚,周宏伟,刘 默,邢 丽,冯少美,杨 娜,彭朝津,杨清明
(解放军总医院第一附属医院老年肿瘤血液科,北京 100048)
多发性骨髓瘤(multiple myeloma,MM)是一种单克隆浆细胞增多的B细胞恶性肿瘤,多发于老年人,常合并肾功能受损。其大剂量放疗或化疗、自体干细胞移植受到临床限制,传统的化疗仅有37%~63%的病例能得到控制[1]。波替单抗(硼替佐米,万珂,bortezomib,Velcade)是新型的蛋白酶体抑制剂类抗肿瘤药物,国外临床研究结果显示波替单抗对合并肾衰竭病例有良好的肾功能挽救作用。目前国内用于老年患者治疗的报道尚不多见,特别是老年患者合并肾功能不全的病例,其疗效有待提高。本研究分析了近年来解放军总医院第一附属医院老年肿瘤血液科使用波替单抗为主的化疗方案治疗46例老年MM合并或不合并肾功能不全患者的疗效和不良反应,并进一步探讨初治或复治MM患者的疗效和不良反应。
1 对象与方法
1.1 对象
所有患者来自2007年1月至2012年12月接受住院治疗的老年MM患者,诊断符合2001年世界卫生组织(WHO)诊断标准[2],肾功能不全诊断标准依据文献[3]。患者共46例,男性26例,女性20例。中位年龄69(60~75)岁。依据肾功能是否正常分为肾功能不全组14例,肾功能正常组32例。依据是否初治分为初治组25例,复治组21例,复治患者既往曾用包括长春新碱(vincristine)联合表柔比星(阿霉素,epirubicin)与地塞米松(dexamethasone)和美法仑(melphalan)为主的联合方案(M2、MP、MPT)等标准化疗方案但未缓解或缓解后复发。血常规基线水平白细胞计数(4.5±1.1)×109/L,血红蛋白(88.7±25.1)g/L,血小板(116.0±48.7)×109/L。患者一般资料见表1。
1.2 治疗方法
46例患者应用波替单抗为主的方案,包括BAD方案(波替单抗剂量为1.3mg/m2,第1,4,8,11天,表柔比星10mg/m2,第1,4,8,11天,地塞米松15~20mg/d,第1~4天,第8~11天,3周为1个疗程);BMD方案(波替单抗剂量为1.3mg/m2,第1,4,8,11天,美法仑2mg,每日3次,第1~7天,地塞米松10mg/d,第1~7天,3周为1个疗程);BD方案(波替单抗剂量为1.3mg/m2,第1,4,8,11天,地塞米松15~20mg/d,第1~4天,第8~11天,3周为1个疗程)。接受治疗的中位疗程数为3(2~11)个疗程。肾功能不全患者首次治疗时表柔比星剂量适当酌减,肾功能改善后剂量增至正常。

表1 46例老年多发性骨髓瘤患者一般资料Table 1 Characteristics of 46 elderly patients with multiple myeloma(n)
1.3 疗效评价
采用国际骨髓瘤工作组2006年制订的统一疗效标准[1]。疗效判断分别为完全缓解(complete remission,CR)、非常好的部分缓解(very good partial remission,VGPR)、部分缓解(partial remission,PR)、病情稳定(stable disease,SD)、病情进展(progression of disease,PD)。观察总反应率(overall response rate,ORR)=CR+VGPR+PR+SD。观察并统计患者美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)评分、肾功能、微球蛋白、血红蛋白、骨髓瘤细胞的改善情况以及不良反应的发生情况。
1.4 统计学处理
应用SPSS13.0软件进行统计学分析,采用四格表精确Fisher检验,治疗前后指标的变化采用t检验。P<0.05为差异有统计学意义。
2 结 果
2.1 波替单抗治疗方案对老年初治和复治MM患者的疗效
25例初治患者至少接受2个疗程治疗,疗效评定为:ORR 22例(88.0%),其中CR 4例(16.0%),VGPR 8例(32.0%),PR 10例(40.0%)。其中10例初治患者接受4个疗程治疗,ORR 9例(90.0%),其中CR 3例(30.0%),VGPR 1例(10.0%),PR 5例(50.0%)。9例患者接受6个疗程治疗,ORR 9例(100.0%),CR 2例(22.0%),VGPR 2例(22.0%),PR 5例(55.0%)。达到最佳疗效的中位疗程数为3(2~6)个疗程。21例复治MM患者全部接受2个疗程,ORR 16例(76.2%),CR 1例,VGPR 2例,PR 13例。其中20例完成4个疗程治疗,ORR 15例(75.0%),CR 1例,VGPR 2例,PR12例。达到最好疗效的中位疗程数为3(2~5)个疗程。治疗2个疗程后初治组ORR为88.0%(22/25),复治组ORR 76.2%(16/21),两组间差异无统计学意义(P>0.05)。治疗4个疗程后初治组ORR 90.0%(9/10),复治组ORR 75.0%(15/20),初治组有效率明显高于复治组,差异有统计学意义(P<0.01)。
2.2 波替单抗治疗方案对老年MM伴或不伴肾功能不全患者的疗效
完成2个疗程时14例肾功能不全组老年MM患者ORR达78.6%(11例),CR 1例,VGPR 2例,PR 8例;32例肾功能正常组老年MM患者ORR达84.4%(27例),CR 4例,VGPR 8例,PR 15例。完成4个疗程的11例肾功能不全组患者ORR达90.9%(10例),CR 1例,VGPR 3例,PR6例;19例肾功能正常组患者ORR达73.7%(14例),CR3例,PR 11例。在2个或4个疗程治疗后,两组间疗效分析显示差异均无统计学意义(P>0.05)。
2.3 肾功能不全老年患者治疗后肾功能、血红蛋白、生活质量评分的变化
治疗2个疗程后患者肌酐、骨髓瘤细胞数、微球蛋白均较治疗前显著下降,肌酐清除率和血红蛋白较治疗前显著提高,差异均有统计学意义(P<0.05,P<0.01),ECOG评分较治疗前改善,但差异无统计学意义(P>0.05;表2)。
2.4 不良反应和安全性评判
根据WHO抗癌药物不良反应分类,在治疗中和治疗后出现的主要不良反应为周围神经炎、胃肠道反应、血小板减少、血红蛋白、白细胞减低、感染等,经对症处理均可好转。其发生频率和严重程度对临床治疗无明显影响(表3)。
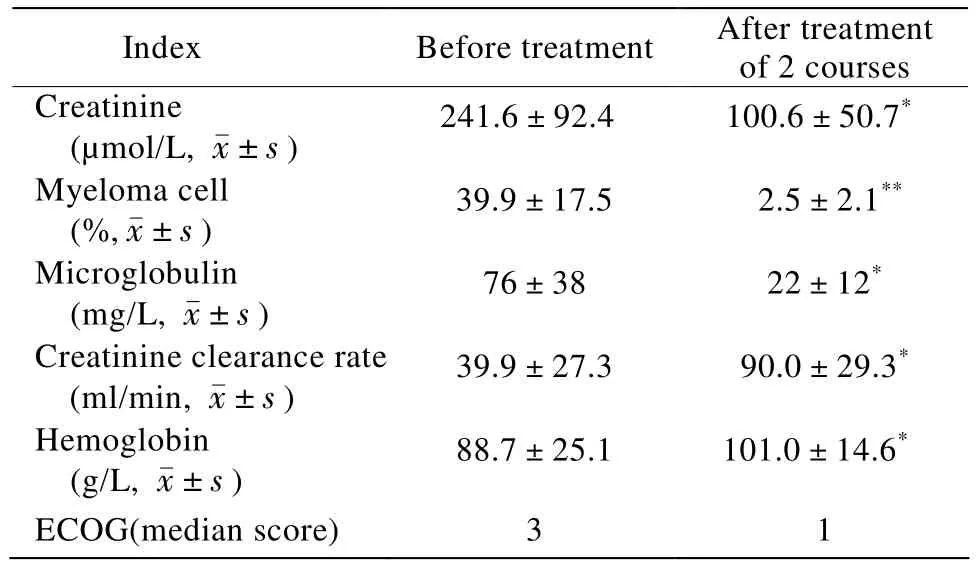
表2 肾功能不全老年MM患者治疗前后指标比较Table 2 Comparison of index in the elderly MM patients before and after treatment (n=14)

表3 波替单抗治疗不良反应发生情况Table 3 Adverse reactions of bortezomib treatment(n)
3 讨 论
MM是一种以骨髓单克隆浆细胞增多为特征的B细胞恶性肿瘤,中老年人易发病,>60岁的老年人发病率尤高。传统的化疗,一些新药及自体造血干细胞移植已达到45%~80%的缓解率和较好的无病长期生存期,但对于伴有肾功能不全的MM患者,则由于肾毒性而不能耐受传统的化疗,影响其疗效及长期生存[4]。近年来采用以波替单抗为主的化疗方案治疗,疗效已得到明显改善。但对于老年MM患者,特别是伴有肾功能不全者,由于报道不多,其疗效和肾功能改善情况有待进一步探索[5]。
本组老年MM患者的初治和复治病例均取得较好的疗效,较传统化疗方案的ORR增高[6]。初治组与复治组的疗效在2个疗程时无显著性差异,4个疗程时初治组疗效显著高于复治组,6个疗程时,ORR最高。即无论初治或复治病例应用波替单抗为主的化疗方案均可达到良好的疗效,但不宜过早停药,当治疗4~6个疗程或更多时,疗效随着疗程的增加逐渐提高,提示延长应用波替单抗的方案可以提高疗效。本组治疗结果显示老年MM患者伴有肾功能不全与肾功能正常者疗效相近,即波替单抗对于有肾功能损害的老年MM患者也可达到较好的疗效,进一步提示以波替单抗为主的方案治疗老年肾功能不全患者的优势,给更多的老年患者带来了希望。
本研究结果显示,老年肾功能不全患者在2个疗程后肾功能均有不同程度的恢复,血肌酐较治疗前明显下降,内生肌酐清除率较治疗前明显升高,且差异有统计学意义,提示使用波替单抗为主的方案可以很快改善患者肾功能,尽早脱离透析。患者的ECOG评分从治疗前的3分变为治疗后的1分,显示生活质量改善。虽然其差异无统计学意义,可能是由于波替单抗治疗后出现的神经末梢毒性或乏力等不良反应导致部分患者ECOG评分增高,使统计结果受到影响。
波替单抗的常见不良反应有血小板减少、末梢神经炎、乏力、腹泻、感染等[6]。其中结核分枝杆菌感染[7]和病毒感染较常见,本组中有4例发生病毒感染,包括3例带状疱疹和1例H1N1病毒感染,经治疗后感染控制。本组老年MM患者治疗后感染及其他不良反应的发生率与文献报道类似,未发现这些不良反应在老年患者中增多或加重,提示波替单抗为主的化疗方案治疗老年MM患者具有较好的安全性。
波替单抗的联合治疗方案对老年MM伴或不伴肾功能不全的患者取得了初步的疗效,且安全性良好。本研究中心拟进一步积累病例,延长治疗后随访时间,以期对波替单抗为主的化疗方案治疗老年MM患者长期的总生存期及无进展生存期等进行有意义的评价。
【参考文献】
[1]Yang P,Zhang WJ,Jing HM,et al.Retrospective analysis of 71 cases of multiple myeloma[J].J Exp Hematol,2009,17(6):1573-1576.[杨 萍,张文娟,景红梅,等.71例初治多发性骨髓瘤的回顾性分析[J].中国实验血液学杂志,2009,17(6):1573-1576.]
[2]Zhang ZN,Shen T.Standard for Diagnosis and Treatment of Blood Diseases[M].Beijing:Science Press,2007,232-234.[张之南,沈 悌.血液病诊断及疗效标准[M].北京:科学出版社,2007:232-234.]
[3]Li LS,Liu ZH.Chinese Kidney Diseases[M].Beijing:People’s Military Medical Press,2008:1270.[黎磊石,刘志红.中国肾脏病学[M].北京:人民军医出版社,2008:1270.]
[4]Sellner L,Heiss C,Benner A,et al.Autologous retransplantation for patients with recurrent multiple myeloma:a single-center experience with 200 patients[J].Cancer,2013,119(13):2438-2446.
[5]Cao ZG,Liu M,Zhou HW,et al.Clinical study of bortezomib for treatment of multiple myeloma complicated with renal failure[J].Chin J Hematol,2013,34(1):74-75.[曹志刚,刘 默,周宏伟,等.波替单抗治疗多发性骨髓瘤合并肾功能衰竭的临床研究[J].中华血液学杂志,2013,34(1):74-75.]
[6]Ogawa Y,Suzuki K,Sakai A,et al.Phase Ⅰ/Ⅱ study of bortezomib-melphalan-prednisolone(VMP)for previously untreated Japanese patients with multiple myeloma[J].Cancer Sci,2013,14(7):912-919.
[7]Ahn JS,Rew SY,Yang DH,et al.Poor prognostic significance ofMycobacterium tuberculosisinfection during bortezomib-containing chemotherapy in patients with multiple myeloma[J].Blood Res,2013,48(1):35-39.

