非酒精性脂肪性肝病相关肝细胞癌的临床研究进展
张启迪 陆伦根
●述 评
非酒精性脂肪性肝病相关肝细胞癌的临床研究进展
张启迪 陆伦根
脂肪性肝病(FLD)包括酒精性脂肪性肝病、非酒精性脂肪性肝病(NAFLD)以及其他原因所致脂肪肝等三个类型。随着饮食结构的改变、人口老龄化,NAFLD的发病率逐年增加,在我国因肥胖等所致的FLD明显多于因饮酒所致的FLD。此外,流行病学研究表明,NAFLD增加原发性肝癌,尤其是肝细胞癌(HCC)风险。因此,本文就我院一例患者及当前NAFLD与HCC的诊疗指南谈谈NAFLD与HCC的关系、诊疗方面的新进展。
1 NAFLD相关HCC流行病学
NAFLD与遗传易感性和胰岛素抵抗密切相关,包括非酒精性单纯性脂肪肝(NAFL)、非酒精性脂肪性肝炎(NASH)及NASH相关肝硬化。
我国虽无全国范围的普查,但东南沿海城市成人NAFLD患病率在15%左右,已成为慢性肝病的重要病因。据估计,未来二十年我国NAFLD的患病率将增加一倍。NAFLD是糖尿病和肥胖在肝脏的表现,是肥胖、糖尿病与HCC间联系的关键桥梁之一。肥胖症患者NAFLD患病率在60%~90%,糖尿病患者NAFLD患病率为28%~55%。最近的荟萃分析表明,HCC患病风险在超重者为体重正常者的1.17倍,肥胖者风险增加89%。研究显示糖尿病增加HCC发生风险2.16倍。
NAFLD可经NASH、肝硬化和HCC三个发展阶段,研究显示NAFLD相关肝硬化HCC年累计发病率约为2.6%,低于慢性丙型肝炎肝硬化和慢性乙型肝炎(CHB)肝硬化的发病率。然而,全球因隐源性肝硬化所致HCC占15%~30%,超过一半的隐源性肝硬化存在NAFLD或代谢综合征组分。
然而,无肝硬化的NAFLD患者也可能发生HCC。2004年以来,至少报道了116例经组织学证实为NAFLD但无肝硬化的HCC患者。我们的病例即是经病理证实为NASH但无肝硬化而并发HCC的病例。一般来说,与病毒性肝病所致的HCC相比,NAFLD所致的HCC在老年、伴代谢性疾病患者中多见,其肝功能受损较轻,AFP升高不明显。
2 NAFLD相关HCC诊断
本例患者,老年男性,右上腹部胀痛不适1周,除右上腹轻压痛外,腹部无阳性体征发现。超声提示肝内可疑占位,上腹部增强CT考虑原发性肝癌。肝脏增强CT是目前肝癌诊断和鉴别诊断最重要的影像学检查方法。通常,CT平扫下肝癌多为低密度占位,边缘有清晰或模糊的不同表现,部分有晕圈征。CT增强扫描时,HCC的影像学典型表现为在动脉期呈显著强化,在静脉期强化不如周边肝组织,而在延迟期则造影剂持续消退,具有高度特异性。本例符合原发性肝癌典型的CT表现。
常用于肝癌诊断和鉴别诊断的影像学检查还有腹部超声,主要用于初步筛查;磁共振成像对于小肝癌的诊断优于CT;选择性肝动脉造影(DSA),目前多用数字减影血管造影,可以明确显示肝脏小病灶及其血供情况。DSA为侵入性检查,可用于其他检查后仍无法确诊的患者。正电子发射计算机断层成像(PET-CT),既可由PET功能显像反映肝脏占位的生化代谢信息,又可通过CT形态显像进行病灶的精确解剖定位,但PET-CT肝癌临床诊断的敏感性和特异性还须进一步研究,且其价格较高,尚未普及,故不作为首选。
血清AFP是诊断肝癌的重要指标,但在NAFLD相关的HCC中一般升高不明显,这值得临床医生注意。本例患者AFP仅轻度升高,肝功能仅检出GGT升高。病毒学指标、免疫学指标、铜蓝蛋白、铁蛋白正常,无饮酒嗜好,而有肥胖、高血压史、高血脂史等代谢综合征成分,考虑导致HCC的慢性基础肝病为NAFLD,经术后病理证实为NASH。
NAFLD的诊断主要依据我国2010年1月修订《非酒精性脂肪性肝病诊疗指南》,其标准须符合以下3个条件:①无饮酒史或折合乙醇摄入量男性<140g/周,女性<70g/周;②除外病毒性肝炎、药物性肝病、全胃肠外营养、肝豆状核变性、自身免疫性肝病等可致脂肪肝的特定疾病;③肝活检组织病理学改变符合脂肪性肝病诊断标准。
将NASH与NAFI区分开非常重要,因为NAFL通常不会发生肝脏严重并发症,但NASH患者可进展为肝纤维化、肝硬化,进而发生肝癌;同时NASH也可不经肝硬化,直接并发HCC,本例即是经病理证实为NASH但无肝硬化发生HCC的病例。
NASH病理学改变主要为肝细胞脂肪变性、气球样变和小叶内炎症,伴或不伴纤维化。虽然目前肝组织活检是诊断NASH金标准,但成本高、取样误差和有创性限制了该方法的广泛使用。因此,NASH无创诊断方法是当前研究的热点之一。
NASH血清学指标主要包括角蛋白-18(CK-18)、转化生长因子β1、天冬氨酸氨基转移酶(AST)/血小板比值、胰岛素抵抗稳态评估,其中最好的是CK-18。CK-18是肝细胞凋亡中半胱天冬酶的底物,在肝细胞凋亡过程中,CK-18被半胱天冬酶裂解为CK-18片段后释放入血。而肝细胞凋亡是NAFLD进展至NASH的关键事件。
多项研究证实,NASH患者的血清CK-18片段显著升高,迪亚卜(Diab)等选择CK-18片段界值为252U/L,敏感性及特异性分别为82%和77%;选择界值为275U/ L,敏感性及特异性分别为77%和100%,但需要大样本临床试验的支撑。
在影像学检查方面,B超、CT、磁共振成像均不能有效鉴别NAFI及NASH。瞬时弹性成像有助于临床医师判断NAFLD患者是否为桥接纤维化和(或)肝硬化高风险人群,但同样不能用于早期鉴别NASH和NAFL。
总之,目前仍无可取代肝组织活检的无创检查方法,当患者伴有以下惰况时建议行肝组织活检:①常规检查和诊断性治疗未能明确诊断的患者;②进展性肝纤维化高危人群,但缺乏临床或影像学证据。
NASH相关肝硬化患者应进行肝癌筛查。NAFL并发HCC非常罕见,且预后较好,故不需要常规监测肝癌。
然而,鉴于肥胖和糖尿病的全球流行,且非酒精性脂肪性肝病(NAFLD)相关HCC可发生于无肝硬化阶段,因此,对于无肝硬化的NASH患者,是否需要和如何选择其中高危人群进行HCC监测,值得我们深入思考。
3 NAFLD相关HCC防治
3.1 外科治疗 外科手术是肝癌的首选治疗方法,主要为肝切除术和肝移植术。据统计仅20%的患者适合接受手术治疗,可采用局部治疗(局部消融治疗、肝动脉介入治疗)、现代精确放疗(三维适形放疗、调强适形放疗、立体定向放疗)、分子靶向药物(索拉非尼)能减轻症状、改善生活质量和延长生存期。
对成功行治愈性治疗的HCC患者,还应该进行定期随访,通常在治疗后的前3年每3个月随访1次;治疗后的3~5年每4~6个月随访 1次;5年后可改为6~12月随访1次。尽管一般NAFLD相关HCC的病理分化较好,但与其他慢性肝病所致的HCC相比,NAFLD相关HCC的5年生存率无显著差异,心血管疾病带来的死亡似乎值得重视。
3.2 基础治疗 NAFLD相关HCC的关键在于治疗NAFLD、改善胰岛素抵抗、防治代谢综合征。NAFLD的基础治疗为改变生活方式,纠正不良生活方式和行为,增加有氧运动,通常须有一定程度体质指数(BMl)下降才能改善包括NAFLD在内的代谢综合征组分。
基础治疗目标为16~26周持续体重下降,并能在以后保持这种生活方式改变,包括饮食、运动和行为治疗(表1)。
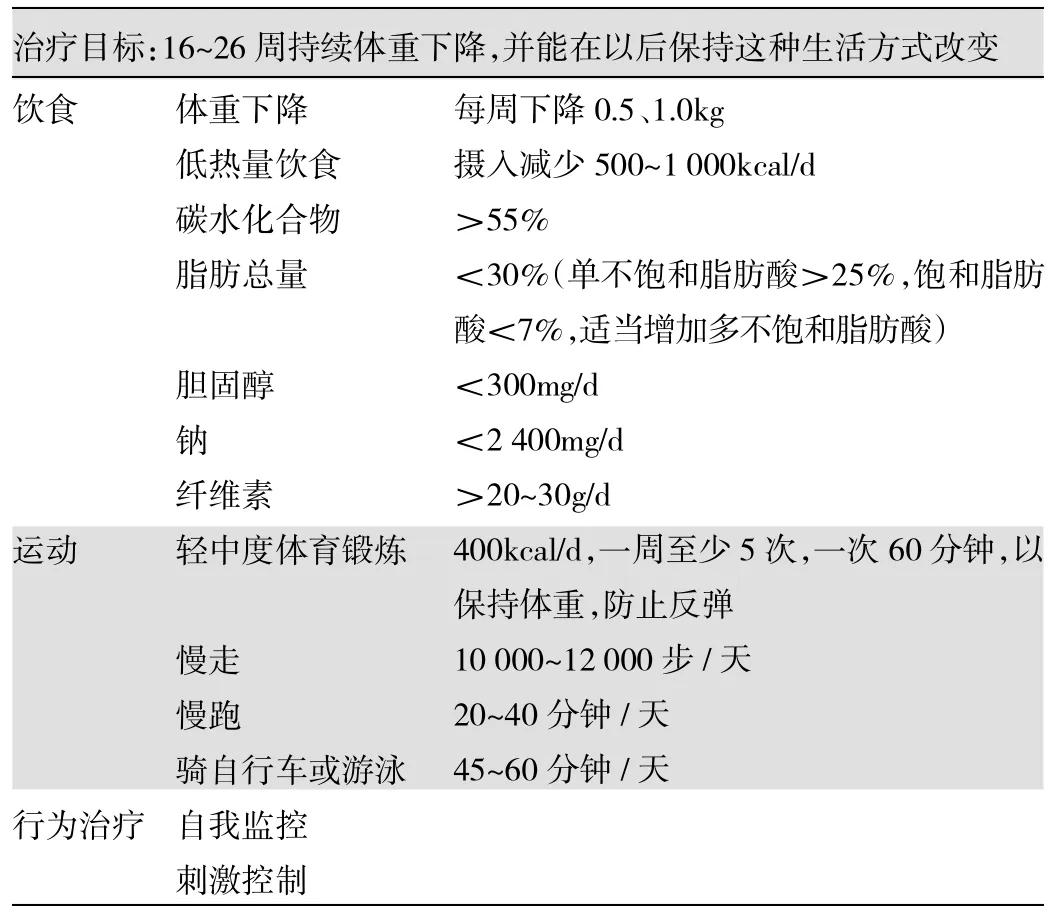
表1 NAFLD的基础治疗
3.3 药物治疗 NAFLD药物治疗目的是减缓减少肝硬化、肝癌及肝衰竭等终末期肝病的发生,降低患者肝脏相关疾病病死率。临床应用药物包括胰岛素增敏剂、抗氧化剂和肝细胞保护剂、降脂药3类。
胰岛素抵抗在NAFLD发病中发挥重要作用。二甲双胍除不仅能改善胰岛素抵抗,还可缓解肿瘤坏死因子α(TNF-oL)诱导所致的肝脂肪变性、炎症以及纤维化等。研究显示,口服二甲双胍(850mg/d)联合生活方式改变治疗NAFLD,能降低血清转氨酶、改善胰岛素抵抗及肝脂肪变性。但也有研究显示,二甲双胍在NAFLD中对肝脂肪变性无改善作用,此外二甲双胍可致乳酸升高,在治疗期间应监测乳酸水平。
罗格列酮或吡格列酮为噻唑烷二酮类药物,通过激动过氧化物酶体增殖物活化受体(PPAR),增加脂肪细胞、骨骼肌细胞对胰岛素敏感性,抑制脂质过氧化和TNF-α的活性。罗格列酮(8mg/d)和吡格列酮(30mg/d)能改善NAFLD患者血清转氨酶水平和胰岛素抵抗,但未改善肝纤维化。
然而,NAFLD合并糖尿病是HCC的独立危险因素,治疗胰岛素抵抗和高胰岛素血症对于预防HCC形成具有重要意义。尽管当前HCC指南没有关于NAFLD、肥胖和糖尿病相关HCC的特别推荐,但胰岛累增敏剂长期治疗可能具有预防HCC和改善HCC预后。
维生素E是一种脂溶性抗氧化剂,一定程度上能保护肝脏细胞免受氧化应激造成的损伤。美国2012年《NAFLD诊疗指南》推荐:①非糖尿病肝活检证实的NASH患者每日服用800IU维生素E,能够改善肝组织学,可作为NASH患者的一线治疗用药;②除非有进一步的证据,维生素E不推荐用于合并糖尿病的NASH患者、未行肝活检的NAFLD患者、已进展至肝硬化的NASH患者和病因不明的肝硬化患者。
熊去氧胆酸可降低胆汁中疏水性胆汁酸比例而保护肝细胞,调节免疫和氧化。虽然大剂量熊去氧胆酸[28~35mg/(kg·d)]可改善NASH患者胰岛素抵抗,肝酶水平,但对肝组织学作用有限,指南不推荐熊去氧胆酸用于治疗NAFLD或NASH患者。N乙酰半胱氨酸(NAC)是还原型谷胱甘肽的前体,可减轻氧化应激和脂质过氧化。NAC([200mg/d)可显著改善患者肝功能及肝脂肪变性。
越来越多的研究表明,降脂药物不仅能降低NAFLD患者血脂水平,还能改善患者肝功能,常用的降脂药物为他汀类药物。美国2012年《NAFLD诊疗指南》推荐:①尚无足够证据表明他汀类药物增加NAFLD/ NASH患者药物性肝损伤风险,可用于治疗NAFLD/ NASH患者的血脂异常;②除非有随机临床试验以组织学终点证明他汀类的有效性,否则不应用于NASH的一线治疗。
益生菌和益生元制剂在NAFLD中受到越来越多的重视,与脂肪生成、糖耐受和血浆内毒素(LPS)水平负相关,而且还可能抑制宿主与肥胖和炎症的基因过表达。实验研究显示,益生菌可减轻NAFLD大鼠的肝脏脂肪变性、炎症和纤维化。然而,尚无大规模的临床研究来评估这一新方法的疗效和不良反应。
4 小结
NALFLD本身与其他相关危险因素协同正日益增加HCC的发病率。由于代谢综合征的全球流行,且NAFLD相关的HCC很大一部分可发生于无肝硬化阶段,因此,我们可能需要转变HCC的监测模式。防治NAFLD、肥胖和糖尿病仍是管理NAFLD相关HCC最好的策略。
病例介绍
患者男性,75岁,因“右上腹部胀痛不适1周”来我院消化科门诊。患者既往有高脂血症28年、脂肪肝病史20年,高血压病史15年,无糖尿病、输血及吸烟饮酒史。平素服用卡托普利、硝苯地平和辛伐他汀。
体检:血压140/85mmHg,体质指数(BMl)为29.5kg/m2,右上腹轻压痛,无反跳痛,余无异常,
患者肝功能除γ谷氨酰转肽酶(GGT)为120U/L以外,余无异常。肝、胆、胰、脾、肾彩超示:脂肪肝,肝内可疑占位。
进一步检查甲胎蛋白(AFP)为58ng/ml,上腹部增强CT示:肝第V段见一团块状不均匀密度减低影,边界清楚,大小为3.5cm×4.2cm,增强扫描时动脉期明显强化,静脉期强化效应减弱,延迟期呈不均匀低密度灶,考虑HCC可能性大。病毒学指标:乙肝三系、HBV DNA、抗-HCV均为阴性,自身免疫性抗体(-),血清铁蛋白和铜蓝蛋白正常。患者在我院肝胆外科接受部分肝叶切除术。
切除组织的肿瘤区域病理示:中度分化HCC,而肿瘤旁组织病理学示:小叶内肝细胞中度脂肪变性(>30%),中度门管区及其周围炎症(G2),肝细胞气球样变,伴细胞周及门管区纤维化(S2)。
(本文转载自《中国医学论坛报》2014年7月24日第40卷第27期总第1412期)
200080 上海交通大学附属第一人民医院

