大孔树脂分离纯化松潘乌头总生物碱研究
王小芳, 张喜民, 邓月婷, 卢 英, 吴秀琴, 贾继禧
(甘肃陇神戎发药业股份有限公司,甘肃 兰州 730101)
松潘乌头(AconitunsungpanenseHand-Mazz)[1]为毛茛科乌头属植物,主要分布在甘肃、青海、四川、陕西、宁夏、山西等地。别名火焰子、蔓乌药、羊角七、藤乌药。民间用于治疗跌打损伤、类风湿性关节炎引起的疼痛和红肿等症状[2-5]。本课题组在前期对其化学成分及药效学方面进行了试验研究,发现松潘乌头的有效成分总生物碱,表现出较强的镇痛、抗炎作用。为了深入研究开发松潘乌头的可利用价值,以富集确定有效部位为目的,本实验采用大孔树脂对其总生物碱提取纯化工艺进行研究,提高其生物碱量,为下一步制剂研究以及新药申报等方面的工作提供研究依据。
1 材料与仪器
1.1 材料 松潘乌头(AconitunsungpanenseHand-Mazz) 采自甘肃天水,由甘肃林业职业技术学院任继文教授鉴定。
1.2 仪器及试剂 KQ-500M超声波清洗仪(东莞市科桥超声波设备有限公司);TU-1901紫外分光光度计(北京普析通用仪器有限责任有限公司);YP502N电子天平(上海菁海仪器有限公司);乌头碱对照品(中国食品药品检定研究院);氨水(分析纯);硫酸(分析纯);氢氧化钠(分析纯);三氯甲烷(分析纯);乙醚(分析纯);溴甲酚绿(分析纯);冰醋酸(分析纯);无水硫酸钠(分析纯);D101、AB-8、X-5、D-001(安徽三星树脂公司);NKA-9(天津波鸿树脂科技有限公司)。
2 方法与结果
2.1 松潘乌头总生物碱的制备 称取粉碎后过60目筛的松潘乌头药材200 g,置提取设备中,用10%碳酸钠溶液润湿,拌匀,放置4 h,加入75%的乙醇1 000 mL,充分搅拌,功率为500 W超声提取[6]30 min,重复操作3次,合并提取液,减压回收乙醇得松潘乌头总生物碱浸膏。
2.2 总生物碱测定(酸性染料比色法)[7-8]
2.2.1 乌头碱对照品溶液的制备 精密称取乌头碱对照品0.029 8 g,置100 mL量瓶中,用0.01 mol/L盐酸溶解并稀释至刻度,即得乌头碱对照品质量浓度为0.298 mg/mL。
2.2.2 供试品溶液的制备 精密称取“2.1”项制备的松潘乌头总生物碱浸膏2 g,置100 mL量瓶中用0.01 moL的盐酸溶解并稀释至刻度,即得松潘乌头总生物碱质量浓度为20 mg/mL。
2.2.3 测定波长的选择 精密吸取乌头碱对照品溶液及供试品溶液各1.0 mL,置于具塞试管中,加氨试液0.5 mL,用乙醚∶三氯甲烷(体积比3∶1)4 mL提取两次,合并提取液,蒸干,残留物加0.01 mol/L盐酸1.0 mL溶解,加pH 3.05的醋酸盐缓冲液5.0 mL与溴甲酚绿指示液2.0 mL,摇匀,再精密加人三氯甲烷8.0 mL,充分振摇,静置,分取三氯甲烷层,加无水Na2SO4脱水后,以0.01 mol/L盐酸同法作空白。分别在200~800 nm波长范围内进行扫描。结果表明,乌头碱对照品和供试品溶液在416 nm处均有最大吸收,故选择416 nm为检测波长。
2.2.4 标准曲线的制备 精密量取对照品溶液0.1、0.25、0.5、0.75、1.0 mL,置于具塞试管中,再分别补加0.01 mol/L的盐酸0.9、0.75、0.5、0.25、0 mL之后,按照波长选择的方法,以0.01 mol/L盐酸同法作空白在416 nm下测定吸光度。以乌头碱对照品质量浓度为横坐标,吸光度为纵坐标,绘制标准曲线,得回归方程Y=0.191 2x-0.008 8,r2=0.999 8,线性范围为0.029 8~0.298 mg/mL。
2.2.5 精密度试验 精密量取0.298 mg/mL乌头碱对照品溶液1.0 mL,置于具塞试管中,参照“2.2.4”项下方法操作,于416 nm处测定吸光度,连续测定6次。结果RSD为0.73%,说明仪器所测数据准确可靠。
2.2.6 重复性试验 精密称取同一批制备的松潘乌头总生物碱浸膏6份,各2 g,分别按“2.2.2”项下方法制备供试品溶液,按“2.2.4”项下方法操作,于416 nm处测定吸光度,结果RSD为0.89%。表明该方法重复性良好。
2.2.7 稳定性试验 精密吸取“2.2.2”项下制备的供试品溶液1.0 mL,按“2.2.4”项下方法操作,显色后分别在0、5、15、25、35、45、55 min于416 nm处测定吸光度,RSD为0.75%。结果表明,该方法在55 min内稳定。
2.2.8 加样回收率试验 精密吸取6份“2.2.2”项下制备的供试品溶液各1.0 mL,分别精密加入1.0 mL乌头碱对照品溶液(0.298 mg/mL),混匀,比色法测定吸光度。根据回归方程计算回收率。乌头碱的平均回收率为99.8%,RSD为2.46%。
2.2.9 样品的测定 定量取上柱后的洗脱液旋转蒸干,残留物加定量的0.01 mol的盐酸溶解,按上述乌头碱对照品的处理方式进行测定。
2.3 大孔树脂纯化松潘乌头生物碱
2.3.1 大孔树脂的预处理 用体积分数为95%乙醇将树脂浸泡24 h,使其充分溶胀,然后用乙醇清洗至洗出液与水混合(体积比1∶5)无白色浑浊后,再用大量蒸馏水洗去乙醇,备用。
2.3.2 大孔树脂的筛选 通过静态吸附法对D101、X-5、AB-8、NKA-9及D-001型树脂进行筛选,确定纯化松潘乌头生物碱的树脂类型[9]。具体操作如下:精密称取10 g树脂D101、X-5、AB-8、NKA-9及D-001,经过预处理之后分别置于100 mL锥形瓶中,加入过量松潘乌头生物碱提取液,室温条件下振摇24 h,使之充分吸附。测定吸附后松潘乌头生物碱提取液中总生物碱的量。将静态吸附饱和的树脂,加体积分数为95%的乙醇溶液,在室温条件下振摇24 h,测定乙醇中生物碱的量。重复3次,根据测定的结果,计算各树脂的平均静态吸附率与解吸附率,结果见表1。
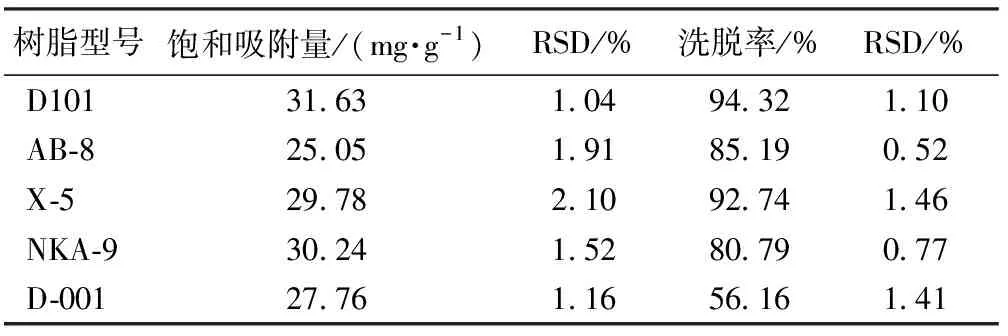
表1 树脂的吸附率与洗脱率
由表1可见,大孔吸附树脂D101的饱和吸附量及洗脱率均优于其余树脂,因此,选择D101树脂进行工艺参数考察。
2.3.3 单因素试验 将预处理后的D101树脂装入D3.5 cm × 30 cm的玻璃柱中,树脂填装高度为20 cm,水洗至无醇味。考察上样液质量浓度、上样液pH、洗脱液质量浓度及洗脱液pH,对D101大孔树脂吸附性能及洗脱参数的影响。
2.3.3.1 上样液质量浓度的考察 将5份定量的松潘乌头总生物碱提取液分别稀释成0.10、0.15、0.20、0.25、0.50 g/mL,以1.5 BV/h体积流量上样,检测采用酸性条件下与碘化铋钾反应产生橘红色沉淀泄漏;待吸附饱和之后测定吸附剩余液中总生物碱的量,重复3次,根据测定的结果,计算各质量浓度下平均吸附量,结果见表2。
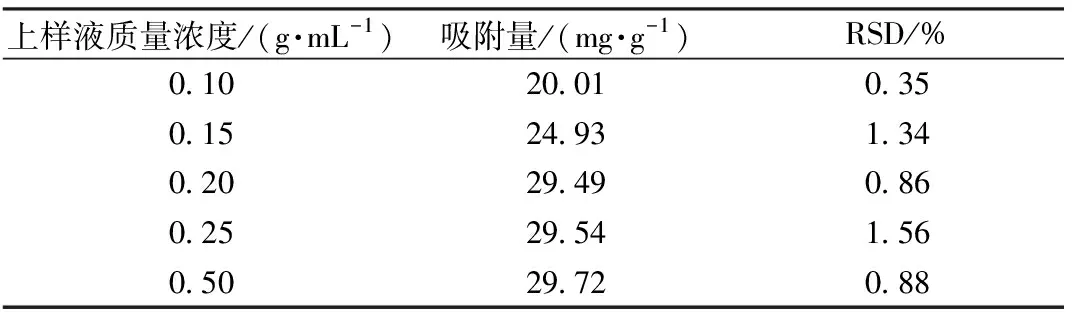
表2 松潘乌头生物碱提取液质量浓度对D101吸附量的影响
表2表明,随着松潘乌头生物碱提取液质量浓度的增大,D101对松潘乌头生物碱的吸附量逐渐增加,当质量浓度为0.20 g/mL,D101对松潘乌头生物碱的吸附量达到29.49 mg/g,此后质量浓度增加,吸附量没有显著增加,说明质量浓度为0.2 g/mL时,D101对松潘乌头生物碱的吸附量已接近饱和。因此,在D101动态吸附松潘乌头生物碱的实验中,最佳质量浓度为0.2 g/mL。
2.3.3.2 上样液pH的考察 取3份等量的松潘乌头总生物碱提取液,用氨水分别调pH于4、5、6之后定容,使其质量浓度为0.20 g/mL,以1.5 BV/h体积流量上样,检测采用酸性条件下与碘化铋钾反应产生橘红色沉淀为泄漏;待吸附饱和之后测定吸附剩余液中总生物碱的量。重复3次,根据测定的结果,计算不同上样液pH下平均吸附量,结果见表3。
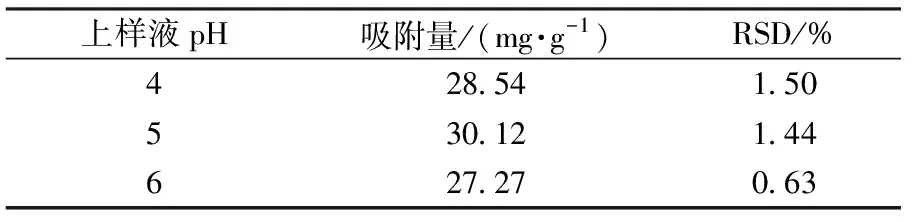
表3 松潘乌头生物碱提取液pH对D101吸附量的影响
表3表明,松潘乌头总生物碱提取液的pH为5时,D101对松潘乌头生物碱的吸附量达到最高30.12 mg/g,所以本实验选择总生物碱提取液的pH为5时上样。
2.3.3.3 洗脱液pH的考察 取4份0.2 g/mL、pH5的松潘乌头总生物碱提取液,分别以1.5 BV/h体积流量上样,检测采用酸性条件下与碘化铋钾反应产生橘红色沉淀为泄漏;待吸附饱和之后,用蒸馏水以2 BV/h的体积流量对杂质进行洗脱,再分别用pH为4、5、6、7,体积分数为95%的乙醇以2 BV/h的体积流量对总生物碱进行洗脱,收集洗脱液,测定洗脱液中总生物碱的量。重复3次,计算其平均值,结果见表4。
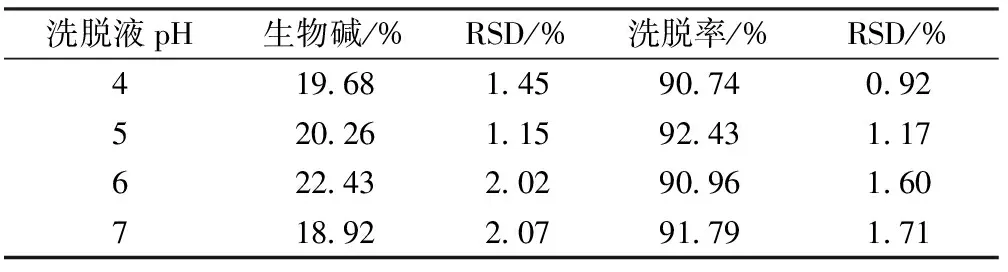
表4 洗脱液pH对生物碱纯化率的影响
表4表明,洗脱液pH从4增加到6,洗脱液中总生物碱的量也随之增大;而pH从6增加到7,洗脱液中总生物碱的量反之降低;随着pH的变化,洗脱率没有明显的变化;因此,此实验选择洗脱液pH为6进行洗脱。
2.3.3.4 洗脱液体积分数的考察 取5份0.2 g/mL、pH5的松潘乌头总生物碱提取液,分别以1.5 BV/h体积流量上样,检测采用酸性条件下与碘化铋钾反应产生橘红色沉淀为泄漏;待吸附饱和之后用5 BV的蒸馏水以2 BV/h的体积流量对杂质进行洗脱,再用pH为6、体积分数为40%、50%、60%、75%、95%的乙醇以2 BV/h的体积流量对总生物碱进行洗脱,收集洗脱液,测定洗脱液中总生物碱的量。平行3组,计算平均值,结果如下表所示:
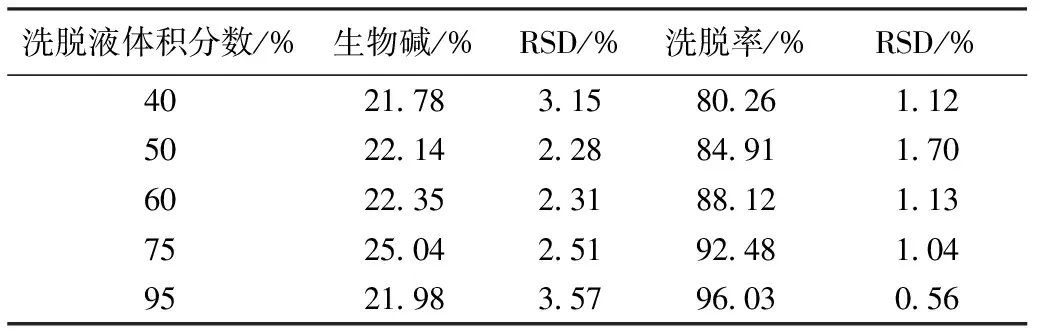
表5 洗脱液体积分数对生物碱纯化率的影响
表5表明,体积分数为75%的乙醇洗脱液中总生物碱的量较高,而40%、50%、60%、95%的洗脱液中总生物碱含量相差不大;洗脱率随着乙醇洗脱液体积分数的增加而增大,故确定洗脱液的体积分数为75%。
2.3.4 响应面试验
2.3.4.1 响应面试验设计及结果 根据单因索试验结果,选取上样液pH、上样液质量浓度、乙醇体积分数等3个因素进行试验设计结果见表6。
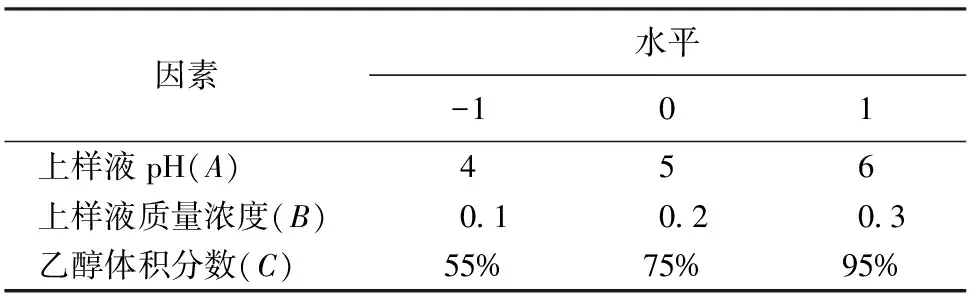
表6 响应面实验法因素和水平
2.3.4.2 响应面分析方案及结果 结合单因素试验结果,进行BoX-Behnken中心组合实验设计,利用Design-Expert 7.0软件进行数据拟合,建立数学模型,并获得大孔树脂D101纯化松潘乌头总生物碱工艺的最佳条件,响应面分析试验设计方案与试验结果见表7。
2.3.4.3 模型的建立及其显著性检验 利用Design-Expert 7.0 软件对表7试验数据进行多元回归拟合,得到生物碱量(Y)对上样液pH(A)、上样液质量浓度(B)、乙醇体积分数(C)的二次多项回归模型为:
Y=222.96-4.43A-2.57B+0.45C-5.64AB+5.92AC-0.68BC-31.52A2-13.97B2-17.87C2
对该模型方程求一阶偏导数等于零,求出最佳条件为:上样液pH为5.0、上样液质量浓度为0.2 g/mL、洗脱液乙醇的体积分数为75%。该回归模型进行方差分析,结果见表8。
根据统计学相关知识对方差分析表进行分析,模型的P<0.000 1,模型失拟项(P=0.125 5)不显著,说明可以用该模型来分析和预测大孔树脂D101纯化松潘乌头总生物碱的工艺结果。从回归方程模型因变量的方差分析可知:模型的一次项A差异显著;交叉项AB、AC差异显著;二次项A2、B2、C2差异极显著,说明所选因素与响应值之间不是简单的线性关系。依据回归方程的系数值和方差分析表可知,在响应面的试验范围内因素的主效应关系为:上样液pH>上样液质量浓度>洗脱液体积分数。
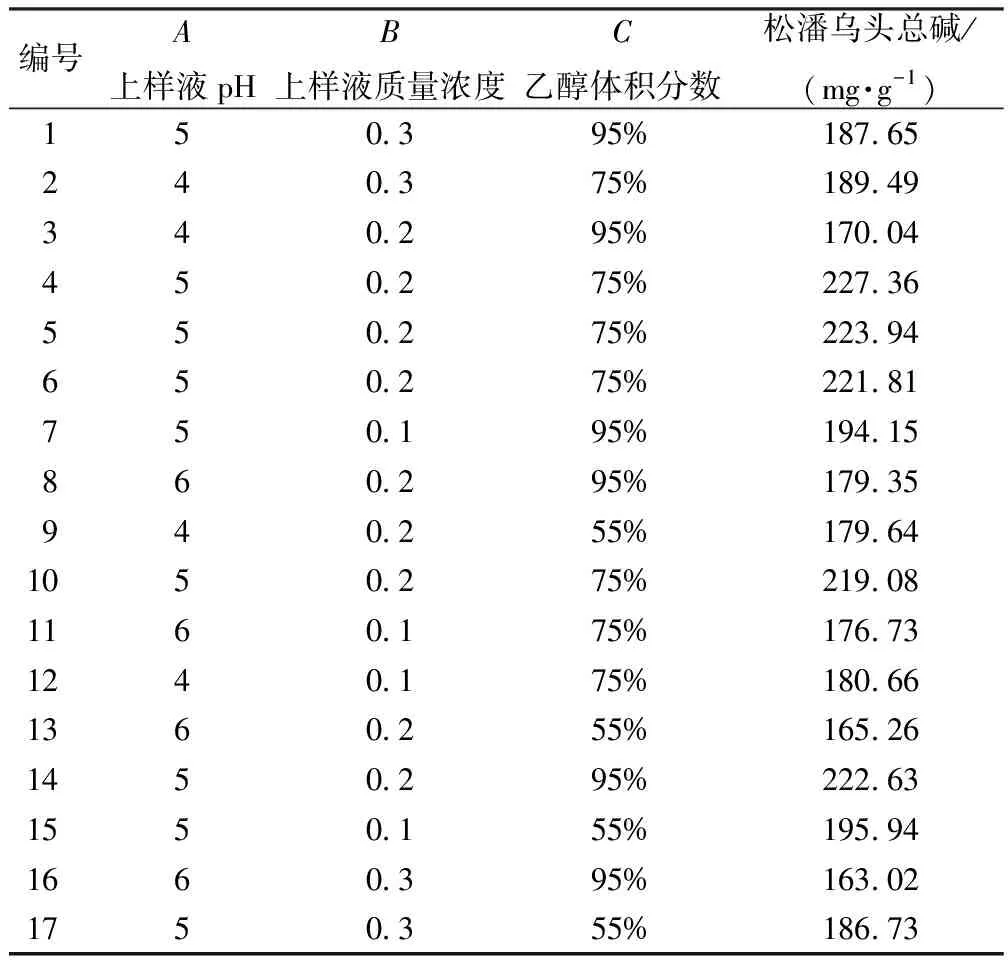
表7 响应面方案及试验结果
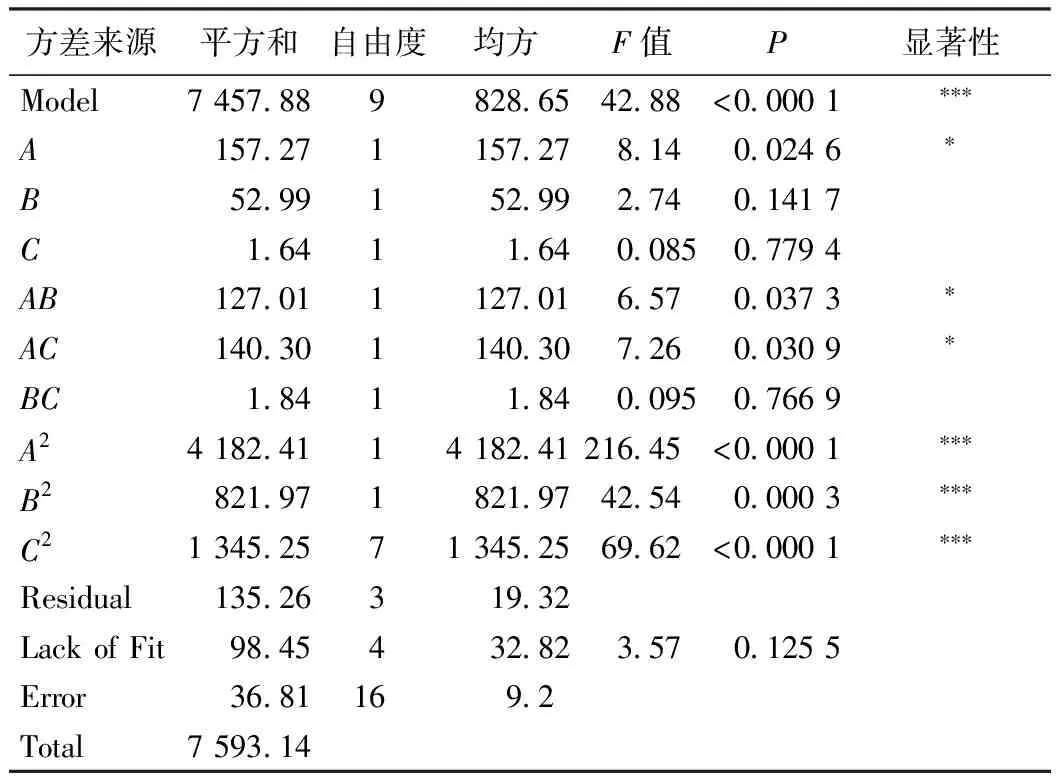
表8 回归模型方差分析
2.3.4.4 响应曲面分析 由多元回归方程可以得到不同因素对成分量影响的响应面及其等高线图。等高线图表示在同一椭圆形的曲线上,生物碱的量是相同的。在椭圆形区域中心,生物碱量最高,由中心向边缘逐渐降低。响应曲面坡度越陡峭,表明响应值对于操作条件的改变非常敏感,而曲面坡度相对平缓,表明操作条件的改变对响应值的改变会比较小。根据上述性质可以看出:上样液质量浓度与上样液pH,上样液pH与洗脱液体积分数存在明显的交互效应,而上样液质量浓度与洗脱液体积分数交互效应不明显。见图1~图3。
2.3.4.5 最优工艺条件求取与验证 通过Design-Expert 7.0软件求得大孔树脂D101纯化松潘乌头总生物碱的最佳工艺条件如下:上样液质量浓度为0.2 g/mL,上样液pH为5.0,洗脱液体积分数为75%,在此条件下进行6次验证试验,则松潘乌头总生物碱的平均含有量为223 mg/g,RSD为1.78%。表明实验设计和响应面法优化得到的提取工艺参数准确可靠,具有实用价值。
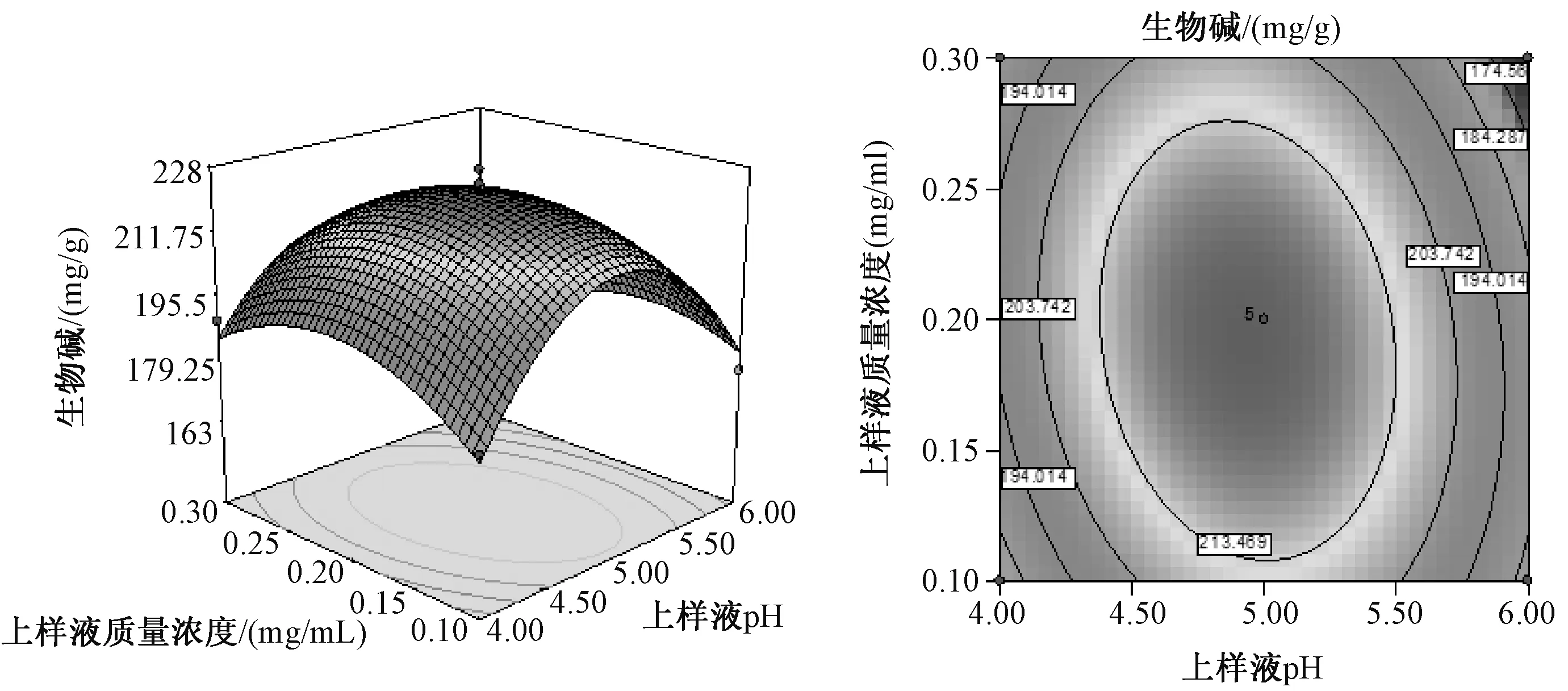
图1 上样液质量浓度和上样液pH对纯化率的影响
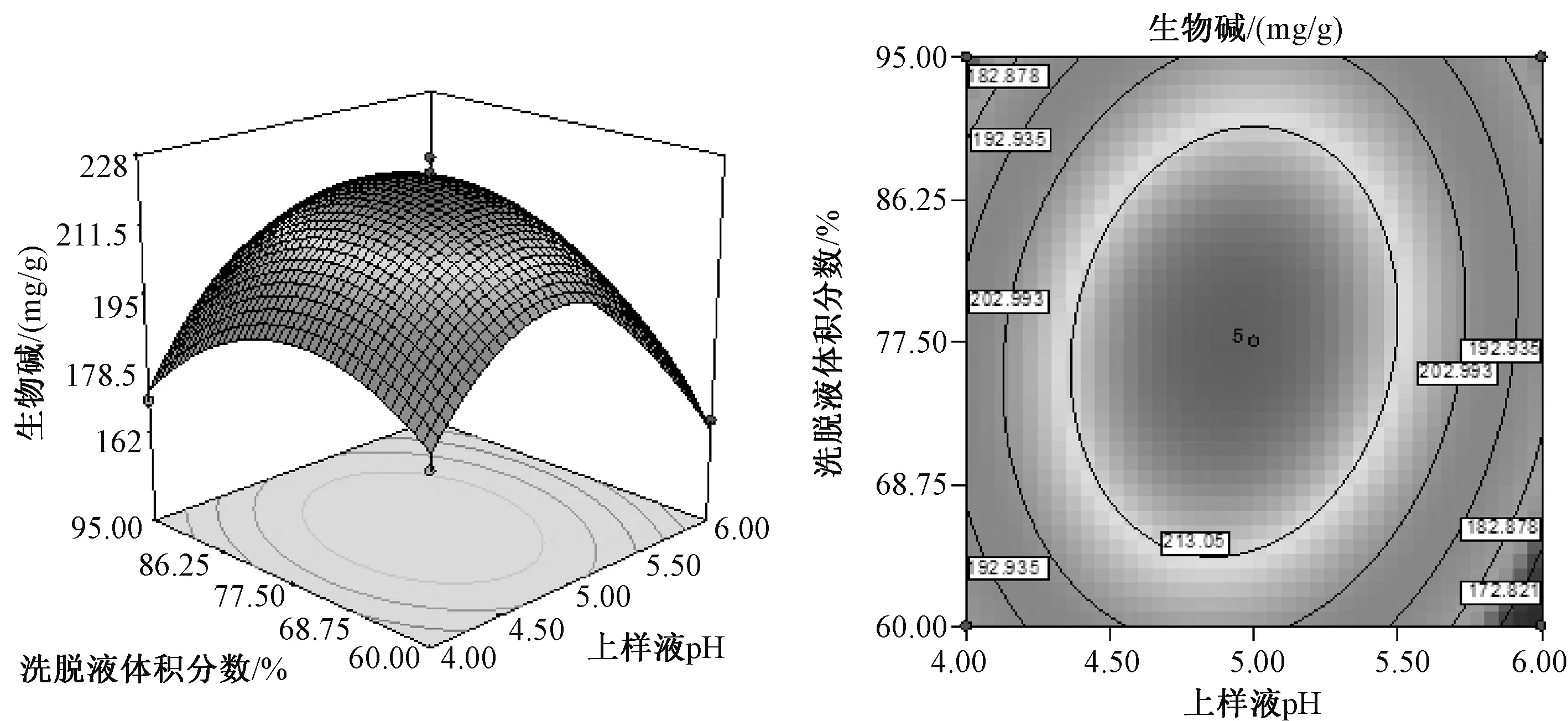
图2 上样液pH和洗脱液体积分数对纯化率的影响
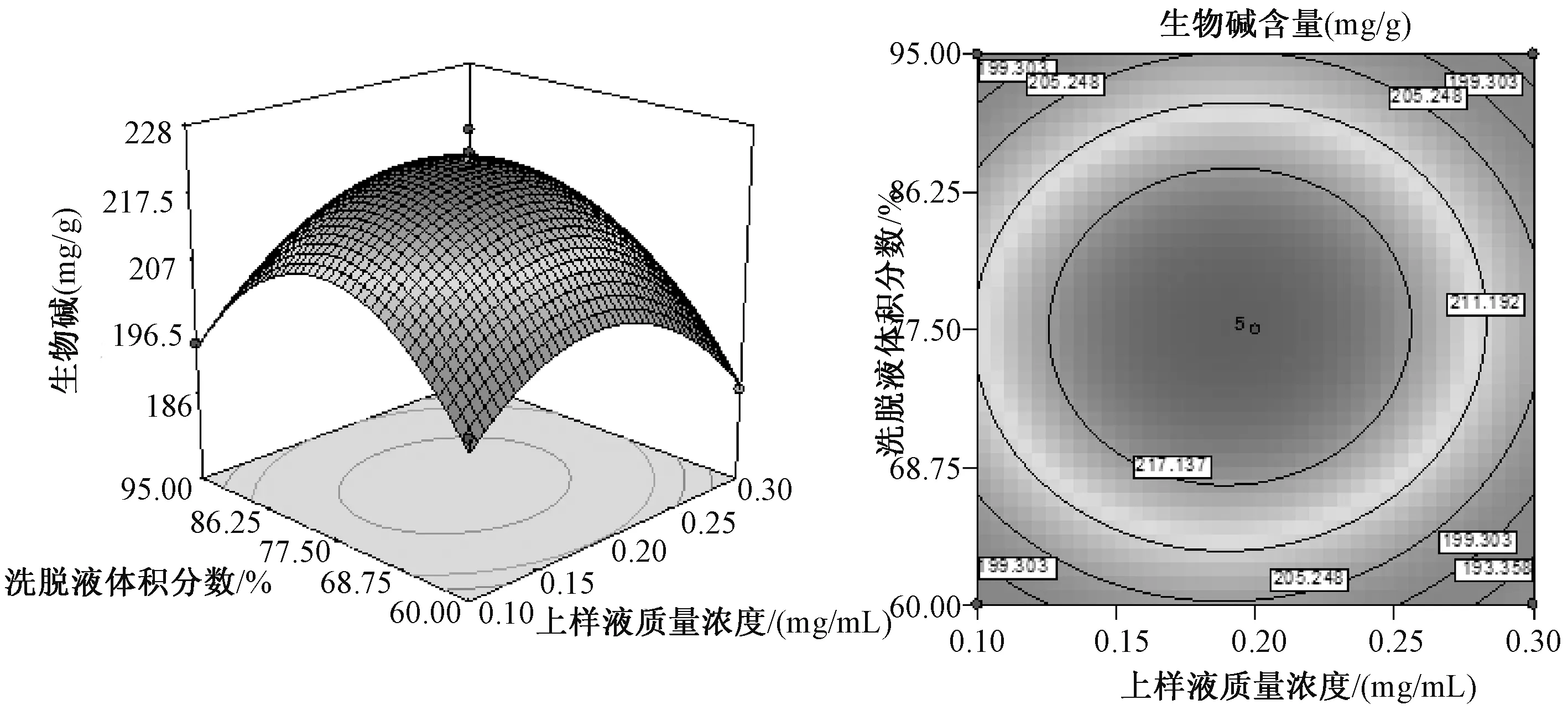
图3 上样液质量浓度和洗脱液体积分数对纯化率的影响
3 讨论
本实验采用大孔吸附树脂D101,通过单因素试验和响应面回归分析法,达到了纯化松潘乌头总生物碱的工艺目的。考察了上样液质量浓度、上样液pH值、洗脱液体积分数和洗脱液pH对大孔吸附树脂D101纯化松潘乌头总生物碱的影响,响应面法研究表明大孔吸附树脂D101纯化松潘乌头总生物碱的最佳工艺条件为:松潘乌头提取液质量浓度为0.2 g/mL,pH为5.0,乙醇洗脱体积分数为75%,在此条件下松潘乌头含有量为22%,工艺简便,参数稳定可靠,因此,大孔吸附树脂D101适宜于松潘乌头总生物碱的分离纯化,通过中试研究可应用于工业生产,也为相关研究的进一步开展提供了可靠的实验依据。
参考文献:
[1] 佟姝丽, 崔九成, 袁菊丽. 松潘乌头的研究进展[J]. 陕西中医, 2007, 28(7): 900-902.
[2] 李洪刚, 李广义. 松潘乌头二萜生物碱的研究[J]. 药学学报, 1988, 23(6): 461-463.
[3] 王 锐, 倪京满, 胡兆勇, 等. 松潘乌头中的二萜生物碱研究[J]. 兰州医学院学报, 1991, 17(4): 201-204.
[4] 刘铭佩. 松潘乌头总碱的镇痛作用[J]. 中药药理与临床, 2007, 23(1): 36-37.
[5] 党月兰, 胡兆勇, 吴福祥. 松潘乌头总碱的镇痛作用和身体依赖性的实验研究[J]. 中国药物依赖性通报, 1993, 2(4): 242-246.
[6] 马学毅.一种松乌甲素的制备方法:中国,CN101851202[P].2010-10-06.
[7] 黄建明, 郭济贤, 陈万生. 大孔树脂对草乌生物碱的吸附性能及纯化工[J]. 复旦学报:医学版, 2003, 30(3): 267-269.
[8] 李文兰, 王艳萍, 季宇彬, 等. 应用AB-8大孔树脂纯化新乌头碱和乌头总碱[J].中国天然药物,2006,4(5):355-359.
[9] 万里翔, 杨小生, 侯大斌. 大孔树脂D-101、X-5、AB-8对乌头总碱的纯化工艺[J]. 湖北农业科学,2008, 47(6): 711-714.