基于微流控芯片的动态胚胎培养
王 维 苏 宁 钟志敏 彭娅娅 梁广铁
广东省广州市第一人民医院生殖健康与不孕症专科(510180)
辅助生殖技术(ART)主要是运用医学技术对卵细胞、精子、受精卵和胚胎进行人工操作,以达到受孕目的,而早期胚胎的体外培养是该技术中的一个重要环节[1]。国内外学者在该领域已经进行了大量卓有成效的研究,但到目前为止,大多数研究者都将注意力集中在培养液配方改良上,而忽略了胚胎的培养方法对胚胎体外培养的贡献。事实上胚胎在体内的发育环境是动态的,受精卵从输卵管壶腹部向子宫腔移动,受精卵周围的化学环境和物理环境也在不断发生变化[2-4]。微流控芯片的出现为解决以上问题提供了新的思路至上。微流控芯片技术是一种以在微米尺度空间内对流体进行操控为主要特征的科学技术,一方面,微流控通道具有与体内微血管相似的尺寸,在这个尺度下流体所具有的层流特性便于实现精确的流体控制;另一方面,微管道的形状和尺寸可以灵活设计,从而更好地模拟生理环境,有效模拟组织或器官的结构和功能[5]。前期研究报导了一系列基于微流控芯片的精子分选、受精以及胚胎发育等单元操作技术[6-8],在这些工作基础上,本研究旨在设计创新一种动态的物理培养系统--微流控培养系统,模拟体内动态环境,以连续灌流方式实现胚胎与外界物质交换,观察与检测胚胎体外发育情况,以便支持并改善早期胚胎的体外发育效果。
1 材料与方法
1.1 动物与试剂
1.1.1 实验动物 选择购自广东省实验动物中心无特定病原菌(SPF级,三级动物)6~8周龄体重28~32g的KM雌性小鼠45只、8~10周龄体重35~40g的KM雄性小鼠50只,常规饲养。
1.1.2 试剂 聚二甲基硅氧烷(PDMS)购自美国Dow Corning公司;SU-8 3025光刻胶购自美国 Microchem公司;孕马血清促性腺激素(PMSG)、人绒毛膜促性腺激素(hCG)购自杭州动物药品厂;体外受精-胚胎培养所需试剂取卵-胚胎处理液(GMOPS PLUS)、洗精受精液(G-IVF PLUS)、卵裂胚培养液(G-1PLUS)、囊胚培养液(G-2PLUS)、超纯培养油(OVOIL)购自瑞典Vitrolife公司。
1.2 微流控芯片的设计与构建
使用制图软件CorelDraw画出微流控芯片的结构图,采用软刻蚀工艺[9]制造如图1所示的微流控芯片,芯片尺寸为76mm×34mm。整个微流控芯片系统包含四层结构,基底层为平板玻璃,其余各层为PDMS材质。图2显示了装置的三维示意图。“基底层”是一层玻璃,是整个芯片培养系统的基底。“定位层”包含了16个突起的八扇瓣的受精卵-胚胎定位孔,定位孔是由八个扇瓣形成开放的圆柱状结构,直径为2mm,每个相邻扇瓣之间的间隙是50 μm,每个扇瓣的高度为250μm。第三层为通道层,与微量注射泵相连。受精卵、胚胎培养时的物质交换均在此层实现。“通道层”包含了培养液入口通道,受精卵-胚胎定位池,废液出口通道。“顶层”是一层PDMS盖板,覆盖定位池以避免水分的挥发、防止污染,保持培养环境的稳定。
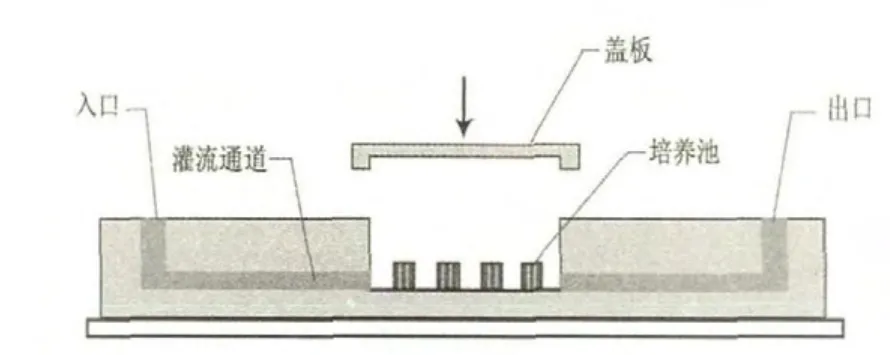
图1 微流控芯片示意图(侧面)

图2 微流控芯片三维示意图
1.3 生殖细胞的准备和体外受精[10]
1.3.1 精子的准备 选择8周龄以上、体重>35g、雄性特征明显的雄鼠,颈部脱臼致死,剖开腹部取出附睾及输精管,置于1ml G-MOPS液中,洗涤组织块后,移入盛有已平衡过夜的1ml G-IVF PLUS液的培养皿中,将附睾尾剪开数个小口,轻轻挤压使精子挤入G-IVF PLUS受精液,置于37℃、饱和湿度、5%CO2培养箱中1h,使精子继续获能。将精子悬液整倍稀释,观察精子活力和用精子计数板计算精子浓度。
1.3.2 卵母细胞的收集 选择6周龄以上、体重>28g的健康雌鼠,每只雌鼠腹腔注射10UPMSG,间隔48h后再腹腔注射5UhCG。将上述处理的雌鼠于注射hCG后13~17h,颈部脱臼致死,剖开腹部取其输卵管置于1ml G-MOPS液中,自输卵管壶腹部取出卵冠丘复合体(OCCC),将OCCC移入已平衡过夜的G-IVF PLUS受精液的微滴中清洗3遍后,移入250μl G-IVF PLUS受精液滴中,然后放入培养箱等待获能的精子。
1.3.3 体外受精 获能结束后,将精子加入已经含有OCCC的G-IVF PLUS受精液滴中,并最终使受精液中精子的浓度为0.5×106~1×106/ml,置于37℃、饱和湿度、5%CO2培养箱中受精5~6h。
1.3.4 受精率的检测 受精结束后,用捡卵针将卵子移入预热的G-MOPS液滴中,并轻轻吹打以洗掉透明带上粘附的精子,反复洗3~5次后,将卵子移入G-1PLUS培养液滴中,观察卵子雌雄原核来评价是否受精,并分离具有雌雄原核的受精卵备用。
1.4 微流控培养系统与微滴培养方法对照实验
1.4.1 对照组实验(常规微滴培养法) 在进行早期培养的前一天晚上,将G-1PLUS培养液在直径为35mm的培养皿上做成20μl的小滴,用石蜡油覆盖,置于37℃、饱和湿度、5%CO2培养箱中平衡过夜。早期培养时,首先用3个预平衡的培养液滴清洗受精卵3遍,然后将受精卵移入剩余的液滴,每个液滴放10个受精卵,将培养皿放入培养箱(37℃、饱和湿度、5%CO2)进行培养,每24h更换一次培养液。培养72h后将>8细胞的胚胎移至G-2PLUS囊胚培养液中,操作同前。分别在培养24、48、72和96h后观察记录胚胎的发育情况。
1.4.2 微流控芯片装置上胚胎培养 芯片和聚四氟乙烯毛细管在使用之前80℃烘烤1h,微量注射器在75%酒精中浸泡6h后用灭菌蒸馏水冲3次。移卵前夜,整个微流控芯片装置放入150mm细胞培养皿中,以高压灭菌水覆盖(121℃,15min高压),紫外照射30min左右,放入培养箱(37℃、饱和湿度、5%CO2)中平衡过夜。移卵前,微流控芯片装置用G-IVF液预处理,以改善亲水性。使用时在超净工作台上将芯片与注射器通过毛细管连接。然后用G-1PLUS培养液清洗一遍,再加入G-1PLUS培养液使其充满管道。用微量移液器吸取体外受精获得的受精卵,加入定位单元,尽量保证每个单元中仅有一个受精卵。定位完成后装置以PDMS盖板覆盖,放入培养箱(37℃、饱和湿度、5%CO2)中培养。微量注射泵抽取1ml G-1PLUS培养液,以一定的速度持续灌流。培养72h后,换取1ml G-2 PLUS培养液继续灌流。实验期间,分别在培养24 h、48h、72h和96h后观察记录胚胎的发育情况。
1.4.3 微流控培养系统培养液流速的优化 以5、10、20和30μl/h四种不同流速作为试验流速,并分别以这四种流速对小鼠的受精卵进行体外培养,以囊胚出现比率为检测目标,对培养效果进行观察和比较,来评估培养液流速对胚胎发育的影响。每组培养纵向重复3次,取平均值参与最终比较。
1.5 统计学分析
采用统计软件SPSS 18.0进行统计学分析,微流控培养系统培养液不同流速获得囊胚数之间的比较采用单因素方差分析,两种培养系统获得的各种胚胎发育率之间的比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 微流控培养系统培养液流速的优化
4种不同流速各培养48个小鼠受精卵,由表1可知,流速为10μl/h时对胚胎的培养效果最好,培养96h后获得的囊胚率最高,与其他3种流速比较,差异有统计学意义(P<0.01)。后期试验采取的流速为10μl/h。

表1 不同流速对小鼠体外受精胚胎发育的影响(培养96h)
2.2 微流控培养系统与微滴培养法对小鼠体外受精胚胎发育的比较
由表2可见,受精卵在微流控培养系统2~4细胞发育率与微滴培养系统比较,差异无统计学意义(χ2=1.021,P>0.05)。而微流控培养系统与微滴培养系统的5~8细胞发育率、桑葚胚发育率和囊胚发育率相比,各级胚胎的发育均有显著改善,两组比较差异均有统计学意义(χ2=5.141,P<0.05;χ2=4.325,P<0.05;χ2=5.519,P<0.05)。

表2 不同培养方法对胚胎发育的影响
3 讨论
胚胎质量是影响人类ART成功率的一个重要因素,而对其起关键性作用的是胚胎体外培养条件,包括培养液成分和培养体系。根据胚胎不同发育时期对营养成分的不同需求,序贯培养系统的发明有效地弥补了单一培养液的不足,使获得高质量囊胚进行移植成为现实,无疑在很大程度上提高了ART的成功率。然而,物理微环境也可能是影响体外胚胎发育的重要因素,但往往易被人们忽略。胚胎之所以能在体内很好发育主要原因在于保证其正常发育的环境是一个既能合理提供营养又能及时清理废物的动态培养环境[11]。随着胚胎的体外培养系统的发展,模拟体内着床前胚胎经历的机械性的和生化的环境,将能够提高对调节正常胚胎生长发育机制的理解,也可能改善实验室内体外培养的胚胎发育潜能[12]。早在1973年,Hoppe等[13]就探讨了培养箱中连接摇动器产生的物理刺激对小鼠卵母细胞受精的影响,结果表明,培养液体积及摇动时间对受精率并无显著影响。2010年,Matsuura等[14]探讨了倾斜胚胎培养系统(TECS)对小鼠胚胎培养的影响,发现在特定的培养条件下,TECS可显著提高小鼠胚胎发育潜能。Cabrera等[15]首次将微流体装置用于培养小鼠1-细胞胚胎,其孵化囊胚数和内细胞团数均显著高于静置培养体系,且与体内来源的囊胚相似。此外,也有报道表明,微流体培养体系不仅有利于小鼠植入前胚胎发育,而且提高了胚胎的种植率和继续妊娠率,有效降低了流产率[16]。
本研究为了模拟体内输卵管的结构和功能,设计的多层微流控芯片培养系统,其特色在于以带有微间隙的微柱状定位孔支撑胚胎的发育,定位孔藉由间隙与灌注培养液进行物质交换,避免了流体剪切力对胚胎的损害,通过自动控制培养液灌流速度,在一个密闭的环境中补充培养液而无需在培养箱外操作,避免了胚胎应激,为胚胎提供一个稳定的梯度培养环境。同时及时排除代谢产物,消除代谢物蓄积对胚胎生长发育的不利影响,有效模拟了输卵管的内部微环境。通过本试验研究显示,培养液灌流速度对胚胎培养效果影响显著。在培养液流速为10μl/h时,能够较好地支持小鼠受精卵发育到囊胚。分析原因可能是:胚胎之间可能分泌一些相互促进彼此发育的物质,流速过快使这种促进物质损失,有可能影响胚胎的发育的代谢平衡,同时当流速太快时,胚胎受到液体剪切力的影响,可能抑制了胚胎的发育。当流速太低时,由于芯片材料PDMS具有透气性,培养孔内液体蒸发相对较快,影响胚胎发育微环境的渗透压导致胚胎发育不良。只有在合适的流速时不会对胚胎群发育过程中建立的微环境造成太大的冲击,因而获得较好的培养效果。
试验比较了微流控动态培养系统与传统微滴静态培养方法获得的2~4细胞发育率、5~8细胞发育率、桑葚胚发育率和囊胚形成率,这些指标动态地反映了体外受精卵胚胎的发育状况。结果显示,虽然两组的2~4细胞发育率大致相当,但在胚胎逐渐发育的过程中体现出明显差异,微流控培养系统5~8细胞发育率、桑葚胚发育率和囊胚形成率均明显高于对照组微滴培养组。相对于常规培养方法,本研究发展的微流控动态培养系统更有利于提高胚胎的发育潜能,分析其原因可能为:微滴法培养情况下,液滴中胚胎和培养液处于相对静止状态,随着胚胎代谢活动的逐渐增强,各类代谢产物的累积速度不同,胚胎毒性物质的积累或营养物质的消耗等,阻碍了胚胎的发育。而微流控芯片动态培养可能打破了胚胎局部的环境梯度,清除胚胎生长过程中有害产物,补充营养物质,对胚胎上的机械受体提供物理刺激激活营养信号通路等,或者是以上多种因素的综合作用,促进了体外受精卵胚胎的发育。
综上所述,胚胎培养过程中的物理微环境会影响胚胎质量。本研究发展了一种基于微流控芯片的胚胎动态培养方法,通过控制液体的流动达到更换和调整培养液,并把胚胎培养的空间尽可能控制在一个较小区域,模拟体内胚胎输卵管的机械和生化环境实现了胚胎的动态培养。这种方法能有效提高胚胎的发育潜能,成为一种新的人类胚胎体外培养的有力工具。在以后的研究中可尝试连接纳米传感器或探针对培养液或胚胎进行在线诊断,如监测液体的pH值、温度波动、液体流速及细胞的体积,以便实时监控液体渗透压变化。通过传感器监测,获得胚胎在发育过程中需要哪些营养成分的信息,然后根据胚胎的不同需要选择特殊的培养基或添加特定的因子,从而设计出针对不同胚胎需求的“个性化”培养基,选择发育潜能最高的胚胎进行移植,从而提高体外受精-胚胎移植的成功率,改善妊娠结局。
[1] 卢惠琳,卢光琇.人类生殖与生殖工程[M].郑州:河南科学技术出版社出版,2001:98.
[2] Fauci LJ,Dillon R.Biofluidmechanics of reproduction[J].Annu Rev Fluid Mech,2006,38(1):371-394.
[3] Hardy K,Spanos S.Growth factor expression and function in the human and mouse preimplantation embryo[J].J Endocrinol 2002,172:221-236.
[4] Leese HJ,Tay JI,Reischl J,et al.Formation of Fallopian tubal fluid:role of a neglected epithelium[J].Reproduction,2001,121:339-346.
[5] Gary D.Smith GD,Shuichi Takayama,et al.Rethinking In Vitro Embryo Culture:New Developments in Culture Platforms and Potential to Improve Assisted Reproductive Technologies[J].Biol Reprod,2012,86(3):62,1-10.
[6] 王维,黎维生,彭娅娅,等.微流控芯片在精子分选中的应用[J].中华检验医学杂志,2009,32(8):920-923.
[7] 王维,梁广铁,彭娅娅,等.微流控芯片精子分选法对精子常规参数及DNA完整性的影响[J].中华男科学杂志,2011,17(4):301-304.
[8] 李伟萱,梁广铁,严伟,等.微流控芯片子宫[J].分析化学,2013,41(4):467-472.
[9] 林炳承,秦建华.图解微流控芯片实验室[M].北京:科学出版社,2008:145-180.
[10] 纳吉.小鼠胚胎操作实验手册[M].孙青原,陈大元译.北京:化学工业出版社,2006:411-425.
[11] Swain JE,Smith GD.Advances in embryo culture platforms:novel approaches to improve preimplantation embryo development through modifications of the microenvironment[J].Hum Reprod Update,2011,17(4):541-557.
[12] Perin PM,Maluf M,Januario D,et al.Comparison of the efficacy of two commercially available media for culturing one-cell embryos in the in vitro fertilization mouse model[J].Fertil Steril,2008,90:1503-1510.
[13] Hoppe PC,Pitts S.Fertilization in vitro and development of mouse ova[J].Biol Reprod,1973,8(4):420-426.
[14] Matsuura K,Hayashi N,Kuroda Y,et al.Improved development of mouse and human embryos using a tilting embryo culture system[J].Reprod Biomed Online,2010,20(3):358-364.
[15] Cabrera L,Heo Y,Ding J,et al.Improved blastocyst development with microfluidics and braille pin actuator enabled dynamic culture[J].Fertil Steril,2006,87(3):S43.
[16] Heo YS,Cabrera LM,Bormann CL,et al.Dynamic microfunnel culture enhances mouse embryo development and pregnancy rates[J].Hum Reprod,2010,25(3):613-622.

