含氮碳量子点的电化学制备及其在铜离子检测中的应用
罗宗乾,张艮,刘芳玲,王荣
(上海师范大学生命与环境科学学院,上海200234)
0 引言
碳量子点是尺寸小于10 nm分散的类球形荧光碳纳米颗粒[1],是荧光碳纳米材料中最主要的一种[2~8]。与传统的染料分子和半导体量子点相比,它不仅荧光强而稳定、耐光漂白、无光闪烁现象,而且激发光谱宽而连续,可实现一元激发多元发射。其低毒特性,良好的生物相容性和环境安全性以及水溶性确保了碳量子点可以放心地应用于活体细胞的检测,不用担心荧光材料对活体细胞的影响而导致误诊,也可以长时间研究细胞中生物分子之间的相互作用[9]。与无机量子点相似[10],碳量子点的发射光谱跨度很大,从可见光谱区一直延伸到近红外光谱区[11],这个优点弥补了普通荧光试剂在近红外光谱区品种少的不足[1,12]。此外,碳量子点既可用于单光子成像,又可用于双光子成像,有望替代无机量子点成为生物医学领域中最具应用前景的环境友好型荧光纳米材料。目前,已有多篇文献报道碳量子点被用作荧光探针应用于细胞和活体的荧光观测[13~15]。
已报道的碳量子点合成方法有很多[9,11,13,14],电化学方法合成碳量子点由于操作简单、设备要求低、可重复性强、产品稳定,不必进行进一步的修饰处理,只需要离心分离就可以得到发光碳纳米颗粒,而被许多研究者采用。在电化学法制备碳纳米颗粒的过程中,工作电极一般为导电的碳素材料,在一定的电流或电势下,借助电解液阳极氧化,从工作电极上剥离下细小的碳纳米颗粒[16]。2007年Zhou课题组[17]通过电化学的方法电解多壁碳纳米管制备发光碳量子点。以四丁铵高氯酸盐(TBAP)的脱气乙腈溶液为支持电解质,多壁碳纳米管做工作电极、铂电极做对电极、Ag/AgClO4做参比电极,实验过程中,通过观察电解液的溶液变化来控制合成的进度,反应得到的碳量子点粒径大小在2.8 nm左右,该碳量子点具有良好的水溶性。Lee课题组[18]是通过电化学的方法氧化石墨棒来制备荧光碳量子点,通入直流电源,阴阳极都用石墨棒做电极,配成100 mL的溶液(乙醇∶水=99.5∶0.5),慢慢加入氢氧化钠(0.2~0.4 g),电流密度控制在10~200 mA/cm2,可以制的荧光强度很强的碳量子点,他们是通过控制电流密度的大小来控制碳量子点的颗粒大小。Chi课题组[19]是通过电解石墨棒的方法来制备发光的碳量子点。石墨棒做工作电极、铂网做对电极、Ag/AgClO4做参比电极,在磷酸缓冲溶液中(pH7.0),控制电压-3 V~+3 V用循环伏安扫描的方法,制备碳量子点。随着反应的进行,溶液的颜色由黄色逐渐变化到深褐色,最后得到的碳量子点粒径大小为2 nm左右。Du等[20]以石墨棒为工作电极和对电极,Ag/AgCl(1 mol/L KCl)电极为参比电极,分别置于0.1 mol/L的乙醇钠的乙醇溶液的电解液中。在0~10 V电压下(扫速:0.5 V/s)循环伏安法电解60 min,溶液由无色变为黄色,最后到暗棕色。透析除去乙醇钠获得尺寸3.12 nm、发蓝绿光的碳量子点。作者认为该碳量子点的发光机理主要是碳纳米颗粒含有稳定的富氧基团。Kang等[21]将无水乙醇与蒸馏水按体积比为10∶90混合,再加入NaOH配制得到电解液;在直流电作用下反应2~4 h,并通过柱层分析法分离得到碳量子点。该量子点直径小于3 nm,具有较强的蓝绿色荧光(量子产率约为12%),并且指出不同的电流密度可以粗略控制碳量子点的发光。
常见的碳量子点通常以乙醇、葡萄糖等含氧化合物作为碳源。最近,Ma[22]与Liu课题组[23]分别用葡萄糖和4,7,10-trioxa-1,13-tridecanediamine(TTDDA),丙三醇和TTDDA通过微波辅助的方法,合成了含氮的碳量子点。这些含氮量子点由于表面存在活性的氨基,便于进一步的表面修饰,且其荧光特性也与常见的碳量子点存在差异。Wang等[24]以三聚氰胺和丙三醇为原料在酸催化的条件下,通过热解的方式制备了具有良好上转换特性的含氮碳量子点。此外,Zhang[25]和Zhu等[26]以乙二胺为氮源,分别用丙烯酸和柠檬酸为碳源,通过微波合成的方法制备了含氮的碳量子点。
该文使用乙二胺为原料,通过电化学合成的方法,制备了含氮碳量子点,并将其应用于Cu2+的荧光定量分析。
1 实验部分
1.1 实验试剂与仪器
无水乙二胺(H2NCH2CH2NH2)、二氯甲烷(CH2Cl2)、高氯酸锂(LiClO4·3H2O)购自国药集团,以上试剂均为分析纯。
F-2700荧光分光光度计(Hitachi,日本),DZF-6050型真空干燥箱(上海华连医疗器械有限公司),Agilent 8453紫外可见分光光度计(AgilentTechnologies,美国),透射电子显微镜(TEM 2010,JEOL,日本),pHS-3C型酸度计(上海雷磁仪器厂),LA 410UV紫外光源(HAYASHI,日本),IKA磁力搅拌器(德国),IKA旋转蒸发仪(德国),傅立叶红外光谱仪(AVATAR-370DTGS)。
1.2 含氮碳量子点的制备
首先用量筒量取无水乙二胺100 mL,在烧杯中加入高氯酸锂(LiClO4·3H2O)1.6 g,慢慢搅拌溶解,然后通氮气30 min左右,再分别用直径为0.5 cm的石墨棒做反应的阴阳极,通入直流电源,电流密度的控制范围大约在20~100 mA/cm2。在反应的过程中看到阴极周围有气泡产生,随着反应的进行,溶液的颜色逐渐变化,由无色到浅黄色,最后到灰绿色。反应一直在氮气保护下进行,反应持续了大约4个小时左右。反应结束后,用砂芯漏斗抽滤,抽滤后得到的溶液颜色是亮黄色的,用旋转蒸发仪在65℃下旋干,然后用水溶解,用二氯甲烷萃取,得到粒径大小均一的含氮碳量子点。
2 结果与讨论
2.1 含氮碳量子点的元素分析
表1给出了所合成的含氮碳量子点的元素分析结果,其元素含量为:C 53.03%,N 33.28%,H 5.44%,和O 8.25%(计算得出)。比较含氮碳量子点和原料乙二胺的元素分布可以看出含氮碳量子点的C/N比略高于乙二胺的C/N比,说明量子点中的部分碳元素可能来自于石墨电极。
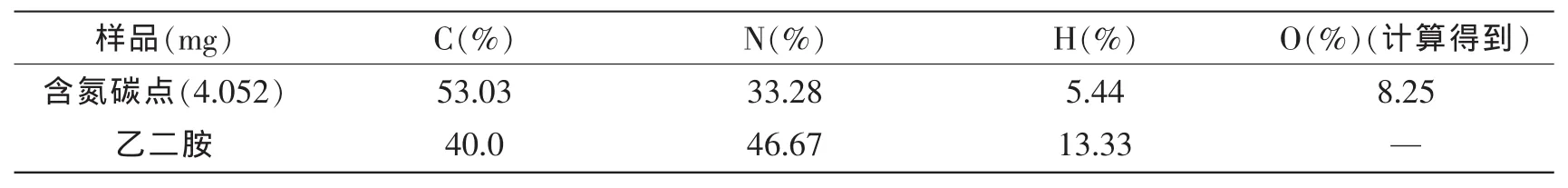
表1 含氮碳量子点的元素分析表Tab.1 Elemental analysis results of nitrogen-containing carbon quantum dots
2.2 含氮碳量子点的红外光谱
图1给出了分别以乙醇或乙二胺为原料制备含氮碳量子点的红外谱图。图1(a)中峰值在~1 666 cm-1显示的是C=O群的振动峰存在,在~3 405 cm-1则显示的是-OH峰,这些数据说明合成的碳量子点表面含有羧基(-COOH)与羟基(-OH)官能团。图1(b)显示含氮碳量子点的红外光谱,图中峰值出现在~3 423 cm-1处的伸缩振动峰为-NH的峰,在~1 475 cm-1的弯曲振动峰显示的是-NH的峰,由此说明合成的含氮碳量子点含有-NH键。
2.3 含氮碳量子点的透射电镜图
图2为含氮量子点的TEM图与HR-TEM,TEM结果显示制得的含氮碳量子点平均粒径约为5 nm左右,与以乙醇为原料制得的碳量子点的平均粒径相仿[17]
2.4 含氮碳量子点的紫外吸收光谱
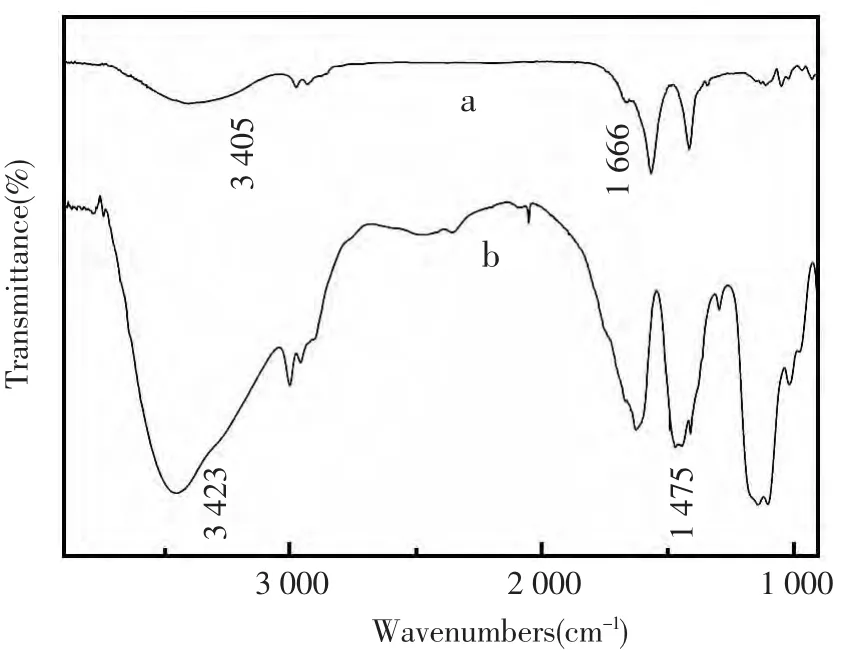
图1 (a)碳量子点,(b)含氮碳量子点的红外光谱图Fig.1 FTIR spectra of as-prepared CDs(a),(b)nitrogencontaining quantum dots
从图3含氮碳量子点的紫外吸收光谱图中,可以看出其紫外吸收光谱图(a线)与碳量子点(以乙醇为原料制备,b线)相似,在200~300 nm左右有吸收。
2.5 含氮碳量子点的单光子激发荧光光谱

图2 含氮量子点的TEM图与HR-TEM图Fig.2 TEM and HR-TEM images of the nitrogen-containing carbon quantum dots
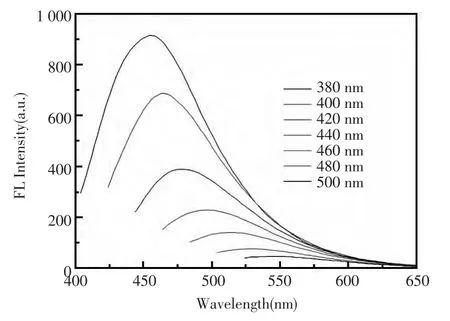
图4 含氮碳量子点的紫外吸收光谱Fig.4 One-photon luminescence spectra of the nitrogencontaining carbon quantum dots
图4为不同激发波长下(380 nm、400 nm、420 nm、440 nm、460 nm、480 nm、500 nm)含氮碳量子点的荧光光谱图。由图可知,在365 nm的紫外灯照射下,样品发出明显的蓝光,并且荧光强度很强。随着激发波长的增大,含氮碳量子点的发射光谱逐渐红移,这可能是由于含氮碳量子点粒子间的不同表面状态和不同粒径大小差异所造成的[25]。
2.6 含氮碳量子点在双光子激发下的荧光光谱
由图5可知,含氮碳量子点在双光子(λex=800 nm)激发下,在475 nm处有较强发射峰。这与其在400 nm光激发下的发射峰位置相近(图4),说明了含氮碳量子点也有双光子发射的能力。
2.7 溶液pH对含氮碳量子点荧光的影响
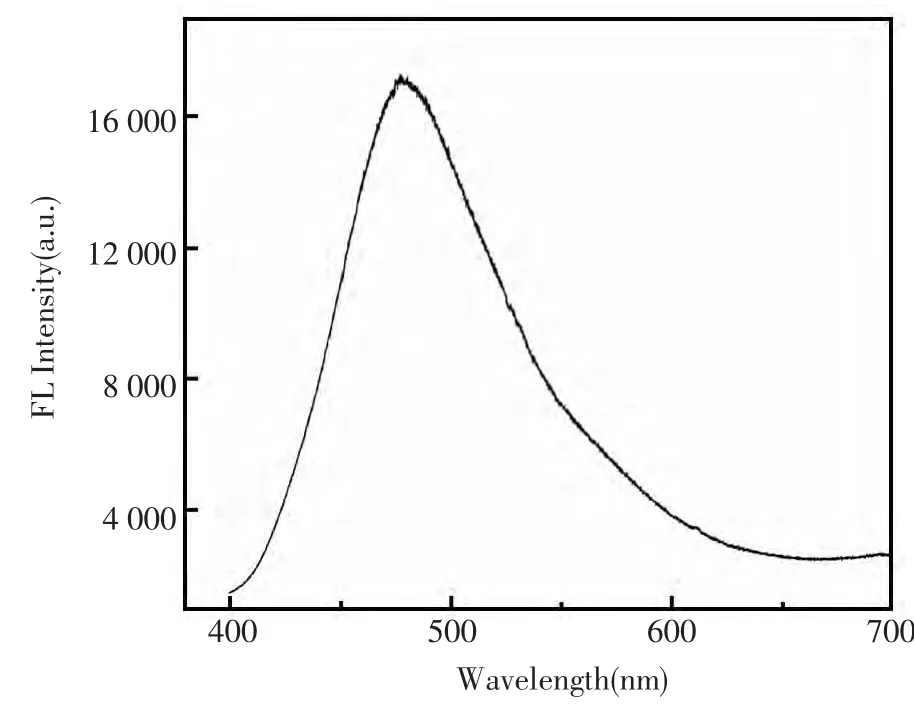
图5 含氮碳量子点在双光子激发条件下荧光发射光谱图Fig.5 Two-photon(800 nm excitation)luminescence spectra of the nitrogen-containing carbon quantum dots
实验测定了不同pH值的溶液中,功能化碳量子点在400 nm光激发下的荧光响应。图6可以看出,其荧光强度在pH值为3.0~9.0的范围内没有明显变化,说明其具有较好荧光稳定性。
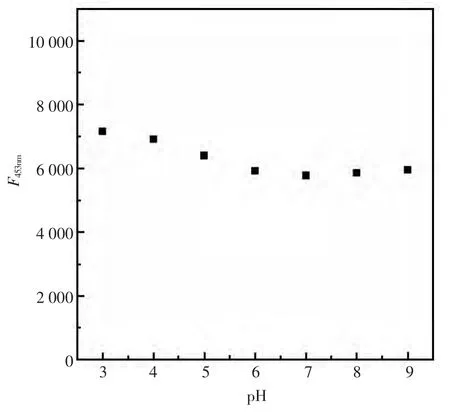
图6 含氮碳量子点在不同pH值条件下的荧光光谱图Fig.6 Fluorescent responses of nitrogen-containing carbon quantum dots(0.02 mg/mL)in PBS buffer with pH ranging from 3.0 to 9.0.Excitation wavelength:400 nm
2.8 铜离子对含氮碳量子点的荧光淬灭作用及其测定
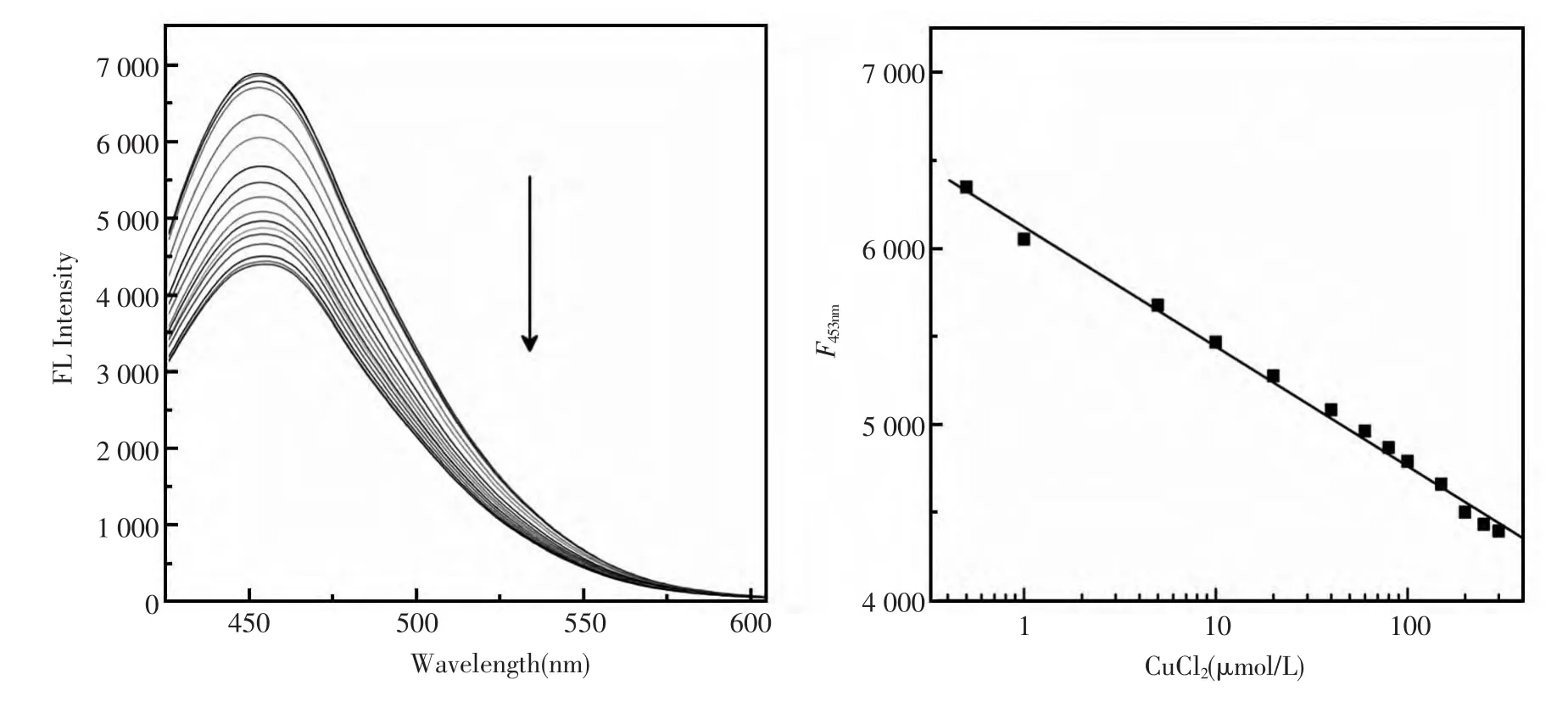
图7 不同铜离子浓度存在时含氮碳量子点的荧光发射光谱图Fig.7 Left One-photon fluorescence spectra of nitrogen-containing quantum dots(0.02 mg/mL)upon the addition of different concentrations of Cu2+ions(0~300 μmol/L)in PBS(pH7.4).Excitation wavelength:400 nm.Right Plot of fluorescence intensity changes at 453 nm of nitrogen-containing quantum dots with the addition of Cu2+
图7为含氮碳量子点对Cu2+离子浓度响应的荧光发射光谱图以及线性关系图。从图中可以看出,在激发波长为400 nm条件下,随着Cu2+离子浓度的增加,含氮碳量子点(0.02 mg/mL)荧光强度逐渐下降。在Cu2+离子浓度0.5~250 μmol/L范围内,453 nm处荧光发射峰强度与Cu2+离子浓度的对数呈良好的线性关系,当Cu2+离子浓度达到300 μmol/L后,体系荧光强度不再随Cu2+离子浓度的增加而减小。含氮碳量子点与铜离子反应后发生荧光猝灭机理,推测可能是由于其与铜离子络合后,将有利于激发电子转移,从而导致其荧光被猝灭。
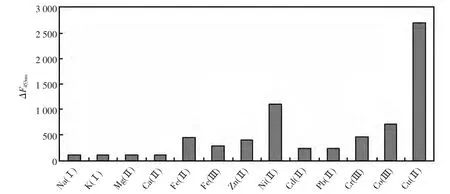
图8 不同金属离子对含氮碳量子点荧光强度的影响Fig.8 The influence of different metal ions on the fluorescent of nitrogen-containing carbon quantum dots
实验同时测定了其他常见金属离子对含氮碳量子点荧光强度的影响,结果如图8所示。其中含氮碳量子点浓度为0.02 mg/mL,加入的铜离子浓度为10 μmol/L,钠离子、钾离子浓度为铜离子的50倍,其他的金属离子(镁离子、钙离子,亚铁离子、铁离子、锌离子、镍离子、镉离子、铅离子、铬离子、钴离子)为铜离子浓度的10倍。结果显示除镍离子外,这些金属离子均不会对该实验产生明显的干扰,说明了含氮碳量子点对铜离子的检测具有较好的选择性。
3 结论
以乙二胺为原料,应用电化学方法成功合成了含氮碳量子点。该含氮碳量子点在pH=3~9的溶液中具有稳定的荧光响应,其他金属离子对其干扰很小,因而可用于溶液中微量铜离子浓度的荧光定量分析。
[1]Baker S N,Baker G A.Luminescent Carbon Nanodots:emergent Nanolights.[J].Angewandte Chemie,International Edition,2010,49(38):6 726~6 744,S6 721~S6 726.
[2]Tang B,Xing Y,Li P,et al.A Rhodamine-Based Fluorescent Probe Containing a Se-N Bond for Detecting Thiols and Its Application in Living Cells[J].Journal of the American ChemicalSociety,2007,129(38):11 666~11 667.
[3]Koide Y,Urano Y,Kenmoku S,et al.Design and Synthesis of Fluorescent Probes for Selective Detection of Highly Reactive Oxygen Species in Mitochondria of Living Cells[J].Journal of the American Chemical Society,2007,129(34):10 324~10 325.
[4]Qian H,Dong C,Weng J,et al.Facile one-pot synthesis of luminescent,water-soluble,and biocompatible glutathione-coated CdTe nanocrystals[J].Small,2006,2(6):747~751.
[5]Cao Y,Banin U.Growth and Properties of Semiconductor Core/Shell Nanocrystals with InAs Cores[J].Journal of the American Chemical Society,2000,122(40):9 692~9 702.
[6]Madhankumar A B,Slagle-Webb B,Mintz A,et al.Interleukin-13 receptor-targeted nanovesicles are a potential therapy for glioblastoma multiforme[J].Molecular Cancer Therapeutics,2006,5(12):3 162~3 169.
[7]Resch-Genger U,Grabolle M,Cavaliere-Jaricot S,et al.Quantum dots versus organic dyes as fluorescent labels[J].Nature Methods,2008,5(9):763~775.
[8]孙宝全,徐咏蓝,衣光舜,等.半导体纳米晶体的光致发光特性及在生物材料荧光标记中的应用[J].分析化学,2002,30(09):1 130~1 136.
[9]Yang S,Wang X,Wang H,et al.Carbon Dots as Nontoxic and High-Performance Fluorescence Imaging Agents[J].Journal of Physical Chemistry C,2009,113(42):18 110~18 114.
[10]Sun Y,Zhou B,Lin Y,et al.Quantum-Sized Carbon Dots for Bright and Colorful Photoluminescence[J].Journal of the American Chemical Society,2006,128(24):7 756~7 757.
[11]Sun Y,Wang X,Lu F,et al.Doped Carbon Nanoparticles as a New Platform for Highly Photoluminescent Dots[J].Journal of Physical Chemistry C,2008,112(47):18 295~18 298.
[12]Zhao Q,Zhang Z,Huang B,et al.Facile preparation of low cytotoxicity fluorescent carbon nanocrystals by electrooxidation of graphite[J].Chemical Communications(Cambridge,United Kingdom),2008,41:5 116~5 118.
[13]Cao L,Wang X,Meziani M J,et al.Carbon Dots for Multiphoton Bioimaging[J].Journal of the American Chemical Society,2007,129(37):11 318~11 319.
[14]Yang S,Cao L,Luo P G,et al.Carbon Dots for Optical Imaging in Vivo[J].Journal of the American Chemical Society,2009,131(32):11 308~11 309.
[15]Ray S C,Saha A,Jana N R,et al.Fluorescent Carbon Nanoparticles:Synthesis,Characterization,and Bioimaging Application[J].Journal of Physical Chemistry C,2009,113(43):18 546~18 551.
[16]齐宝平,龙艳敏,包蕾,等.电化学方法在荧光碳点研究中的应用[J].电化学,2011,17(03):271~277.
[17]Xu X,Ray R,Gu Y,et al.Electrophoretic Analysis and Purification of Fluorescent Single-Walled Carbon Nanotube Fragments[J].Journal of the American Chemical Society,2004,126(40):12 736~12 737.
[18]Li H,He X,Kang Z,et al.Water-soluble fluorescent carbon quantum dots and photocatalyst design[J].AngewandteChemie,InternationalEdition,2010,49(26):4 430~4 434,S4 430~S4 431.
[19]Zheng L,Chi Y,Dong Y,et al.Electrochemiluminescence of Water-Soluble Carbon Nanocrystals Released Electrochemically from Graphite[J].Journal of the American Chemical Society,2009,131(13):4 564~4 565.
[20]杜海军.石墨烯和荧光碳纳米颗粒的制备及其电化学特性的研究[D].华南理工大学,2010.
[21]Li H,Ming H,Liu Y,et al.Fluorescent carbon nanoparticles:electrochemical synthesis and their pH sensitive photoluminescence properties[J].New Journal of Chemistry,2011,35(11):2 666~2 670.
[22]Song Y,Shi W,Chen W,et al.Fluorescent carbon nanodots conjugated with folic acid for distinguishing folatereceptor-positive cancer cells from normal cells[J].Journal of Materials Chemistry,2012,22(25):12 568~12 573.
[23]Liu C,Zhang P,Tian F,et al.One-step synthesis of surface passivated carbon nanodots by microwave assisted pyrolysis for enhanced multicolor photoluminescence and bioimaging[J].Journal of Materials Chemistry,2011,21(35):13 163~13 167.
[24]Wang C,Wu X,Li X,et al.Upconversion fluorescent carbon nanodots enriched with nitrogen for light harvesting[J].Journal of Materials Chemistry,2012,22(31):15 522~15 525.
[25]Zhang P,Li W,Zhai X,et al.A facile and versatile approach to biocompatible“fluorescent polymers”from polymerizable carbon nanodots[J].Chemical Communications(Cambridge,United Kingdom),2012,48(84):10 431~10 433.
[26]Zhu S,Meng Q,Wang L,et al.Highly Photoluminescent Carbon Dots for Multicolor Patterning,Sensors,and Bioimaging[J].Angewandte Chemie,International Edition,2013,52(14):3 953~3 957.
- 化学传感器的其它文章
- 明胶纳米银的一锅式合成及其高效催化性能的研究

