慢性肾脏病肥胖患者低能量饮食对减重干预的Meta分析
王 宇 姜明霞 吴梦梦 郑锦锋
肥胖症是由多因素引起的体内脂肪堆积过多或分布异常,导致体重增加的一种慢性代谢性疾病。大量流行病学调查发现,肥胖增加包括慢性肾脏病(CKD)、终末期肾病(ESRD)、肾结石和肾癌等一系列肾脏疾病的发病风险。在美国超重和肥胖人群中,男女患肾脏疾病的概率分别为24.2%和33.9%,其他工业化国家超重及肥胖者中男女发病率也分别达到13.8%和24.9%[1]。肥胖不仅仅是CKD的危险因素,同时加重肾单位负担,加速肾功能衰竭的进程。Ejerblad等[2]观察发现,不同年龄段的男性肥胖者[体质量指数(BMI)≥ 30 kg/m2]和病理性肥胖症女性(BMI≥35 kg/m2)发生慢性肾衰竭的风险是正常人群(BMI<25 kg/m2)的3~4倍。此外,肥胖还增加肾移植失败的危险性[3]。进一步研究显示,BMI≥30 kg/m2肾脏疾病患者出现移植失败、死亡和心血管死亡率的相对危险性增加20%~40%,因此,很多移植中心将BMI≥35 kg/m2列为肾移植禁忌证[4]。近年来,在我国肥胖的发病率呈明显上升趋势,肥胖相关的肾脏病患者也越来越多,研究如何进行营养干预减重以改善患者的体重及肾脏功能具有十分重要的意义。本研究旨在进一步明确低能量饮食减重干预对CKD肥胖患者的影响。
资料与方法
文献检索策略文献主要通过计算机检索Medline、EMBase、PubMed、中国生物医学文献数据库和万方数据库获得。英文检索词:chronic kidney disease、obesity、weight loss、low caloric diet;中文检索词:慢性肾脏病、肥胖、减重、低能量饮食。文献检索年限为从建库至2014年1月。
文献筛选
文献纳入标准(1)文献的研究类型为已公开发表的随机对照临床试验或自身前后对照试验;(2)研究因素包括CKD肥胖患者的非手术干预减重;(3)超重或肥胖诊断符合WHO标准:BMI>25 kg/m2或BMI>30 kg/m2;(4)干预措施为低能量饮食干预,随访≥4周;(5)各文献结局指标为24h尿蛋白定量水平。
文献排除标准(1)不符合纳入标准的文献;(2)原始数据记录不完整;(3)排除重复发表的文献,排除综述、评论或讲座;(4)不能提供统计学内容的文献。
文献质量评价纳入文献采用纽卡斯尔-渥太华量表(NOS)进行质量评价,该标准包括病例组与对照组选择方法、病例组与对照组的可比性、接触暴露评价方法三方面,同时还包括其他的若干小项目,如病例的诊断以及定义是否恰当、病例的代表性和对照的定义等,评价结果用☆表示,最佳质量文献为10颗☆,至少5颗☆的文献可被纳入
Meta分析。
统计学方法采用stata 10.0进行分析,明确资料类型选择适当的效应指标,对计量资料进行一致性检验(卡方检验),存在同质性者(P>0.05)采用固定效应模型进行Meta分析,反之采用随机效应模型。
结 果
纳入文献的一般情况按照文献检索策略共检索到相关文献25篇,其中综述6篇、病例报告2篇、实验性研究8篇(动物实验1篇、随机对照试验4篇、非随机对照试验3篇)、观察性研究9篇(队列研究2篇,横断面调查7篇)。根据纳入和排除标准,文献筛选流程及结果见图1,最后筛选出3篇文献进行Meta分析[5-7]。共计样本量51例,其中第1项研究为自身前后对照试验,其余2项为随机对照试验(表1)。
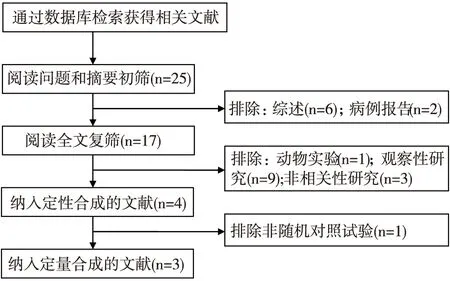
图1 文献筛选流程及结果
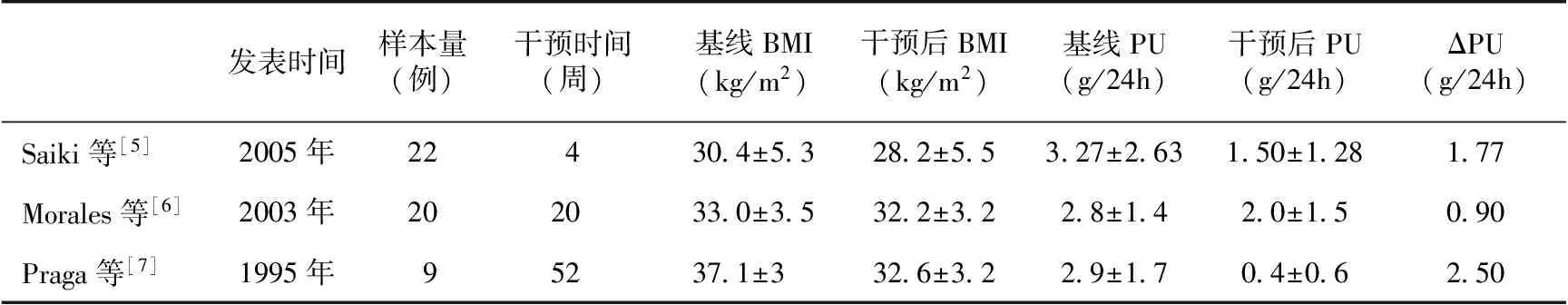
表1 低能量饮食与慢性肾脏病肥胖患者减重干预研究结果
纳入文献方法学质量评价结果纳入文献质量评价如下:对超重或肥胖的定义和诊断正确,病例具有较好的代表性,干预组和对照组具有可比性,干预组具有可靠的病史记录,但未采用盲法(☆),干预组和对照组干预方法不同(☆),总体评价为7颗☆,属于质量较高的文献,可纳入Meta分析。
低能量饮食与24h蛋白尿定量相关性的Meta分析结果
异质性检验各研究资料不存在异质性(χ2=4.46,P=0.108,自由度=2,I2=55.1%,P>0.05),存在同质性,故采用固定效应模型进行Meta分析。
Meta分析结果本次纳入的研究,均采用低能量饮食干预,收集干预组患者干预前后的24h尿液,分析尿蛋白分泌量的变化,结果显示体重下降能够减少患者的蛋白尿(图2)。
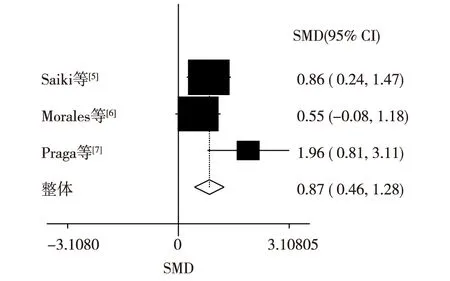
图2 低能量饮食与24h蛋白尿定量相关性Meta分析
讨 论
世界卫生组织预测到2015年全球大约有23亿成人超重,超过7亿人达到肥胖。越来越多的研究认为,质量过大与肾脏的结构性/功能性损伤密切相关。大部分肥胖相关的肾小球疾病患者都存在轻度肥胖、内脏脂肪肥胖、少量蛋白尿、残留的内生肌酐清除率和局灶节段性肾小球硬化症。与瘦的受试者相比,严重肥胖者肾小球滤过率(GFR)和肾脏血浆流量分别增高51%和31%[8]。微量白蛋白尿是CKD最早的标志物,病程可进展为明显的蛋白尿,它也是CKD发展为ESRD的提示物[9]。预防肾脏和心血管终末期疾病(PREVEND)的研究发现,体质量改变与蛋白尿的变化是平行的[10]。微量白蛋白尿(30~300 mg/d)在男性正常体重者中的发生率为9.5%,超重者增长到18.3%,而肥胖者为29.3%;不同体重女性微量白蛋白尿的发生率分别为6.6%、9.2%和16.0%[9]。进一步研究发现,体重降低和尿蛋白及微量白蛋白尿的减少呈正相关,当体重每下降1 kg,尿蛋白和微量白蛋白尿可分别减少110 mg和1.1 mg[11]。Ishizaka等[12]发现,既往存在微量/大量蛋白尿(≥30 mg/g·Cr)的男性,一年内腰围减少≥2.8 cm或BMI减少≥0.42 kg/m2,能够显著降低微量/大量蛋白尿的风险。此外,那些既往没有微量/大量蛋白尿或低eGFR[eGFR<60 ml/(min·1.73 m2)]的男性一年内BMI增长≥0.33 kg/m2,则出现微量/大量蛋白尿或低eGFR的危险性增加。
动物试验已经证实,对Zucker肥胖大鼠在生命早期(6或12周龄)进行饮食限制,是预防肾小球损伤最有力的干预方式[13]。很多临床研究和病例报告也显示通过能量限制进行的减重能够减少蛋白尿,原因是严重肥胖患者往往存在肾脏血液动力学异常,减重后肾脏血流量、GFR及白蛋白排泄率均有所改善[14]。常规以高膳食纤维、低能量和运动为基础的减重策略并不适合CKD患者,有关糖尿病肾病的饮食治疗则认为高能量、低蛋白饮食能够改善肾脏功能和蛋白尿,但是膳食蛋白摄入似乎不能完全解释肥胖相关的GFR和蛋白尿水平的变化[15]。在一项为期4周的进行低能量[11~19 kcal/(kg·d)]、正常蛋白质[0.9~1.2 g/(kg·d)]且含有部分补充剂的配方饮食的前瞻性研究中,干预结束后受试者体重平均下降6.2±3.0 kg,收缩压、血清肌酐(SCr)、血尿素氮(BUN)、尿蛋白和8-羟基脱氧鸟苷分别显著下降7.5±12.7 mmHg、41.6±23.9 μmol/L、1.50±1.61 mmol/L、1.8±1.7 g/d和3.1±3.6 ng/mg肌酐。没有受试者出现SCr和尿蛋白增加,且SCr和尿蛋白与体重及内脏脂肪面积呈正相关。上述结果提示采用低能量正常蛋白质饮食减重能够在短期内安全地改善肥胖的糖尿病肾病患者的肾功能和蛋白尿情况[5]。另一项研究随机分配(2∶ 1)30例超重(BMI>27 kg/m2)患或未患糖尿病的蛋白尿肾病患者,在5月内分别采用低能量正常蛋白质饮食或维持日常饮食,结果发现,低能量正常蛋白质饮食组患者体重和BMI显著下降,而对照组患者体重和BMI显著增加;低能量正常蛋白质饮食组患者蛋白尿减少31.2%±37%(24h尿蛋白定量从2.8±1.4 g/24h降至1.9±1.4 g/24h),对照组则呈增加趋势;低能量正常蛋白质饮食组肾脏功能保持稳定,而对照组显著恶化[6]。在国内63例肥胖相关的肾小球疾病患者在内科医生监督下,进行包含饮食和运动干预的减重项目6月后,其中27例患者体重下降8.29%±4.00%且蛋白尿平均减少35.3%,而24月后,27例患者BMI减少9.20%±3.78%,尿蛋白排泄减少51.33%,而血清三酰甘油、BUN和血压水平也呈现下降趋势。相反,BMI增长的患者尿蛋白增加28.78%。多变量回归分析显示BMI的改变是蛋白尿唯一的指示剂。该研究认为肥胖相关的肾小球疾病患者进行减重干预对减少蛋白尿是有益的,这种功能不能被传统的药物治疗所替代[16]。Cook等[17]的一项涉及低脂肪、低能量的膳食、个体化的运动处方及奥利司他药物治疗(120 mg,3次/d)综合多学科的体重管理项目的研究认为,CKD肥胖患者体重显著降低、运动功能得到改善后,可能允许这部分患者获得移植的概率更大,且与长期透析相比得到更高的生活质量[17]。上述CKD患者减重研究均认为,通过非手术干预获得的体重下降能够减少蛋白尿和血压,似乎还能预防进一步地肾功能减退。
本研究回顾分析了1990年1月至2014年1月有关低能量饮食干预CKD肥胖患者的文献,并提供了综合分析结果。Meta分析结果表明,进行低能量饮食干预后患者体重下降,24h尿蛋白排泄水平明显低于减重前。本研究采用系统评价的方法,综合同类研究结果,有效地增加了样本量,提高了检验效能,但也存在着不足之处。一方面选入的文献未进行发表偏倚评估,由于目前国内外单纯采用饮食干预CKD肥胖患者的研究极少,因此本文纳入的研究数量少、样本量不足;另一方面本研究只进行了干预组患者24h尿蛋白水平分析,由于纳入的3项研究中第一项为自身前后对照设计,而后两项为随机对照试验,鉴于第一项研究缺少对照组数据,不利用文献的综合分析,因此只进行了采用低能量饮食干预的患者减重前后的24h尿蛋白水平分析。尽管采用自身前后对照设计在治疗效果外推上存在一定的局限性,但根据目前的研究现状[18],故认为低能量正常蛋白质的饮食减重干预有益于CKD肥胖患者的症状改善。
1Wang Y,Chen X,Song Y,et al.Association between obesity and kidney disease:a systematic review and meta-analysis.Kidney Int,2008,73(1):19-33.
2Ejerblad E,Fored CM,Lindblad P,et al.Obesity and risk for chronic renal failure.J Am Soc Nephrol,2006,17(6):1695-1702.
3Wolf G.After all those fat years:renal consequences of obesity.Nephrol Dial Transplant,2003,18(12):2471-2474.
4Meier-Kriesche HU,Arndorfer JA,Kaplan B.The impact of body mass index on renal transplant outcomes:a significant independent risk factor for graft failure and patient death.Transplantation,2002,73(1):70-74.
5Saiki A,Nagayama D,Ohhira M,et al.Effect of weight loss using formula diet on renal function in obese patients with diabetic nephropathy.Int J Obes (Lond),2005,29(9):1115-1120.
6Morales E,Valero MA,León M,et al.Beneficial effects of weight loss in overweight patients with chronic proteinuric nephropathies.Am J Kidney Dis,2003,41(2):319-327.
7Praga M,Hernández E,Andrés A,et al.Effects of body-weight loss and captopril treatment on proteinuria associated with obesity.Nephron,1995,70(1):35-41.
8Chagnac A,Weinstein T,Korzets A,et al.Glomerular hemodynamic in severe obesity.Am J Physiol Renal Physiol,2000,278(5):F817-F822.
9de Jong PE,Verhave JC,Pinto-Sietsma SJ et al.Obesity and target organ damage:the kidney.Int J Obes Relat Metab Disord,2002,26(Suppl 4):S21-S24.
10 Bello AK,de Zeeuw D,El Nahas M,et al.Impact of weight change on albuminuria in the general population.Nephrol Dial Transplant,2007,22(6):1619-1627.
11 Afshinnia F,Wilt TJ,Duval S,et al.Weight loss and proteinuria:systematic review of clinical trials and comparative cohorts.Nephrol Dial Transplant,2010,25(4):1173-1183.
12 Ishizaka Y,Ishizaka N,Tani M,et al.Association between changes in obesity parameters and incidence of chronic kidney disease in Japanese individuals.Kidney Blood Press Res,2009,32(2):141-149.
13 Maddox DA,Alavi FK,Santella RN,et al.Prevention of obesity-linked renal disease:age-dependent effects of dietary food restriction.Kidney Int,2002,62(1):208-219.
14 Chagnac A,Weinstein T,Herman M,et al.The effects of weight loss on renal function in patients with severe obesity.J Am Soc Nephrol,2003,14(6):1480-1486.
15 Friedman AN,Yu Z,Juliar BE,et al.Independent influence of dietary protein on markers of kidney function and disease in obesity.Kidney Int,2010,78(7):693-697.
16 Shen WW,Chen HM,Chen H,et al.Obesity-related glomerulopathy:body mass index and proteinuria.Clin J Am Soc Nephrol,2010,5(8):1401-1409.
17 Cook SA,MacLaughlin H,Macdougall IC.A structured weight management programme can achieve improved functional ability and significant weight loss in obese patients with chronic kidney disease.Nephrol Dial Transplant,2008,23(1):263-268.
18 Navaneethan SD,Yehnert H,Moustarah F,et al.Weight loss interventions in chronic kidney disease:a systematic review and meta-analysis.Clin J Am Soc Nephrol,2009,4(10):1565-1574.

