等离子体引发CeO2低温催化活性协同脱除空气中苯
丁慧贤,赵宇杰,张增凤
(1.黑龙江科技大学环境与化工学院,哈尔滨150022;2.大庆油田有限责任公司第六采油厂试验大队,黑龙江大庆163000)
0 引言
苯是室内空气主要挥发性有机污染物(VOCs)之一,主要来源于装饰、建筑等材料中大量使用的化工原料,如涂料、墙面漆等[1]。苯对人体的伤害非常大,世界卫生组织已确定苯为致畸致癌物质[2-4]。脱除室内空气中污染物苯的研究意义重大。
室内空气污染物具有浓度低、释放期漫长(可长达几年)以及处理量大的特点,给室内空气的净化带来了巨大困难。较为理想方法应该同时具备能耗低、无二次污染物、脱除率高、空速大等特点。常规空气净化方法,如催化氧化法、等离子体法、吸附法、光催化氧化法等,存在能耗高、脱除效率低、产生二次污染等难以解决的问题[5-7]。
近些年发展起来的等离子体与催化剂相结合技术将空气净化技术向前推进了一步,成为该领域的研究热点[8-10]。李党生等[11]给出了等离子体-催化脱除苯的实验结果,当输入能量密度为1 200 J/L时,单纯等离子体脱除甲苯的脱除率为58%,而等离子体与催化剂相结合在同样的条件下苯的脱除率为92%,比单独催化或等离子体脱除苯的脱除率提高很大,同时能耗也大幅下降。Li Jing等[12]发现在等离子体放电区填充Pt/γ-Al2O3催化剂要比填充γ-Al2O3吸附剂脱除苯的脱除率提高20%,同时CO降低50%,脱除单分子苯能耗降低57%。Kim等[13]开展了循环“存储-放电”等离子体-催化脱除VOCs的研究。该方法是将低浓度的VOCs在催化剂上先吸附存储,然后放电脱除,从而降低了能耗。Chavadej等[14]发现,在等离子体放电区添加TiO2催化剂使气相中苯的脱除率由81%提高至91%。这些研究成果可为后续研究提供借鉴,但研究仍然不够完善,或多或少存在能耗高、脱除效率低、产生二次污染等方面的问题。
笔者在前期等离子体与催化结合净化空气的研究工作中发现[15-16],等离子体与催化结合之所以能够提高净化空气的效率,是因为二者之间产生了协同效应,等离子体所产生的活性物种起到了至关重要的作用。为进一步强化协同效应,提高脱除效率,笔者从改变水量、增加活性物种等方面进行了初步研究。
1 实验
1.1 实验装置
实验用介质阻挡放电反应器的结构及实验条件与笔者前期研究工作所采用的相同[8-10],如图1所示。石英管(内径10 mm,厚度1 mm)中心为一直径2 mm的不锈钢管,与交流高压电源输出端相连。管外紧密缠绕宽为30 mm的不锈钢网,且与交流高压电源的接地端相连。放电区体积为2.2 mL,催化剂填充于等离子体放电区域内。首先通入已知组成和质量流量的原料气,当反应器出口浓度等于入口浓度c0时,系统达到稳定状态,开始放电。放电过程要持续一定时间以保证系统达到新的稳定状态。
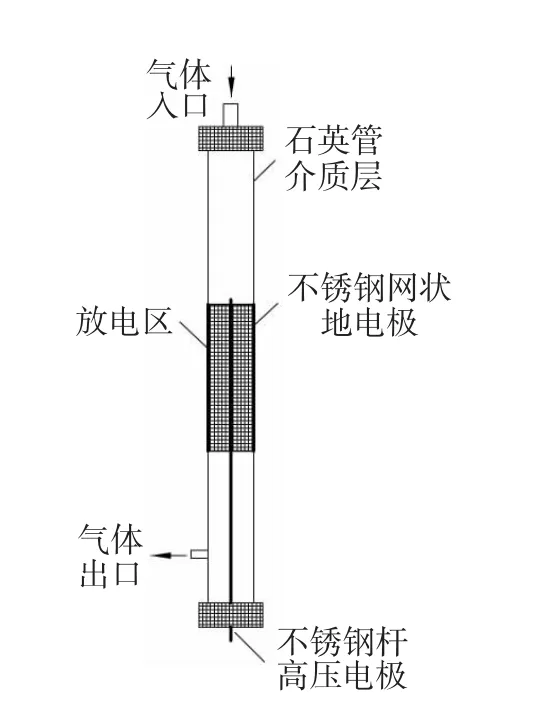
图1 介质阻挡放电反应器Fig.1 Structure of dielectric barrier discharge reactor
采用气相色谱(3420A,北分)在线检测原料气和反应后气体中苯的浓度,使用氢火焰离子检测器、Porapak T色谱柱。如果出口浓度设为cex,则苯的脱除率:
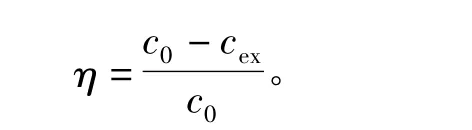
1.2 催化剂的制备
采用溶胶-凝胶法制备CeO2催化剂[8-10]。按照1∶3的化学计量称取一定量的硝酸铈和柠檬酸,用蒸馏水溶解后,置于水浴槽中保持80℃,形成溶胶,恒温脱水成半干燥凝胶。置于110℃干燥箱中干燥,得到体积膨胀的干凝胶,研磨后,于马弗炉中500℃下焙烧,得黄色CeO2粉末。将其压片、研磨、过筛,取颗粒粒径在425~850 μm的CeO2作为催化剂使用。
2 结果与讨论
2.1 水量的影响
将如前制作的体积为2.2 mL、粒径为425~850 μm的CeO2催化剂装入反应器的放电区,控制反应器温度为35℃。原料气苯的体积分数为102×10-6,空气为平衡气,空速为13 650 h-1(气体流量为500 mL/min),放电电压为18 kV。改变原料气中水的分数,考察其对苯脱除率的影响,结果如图2所示。
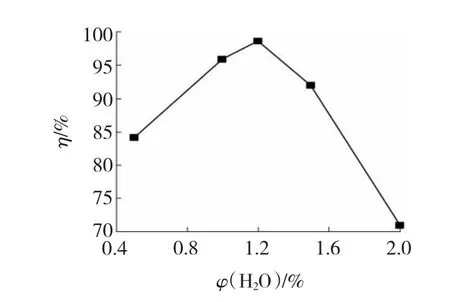
图2 水的体积分数对苯脱除率的影响Fig.2 Influence of moisture content on removal efficiency of benzene
苯的脱除率随水量增加呈先上升后下降的趋势。H2O分子在富能电子的作用下,生成OH·及H·自由基[8-10],OH·自由基可以促进苯的降解和氧化[17]。当水体积分数由0.5%增加至1.0%时,苯的脱除率快速增加至96.0%,说明可以通过增加水量的方式增加OH·自由基,从而提高脱除苯的脱除率。但如果水量继续增加,水的副作用开始显现,因为水的加入不利于放电,水分子易于同放电产生的电子发生解离附着反应(,生成O-、H-和OH-离子,消耗许多能量为6~7.5 eV的电子[18],造成由富能电子碰撞而产生的自由基数量减少。同时,苯分子受富能电子碰撞而分解的几率减小,因而当水的体积分数继续增加至2.0%时,苯的脱除率快速降至71.0%[8-10]。
2.2 放电电压的影响
实验条件不变,H2O的体积分数为1.2%。当放电电压由10 kV增加至16 kV时,苯脱除率由41.0%快速增加至94.4%;当放电电压继续增加至18 kV时,苯的脱除率由94.4%缓慢增加至98.7%(如图3所示)。
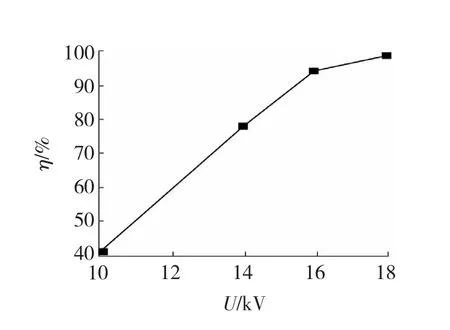
图3 放电电压对苯脱除率的影响Fig.3 Influence of discharge voltage on removal efficiency of benzene
在大气压条件下,介质阻挡放电通常以丝状放电形式存在。放电中具有一定能量的电子与放电气体分子或原子碰撞,产生离子、激发态成分、原子和其他分子碎片等活性成分[19]。增加放电电压使输入的放电能量密度增加,可产生更多富能电子。这些富能电子可将苯分子以及水分子等击碎而产生自由基碎片,并进一步发生系列自由基反应[16],有利于苯脱除。苯分子在等离子体放电区域受到自由基等活性物种的轰击几率也增大,促进了各种活性物种与吸附态苯反应,同时,富能电子和活性自由基与催化剂作用,发生氧化-还原反应,使吸附在催化剂表面上的苯氧化而脱除[8-10]。因此,增大放电电压使苯的脱除率增加。
2.3 初始浓度的影响
实验条件不变[8-10],将CeO2催化剂放入反应器的放电区,放电电压维持在18 kV,空速为13 650 h-1,改变原料气中苯的初始体积分数,考察不同初始体积分数对苯脱除率的影响,如图4。
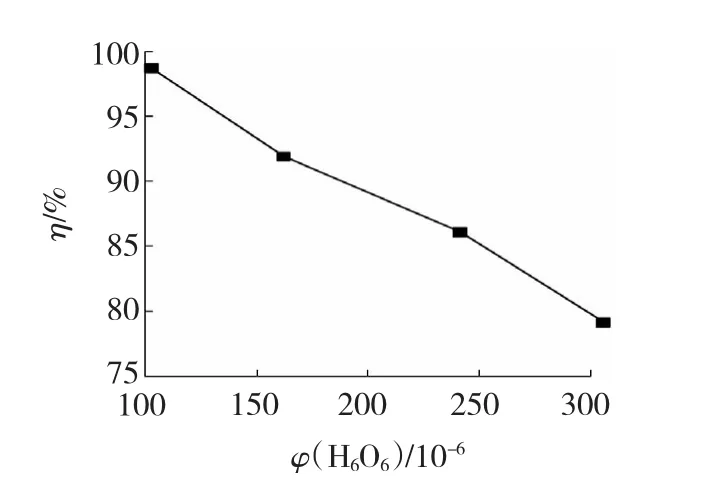
图4 苯体积分数对苯脱除率的影响Fig.4 Influence of concentration on removal efficiency of benzene
结果表明,苯脱除率随着苯初始体积分数的增加而降低。当苯的体积分数为102×10-6时,脱除率为98.7%;当体积分数为242×10-6时,脱除率降为86.0%,而当苯的体积分数为308×10-6时,脱除率继续下降到79.0%。在空速一定、放电电压不变的情况下,随着苯的初始体积分数的增加,苯的转化率逐渐降低。这表明放电电压一定时,由放电产生的自由基等活性物种数量是一定的,输入反应器中苯的初始体积分数增大,意味着每个苯分子与这些活性粒子碰撞而发生有效化学反应的几率相对减少,导致苯的脱除率降低。
2.4 协同效应的影响
以CeO2作为催化剂,保持放电电压为18 kV,空速为13 650 h-1,苯的初始体积分数为102×10-6不变,其他实验条件同前。分别考察单纯催化、单纯等离子体、等离子体与催化剂结合对苯的脱除率的影响,结果如图5所示。
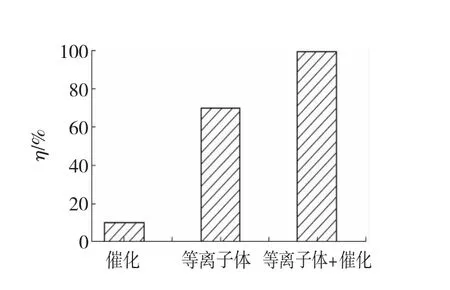
图5 单纯催化剂、单纯等离子体、等离子体与催化剂结合时苯的脱除率Fig.5 Bar diagram showing benzene conversion percentages,produced from plasma-catalysis and plasma only as well as CeO2catalysis
在浓度、电压与空速一定的情况下,采用单纯等离子体时,苯的脱除率为69.5%,在单纯催化时,苯的脱除率为10.0%。而等离子体与催化结合时,苯的脱除率为98.7%,脱除率明显大于纯等离子体放电和纯CeO2催化氧化脱除苯的脱除率两者之和。这表明等离子体与CeO2催化剂结合脱除苯不是纯等离子体放电脱除苯和纯CeO2催化氧化脱除苯二者简单的加和,而是等离子体与CeO2催化剂结合在脱除苯的过程中产生了强烈的协同效应。
2.5 等离子体与CeO2的催化协同效应机理
CeO2在高温时是良好的氧化催化剂,而常温下活性很低。CeO2催化剂在介质阻挡放电等离子体中催化氧化C6H6时表现活性很高,表明等离子体引发了CeO2催化剂低温催化活性,应该是等离子体放电产生的O或HO自由基与催化剂之间产生了强烈作用,促进催化剂完成氧化-还原循环,使C6H6氧化。在等离子体放电产生的富能电子作用下,CeO2释放出一个O自由基将苯氧化,等离子体放电产生的O或HO自由基再将Ce2O3氧化成CeO2完成一个氧化还原循环过程。
3 结论
(1)在等离子体作用下,水量对苯脱除率的影响是双重的。在一定范围内(0.5%~1.2%),水量的增加,会使OH·活性自由基增加,从而促进苯的脱除,提高苯的脱除率。但是,水量过多(超过1.2%),水会加速等离子体中富能电子淬灭,造成由富能电子碰撞而产生的活性自由基数量减少,导致苯的脱除率快速下降。
(2)介质阻挡放电等离子体与CeO2催化剂相结合,能够对空气中苯污染物进行有效脱除。苯的脱除率随着放电电压的增大而增大,随着苯初始体积分数的增加而降低。水量增加,苯的脱除率先升高后下降。在放电电压为18 kV、苯的体积分数为102×10-6、空速为13 650 h-1的情况下,苯的脱除率达98.7%。
(3)介质阻挡放电等离子体与催化剂CeO2结合在脱除空气中的苯污染物过程中产生了显著的协同效应。等离子体放电过程中产生活性物种(O、OH自由基)能够与CeO2催化剂作用,从而引发CeO2催化剂低温催化活性,在催化氧化苯的过程中实现Ce2O3-CeO2之间的氧化-还原转化循环过程。
[1] 许全民,周大勇,周绍宏,等.室内环境污染及其控制[J].广东化工,2013,40(3):113,119.
[2] 陈红新.室内空气环境污染物种类及监测方法[J].广东化工,2013,40(9):125-126.
[3] 李文俊.谈室内空气污染与检测[J].企业科技与发展,2013(17):31-33.
[4] 张玲.室内空气主要污染物的危害及其防治措施[J].安徽建筑,2012(4):190-191.
[5] LARSEN E S,PILAT M J.Design and testing of a moving bed VOC adsorption system[J].Environmental Progress,2007,10(1):75-82.
[6] CHEN H L,LEE H M,CHEN S H,et al.Removal of volatile organic compounds by single-stage and two-stage plasma catalysis systems:a review of the performance enhancement mechanisms,current status,and suitable applications[J].Environ Sci Technol,2009,43(7):2216-2227.
[7] TIAN HUA,HE JUNHUI.An advance in complete oxidation of formaldehyde at low temperatures[J].Science Foundation in China,2009,17(2):36-38.
[8] 丁慧贤.大气压下等离子体与催化协同低温脱除气相中甲醛研究[D].大连:大连理工大学,2008.
[9] 丁慧贤,张增凤,徐占春.常温常压下等离子体催化脱除空气中的苯[J].黑龙江科技学院学报,2012,22(1):9-13.
[10] 丁慧贤.低温等离子体与催化剂氧化脱除甲醛的研究[J].福建工程学院学报,2012,10(1):60-64
[11] 李党生,冯涛,姚水良.低温等离子体与催化剂联用降解空气中低浓度的苯[J].科学与技术,2007,30(10):65-66.
[12] LI JING,HAN SHITONG,BAI SHUPEI,et al.Effect of Pt/γ-Al2O3catalyst on nonthermal plasma decomposition of benzene and byproducts[J].Environmental Engineering Science,2011,28(6):395-403.
[13] KIM H H,OGATA A,FUTAMURA S.Oxygen partial pressuredependent behavior of various catalysts for the total oxidation of VOCs using cycled system of adsorption and oxygen plasma[J].Applied Catalysis B:Environmental,2008,79(4):356-367.
[14] CHAVADEJ S,KIATUBOLPAIBOON W,RANGSUNVIGIT P,et al.A combined multistage corona discharge and catalytic system for gaseous benzene removal[J].J Mol Catal A Chem,2007,263(1/2):128-136.
[15] DING HUIXIAN,ZHU AIMIN,YANG XUEFENG,et al.Removal of formaldehyde from gas streams via packed-bed dielectric barrier discharge plasmas[J].Journal of Physics D:Applied Physics,2005,38(23):4160-4167.
[16] DING HUIXIAN,ZHU AIMIN,LU FUGONG,et al.Low-ternperature plasma-catalytic oxidation of formaldehyde in atmospheric pressure gas streams[J].Journal of Physics D:Applied Physics,2006,39(16):3603-3608.
[17] 蒋洁敏,吴玉萍,侯惠奇.氧化铂对DBD处理含苯废气的影响研究[J].化学世界,2002(S1):89-90.
[18] MELTON C E.Cross sections and interpretation of dissociative attachment reactions producing OH-,O-,and H-in H2O[J].J Chem Phys,1972,57(10):4218-4225.
[19] ELIASSON B,KOGELSCHATZ U.Modeling and applications of silent discharge plasmas[J].IEEE Trans Plasma Sci,1991,19(2):309-323.

