星点设计-效应面法在阿魏酸哌嗪脉冲释药片处方优化中的应用
王 乐,陈 晶,薛 娜,边虹铮,杨 欣
(河北化工医药职业技术学院制药工程系,河北 石家庄 050026)
口服脉冲给药系统适用于支气管哮喘、心血管疾病、关节僵硬等具有昼夜节律性疾病,服用后可经过预定时滞后在疾病治疗所需时间释放药物,提高患者用药的顺应性和药效,减少不良反应[1-4]。星点设计是近年来药学工作者采用较多的优化方法,与传统的正交等设计法相比,具有方法简便、拟合数据预测性好等优点[5-7]。阿魏酸哌嗪(piperazine ferulate),3-甲氧基-4-羟基桂皮酸哌嗪,系从川芎中提取分离出的阿魏酸与哌嗪成盐得到的,临床上可用于脑梗死、冠心病等心血管疾病的治疗[8]。本文以阿魏酸哌嗪为模型药物,采用薄膜包衣技术制备脉冲释药片,通过星点设计-效应面法优化其处方,实现在疾病发作的最佳时间释放药物。
1 材料与方法
1.1 材料:阿魏酸哌嗪(武汉银河化工有限公司,批号090801,纯度99.1%),微晶纤维素(德国JRS公司),乳糖(德国Meggle公司),羧甲基淀粉钠(sodium carboxymethyl starch,CMS-Na,台湾永日化学工业股份有限公司),聚乙烯吡咯烷酮(polyvinglpyrrolidone,PVP K30,美国ISP公司),乙基纤维素(ethyl cellulose,EC 10cp,泰安瑞泰纤维素公司),柠檬酸三乙酯(triethyl citrate,TEC,蚌埠丰原医药科技公司),PEG6000(上海高南化工厂)。
1.2 仪器:薄膜包衣设备(自制);D-800型智能溶出试验仪(天津大学无线电厂);UV-2450紫外可见分光光度计(日本岛津);TDP 单冲式压片机(上海第一制药机械厂)。
1.3 方法
1.3.1 脉冲释药片的制备
1.3.1.1 片芯的制备:将阿魏酸哌嗪与乳糖、微晶纤维素、羧甲基淀粉钠等按处方比例混合均匀,用10%PVP K30的95%乙醇溶液作为黏合剂制备软材,过18目筛制粒,55℃干燥2h,过18目筛整粒,加入1%硬脂酸镁,混匀后压制成硬度为6kg、每片含阿魏酸哌嗪100mg,片质量为250mg。
1.3.1.2 包衣片的制备:使用80%乙醇将EC溶解后配成浓度为5%的溶液,并加入少量PEG6000、滑石粉和TEC。包衣液中各成分含量如下,EC为5%,PEG6000为6%(按EC用量计),滑石粉25%(按EC用量计),TEC为10%(按EC用量计)。包衣过程中,包衣锅转速为20r/min,包衣液流速3mL/min,片床温度控制在39~41℃,进风温度为62~64℃,出风温度为30~32℃。
1.3.2 体外释放度的测定方法
1.3.2.1 标准曲线的建立:精密称取阿魏酸哌嗪,用新鲜脱气纯化水为介质,配制浓度分别为0.001 2、0.002 4、0.003 6、0.004 8、0.006 0、0.007 2g/L的溶液,在310nm处测定吸收度,经线性回归后标准曲线为A=100.29C+0.021,r=0.999 8,表明吸收度与浓度之间线性关系良好。
1.3.2.2 体外释放度测定:取脉冲释药片照中国药典2010年版附录XC第一法操作[9],以1 000mL新鲜脱气纯化水为溶出介质,温度为(37.0±0.5)℃,转速为50r/min。于规定时间取样后经0.45μm微孔滤膜滤过,取续滤液经稀释后在310nm波长处测定吸收度,计算药物累积释放度。以药物累积释放度达到10%的时间作为药物释放的时滞。
2 结 果
2.1 星点设计:在预实验的基础[10]上,采用星点设计对片芯中CMS-Na用量(X1,mg)和包衣层厚度(X2,%)进行2因素5水平的优化,见表1。按照所设计的处方制备脉冲释药片并测定体外释放度,以释药时滞作为考察指标,实验设计及结果见表2。

表1 星点设计的考察因素水平及实际物理量Table 1 Levels of independent variables and their physical forms
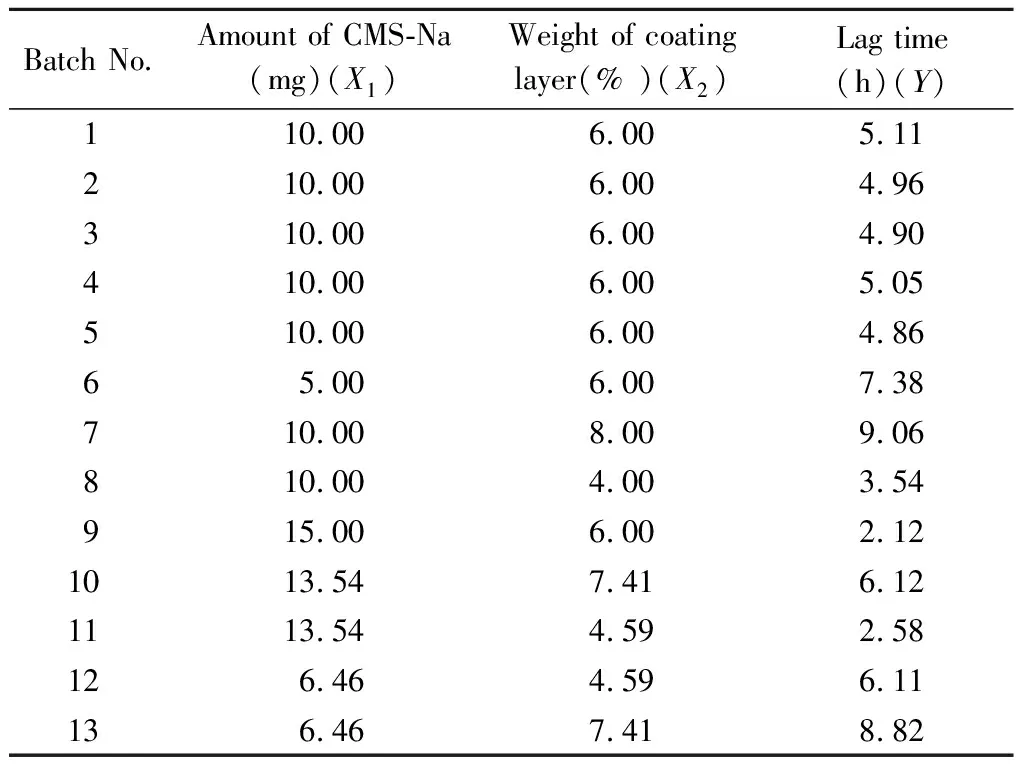
表2 实验设计及结果Table 2 Experimental design and results
2.2 方程拟合:采用Design Expert 7.1软件,以释药时滞为因变量Y,CMS-Na用量、包衣层厚度为因变量X1、X2分别进行多元线性回归和二次多项式回归。拟合后的多元线性方程为Y=2.810-0.483X1+1.242X2(r=0.951 0,P<0.000 1);二次多项式方程为Y=18.342-0.704X1-3.718X2-0.001X12+0.379X22+0.042X1X2(r=0.992 2,P<0.000 1)。二次多项式由于拟合系数更高,因此更适合对本实验进行优化分析。
3.3 处方优化及预测性评价:采用Design Expert 7.1软件,对上述拟合的二次多项式绘制二维等高线图和三维效应面图,结果见图1,2。

图1 释药时滞与CMS-Na用量、包衣层厚度的二维等高线图
Figure1Two-dimensionalcontoursmapsoflagtimeinvitrowithamountofsodiumcarboxymethylstarchandweightofcoatinglayer
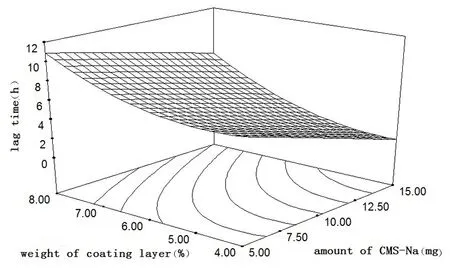
图2 释药时滞与CMS-Na用量、包衣层厚度的三维效应面图
Figure2Three-dimensionalresponsesurfaceoflagtimeinvitrowithamountofsodiumcarboxymethylstarchandweightofcoatinglayer
考虑到阿魏酸哌嗪脉冲释药片用来治疗心脑血管疾病,而此类疾病发作具有昼夜节律性,在凌晨发作频率较高,因此控制脉冲释药片在口服5~6h后释放药物可更好的发挥药物的疗效。为考察拟合后的二次多项式对试验结果预测的准确性,在图1时滞为5~6h的优选区域内选择4个处方点,分别为处方1-X1为7,X2为5;处方2-1为9,X2为6;处方3-X1为11,X2为6.5;处方4-X1为13,X2为7。每个处方均制备三批样品,分别测定其体外释放时滞,并以偏差表示预测时滞与实测时滞的偏离程度,结果见表3。偏差=[预测时滞-实测时滞)/预测时滞]×100%。


Batch No.Predicted lag time(h)Observed lag time(h) Bias(%)15.725.62±0.11-2.00±1.2225.535.48±0.15-3.20±3.6235.335.30±0.1-0.57±3.4545.395.48±0.122.03±1.55
由结果可知,所选4个处方实测时滞与预测时滞的偏差在±3.2%以内,说明本文拟合的二次多项式方程可较好的描述因变量与自变量之间的关系,预测性良好。
3 讨 论
本实验采用优良性能的崩解剂及水不溶性包衣材料制备了阿魏酸哌嗪脉冲释药片。脉冲片经口服后,水分会通过包衣层中致孔剂形成的孔道逐渐渗透进入片芯,使片芯内崩解剂膨胀,直至将包衣层胀破,释放药物。在预实验的基础上,本文通过星点设计安排实验并对实验结果进行了数学方程的拟合,在优选处方范围内预测时滞与实测预测时滞接近,表明该方程对实验结果具有较好的预测性,可用于阿魏酸哌嗪脉冲释药片处方的优化。
[1] 孟建强,任麒,刘丽媛.时辰药理学与多次脉冲给药的应用[J].中国新药与临床杂志,2010,29(8):576-580.
[2] 周闺臣,邹豪,钟延强.三种自身触发的脉冲给药系统[J].第二军医大学学报,2010,31(7):782-786.
[3] 纪立伟,潘振华,陈桂兰.口服脉冲式药物输送系统及国内研究进展[J].河北医科大学学报,2001,22(5):313-315.
[5] 吴伟,崔光华.星点设计-效应面优化法及其在药学中的应用[J].中草药,2000,27(5):292-298.
[6] 刘艳杰,项荣武.星点设计效应面法在药学试验设计中的应用[J].中国现代应用药学,2007,24(6):455-457.
[7] 王利胜,程龙,吴阳,等.星点设计-效应面法优化盐酸普罗帕酮缓释片处方[J].中国现代应用药学,2012,29(11):998-1001.
[8] 郭玉麟,钟三宝.阿魏酸哌嗪的合成及其药理与临床研究[J].华西药学杂志,1987,2(1):52-54.
[9] 国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:附录85-86.
[10] 王乐,陈晶,边虹铮.阿魏酸哌嗪脉冲释药片的制备及其体外释药影响因素考察[J].中国现代应用药学,2012,29(4):342-345.

