高效氟苯尼考粉剂研究
刘怀珠,张建平,胡海英,赵清斌,张正全
(1.郑州大学药学院,河南 郑州450001;2.上海邦森生物科技有限公司,上海 奉贤201422)
氟苯尼考(Florfenicol),是一种新型兽医专用广谱抗菌药,具有抗菌后效应显著、无潜在致再生障碍性贫血作用等特点。2010年版《中国兽药典》已收载氟苯尼考粉剂、注射剂、溶液剂等。据报道,不同厂家的氟苯尼考产品在使用中也存在显著差异,所以目前国内重点研究了氟苯尼考快速溶出制剂,如氟苯尼考包合物研究[1]、氟苯尼考纳米乳研究[2]等。但其固体口服给药疗效仍差于国外同类产品,鉴于此,课题组已对氟苯尼考的溶解度行为、脂水分配系数[3]及其在体生物吸收行为进行了研究[4],结果显示、氟苯尼考溶解度低(1.2mg/mL)、脂水分布系数P在2.5左右,本应有利于药物的吸收[5],但药物吸收速度却较慢,2 h仅吸收17.875%[4]。因此,本试验拟采用无定形技术和药物吸收促进技术,提高氟苯尼考在水中的溶解度和通过生物膜的速度,以保证药物能够快速溶出和吸收。
1 材料与方法
1.1 试验材料 氟苯尼考原料药(湖北龙翔药业有限公司,含量99.9%,批号∶101152)、国外产品对照(批号:RKPB1575)、甲醇(色谱纯)、吐温-80(化学纯)、淀粉(药用),其余试剂均为分析纯。
1.2 试验仪器 Angilent-1200高效液相色谱仪(美国安捷伦公司);AKasil C18色谱柱(Agela Tech⁃nologies)、RC-6溶出度测试仪(天津市光学仪器厂);BUCHIB-290微型喷雾干燥器(瑞士,BUCHI公司)。
1.3 试验动物 普通级昆明系小鼠,体重18~22 g,河南省实验动物中心,合格证号:410118;清洁级健康大鼠,体重200±10 g,郑州大学实验动物中心,合格证号:SCXK(豫)2012-0002。
1.4 氟苯尼考含量测定方法[4]采用高效液相色谱法,在波长为224 nm处进行氟苯尼考的含量测定,结果应符合含量测定要求。
1.5 氟苯尼考高效粉剂处方优化试验
1.5.1 氟苯尼考吸收促进剂的筛选 将适量氟苯尼考原药用水溶解并稀释成0.1mg/mL的氟苯尼考水溶液,分别加入吸收促进剂乙二胺四乙酸二钠盐、十二烷基硫酸钠盐、胆酸盐、吐温-80,制成含0.1%吸收促进剂的氟苯尼考溶液;另取对应量国外粉剂(阳性对照),用水溶出药物,过滤并稀释至相同浓度;同样操作,以氟苯尼考水溶液为阴性对照。取试验前禁食12 h不禁水大鼠18只,称重并编号,随机分6组,依照张建平[4]氟苯尼考大鼠肠吸收方法,分别给予大鼠上述6种不同氟苯尼考水溶液,进行大鼠肠循环试验,平行操作,检测氟苯尼考在体大鼠肠的吸收情况,以氟苯尼考的肠吸收百分率为评价指标。
1.5.2 氟苯尼考吸收促进剂的再优化 取适量氟苯尼考原药用水溶解并稀释成0.1mg/mL的氟苯尼考水溶液,同时加入吸收促进剂EDTA和SDS,制成含0.2%吸收促进剂的氟苯尼考溶液;另取对应量国外产品(阳性对照),用水溶出药物,过滤,用水稀释至相同浓度;同样操作,以氟苯尼考原料药为阴性对照。按照1.5.1项下方法操作。
1.5.3 氟苯尼考高效粉剂的制备[6]称取氟苯尼考10 g,用丙酮60mL溶解,备用。另称取多孔性微粉硅胶45 g、淀粉44.5 g,用水450mL分散,再加入EDTA 0.5 g,SDS 0.5 g溶解;将氟苯尼考的丙酮溶液加入到含有多孔性微粉硅胶和淀粉的混悬液中,快速搅拌、喷雾干燥,优化操作条件为:进风温度150℃~180℃,出风温度40℃~50℃,喷雾空气流量30~45m3/h,喷雾压力0.5~0.6Mpa,控制真空度在20~50mbar之间,收集产品再60℃~70℃干燥5 h,即得产品。
1.6 体外溶出试验 按中华人民共和国兽药典2010年版一部附录97第二法(桨法),以氟苯尼考原料药对比考察优化后产品溶出·速率。溶出介质为脱气的去离子水900mL,温度37℃,转速100 r/min,分别于0、5、10、15、20、30、45、60min处取样5 mL,同时补等量同温介质5 mL,经0.2μm微孔滤膜过滤,HPLC法测定药物浓度,计算各时间点的累积溶出率。
1.7 生物利用度对比试验 取优化后的氟苯尼考粉、氟苯尼考原料药、国外产品适量分别用水溶解过滤,制得浓度为0.5mg/mL的氟苯尼考水溶液3份,备用。将小鼠称重并编号,随机分3组,每组36只,禁食12 h但不禁水,灌胃给药50mg/kg体重,分别于给药后0、0.5、1、2、3、4、5、6、8、10、12、24 h眼球取血0.3mL于1%肝素化的离心管中5 000 r/min离心15min,取上层血浆,平行操作。HPLC法测定血药浓度,绘制氟苯尼考药时曲线。将试验结果通过PKSolver药动学处理软件进行拟合;并用SPSS20.0统计软件对数据进行方差分析,P>0.05(双侧)表示差异无统计学意义,P<0.05(双侧)表示差异具有统计学意义P<0.01(双侧)为差异非常显著。
2 结果
2.1 不同吸收促进剂对氟苯尼考吸收的影响 按照1.5.1项下方法,以国外产品为阳性对照、氟苯尼考原料药为阴性对照,对吸收促进剂进行筛选,结果见图1。
由图1可见,各吸收促进剂对氟苯尼考肠吸收有不同程度的影响:EDTA可使药物的肠吸收率达32%,产生最强的吸收促进作用(P<0.01)、SDS次之(P<0.01),胆酸盐和吐温-80对药物的吸收没有显著(P>0.05)促进效果。
依据上述试验结果,按照2.2.2项下方法进行吸收促进剂混合使用,以进一步优化处方,结果见图2。
由图2可见,EDTA和SDS联用后,氟苯尼考的肠吸收率升至40%,药物的吸收速度显著高于原溶液(P<0.05),与国外产品相当(P>0.05)。研究证明,联用EDTA和SDS优选为氟苯尼考的吸收促进剂。
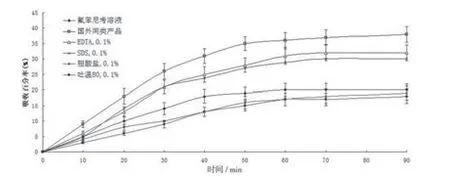
图1 氟苯尼考在体大鼠肠吸收 (100μg/mL)
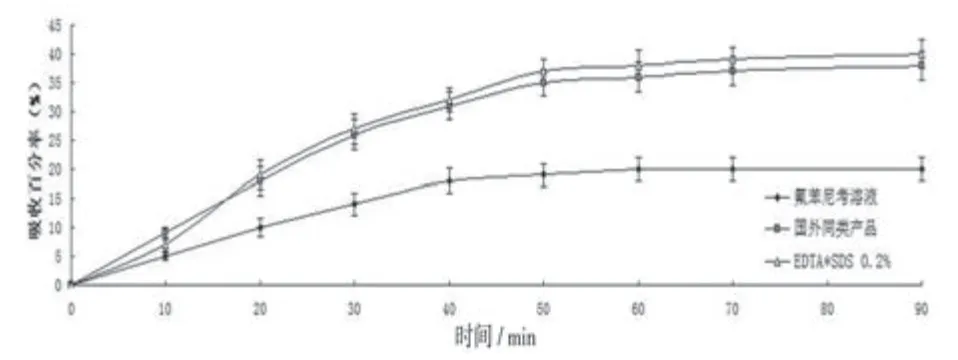
图2 氟苯尼考在体大鼠吸收 (100μg/mL)
2.2 氟苯尼考高效粉体外溶出 按中华人民共和国兽药典2010年版一部附录97第二法(桨法)考察药物溶出速率结果见图3。
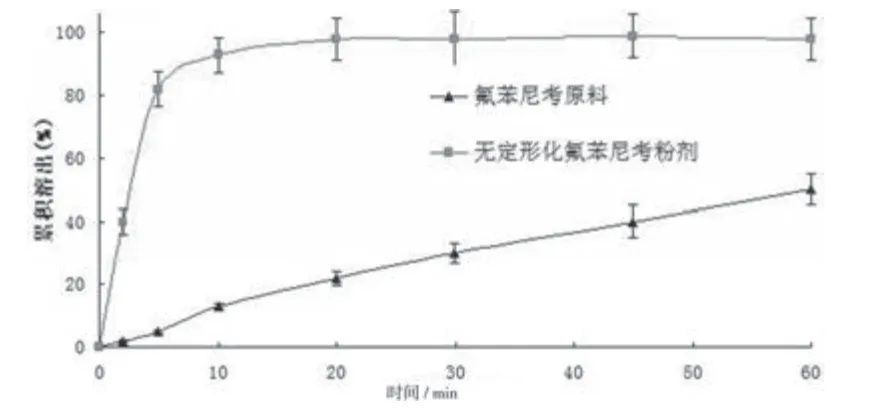
图3 不同时间氟苯尼考累积溶出度
如图3所示:体外溶出5min时,氟苯尼考无定形物(粉)的累积溶出已达85%以上,而氟苯尼考原料药仅释放5%左右,相差17倍。结果表明,氟苯尼考高效粉能显著(P<0.01)提高原料药的溶出速率。
2.3 高效氟苯尼考粉剂生物利用度试验 按照
2.4项下方法对高效氟苯尼考粉生物利用度进行考察,药时曲线见图4。
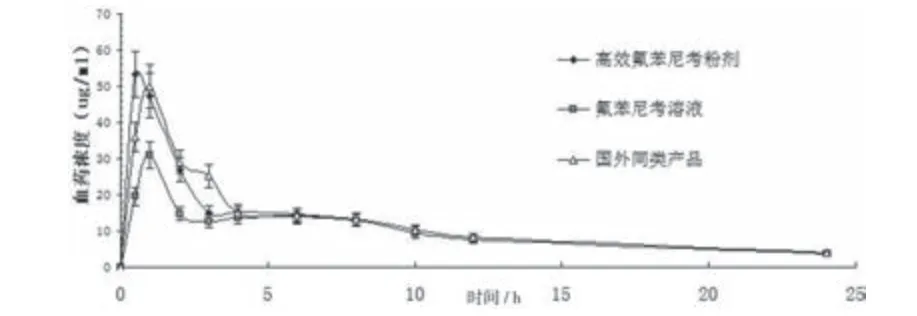
图4 氟苯尼考小鼠灌胃给药药时曲线 (50mg/kg)
将实验数据用PKSolver药动学处理软件进行拟合,结果见表4。
根据C-t曲线和药动学参数可知:本制剂组水溶液小鼠灌胃后,能快速溶出吸收入血,达峰最快且血药浓度最高,36min即达Cmax为54.08μg/mL,是原药溶液的近1倍,与阳性对照55 min达Cmax49.8 6μg/mL相比,差异显著(P<0.05);生物利用度是阳性对照的99.08%、是原药溶液的124.4%。结果表明,本制剂组有效的提高了药物的溶出和吸收速率,改善了药物在体内的吸收和分布,显著提高了药物的生物利用度。
3 讨论
在高效氟苯尼考粉的优化试验中,鉴于吸收促进剂EDTA(螯合效应)和SDS(表面活性剂作用)促进吸收机理的差异和其对药物在体肠吸收的显著促进作用,试验试将其合用,结果证明,EDTA和SDS联用对药物的吸收能产生正协同作用;试验同时采用喷雾干燥法,利用多孔性微粉硅胶的多孔性及高比表面积特征,使药物在其表面高度分散,呈现出一种高能状态,进而达到使药物快速溶出的目的。通过对其生物利用度的考察,本研究制剂达峰最快、时间最短,在体内MRT与国外产品相似,均能很快完全吸收;且由于氟苯尼考是一种浓度依耐型抗生素,剂量后效显著,Cmax越大越有利抗菌素后效应的发挥、药物疗效就越好,所以本制剂最大的Cmax对克服细菌耐药性的产生、提高药物疗效具有重要意义。
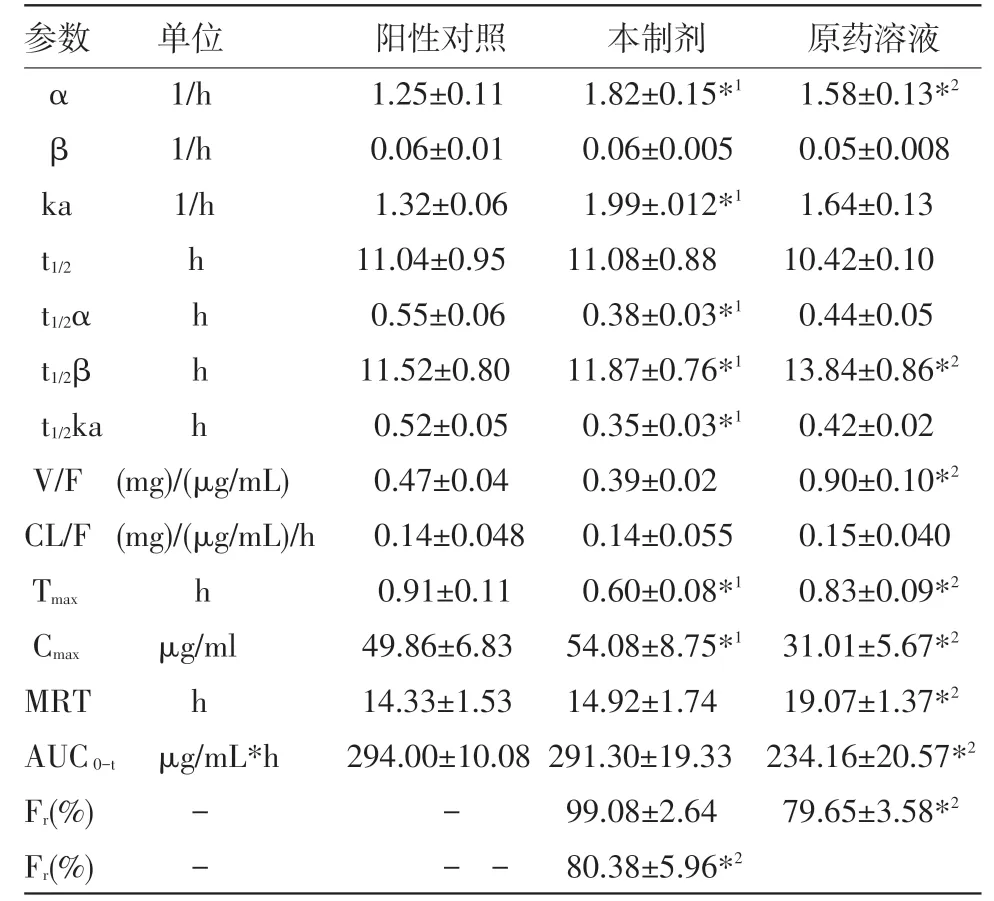
表1 小鼠灌胃相同剂量国外产品、高效氟苯尼考粉和原料液(50mg/kg)的药动学参数(n=3)
4 结论
本试验采用无定形(非晶型)技术和药物吸收促进技术,成功制备了含有氟苯尼考10%、氟苯尼考无定形物吸附载体89.8%、十二烷基硫酸钠盐0.1%和乙二胺四乙酸二钠盐0.1%的高效氟苯尼考粉剂,其在体外能快速释放,体内能快速吸收、血药峰值浓度高、比国外同类产品有更好的治疗效果,且因制备方法简单、成本低,具有推进工业化大生产的前景。
[1]魏海涛,宋敏,李亮华,等.氟苯尼考-β-环糊精包合物的研制[J].华南农业大学学报,2009,30(4):94-97.
[2]刘安刚,李引乾,孙娇,等.氟苯尼考纳米乳的制备及品质评价[J].西北农业学报,2011,20(6):44-49.
[3]Jafvert C T,Kulkarni P P.Buckminster fullerene’s octanol-water partition coefficient and aqueous solubility[J].ENVIRONMEN⁃TAL SCIENCE&TECHNOLOGY,2008,42(16):5945-5950.
[4]张建平,胡海英,张正全.氟苯尼考在大鼠体肠吸收特征试验[J].中国兽医杂志,2013,49(6):71-74.
[5]沙先谊,方晓玲.预测药物小肠吸收的数学模型和细胞模型[J].中国药学杂志,2003,38(12):973-975.
[6]张正全,赵清斌,刘寒,等.高效氟苯尼考粉剂组合物及其制备方法[P].中国专利:201210411002.0.

