满足6 种金属元素测定的混合基体改进剂的选择
耿中华,陈尚龙,张建萍,巫永华 ,高良鹏
(1.徐州工程学院食品(生物)工程学院,江苏 徐州 221111;2.徐州工程学院 江苏省食品资源开发与质量安全重点建设实验室,江苏 徐州 221111)
满足6 种金属元素测定的混合基体改进剂的选择
耿中华1,2,陈尚龙1,2,张建萍1,2,巫永华1,2,高良鹏1
(1.徐州工程学院食品(生物)工程学院,江苏 徐州221111;2.徐州工程学院 江苏省食品资源开发与质量安全重点建设实验室,江苏 徐州221111)
找出满足Al、Cd、Pb、Cu、Mn和Cr测定的混合基体改进剂及其最佳添加体积。比较了9 种单一基体改进剂和4 种混合基体改进剂对这6 种金属元素测定的影响,通过F检验和t检验,检验本法和国标方法之间是否有显著差异。结果表明,含10 g/L磷酸二氢铵和1 g/L酒石酸的混合基体改进剂能满足这6 种金属元素的测定,最佳添加体积为7 μL,本法与国标方法没有显著差异,本法加标回收率为93.3%~105.2%。以此建立的方法快速、准确、稳定,具有较高的实用价值,为食品中多元素检测提供科学依据。
金属元素;基体改进剂;高分辨-连续光源石墨炉原子吸收光谱法
Al在肾、肝、脑等器官中蓄积,损伤脏器,降低免疫力,对神经系统有明显的危害[1-2];Cd在肾脏和肝脏蓄积,引起肾脏慢性中毒[3-4];Pb造成神经、消化、血液、泌尿等多个系统损害,严重影响人体内正常的新陈代谢[5]。Cu、Mn、Cr是人体必需微量元素,摄入过多或过少会对人体健康产生不良影响。Cu在人体内参与造血过程和铁的代谢[4];Mn是人体内多种酶的重要组成元素,影响酶的活性[6];Cr有一定的毒性,六价Cr毒性大,是一种致癌物[7]。近年来,金属污染越来越严重[8],食品中金属元素的含量受到人们的关注。目前,金属元素检测方法主要有原子吸收光谱(atomic absorption spectrometry,AAS)和电感耦合等离子体质谱(inductively coupled plasma mass spectrometry,ICP-MS)检测速度最快[9-10],因其价格昂贵、维护成本高等缺点严重影响其被普遍使用。AAS以其较高的灵敏度和分析精度被广泛应用,成为检测食品中金属元素的首选方法[11-15]。
食品种类众多、成分复杂,检测金属元素时,常存在干扰,造成较大的测量误差。为了解决该问题,常选择添加一定量合适的基体改进剂,消除干扰[16-19]。目前,对一种能同时满足多种金属元素测定的混合基体改进剂的研究甚少。本研究用微波消解样品,使用高分辨-连续光源原子吸收光谱(high resolution-continuum sourceatomic absorption spectrometry,HR-CS AAS)仪研究单一基体改进剂和混合基体改进剂对多种金属元素测定的影响,寻找能满足Al、Cd、Pb、Cu、Mn和Cr测定的混合基体改进剂,建立快速、准确地检测方法。
1 材料与方法
1.1材料与试剂
煎饼(现做)、饼干、馒头、面条和奶粉(均在保质期内,其中饼干、馒头和奶粉采用真空包装)市购。
浓硝酸、磷酸二氢铵、质量分数30%过氧化氢(均为优级纯)国药集团化学试剂有限公司;乙二胺四乙酸、抗坏血酸、柠檬酸、酒石酸、硫酸铵、硝酸镁、十二烷基硫酸钠、硝酸钯(均为分析纯)天津市福晨化学试剂厂;Al、Cd、Pb、Cu、Mn和Cr标准溶液(1.000 g/L)国家化学试剂质检中心;18.2 MΩ·cm超纯水;氩气(纯度>99.99%);玻璃器皿和聚四氟乙烯微波消解罐均用体积分数5%硝酸(以浓硝酸为基准)溶液浸泡24 h以上,使用前,用去离子水冲洗3 遍,再用超纯水冲洗3 遍。
1.2仪器与设备
ContrAA 700高分辨连续光源原子吸收光谱仪(配有MPE60自动进样器)德国Analytik Jena公司;CascadaTM实验室超纯水系统美国Pall公司;XT-9900型智能微波消解仪、XT-9800多用预处理加热仪上海新拓微波溶样测试技术有限公司;FA-2004B电子天平上海越平科学仪器有限公司;220V-AC电子电炉(0~2 000 W)上海树立仪器仪表有限公司;移液器德国Eppendorf公司。
1.3方法
1.3.1仪器工作条件
高分辨-连续光源石墨炉原子吸收光谱法(high resolution-continuum source graphite furnace atomic absorption spectrophotometry,HR-CS GFAAS)测定食品中Al、Cd、Pb、Cu、Mn和Cr。所用载气为高纯氩气;基体改进剂为混合基体改进剂H1,即含10 g/L磷酸二氢铵和1 g/L酒石酸;添加混合基体改进剂H1的体积为7 μL;进样体积为20 μL。其他工作参数见表1。

表1 HR-CS GFAAS工作参数Table 1 Working parameters of HR-CS GFAAS
1.3.2基体改进剂溶液的配制
准确称取1.00 g磷酸二氢铵置于50 mL小烧杯中,用体积分数0.5%稀硝酸溶液溶解后转移至100 mL容量瓶中,用体积分数0.5%稀硝酸溶液定容至刻度,配制成质量浓度10 g/L磷酸二氢铵溶液。
同理,配制成质量浓度1 g/L抗坏血酸、1 g/L柠檬酸、1 g/L酒石酸、1 g/L硫酸铵、1 g/L硝酸镁、1 g/L十二烷基硫酸钠、1 g/L硝酸钯、乙二胺四乙酸(饱和溶液)。
1.3.3标准工作曲线的配制
用体积分数0.5%稀硝酸溶液将Al标准溶液(1.000 g/L)逐级稀释至质量浓度100 μg/L的标准使用液,再通过MPE自动进样器实现标准曲线质量浓度梯度为10、25、50、75、100 μg/L。
同理,配制质量浓度5 μg/L Cd标准使用溶液、50 μg/L Pb标准使用溶液、20 μg/L Cu标准使用溶液、10 μg/L Mn标准使用溶液、20 μg/L Cr标准使用溶液。
1.3.4样品处理
取适量的样品至于干燥的玛瑙研钵中,充分研磨后,制成粉末状样品,装入自封袋中备用,并贮藏在干燥器中。
准确称取0.5 g左右(精确至0.1 mg)样品放入干燥的聚四氟乙烯微波消解罐,加入2 mL超纯水湿润样品后,再加入5 mL浓硝酸和1 mL质量分数30% H2O2溶液。多用预处理加热仪处理1~2 h左右(从40 ℃逐步加热到120 ℃)后,按表2中消解条件密闭微波消解。完成后得透明溶液,移至50 mL小烧杯中,在通风橱内加热赶酸至近干,用体积分数0.5%稀硝酸多次冲洗小烧杯中的样液,将冲洗液移至25 mL容量瓶中,用体积分数0.5%稀硝酸定容至刻度,摇匀备用,按实验方法做空白实验。

表2 微波消解条件Table 2 Microwave digestion conditions
2 结果与分析
2.1介质及其体积分数的选择
原子吸收光谱分析中,合适的介质可有效降低干扰,提高灵敏度。选择硝酸、盐酸和硫酸作为介质定容待测样品和空白,测定6 种金属元素的吸光度。结果表明,硝酸介质的吸光度普遍偏高且空白值低,这与周聪[20]研究结果一致。研究体积分数0.5%、1.0%、2.0%、3.0%、5.0%的稀硝酸为介质对吸光度的影响,结果表明,稀硝酸体积分数(≥0.5%)对吸光度没有显著影响,实验选择体积分数0.5%稀硝酸作为介质。
2.2单一基体改进剂的优化
根据文献报道[21-24],测定不同元素添加的基体改进剂及其添加量不同。实验选择乙二胺四乙酸(饱和溶液)、抗坏血酸(1 g/L)、柠檬酸(1 g/L)、酒石酸(1 g/L)、硫酸铵(1 g/L)、硝酸镁(1 g/L)、十二烷基硫酸钠(1 g/L)、硝酸钯(1 g/L)和磷酸二氢铵(10 g/L)作为基体改进剂,研究对Al、Cd、Pb、Cu、Mn和Cr吸光度的影响,结果如图1所示。

图1 基体改进剂对吸光度的影响Fig.1 Effect of matrix modifiers on the absorbance
由图1可知,不同的基体改进剂对吸光度的影响差异很大。有些基体改进剂没有提高吸光度,反而使吸光度下降,如乙二胺四乙酸、抗坏血酸、柠檬酸、酒石酸、硫酸铵、十二烷基硫酸钠、硝酸钯对Pb的影响。磷酸氢二铵能显著提高Al、Cd、Pb的吸光度,有效改善吸收峰的峰形。因此,测定Al、Cd、Pb时,磷酸氢二铵是首选添加的基体改进剂。同理,测定Cu时,硫酸铵是首选添加的基体改进剂,其次是酒石酸;测定Mn时,除了硝酸镁,添加其他8 种基体改进剂都可以;测定Cr时,除了抗坏血酸,添加其他8 种基体改进剂都可以。
2.3混合基体改进剂的优化
实验表明,上述任何一种单一基体改进剂都不能满足Al、Cd、Pb、Cu、Mn和Cr的测定,为了寻找一种能满足这6 种金属元素测定的基体改进剂,实验将较好的2 种或3 种基体改进剂混合,配制成不同的混合基体改进剂,见表3。研究这些混合基体改进剂对Al、Cd、Pb、Cu、Mn和Cr吸光度的影响,结果如图2所示。

表3 混合基体改进剂Table 3 Mixed matrix modifiers
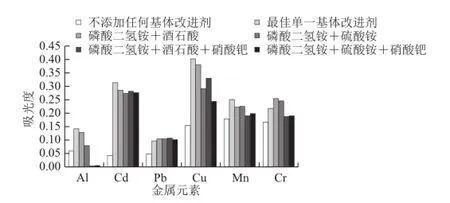
图2 混合基体改进剂对吸光度的影响Fig.2 Effect of mixed matrix modifiers on the absorbance
由图2可知,测定Al、Cd、Cu、Mn时,添加混合基体改进剂比添加最佳单一基体改进剂的吸光度要小,其中下降幅度最小的是混合基体改进剂H1,分别为8.9%(Al)、8.7%(Cd)、5.4%(Cu)、11.1%(Mn),但添加H1比不添加任何基体改进剂的吸光度要大的多,因此最佳混合基体改进剂为H1;测定Pb时,添加不同混合基体改进剂的吸光度相差甚小(≤4.4%),比不添加和添加最佳单一基体改进剂的吸光度都要大,因此添加任一混合基体改进剂都可以;测定Cr时,添加H1比不添加和添加其他基体改进剂的吸光度都要大,因此最佳混合基体改进剂为H1。综上分析,实验选择最佳的混合基体改进剂为H1,即含10 g/L磷酸二氢铵和1 g/L酒石酸。
2.4添加混合基体改进剂体积的优化
添加适量的混合基体改进剂有助于最大限度地消除干扰,提高吸光度。研究混合基体改进剂H1的添加体积对Al、Cd、Pb、Cu、Mn和Cr吸光度的影响,结果如图3所示。

图3 混合基体改进剂的体积对吸光度的影响Fig.3 Effect of the volume of mixed matrix modifier H1 added on the absorbance
由图3可知,添加混合基体改进剂H1能显著地提高吸光度,特别是Cd,这是由于不添加基体改进剂时,灰化温度过高,Cd挥发损失严重,导致吸光度偏低。添加适量的混合基体改进剂H1,可有效地防止Cd的挥发,提高吸光度。在测定Al、Cd、Pb、Cu、Mn和Cr时,吸光度随着添加混合基体改进剂H1体积(≤5 μL)的增大而增大,当体积大于5 μL时,增加趋势趋于平缓,甚至有小幅度下降,因此实验选择添加混合基体改进剂H1的最佳体积为7 μL。
2.5标准工作曲线
在ASpect CS软件中,设置好方法,建立好测定序列,将Al、Cd、Pb、Cu、Mn和Cr的标准使用液、混合基体改进剂H1、空白溶液和样品溶液放入MPE自动进样器的对应位置,使用HR-CS GFAAS进行顺序测定。以质量浓度为横坐标、吸光度为纵坐标,经ASpect CS软件绘制标准工作曲线(非线性)。所得回归方程、相关系数和特征质量浓度见表4。

表4 回归方程、相关系数和特征质量浓度Table 4 Regression equations, correlation coefficients and characteristic concentrations
由表4可知,所有回归方程的相关系数均大于0.992,表明在一定质量浓度范围内,各金属元素的质量浓度与吸光度呈现良好的关系。
2.6样品测定
在选定的工作条件下测定5 种食品中Al、Cd、Pb、Cu、Mn和Cr的含量,结果见表5。

表5 5 种食品中Al、Cd、Pb、Cu、Mn和Cr的含量(n=3)Table 5 Contents of Al, Cd, Pb, Cu, Mn and Cr in five types of food (n=3)

表6 6 F检验和t检验Table 6 le 6 F-F-test and and t-test-test
由表5可知,使用本法和国标方法测定煎饼中Al、Cd、Pb、Cu、Mn和Cr,根据测定的数值,通过F检验和t检验这2 种方法之间是否有显著差异,检验结果见表6。
由表6可知,F值都小于19.0,表明在0.05显著性水平上可认为本法和国标方法的精密度没有显著差异;t值都小于2.78,表明在0.05显著性水平上可认为本法和国标方法没有显著差异。
2.7加标回收率实验
将一定量的标准溶液和样品(煎饼)一起加入到干燥的聚四氟乙烯微波消解罐中进行微波消解,按1.3.4节进行操作,在选定的工作条件下进行测定,计算各金属元素的加标回收率[25],结果见表7。

表7 加标回收率(n=3)Table 7 Recoveries of Al, Cd, Pb, Cu, Mn and Cr in pancakes ( n=3)
由表7可知,加标回收率为93.3%~105.2%,表明以混合基体改进剂H1为基体改进剂,添加体积为7 μL,用微波消解-HR-CS GFAAS测定食品中Al、Cd、Pb、Cu、Mn和Cr,结果准确可靠。
3 结 论
实验选择体积分数0.5%硝酸作为介质,系统地分析了9 种单一基体改进剂对Al、Cd、Pb、Cu、Mn和Cr测定的影响,确定了每种元素最佳的单一基体改进剂。将较好的2 种或3 种基体改进剂混合,研究它们对这6 种金属元素测定的影响。结果表明,含10 g/L磷酸二氢铵和1 g/L酒石酸的混合基体改进剂能满足这6 种金属元素的测定且最佳添加体积为7 μL。在此条件下,使用本法测定了煎饼、饼干、馒头、面条和奶粉这5 种食品中Al、Cd、Pb、Cu、Mn和Cr的含量。通过F检验和t检验检验出本法与国标方法之间没有显著差异,且本法加标回收率为93.3%~105.2%。表明该混合基体改进剂能有效地消除干扰,满足6 种金属元素的测定,所建立的方法对食品中这6 种金属元素的测定具有重要的参考价值。
[1]IEGGLI C V S, BOHRER D, DO NASCIMENTO P C, et al. Determination of aluminum, copper and manganese content in chocolate samples by graphite furnace atomic absorption spectrometry using a microemulsion technique[J]. Journal of Food Composition and Analysis, 2011, 24(3): 465-468.
[2]任婷, 赵丽娇, 钟儒刚. 高分辨连续光源石墨炉原子吸收光谱法测定面制食品中的铝[J]. 光谱学与光谱分析, 2011, 31(12): 3388-3391.
[3]刘全德, 李超, 宋慧, 等. 石墨炉原子吸收法分析食醋中镉测定条件的响应曲面法优化[J]. 食品科学, 2011, 32(22): 196-200.
[4]AJTONy Z, SZOBOSZLAI N, SUSKO E K, et al. Direct sample introduction of wines in graphite furnace atomic absorption spectrometry for the simultaneous determination of arsenic, cadmium, copper and lead content[J]. Talanta, 2008, 76(3): 627-634.
[5]梁剑锋, 李亚. 石墨炉原子吸收光谱法测定龟苓膏粉中铅含量[J].现代食品科技, 2011, 27(11): 1419-1420; 1371.
[6]陈尚龙, 刘全德, 李超, 等. 微乳液直接进样-石墨炉原子吸收光谱法测定食用油中的锰[J]. 食品科学, 2011, 32(18): 278-281.
[7]TÜZEN M. Determination of heavy metals in fish samples of the middle Black Sea (Turkey) by graphite furnace atomic absorption spectrometry[J]. Food chemistry, 2003, 80(1): 119-123.
[8]FABIO G L, DANIEL L G B, RENNAN G O A, et al. Determination of heavy metals in activated charcoals and carbon black for Lyocell fiber production using direct solid sampling high-resolution continuum source graphite furnace atomic absorption and inductively coupled plasma optical emission spectrometry[J]. Talanta, 2010, 81(3): 980-987.
[9]LI yuwei. Determination on heavy metals content of achyranthes bidentata blume through inductively coupled plasma mass spectrometry (ICP-MS)[J]. Journal of Anhui Agricultural Sciences, 2008, 33(36): 14582-14584.
[10] ISELA L, MARTA C, SANDRA G, et al. Simplif i ed and miniaturized procedure based on ultrasound-assisted cytosol preparation for the determination of Cd and Cu bound to metallothioneins in mussel tissue by ICP-MS[J]. Talanta, 2012, 93(15): 111-116.
[11] SARDANS J, MONTES F, PEÑUELAS J. Determination of As, Cd, Cu, Hg and Pb in biological samples by modern electrothermal atomic absorption spectrometry[J]. Spectrochimica Acta Part B: Atomic Spectroscopy, 2010, 65(2): 97-112.
[12] LUANA S N, JOSE T P B, ANDREA P F, et al. Multi-element determination of Cu, Fe, Ni and Zn content in vegetable oils samples by high-resolution continuum source atomic absorption spectrometry and microemulsion samplepreparation[J]. Food Chemistry, 2011, 127(2): 780-783.
[13] AFKHAMI A, SABER-TEHRANI M, BAGHERI H, et al. Flame atomic absorption spectrometric determination of trace amounts of Pb (Ⅱ) and Cr (Ⅲ) in biological, food and environmental samples after preconcentration by modified nano-alumina[J]. Microchimica Acta, 2011, 172(1/2): 125-136.
[14] ALINE R B, EMILENE M B, CÉLINE L, et al. Method development for the determination of cadmium in fertilizer samples using highresolution continuum source graphite furnace atomic absorption spectrometry and slurry sampling[J]. Spectrochimica Acta Part B, 2011, 66(7): 529-535.
[15] ZHAO Lijiao, REN Ting, ZHONG Rugang. Determination of lead in human hair by high resolution continuum source graphite furnace atomic absorption spectrometry with microwave digestion and solid sampling[J]. Analytical Letters, 2012, 45(16): 2467-2481.
[16] EL HIMRI M, EL HIMRI A, PASTOR A, et al. Influence of the measurement medium and matrix modifiers on the determination of silicon in waters by graphite furnace atomic absorption spectrometry[J]. Journal of Applied Sciences and Environmental Management, 2013, 17(1): 37-41.
[17] 肖开提·阿布力孜, 沙尼亚·托乎提, 阿布力孜·伊米提, 等. GF-AAS法测定处理污水灌溉土壤中铅最佳基体改进剂的选择及其应用[J].光谱学与光谱分析, 2008, 28(6): 1410-1412.
[18] 冯银凤, 黄诚, 周日东, 等. 基体改进剂在石墨炉原子吸收法测定食品中铅的探讨[J]. 中国卫生检验杂志, 2005, 15(4): 450; 472.
[19] 马旭, 丁永生, 庞艳华, 等. 石墨炉原子吸收加基体改进剂测定海水中镉[J]. 分析化学研究简报, 2005, 33(3): 343-346.
[20] 周聪. 硝酸作基体改进剂塞曼石墨炉原子吸收法测定海水中的铅和镉[J]. 光谱学与光谱分析, 1996, 16(4): 68-71.
[21] ACAR O, KALFA O M, yALCINKAyA O, et al. Assessment of arsenic, chromium, copper and manganese determination in thermal spring waters by electrothermal atomic absorption spectrometry using various chemical modif i ers[J]. Analytical Methods, 2013, 5(3): 748-754.
[22] DOBROWOLSKI R, PAWLOWSKA-KAPUSTA I, DOBRZyNSKA J. Chromium determination in food by slurry sampling graphite furnace atomic absorption spectrometry using classical and permanent modif i ers[J]. Food Chemistry, 2012, 132(1): 597-602.
[23] 秦樊鑫, 张明时, 胡继伟, 等. 氯化钯作基体改进剂GFAAS法测定中药材中微量铅的研究[J]. 光谱学与光谱分析, 2007, 27(7): 2123-2126.
[24] 李月欢, 徐淑暖, 彭寨玉, 等. 混合基体改进剂测定尿镉[J]. 中国卫生检验杂志, 2007, 17(4): 637-638; 689.
[25] 郭金英, 李丽, 刘开永, 等. 石墨炉原子吸收光谱直接进样法测定红葡萄酒中铅[J]. 食品科学, 2009, 30(18): 233-236.
Screening of Mixed Matrix Modifiers for Determination of Six Metal Elements in Food Matrices
GENG Zhong-hua1,2, CHEN Shang-long1,2, ZHANG Jian-ping1,2, WU Yong-hua1,2, GAO Liang-peng1
(1. College of Food (Biological) Engineering, Xuzhou Institute of Technology, Xuzhou221111, China; 2. Jiangsu Key Construction Laboratory of Food ResourcesDevelopment and Quality Safe, Xuzhou Institute of Technology, Xuzhou221111, China)
A mixed matrix modifier with optimum volume for the determination of Al, Cd, Pb, Cu, Mn and Cr in food samples was found by comparing the effects of nine individual matrix modifiers and four mixed ones on the results of determination of the six metal elements by high resolution-continuum source graphite furnace atomic absorption spectrometry (HR-CS GFAAS). By using F-test and t-test, we examined whether there were significant differences between the developed method and the national standard method. A mixed matrix modifier consisting of ammonium dihydrogen phosphate (10 g/L) and tartaric acid (1 g/L) was found to be the most suitable one, and its optimum volume was 7 μL. There was no significant difference between this method and the national standard method and the spiked recoveries of our method ranged from 93.3% to 105.2%. The method developed in this study proved rapid, accurate and stable with a high practical value. It can provide a scientific basisfor multi-element determination in food samples.
metal element; matrix modifier; high resolution-continuum source graphite furnace atomic absorption spectrometry (HR-CS GFAAS)
O657.31
A
1002-6630(2014)14-0175-05
10.7506/spkx1002-6630-201414034
2014-04-08
江苏省食品资源开发与质量安全重点建设实验室资助项目(SPKF201317);国家自然科学基金面上项目(31270577)
耿中华(1979—),男,讲师,博士研究生,研究方向为天然产物的提取及食品分析。E-mail:23749399@qq.com

