α-常春藤皂苷丙烯酸树脂L100-55纳米粒的制备及体外评价
李 颖,尹红然,耿丽娟,游本刚
(1.苏州大学医学部药学院,江苏苏州215123;2.苏州市产品质量监督检验所,江苏苏州215104)
·制剂研究·
α-常春藤皂苷丙烯酸树脂L100-55纳米粒的制备及体外评价
李 颖1,2,尹红然1,耿丽娟1,游本刚1
(1.苏州大学医学部药学院,江苏苏州215123;2.苏州市产品质量监督检验所,江苏苏州215104)
目的采用肠溶材料丙烯酸树脂L100-55作为载体材料,制备α-常春藤皂苷丙烯酸树脂纳米粒(SPD-L100-55-NPs)并进行体外评价。方法采用改良乳化溶剂扩散法制备SPD-L100-55-NPs,以粒径、包封率(EE)和多分散指数(P.I.)为综合指标,通过单因素实验和正交设计实验优化纳米粒的处方工艺,以红外光谱(FT-IR)、X射线衍射(XRD)、差示扫描量热分析(DSC)等对制备的纳米粒进行评价,并考察其体外释放特性。结果制得的SPD-L100-55-NPs纳米粒外观圆整、分布均匀,平均粒径为(63.5±3.6)nm,包封率为98.91%± 0.18%,P.I.为0.198±0.014。药物在纳米粒中被载体材料有效包裹,体外释放具有缓释特性和pH依赖性。结论所制得的纳米粒圆整均匀、包封率高,在体外具有良好的缓释特性和pH敏感性。
α-常春藤皂苷;丙烯酸树脂(L100-55);纳米粒;释放
α-常春藤皂苷[1](saponins PD,SPD)是从中药预知子[2]中提取的三萜皂苷类化合物,具有保肝护肝[3~6]、抗肿瘤[7]等多种药理活性,但SPD难溶于水,口服吸收差,体内生物利用度较低,且对黏膜有较强的刺激性。丙烯酸树脂具有安全、无毒,理化性能稳定,不被吸收和代谢等优点,在降低药物毒副作用,提高生物利用度和疗效等方面具有重要意义[8]。本研究以肠溶材料丙烯酸树脂Eudragit L100-55为载体材料,制备α-常春藤皂苷丙烯酸树脂L100-55纳米粒,以期降低药物毒副作用并提高其生物利用度。
1 材料与仪器
1.1 材料 α-常春藤皂苷(自制,纯度90%以上);α-常春藤皂苷对照品(中国药品生物制品检定所,批号:111880-201001);丙烯酸树脂L100-55(德国罗姆公司);泊洛沙姆F68(深圳市优普惠实业发展有限公司);乙腈为色谱纯,甲醇等其他试剂均为分析纯。
1.2 仪器 纳米粒度和Zeta电位分析仪(NICOMP 380ZLS,Santa Barbara,USA);LC-15C高效液相色谱仪(日本岛津公司);HPP-5001激光粒度分析仪(英国Malvern公司);Optima max超速冷冻离心机(美国Beckman公司);真空冷冻干燥机(Lg-5A,上海离心机械研究所);H600透射电子显微镜(日立公司,日本);X′Pert-Pro MPD X射线多晶衍射仪(荷兰帕纳科公司);SDT 2960热分析仪(美国TA Instruments公司);MagnaIR550型红外光谱仪(美国Nicolet公司)。
2 方法与结果
2.1 SPD的含量测定
2.1.1 HPLC色谱条件 色谱柱:Cosmosil C18柱(4.6 mm×150 mm,5μm);流动相:乙腈-水-磷酸(42∶58∶0.1);流速:1 mL·min-1;检测波长:203 nm;柱温:35℃;进样量:20μL。
2.1.2 标准曲线的绘制 精密称取SPD对照品10.04 mg,于100 mL容量瓶中,用甲醇溶解并定容,配成浓度100.40μg·mL-1的标准贮备液。
分别精密量取SPD贮备液配制成浓度0.502、5.02、10.04、20.08、40.16、80.32μg·mL-1的标准溶液,按上述色谱条件,取20μL进样,记录药物峰面积。以峰面积(A)对质量浓度(C)进行线性回归,得线性方程为:A=6 533.2C-1 201.9,r=0.999 9(n=5),在0.502~80.32μg·mL-1质量浓度范围内线性关系良好。
2.1.3 精密度 分别取低(0.502μg·mL-1)、中(20.08μg·mL-1)、高(80.32μg·mL-1)3个浓度的样品溶液,一天内重复测定5次,连续测定5 d,SPD的日内、日间RSD均<2%,符合要求。
2.1.4 回收率 取空白纳米粒胶体溶液1 mL,分别加入0.05、2、8 mL的SPD标准母液,加甲醇适量于超声机中超声消解,静置后,用甲醇定容至10 mL,过0.45μm微孔滤膜,HPLC进样20μL,测定SPD的浓度,代入标准曲线方程,得低、中、高浓度的回收率:100.60%±1.92%、97.78%±1.25%和99.00%±1.09%。
2.2 SPD-L100-55-NPs的制备
2.2.1 SPD-L100-55-NPs胶体溶液的制备采用改良乳化-溶剂扩散法[9]制备SPD-L100-55-NPs。称取L100-55与SPD溶解于无水乙醇中,作为有机相;另取F68溶于蒸馏水作为水相。在水浴和磁力搅拌下,将有机相快速注入水相中,搅拌反应一段时间后,转入到高温度水浴中,继续搅拌以挥发有机溶剂,经0.45μm微孔滤膜过滤,即得纳米粒胶体溶液。
2.2.2 SPD-L100-55-NPs冻干粉的制备 取SPD-L100-55-NPs胶体溶液,超滤浓缩至原体积的十分之一。取10%甘露醇溶液1 mL加入到3 mL上述纳米粒浓缩液中,混匀,分装于西林瓶中,至-70℃低温冰箱,冷冻24 h,迅速转入真空冷冻干燥机中,干燥28 h后即得。
2.3 纳米粒的质量评价
2.3.1 粒径和多分散系数的测定 取适量纳米粒胶体溶液用激光散射粒度分析仪测定粒径和多分散系数(P.I.)。
2.3.2 包封率的测定 取适量新鲜制备的SPDL100-55-NPs胶体溶液置于离心管中,低温超速离心45 min(30 000 rpm,4℃),分取20μL上层清液进样,测定,经换算即得游离药量;取1mL纳米粒胶体溶液加入甲醇超声消解后,取20μL进样,经换算得纳米粒溶液中SPD含量即为总投药量。按下列公式计算纳米粒的包封率(EE)。

2.4 单因素考察纳米粒的制备工艺 通过考察丙烯酸树脂L100-55用量(100 mg)、SPD用量(40 mg)、有机相/水相比例(1∶5)、F68用量(200 mg)、搅拌速度(500 rpm)、挥发时间及温度(3 h,50℃)、针头大小及注入速度(7#,15 s)等因素,以EE、平均粒径和P.I.为指标,初步筛选制备纳米粒的处方及工艺条件。括号中数据为考察其他因素时该因素的固定水平,若单因素考察后结果与所固定得数据相左,则选用考察后的较优水平。
2.4.1 丙烯酸树脂L100-55用量的考察 L100-55分别称取100、125、150、175、200 mg,制备纳米粒,结果见表1。随着L100-55用量增加,粒径逐渐增大,P.I.先减小后增大,EE则减小,故其用量不宜过大,在100~150 mg时较优。综合考虑,L100-55用量为125 mg较为适宜。

表1 L100-55用量的考察
2.4.2 SPD用量的考察 SPD分别取10、20、30、40、50 mg,制备纳米粒,结果见表2。随着SPD用量的增加,纳米粒粒径变化不是太大,P.I.值先增大后降低,EE逐渐增大后变化不大,故SPD用量可适当增加,暂定SPD用量为50 mg。
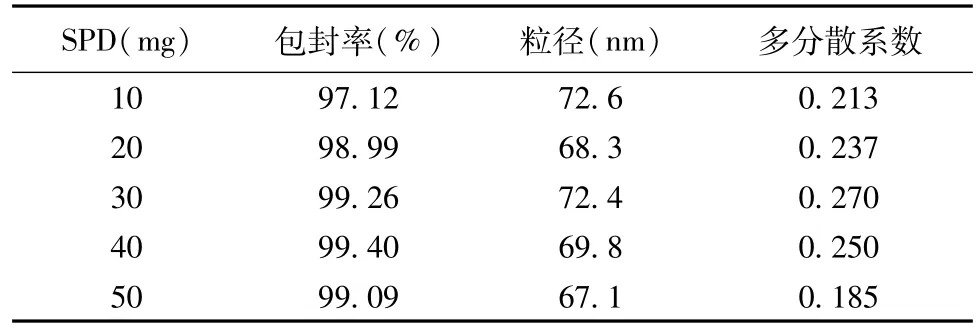
表2 SPD用量的考察
2.4.3 有机相/水相的考察 无水乙醇/水的比例分别为0.5∶5、1∶5、1.5∶5、2∶5,其中水相为50 mL不变,制备纳米粒,结果见表3。由表可见,在1∶5~2∶5之间,EE变化不大,纳米粒粒径和P.I.值都增大,故选取有机相/水相比例为不宜过大,初步确定比例为1∶5。
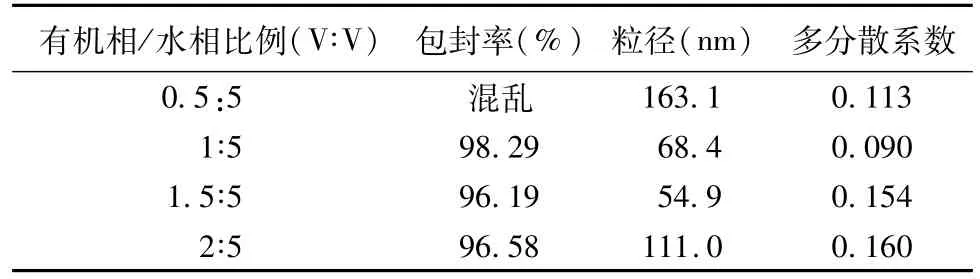
表3 有机相/水相比例的考察
2.4.4 F68用量的考察 分别取50、100、150、200、250、300 mg的F68,制备纳米粒,结果如表4。可见F68在100~250 mg范围内形成的纳米粒较多,粒径分布均匀。综合考虑,F68用量确定为200 mg。

表4 F68用量的考察
2.4.5 挥发时间的考察 在50℃条件下,考察有机相挥发时间,制备纳米粒,结果如表5。可知有机溶剂在挥发温度在50℃、挥发时间为3 h时,粒径较小,EE高,P.I.值较小,粒径分布较集中。
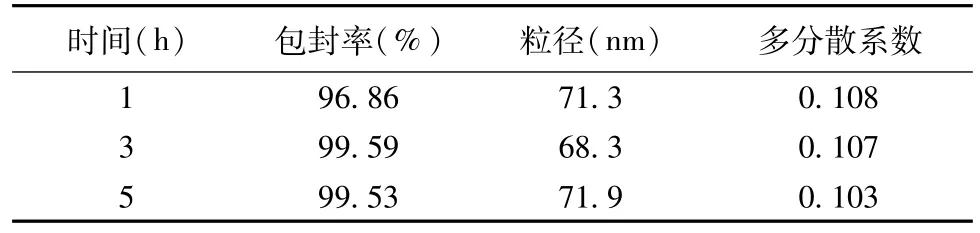
表5 挥发时间的考察
2.4.6 注入速度与针头大小的考察 分别用三种型号针头,三种注入速度将有机相匀速注入水相,制备纳米粒,结果见表6。由此可知针头大小和注入速度对EE和粒径影响不大,选取较小的P.I.值,故有机相选用7#针头在15 s内匀速注入。
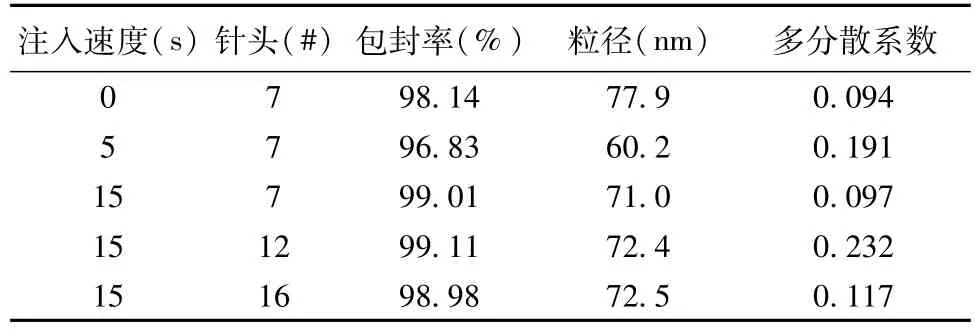
表6 注入速度与针头大小的考察
2.4.7 转速的考察 在不同磁力搅拌速度下,制备纳米粒,结果见表7。可知转速对EE影响较小,对粒径、P.I.值有影响,故转速选用较优的500 rpm。
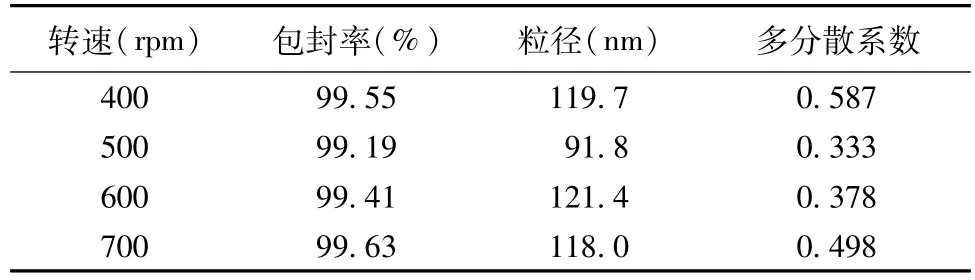
表7 转速的考察
2.5 正交设计优化SPD-L100-NPs制备工艺
综合单因素考察的数据,选取了A:SPD用量、B:有机相/水相比例和C:F68用量三个影响较大的因素,每个因素选择3个水平,使用L9(33)正交表(表8)进行正交设计试验。以a:EE、b:平均粒径和c:P.I.为指标,分别给3个指标0.5、0.3、0.2的权重,采用综合加权评分法[10,11],由于平均粒径、P.I.越小越优,所以综合评分=a/amax×100×0.5+bmin/b ×100×0.3+cmin/c×100×0.2,结果见表9。
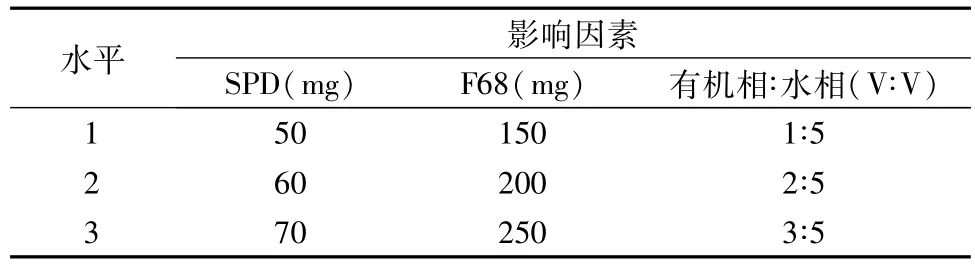
表8 正交设计因素水平表

表9 正交实验结果
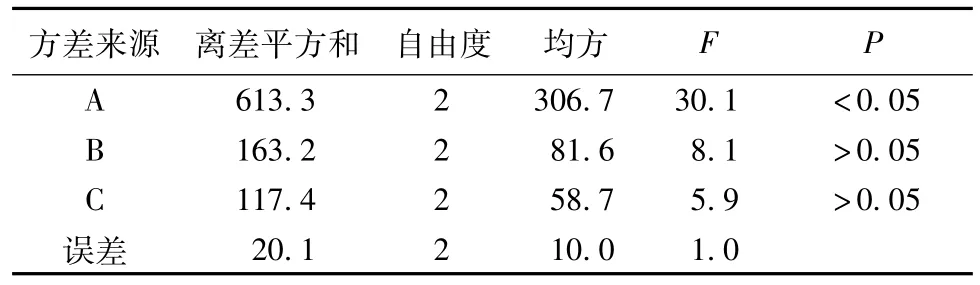
表10 方差分析表
通过直观分析,各因素对指标的影响大小顺序依次为A>B>C,三因素的最佳组合为A1B3C1,即SPD用量为50 mg、F68用量为250 mg、有机相与水相的比例为1∶5。方差分析结果(表10)表明,A因素即SPD用量各水平间具有显著性差异(P<0.05)。
2.6 验证实验 称取125 mg丙烯酸树脂L100-55与50 mg的SPD溶解于10 mL无水乙醇中,超声溶解后,作为有机相;另将250 mg泊洛沙姆188溶于50 mL蒸馏水中作为水相。在30℃水浴、500 rpm磁力搅拌下,将有机相快速注入水相中,继续搅拌反应10 min后,转入到60℃水浴中,搅拌3 h以挥发有机溶剂,经0.45μm微孔滤膜过滤,即得SPD-L100-55-NPs胶体溶液。平行制备3批SPDL100-55-NPs,各项指标见表11,粒径分布见图1。测得包封率98.91%±0.18%,平均粒径(63.5± 3.6)nm,P.I.值0.198±0.014,综合评分98.92,均优于正交实验中的9个处方工艺。

表11 优化工艺制备的纳米粒的各项指标
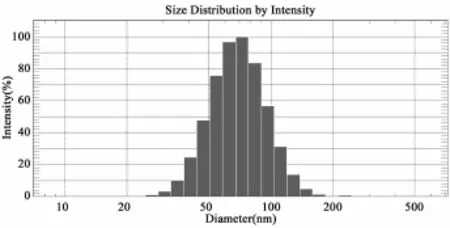
图1 SPD-L100-55-NPs粒径分布图
2.7 SPD-L100-55-NPs纳米粒的表征
2.7.1 纳米粒形态观察 将SPD-L100-55-NPs胶体溶液点样于铜网上,经2%的磷钨酸复染后,用滤纸吸干染液,自然干燥后,置于透射电镜下观察。纳米粒的透射电镜照片见图2,可见纳米粒形态圆整,粒径分布集中,且与激光粒度分析仪的测定结果相近。

图2 SPD-L100-55-NPs透射电镜照片
2.7.2 FT-IR分析 取L100-55、SPD、SPDL100-55物理混合物、Fd-SPD-L100-55-NPs加入适量KBr压片,测得如图3的红外谱图。L100-55曲线中有两个特征峰:3 499 cm-1ν(-OH),1 753 cm-1δ(-C=O)。NPs中的O-H伸缩振动吸收峰红移至3 305 cm-1处,向低波数位移了194 cm-1,这表明形成了一定强度的分子内和分子间氢键;1 753 cm-1处的尖峰强度降低,并有新的吸收峰出现。表明形成了新的物相,掩盖了药物峰,药物被包裹形成纳米粒。
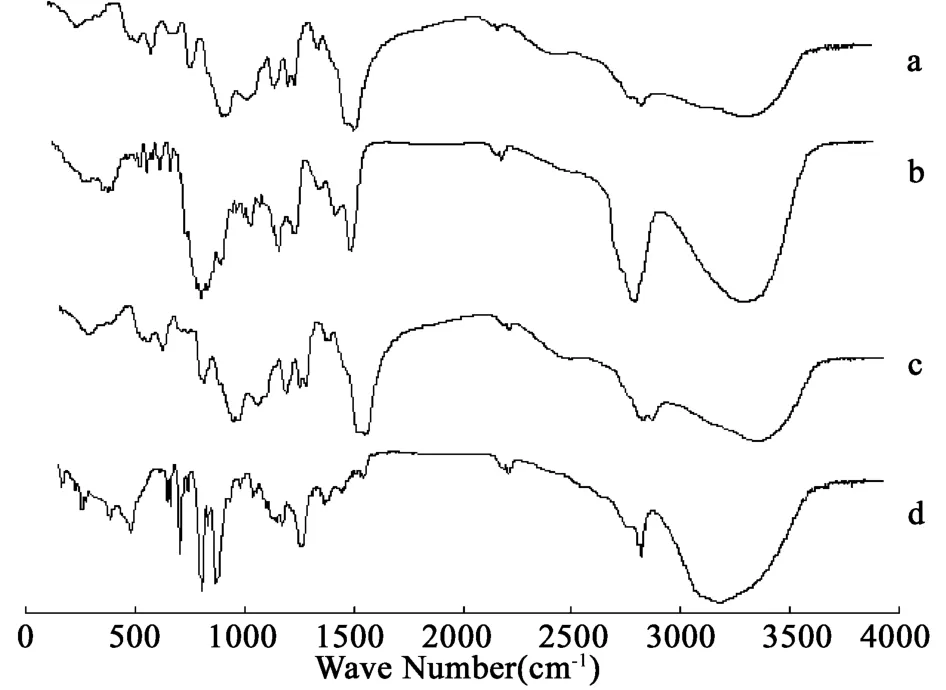
图3 红外光谱图
2.7.3 DSC分析 分别称取L100-55、SPD、SPD-L100-55物理混合物、Fd-SPD-L100-55-NPs约1.0 mg。测试条件:采用热流型测量方法,以空白铝坩埚为参比物,扫描速度为20℃·min-1,扫描范围为0~300℃。得到热流型DSC曲线,见图4。NPs的DSC曲线在158.11和168.45℃处分别出现一新的吸热峰,且SPD(63.47、221.55℃)、S100(68.66、217.06℃)和SPD-L100-55 Mixture(70.78、222.03℃)的原吸热峰被掩盖或被削弱,与NPs曲线有显著的不同,表明生成了新的物相,即有纳米粒形成,结果与FT-IR一致。

图4 DSC曲线图
2.7.4 XRD分析 对L100-55、SPD、SPD-L100-55物理混合物、Fd-SPD-L100-55-NPs进行X衍射。条件为:Cu靶/石墨单色器,电压30 kV,电流20 mA,扫描速度0.1°·s-1,采样时间1 s,扫描范围5~50°。得X-射线衍射图谱见图5。对比图a、b、c、d可见,纳米粒图谱中L100与SPD的特征吸收峰均消失,且有新的峰出现,表明L100与SPD之间发生了较强的相互作用,形成了无定形粉末,载药纳米粒药物峰消失,提示药物已被包裹其中。与FT-IR和DSC的分析结果一致。
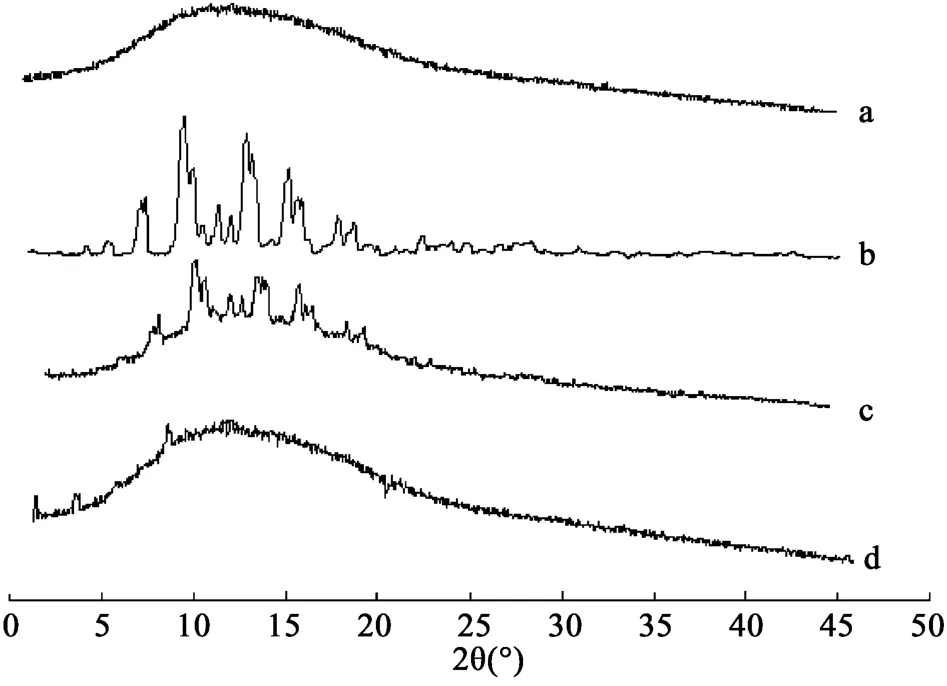
图5 X射线衍射图
2.8 SPD-L100-55-NPs的体外释放特性 采用动态透析法,取纳米粒浓缩液2 mL,置于透析袋中,扎紧两端,分别固定于40%乙醇pH 1.2盐酸溶液和40%乙醇磷酸盐缓冲溶液(pH 5.0、6.8、7.4、8.0)200 mL的释放瓶中,置于(37±0.5)℃的恒温振荡器中,100 rpm振荡。于不同时间点分别取样2 mL,同时补加2 mL相应的同温释放介质。样品经0.45μm微孔滤膜过滤,取续滤液20μL进样,HPLC测定其中SPD的浓度,并计算其累积释放百分率,绘制释放曲线,结果见图6。
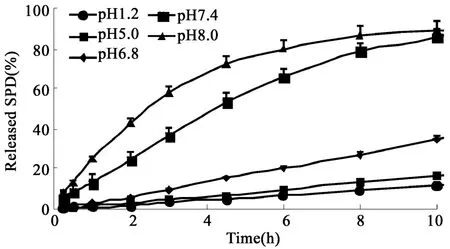
图6 SPD-L100-55-NPs的体外释放曲线(n=3)
从图中可见:SPD-L100-55-NPs释放呈现明显的pH依赖性,药物释放率随着pH值的升高而增大。10 h时在pH<6.8的溶出介质中,药物释放率均<30%;在pH 6.8介质中释放34.8%;在pH>6.8的介质中释药较快,在8 h药物累积释放都达到80%以上。
3 讨论
改良-乳化溶剂扩散法适用于油脂溶性药物和非水溶性载体材料制备纳米粒,其原理为向水相中注入的有机相在乳化剂的作用下形成乳滴,在磁力搅拌作用下通过乳滴内部乙醇和外部水相之间的逆向扩散来包载药物,在乙醇挥发的过程中形成纳米粒子。本研究以水难溶性药物SPD为模型药物,非水溶性材料丙烯酸树脂为载体,通过优化制备工艺和处方设计制备了平均粒径65 nm的纳米粒子,包封率高达99%。
体外释放实验结果表明,纳米粒释药具有pH敏感性和缓释特性。虽然L100-55在pH 5.5以上的介质中易于溶解,但实验发现在pH 6.8时药物释放缓慢,这样在体内可减少胃和小肠上段酶系对药物的代谢作用,使SPD能够在肠道最佳吸收部位达到较高浓度,提高其生物利用度。
[1] 江纪武,肖庆祥.植物药有效成分手册[M].北京:人民卫生出版社,1986:920-921. [2] 王家明,高慧敏,洪玉梅,等.预知子中α-常春藤皂苷的HPLC分析[J].中国药学杂志,2006,41(16):1212-1214.
[3] 时京珍,刘耕陶.黄褐毛忍冬皂甙对对乙酰氨基酚致小鼠肝脏毒性的保护作用[J].药学学报,1995,30(4):311-314.
[4] 时京珍,宛蕾,陈秀芬.黄褐毛忍冬总皂甙对几种化学毒物致小鼠肝损伤的保护作用[J].中药药理与临床,1990,6(1):33-34.
[5] 刘亚平,刘杰,贾宪生,等.黄褐毛忍冬总皂甙对醋氨酚所致肝损伤的保护作用[J].中国药理学报,1992,13(3):209-212.
[6] 刘亚平,刘杰,贾宪生,等.黄褐毛忍冬总皂甙对镉所致急性肝损伤的保护作用[J].中国药理学报,1992,13(3):213-217.
[7] Park HJ,Kwon SH,Lee JH,et al.Kalopanaxsaponin A is a basic saponin structure for the anti-tumor activity of hederagenin monodesmosides[J].Planta Med,2001,67(2):118-121.
[8] 刘善奎,钟延强,孙其荣,等.丙烯酸树脂系列辅料在药物新剂型中的应用[J].药学实践杂志,2002,20(1):12-15.
[9] Dai JD,Wang XQ,Zhang T,etal.Preparation of cyclosporine A pH sensitive nanoparticles and oral pharmacokinetics in rats[J].Yao Xue Xue Bao,2004,39(12):1023-1027.
Preparation and in vitro evaluation of Saponins PD-Loaded Eudragit L100-55 Nanoparticles
LIYing1,2,YIN Hong-ran1,GENG Li-juan1,YOU Ben-gang1
(1.College of Pharmaceutical Science,Soochow University,Suzhou 215123,China;2.Suzhou Institute of Supervision and Inspection on Product Quality,Suzhou 215104,China)
ObjectiveTo prepare and in vitro evaluate Saponins PD loaded Eudragit L100-55 Nanoparticles(SPDL100-55-NPs).MethodsThe SPD-L100-55-NPs were prepared bymodified quasiemulsion solvent diffusion technique.Taking particle size,entrapment efficiency and polydisperse index as comprehensive indexes,the orthogonal test design was used to optimize the preparation process.The characteristics of nanoparticles were determined by FT-IR,X-ray diffraction,DSC,etc.;In vitro releasewas investigated.ResultsNovel nanoparticleswere spherical,average particle size of nanoparticleswas(63.5±3.6)nm,EE 98.91%±0.18%,P.I.0.198±0.014.The release of SPD significantly depended on the pH conditions.ConclusionSPD-L100-55-NPs had high EE and homogeneous size distribution.The effect of drug sustained release of nanoparticleswas significant。
Saponins PD;Eudragit(L100-55);Nanoparticles;Release
R944
A
2095-5375(2014)08-0464-006
国家自然科学基金青年基金(No.81102818)
李颖,女,研究方向:药物分析,E-mail:ly0825ant@163.com
游本刚,男,博士研究生,讲师,研究方向:中药新剂型与新技,Tel:13814809871,E-mail:youbengang@suda.edu.cn

