老年乳腺癌患者应用非蒽环类辅助化疗方案的安全性及耐受性临床研究
芃
北京协和医学院,中国医学科学院肿瘤医院肿瘤内科,北京 100021
老年乳腺癌患者应用非蒽环类辅助化疗方案的安全性及耐受性临床研究
韩颖 李青 徐兵河 张频 袁芃王佳玉 马飞 蔡瑞刚 樊英 李俏
北京协和医学院,中国医学科学院肿瘤医院肿瘤内科,北京 100021
背景与目的:乳腺癌发病率随年龄增长而升高,老年患者占有较大的比例。但由于老年患者所接受的治疗不足、合并症多、身体一般状况差,预后往往较年轻患者差。本研究观察我国老年乳腺癌患者应用以紫杉类为主的非蒽环类辅助化疗方案的安全性和耐受性。方法:2008年11月—2012年1月共有56例接受手术治疗的老年乳腺癌患者,以2∶1比例(≥65岁)入TC组(4或6个周期的多西他赛75 mg/m2和环磷酰胺600 mg/m2,35例)和PC组(4或6个周期的紫杉醇175 mg/m2和环磷酰胺600 mg/m2,21例)。在化疗结束后,根据患者病情,继续进行局部放射治疗和(或)内分泌治疗。结果:本研究共有50例患者按计划完成化疗,2组完成计划化疗的比例均在90%以上。中位随访33个月,中位无复发生存和总生存时间均未达到。PC组和TC组2年无病生存率分别为89.5%(17/19)和90.3%(28/31);2年生存率分别为100%和96.8%(30/31)。非蒽环类辅助化疗方案的主要不良反应为Ⅲ~Ⅳ度中性粒细胞减少、白细胞减少以及Ⅰ~Ⅳ度的脱发、胃肠道反应和周围神经毒性。2组相比,PC组更易出现Ⅲ~Ⅳ度中性粒细胞减少(76.2% vs 48.6%,P=0.044)和不同程度的周围神经毒性(9.5% vs 2.9%)。不能耐受化疗相关不良反应是患者提前终止化疗和减少化疗药物剂量的主要原因。结论:非蒽环类化疗方案的耐受性及安全性好,老年乳腺癌患者能较好地接受以紫杉类为主的化疗方案。PC方案在耐受性和安全性上与TC方案相当,为我国老年乳腺癌患者增加一个安全、低毒的化疗方案的选择。
老年乳腺癌;非蒽环类化疗方案;安全性;耐受性
乳腺癌是威胁女性身心健康的常见恶性肿瘤,其发病率随年龄增长而升高,老年患者占较大比例。在发达国家,有60%以上的乳腺癌新发患者及70%以上的乳腺癌死亡患者为老年患者[1-3]。由于老年患者接受的系统治疗不足、合并症多、身体一般状况差,预后往往较年轻患者差。乳腺癌的术后辅助化疗可提高生存率、降低复发率和死亡率,但目前还缺乏大规模随机分组临床研究来证明化疗在老年患者中的作用,对于老年患者辅助化疗的方案、剂量以及疗程也没有明确的指南[4]。为老年患者选择一类安全、低不良反应的化疗方案成为国内外学者关注的热点。
本研究自2008年11月—2012年1月对老年乳腺癌患者以2∶1比例给予TC方案和PC方案辅助化疗,以探讨我国老年乳腺癌患者对非蒽环类辅助化疗方案的安全性和耐受性,并观察复发及生存情况。
1 资料和方法
1.1 研究对象
2008年11月—2012年1月,中国医学科学院肿瘤医院共收治56例经病理证实的女性乳腺癌患者(≥65岁)。所有入组患者均接受改良根治术或保乳术,并经影像学证实不存在局部或远处转移。以2∶1比例分组,共有35例患者接受TC方案(TC组),21例患者接受PC方案(PC组)。本研究收集了所有入组患者的病史、人口学资料;肿瘤组织形态学和生物特征资料;手术方式以及治疗情况。两组患者体力状况(performance status,PS)评分均≤2分,血常规、肝肾功能正常,无严重心脏疾患,心电图正常。两组患者除了在手术方式上TC组患者更多接受改良根治术外(P=0.003),其余的基本特征均相仿,差异无统计学意义(P>0.05,表1)。
1.2 治疗方法
入组患者接受4或6个周期PC或TC方案化疗。PC组方案:环磷酰胺(cyclophosphamide,CTX)600 mg/m2,第1天,静脉滴注;紫杉醇(paclitaxel,PTX)175 mg/m2,第2天,静脉滴注3 h;每3周重复,共4或6周期。TC组方案:CTX 600 mg/m2,第1天,静脉滴注;多西他赛(docetaxel,Doc) 75 mg/m2,第2天,静脉滴注3 h;每3周重复,共4或6个周期。患者治疗前后检查血常规、血生化、心电图、胸片、腹部超声,必要时行超声心动图测量左心室射血分数(left ventricular ejection fractions,LVEF)。治疗中,每周复查血常规,每个周期化疗前复查血生化及心电图。当出现心脏不良反应,并伴有临床症状时行超声心动图检查测量LVEF。每个周期化疗后对不良反应进行评估。化疗结束后根据患者病情进行局部放射治疗和(或)内分泌治疗。
1.3 不良反应评估和随访
化疗不良反应按照美国国立癌症研究所的常见抗癌药不良反应分级标准(National Cancer Institute Common Toxicity Criteria, NCICTC)3.0版进行评估。因不良反应未按计划完成化疗者,仅参与不良反应统计。生存指标为无病生存期(disease-free survival,DFS)和总生存期(overall survival,OS)。DFS指手术日至肿瘤首次复发转移时间。OS为手术日至死亡或末次随访时间,均按月计算。每3个月随访1次。
1.4 统计学处理
采用SPSS 16.0统计软件对数据进行统计分析。采用生存函数分析法分析DFS和OS,logrank检验比较曲线之间的差异。不同亚组基本资料比较,如为连续变量将采用独立t检验,如为分类变量则采用χ2检测。各项计数资料采用χ2检验,P<0.05为差异有统计学意义。
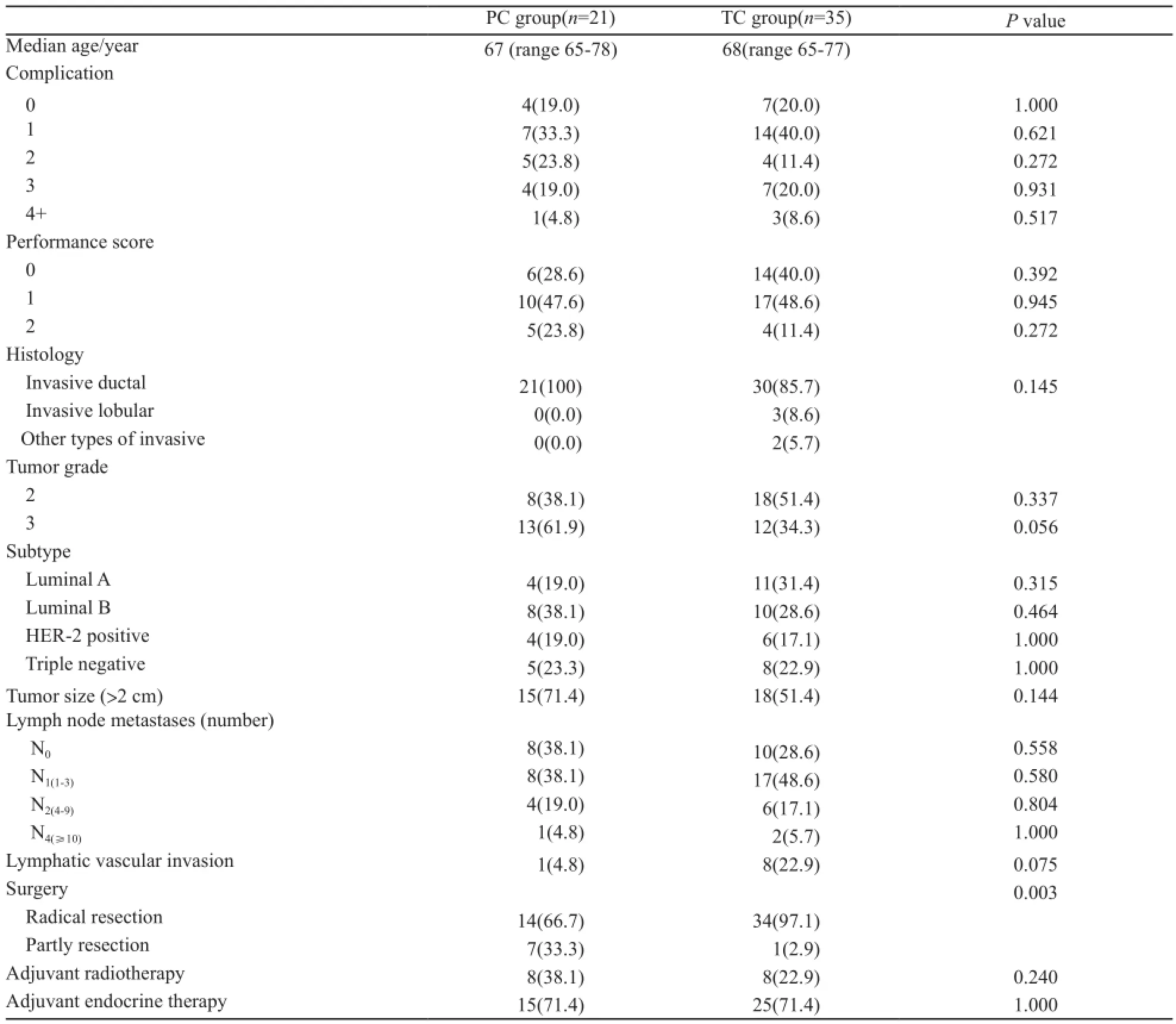
表1 患者一般资料和人口学资料Tab. 1 Clinical information and demographics of the patients included in the study (n=56)
2 结 果
2.1 化疗完成情况
共有50例患者按计划完成化疗。PC组中位化疗周期数为4个,TC组为5个。PC组和TC组分别有93.3%和95.3%的患者完成了预期化疗。按所有治疗周期计算,PTX的标准剂量强度(dose intensity,DI)为每周58.3 mg/m2,实际DI为每周(56.1±2.7) mg/m2,相对剂量强度(relative dose intensity,RDI)为96.2%;Doc的标准DI为每周25 mg/m2,实际DI为每周(24.6±1.49) mg/m2,RDI为95.8%(表2)。
PC组有2例(9.5%)、TC组有4例(11.4%)患者未完成预期的化疗周期数。PC组中,1例患者因合并症较多同时出现Ⅳ度中性粒细胞减少而终止化疗;另1例患者在充分预处理后于第1个周期化疗过程中出现紫杉醇过敏而终止化疗开始内分泌治疗。TC组中,1例因严重胃肠道反应持续时间长而终止化疗;2例因化疗期间合并症加重而终止化疗;另有1例患者由于持续白细胞及中性粒细胞计数偏低而终止化疗。
2.2 复发及生存情况
入组患者的中位随访时间为33个月(11~51个月),在此随访期间内共有5例患者出现了不同位置的复发转移,其中内脏转移1例(肺转移);非内脏转移3例(包括胸壁转移、多发淋巴结转移及骨转移),此外,还有1例患者同时出现内脏及非内脏转移(表3)。PC组无死亡患者,
TC组在复发转移的患者中有1例死亡。由于随访时间较短,中位DFS和OS均未达到。PC组有2例患者在随访期出现复发,TC组为3例,PC组和TC组的无复发率分别为89.5%和90.3%,两组之间差异无统计学意义(P=0.638)。2年生存率分别为100%和96.8%,差异有统计学意义(P=0.620,表3)。
2.3 不良反应
统计结果显示非蒽环类化疗方案主要的血液学毒性为Ⅲ~Ⅳ度中性粒细胞减少和白细胞减少,而对血红蛋白及血小板影响较小。两组均有较高的Ⅲ~Ⅳ度中性粒细胞减少发生率。其中PC组较TC组更易出现较为严重的中性粒细胞减少,分别为76.2%和48.6%,差异有统计学意义(P=0.044),需要密切监测血常规。非血液学不良主要为不同程度的脱发、恶心、呕吐等胃肠道反应,肝功能异常以及周围神经系统不良反应。其中PC组周围神经毒性的发生率较TC组高,分别为9.5%和2.9%。值得注意的是,非蒽环类化疗方案对心脏不良反应较小,仅有极少数患者在化疗过程中出现一过性的LVEF下降(表4)。

表2 化疗完成情况Tab. 2 The completion of chemotherapy
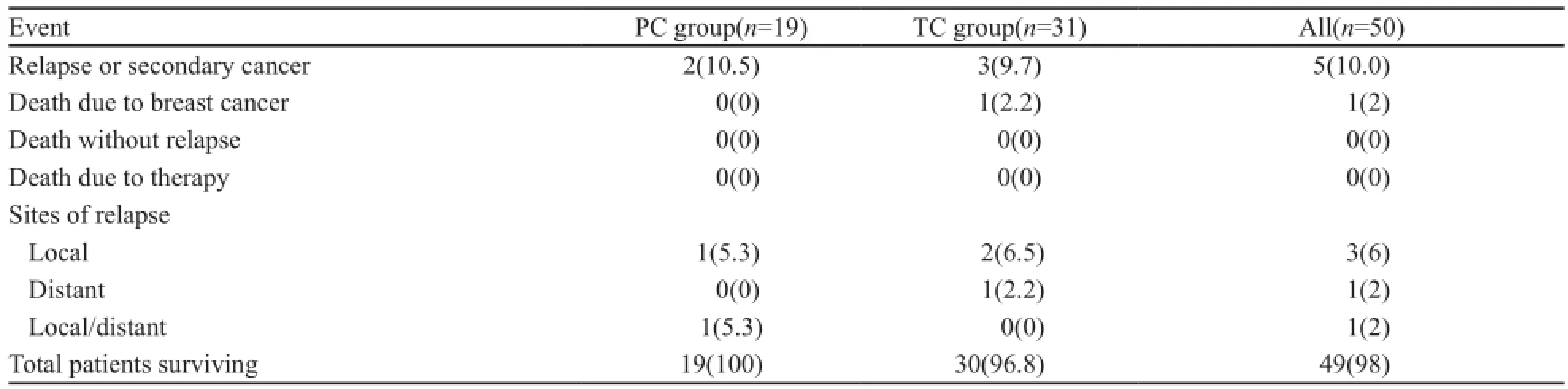
表3 研究终止事件及原因Tab. 3 Events and reasons for study discontinuation[n(%)]
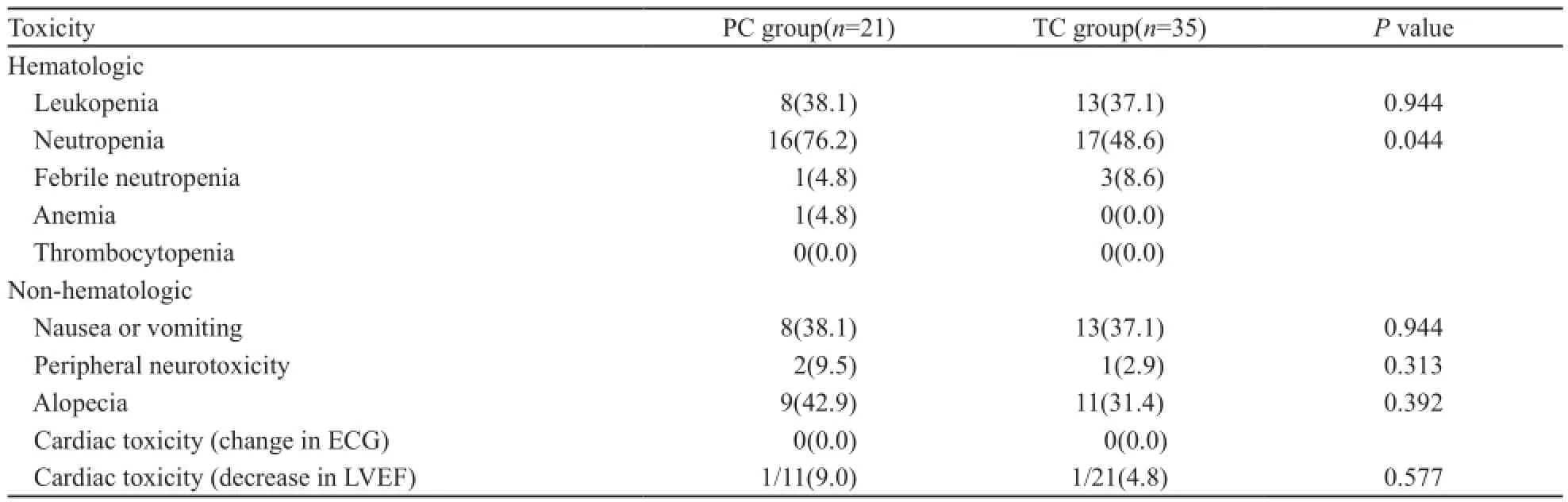
表4 不同治疗组的3~4度不良反应Tab. 4 Grade 3-4 toxicities in 56 patients receiving chemotherapy[n(%)]
3 讨 论
随着我国人口老龄化、工业化进程的加快以及环境污染、吸烟等的影响,老年人乳腺癌的发病率急剧增加。与年轻患者相比,老年乳腺癌的病理表现为DNA双倍体、S期细胞百分比低、P53基因突变率低及表皮生长因子和cerbB2低表达或不表达,以上这些特点均提示老年患者癌细胞增殖较慢[6]。此外,老年乳腺癌肿瘤体积大,病情较晚,可能与老年患者就诊较晚,缺乏定期影像筛查有关[7]。由于老年患者所接受的治疗不足、合并症多、身体一般状况差,预后往往较年轻患者差。系统有效的化学治疗,对淋巴结阳性患者的OS有益,Muss等[8]报道在4项大型淋巴结阳性乳腺癌辅助治疗研究中,虽然只有7%的患者年龄≥65岁,但这些老年患者与年轻患者从较强烈的治疗方案中具有相似的获益率。虽然老年患者会出现较多的不良反应,但总体上能较好的耐受化疗。Fargeot等[9]研究发现,对于年龄≥65岁、激素受体(hormonal receptor,HR)阴性的老年患者,含蒽环类药物治疗可延长患者的DFS。而化疗所引起的不良反应往往限制了化疗药物的使用,减少了化疗药物的剂量。Muss等[10]的一项回顾性多变量分析中显示,年龄与化疗相关死亡率之间存在明显的相关性。该研究共入组了6 487例淋巴结转移的乳腺癌患者,中位随访9.6年。研究结果显示,化疗相关死亡率为0.5%(95%CI:0.4~0.7),其中≤50岁年龄组为0.2%,51~64岁年龄组为0.7%,而≥65岁年龄组为1.5%,与其他两年龄组相比,差异有统计学意义(P<0.001)。该研究提示,老年患者化疗相关死亡率明显高于青年患者。为老年患者选择一类有效且不良反应较低的化疗方案已成为临床医师关注的热点。
乳腺癌术后辅助化疗可提高生存率、降低复发率和死亡率,目前在世界范围内已获得了广泛的认同和应用。而蒽环类药物是乳腺癌化疗中常用的化疗药物,许多患者由于在术后辅助治疗中应用了蒽环类药物而未出现复发,但同时这类药物也存在着心脏不良反应[11-12]。蒽环类药物所引起的心脏不良反应是一种不可逆的非缺血性心肌毒性。患者会出现LVEF的减低和心力衰竭,严重者甚至引发心源性死亡。蒽环类药物引起的心脏不良反应是与剂量累计有关。多项回顾性研究结果显示,当多柔比星的累计剂量达到400~450 mg/m2时,心功能不全的发生率为5%[13],在老年患者中发生心功能不全的比率更高。Pinder等[14]进行的荟萃分析研究了43 338例乳腺癌患者,其中66~70岁接受含蒽环类药物的辅助化疗组与不含蒽环类药物化疗组发生心力衰竭的风险比为1.26(95%CI:1.12~1.42)。含蒽环类药物化疗组10年累计心力衰竭发生率为38%,不含蒽环类药物化疗组为32.5%,而未接受化疗组为29%。而且这一差异随着随访时间的延长更为明显。进一步分析发现对于老年患者,或是有严重合并症的患者其发生心力衰竭的概率更高。蒽环类药物引起的不良反应限制了其在老年乳腺癌患者中的应用。
PTX与Doc均属于紫杉烷类药物,其抗微管作用可改变有丝分裂并引起细胞死亡。大量临床研究证实了紫杉类药物对晚期乳腺癌的卓越疗效,使其在辅助化疗中的应用得以开展[15]。NSABP-28、CALGB9344、BCIRG001等国际多中心临床研究证明了包含紫杉类药物的化疗方案在辅助化疗中的地位,但在疗效上是否优于或等同于含蒽环类药物的化疗方案;对蒽环类药物有禁忌证的患者可否用含紫杉类的方案来替代,国外学者为此开展了相关的研究。Jones等[16]进行的USO9735临床试验比较了AC方案与TC方案在乳腺癌辅助治疗中的疗效。该试验5年随访结果显示,TC组与AC组的DFS差异有统计学意义(TC组为86%,AC组为80%;HR=0.67;P=0.015)。TC组有改善OS的趋势(90% vs 87%;HR=0.76;P=0.13)。7年随访结果显示无论是老年还是年轻患者,TC组的DFS和OS均优于AC组[17]。在化疗相关不良反应上,虽然TC组有较高的中性粒细胞减少性发
热比例,但与AC组相比仍具有较好的耐受性。TC方案与AC方案相比,疗效相当且耐受性好,故于2008年NCCN指南中已将其作为可选用的方案之一。在圣安东尼奥乳腺癌大会上,多数医师愿意考虑TC方案用于早期乳腺癌辅助化疗,并有43%的医师认为TC方案适合有心脏风险的患者。
本研究结果显示,非蒽环类化疗方案的不良反应与之前所述的临床研究报道基本相似。以紫杉类为主的化疗方案在血液学不良反应方面主要为中性粒细胞减少及白细胞减少,而对血红蛋白及血小板的影响较小。Jones等[16]进行的USO9735临床研究结果显示,TC方案出现Ⅲ~Ⅳ度中性粒细胞减少的发生率为61%。本研究中TC组出现Ⅲ~Ⅳ度中性粒细胞减少的发生率为48.6%,PC组为76.2%,两组相比较,PC组更易出现Ⅲ~Ⅳ度中性粒细胞减少(P=0.044),但并没有增加Ⅲ~Ⅳ度白细胞减少的发生率(P=0.944)。而中性粒细胞减少性发热的发生率两组间差异无统计学意义。研究结果提示,应用以紫杉类为主的化疗方案需要更严密的血液学监测,尤其是对老年患者预防性应用重组人粒细胞集落刺激因子可能会提高化疗的安全性和耐受性。
在非血液学不良反应方面,非蒽环类化疗方案的主要不良反应为恶性、呕吐等胃肠道反应、脱发以及不同程度的周围神经毒性。这与紫杉类药物的不良反应是相对应的。进一步比较TC及PC方案两组间不良反应发生率,结果显示,与TC组相比,PC组并没有显著增加患者恶心、呕吐的发生率,亦未显著增加患者肝功能异常的发生率。本研究结果显示,老年组患者对PC方案的耐受性较好。但PC方案更易出现程度不同的周围神经毒性及Ⅲ~Ⅳ度脱发。其发生的原因可能与紫杉醇药物中的聚氯乙烯蓖麻油有关[15],目前国外已有研究证实口服度洛西汀抗抑郁类药物可缓解由于化疗药物所引起的周围神经毒性[18],美国食品药品监督管理局(Food and Drug Administration,FDA)也已批准该类药物治疗由于化疗所引起的周围神经病变。因此,对于一些伴有明显临床症状、影响生活质量和化疗进行的患者可考虑加用此类药物以缓解症状。值得注意的是,以紫杉类为主的化疗方案的心脏毒性,本研究结果显示PC方案与TC方案均未增加心脏毒性,仅有个别患者在治疗过程中出现一过性的LVEF下降。而Jones等[16-17]进行的USO9735临床研究结果也同样显示出TC方案未引起心脏不良反应。
除了探讨非蒽环类化疗方案的安全性,本研究还探讨了以紫杉类为主的化疗方案的耐受性,并进一步比较了PC方案与TC方案。本研究入组患者未完成预定周期化疗的主要原因是不能耐受化疗的不良反应。骨髓抑制、消化道反应以及周围神经毒性是导致化疗药物剂量减少的主要原因。
综上所述,非蒽环类化疗方案的安全性及耐受性良好,即使是老年患者也能较好地耐受以紫杉类为主的化疗方案。PC方案除了有较高的Ⅲ~Ⅳ度中性粒细胞减少及脱发发生率以外,在耐受性及安全性上与TC方案相当。入组患者对于PC方案的较好耐受性及安全性为老年乳腺癌患者提供了一个低毒、可耐受的化疗方案选择。
[1]World Health Organization. WHO Cancer Mortality Database[EB/OL]. 2014. http://www-depdb.iarc.fr/who/menu.htm.
[2]LOUWMAN W J, VULTO J C M, VERHOEVEN R H A, et al. Clinical epidemiology of breast cancer in the elderly [J]. Eur J Cancer, 2007, 43(15): 2242-2252.
[3]SAMI G D, RICHARD M E, GARY M C. Tumor characteristics and clinical outcome of elderly women with breast cancer [J]. J Natl Cancer Inst, 2000, 92(7): 550-556.
[4]DOWNEY L B. Adjuvant treatment of breast cancer in the elderly. Understanding and addressing the challenges [J]. Oncology (Willistion Park), 2008, 22(3): 286-293.
[5]徐兵河. 老年乳腺癌的临床特点及治疗策略[J]. 中国中西医结合杂志, 2008, 20(10): 874-875.
[6]ZAPKA J G, STODDARD A M, COSTANZA M E, et al. Breast cancer screening by mammography: utilization and associated factors [J]. Am J Public Health, 1989, 79(11): 1499-1502.
[7]VAN DE W W, MARKOPOULOS C, VAN DE V C J, et al. Association between age at diagnosis and disease-specific mortality among postmenopausal women with hormone
receptor-positive breast cancer [J]. JAMA, 2012, 307(6): 590-597.
[8]MUSS H B, BERRY D A, CIRRINCIONE C, et al. Toxicity of older and younger patients treated with adjuvant chemotherapy for node-positive breast cancer: the Cancer and Leukemia Group B Experience [J]. J Clin Oncol, 2007, 25(24): 3699-3704.
[9]FARGEOT P, BONNETERRE J, ROCHE H, et al. Diseasefree survival advantage of weekly epirubicin plus tamoxifen versus tamoxifen alone as adjuvant treatment of operable, node-positive, elderly breast cancer patients: 6-years followup results of the French Adjuvant Study Group 08 trial [J]. J Clin Oncol, 2004, 22(23): 4622-4630.
[10]MUSS H B, BERRY D A, CIRRINCIONE C T, et al. Adjuvant chemotherapy in older women with early-stage breast cancer[J]. N Engl J Med, 2009, 360(20): 2055-2065.
[11]GIANNI L, HERMAN E H, LIPSHULTZ S E, et al. Anthracycline cardiotoxicity: from bench to bedside [J]. J Clin Oncol, 2008, 26(22): 3777-3784.
[12]BARRETT-LEE P J, DIXON J M, FARRELL C, et al. Expert opinion on the use of anthracyclines in patients with advanced breast cancer at cardiac risk [J]. Ann Oncol, 2009, 20(5): 816-827.
[13]SWAIN S M, WHALEY F S, EWER M S. Congestive heart failure in patients treated with doxorubicin: a retrospective analysis of the three trials [J]. Cancer, 2003, 97(11): 2869-2879.
[14]PINDER M C, DUAN Z, GOODWIN J S, et al. Congestive heart failure in older women treater with adjuvant anthracycline chemotherapy for breast cancer [J]. J Clin Oncol, 2007, 25(25): 3808-3815.
[15]CORTAZA P, JUSTICE R, JOHNSON J, et al. U.S. Food and Drug Administration approval overview in metastatic breast cancer [J]. J Clin Oncol, 2012, 30(14): 1705-1711.
[16]JONES S E, SAVIN M A, HOLMES F A, et al. Phase Ⅲ trial comparing doxorubicin plus cyclophosphamide with docetaxel plus cyclophosphamide as adjuvant therapy for operable breast cancer [J]. J Clin Oncol, 2006, 24(34): 5381-5387.
[17]JONES S E, SAVIN M A, HOLMES F A, et al. Docetaxel with cyclophoshpamide is associated witih an overall survival benefit compared with doxorubicin and cyclophosphamide: 7-year follow-up of US oncology research trial 9735 [J]. J Clin Oncol, 2009, 27(8): 1177-1183.
[18]SMITH E M, PANG H, CIRRINCIONE C, et al. Effect of duloxetine on pain, function, and quality of life among patients with chemotherapy-induced painful peripheral neuropathy[J]. JAMA, 2013, 309(13): 1359-1367.
Safety and tolerance of non-anthracyclin regimen adjuvant chemotherapy in elderly breast cancer patients
HAN Ying, LI Qing, XU Bing-he, ZHANG Pin, YUAN Peng, WANG Jia-yu, MA Fei, CAI Rui-gang, FAN Ying, LI Qiao (Department of Medical Oncology, Cancer Hospital, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100021, China)
Background and purpose:The incidence of breast cancer increases as patients age, elderly patients account for a large proportion. Due to the insuf fi cient systemic therapy, more complications and poorly physical condition, the prognosis of elderly patients is often worse than the younger. The aim of this study was to investigate the safety and tolerance with non-anthracyclin regimen as adjuvant chemotherapy in elderly breast cancer patients.Methods:From Nov. 2008 to Jan. 2012, 56 patients (≥65 years) after surgical excision were enrolled into this study. The patients were divided into two groups: TC and PC groups. Each patient received 4 or 6 cycles of chemotherapy of PC (175 and 600 mg/m2, respectively; n=21) or TC (75 and 600 mg/m2, respectively; n=35), administered intravenously every 3 weeks, as adjuvant chemotherapy. Radiation therapy (as indicated) and endocrine therapy, for patients with hormone receptor-positive disease, were administered after completion of chemotherapy.Results:In this study, 50 patients completed chemotherapy as plan, the proportion of two groups were above 90%. After a median followup of 33 months, the median disease-free survival(DFS) and overall survival(OS) were not reached. The relapse-free rate and survival rate were 89.5% and 100% in the PC regime group, which were 90.3% and 96.8% in the TC regime group. Major toxicities included: neutropenia, leucopenia, alopecia, nausea, vomiting and various degree of peripheral neuropathy. The incidence of grade Ⅲ-Ⅳ neutropenia was 76.2% in PC group vs 48.6% in TC group (P=0.044). The
Elderly breast cancer; Non-anthracyclin regimens; Safety; Tolerance
10.3969/j.issn.1007-3969.2014.05.008
R737.9
A
1007-3639(2014)05-0367-07
2013-10-21
2014-04-09)
李青 E-mail:cheryliqing@aliyun.com
most common cause for withdrawing from treatment was to be unable to tolerate the adverse effects.Conclusion:Adjuvant chemotherapy with paclitaxel and cyclophosphamide is safe, tolerable and promising for elderly breast cancer patients.

