拉果错盐湖卤水15℃等温蒸发析盐规律研究
吴敬礼,王学魁,董景岗,沙作良
(天津科技大学海洋科学与工程学院,天津 300457)
拉果错盐湖卤水15℃等温蒸发析盐规律研究
吴敬礼,王学魁,董景岗,沙作良
(天津科技大学海洋科学与工程学院,天津 300457)
以西藏拉果错盐湖卤水为研究对象,研究该湖水在15℃蒸发过程中离子的富集规律及析盐规律,为拉果错盐湖资源利用提供基础数据.实验结果表明:在蒸发率为52%时硫酸钠开始析出且在整个蒸发过程中都大量析出;钾在蒸发率为87%时开始析出;锂在蒸发率为82%时达到最高质量浓度2.30g/L,Li2CO3在卤水中已达到该温度下的溶解平衡,会以Li2CO3形式析出;硼在蒸发率为67%时开始大量析出,母液中硼的最高质量浓度为15.92g/L.
拉果错;盐湖;析盐规律;相图
研究蒸发过程析盐规律是盐湖资源开发必不可少的前期科研工作,它们能给盐田设计和各组分分离提取工艺提供基本依据.拉果错位于西藏阿里高原南部,其中心纬度84°05′N,经度32°02′E,湖面海拔4,470,m,属于高原亚寒带干旱区.湖水化学类型属于硫酸钠亚型,富含Li、B、K等有开采价值的元素,含盐量为5.5%~6.5%.迄今为止,对于此盐湖湖水体系的基础性研究鲜有报道[1-2],未见蒸发析盐规律的研究.我国新疆、四川、青海及其他省份也普遍存在硫酸钠亚型卤水[3-5],针对这些盐湖资源,目前进行开发利用研究较少.
1 材料与方法
1.1 实验原料
拉果错湖水具有低Ca2+、Mg2+的特征.湖水密度1.048g/cm3、pH 9.03、黏度1.464,mPa·s,其主要化学成分见表1.
实验所用卤水根据拉果错盐湖卤水组成进行配制,密度1.049g/cm3、pH 9.68、黏度1.253,mPa·s,其主要化学成分见表2.尽管所配制的卤水与该盐湖湖水组成略有差异,由于盐湖湖水离子组成随着季节变化会发生变化,这种差异是可以接受的.
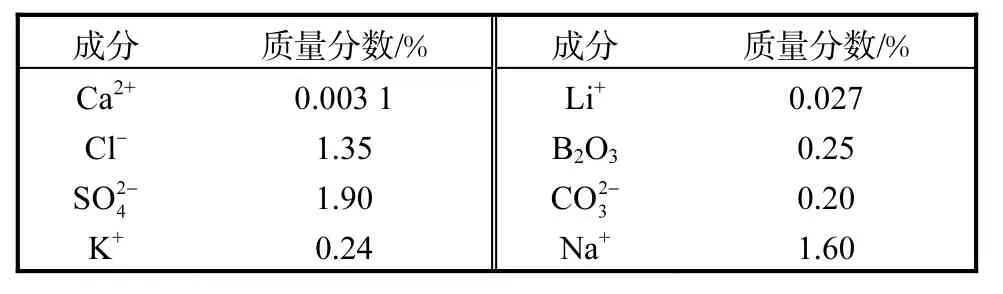
表1 拉果错盐湖卤水主要化学组成Tab. 1 Main chemical composition of the Laguocuo brine
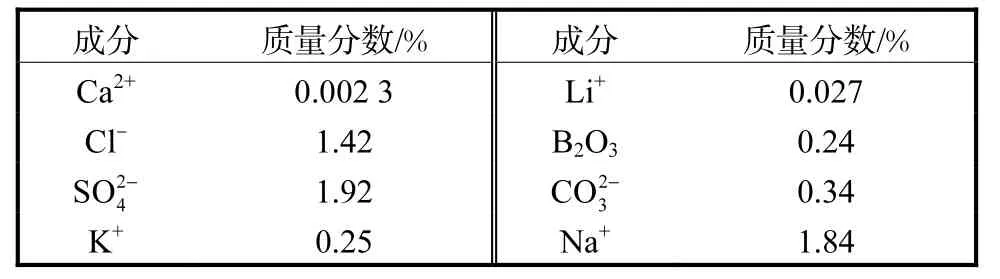
表2 配制卤水主要化学组成Tab. 2 Main chemical composition of the artificially synthesized brine
1.2 实验方法
卤水蒸发析盐实验参考了有关海卤水蒸发析盐规律的研究报道[6-8].青藏高原湖区夏季的日平均气温一般在15℃左右,因此本实验选择在15℃条件下进行析盐规律研究.考虑到若在实验室内进行15℃等温蒸发,不仅耗时较长,而且能源消耗也较大,因此本实验采用高温沸腾蒸发,15℃平衡冷却的实验方法进行盐湖卤水蒸发析盐实验.
将定量的实验卤水置于搪瓷缸,加热至沸腾蒸发.在搪瓷缸中设有搅拌器,以避免因在蒸发过程中固相析出而固结在搪瓷缸底部,影响传热效果.同时控制搅拌速率防止卤水在蒸发过程中溅出搪瓷缸.当蒸发水量接近预定的质量蒸发率(简称蒸发率,后同)时,将蒸发后的试样连同搪瓷缸转移至平衡槽内进行恒温平衡,并准确控制平衡槽温度为15℃,平衡时间至少为3d.平衡期间继续搅拌试样,特别是有大量固相生成的试样.平衡结束后,再次进行称量,以确定出准确的蒸发率,然后进行固液分离,并分别取固相和液相样品进行分析.
蒸发率ω按照式(1)进行计算

式中:m原为蒸发时所配原始卤水质量,g;m剩为蒸发后液相与固相质量,g.
1.3 样品分析方法
液相中各种离子(或物质)含量的分析参照文献[9]进行,具体分析方法如下:用硝酸银容量法测定Cl-含量;用EDTA络合滴定法测定Ca2+、Mg2+含量;用火焰原子吸收光度法测定Li+含量;用四苯硼酸钾重量法测定K+含量;用硫酸钡重量法测定SO含量;用甘露醇容量法测定B2O3含量;用酸碱滴定法测定CO、HCO含量;用差减法计算Na+含量.
液相样品密度采用密度瓶法测定;pH采用pH分析仪测定;黏度采用乌式黏度计测定;水分采用失重法测定.
2 结果与讨论
2.1 分析测定结果
实验卤水15℃等温蒸发,各阶段卤水蒸发率、液相的密度、pH、黏度及化学组成分别见表3、表4.
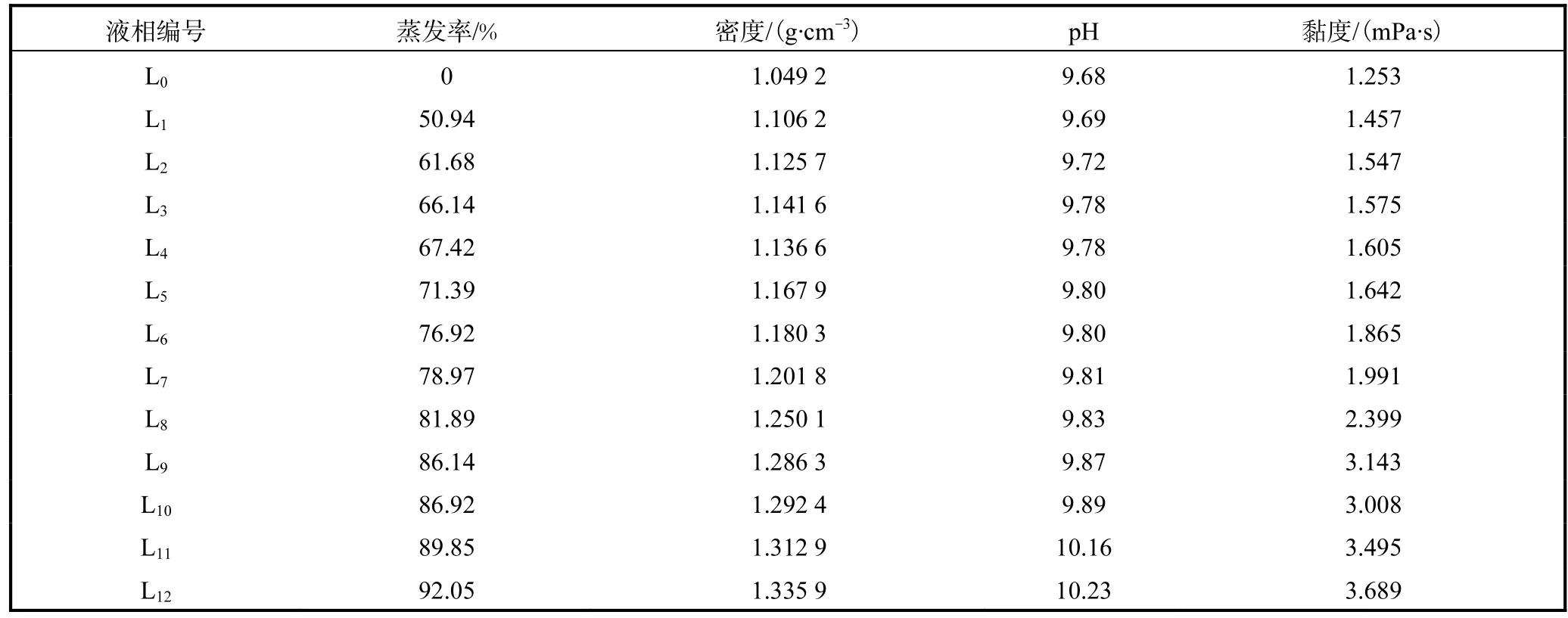
表3 卤水蒸发过程中液相的物化性质Tab. 3 Physicochemical properties of the liquid phase of the evaporation process of brine
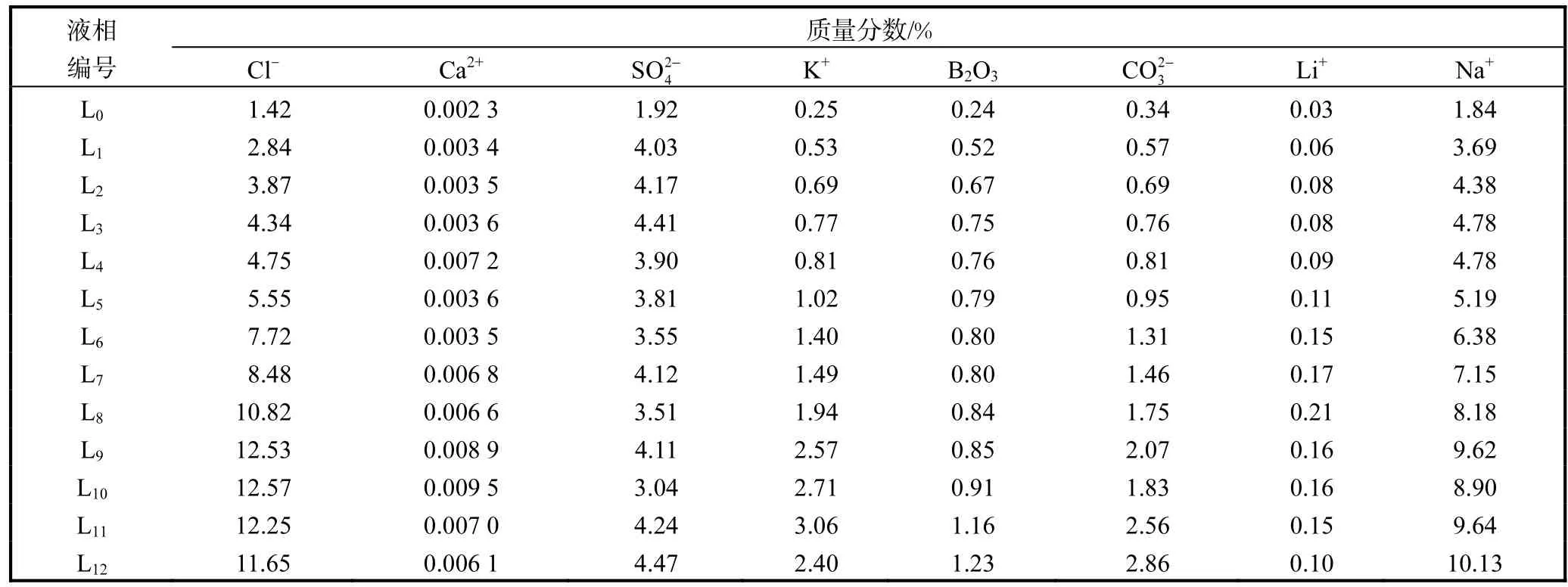
表4 拉果错盐湖卤水15℃蒸发液相组成Tab. 4 Chemical composition of the liquid phase of the Laguocuo brine at 15℃
2.2 主要盐类析出情况
母液中Na+、K+、Cl-、SO的质量分数与蒸发率关系如图1所示.
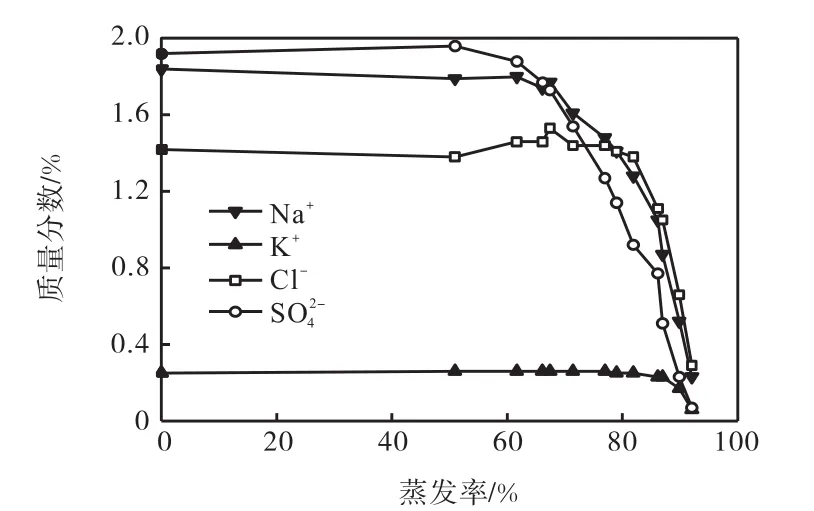
图1 母液中Na+、K+、Cl-、SO的质量分数与蒸发率关系Fig. 1 Relationship between mass fraction of Na+,K+,ClandSOin the mother liquor and the rate of evaporation
15℃蒸发过程中,在蒸发率达到87%之前,K+质量分数基本保持不变,蒸发率达到87%后,K+质量分数迅速降低,含钾盐类开始析出.
2.3 锂、硼的富集
2.3.1 锂的富集行为
拉果错湖水低Ca2+、Mg2+的特征易于Li2CO3提取,液相中主要元素Li+的蒸发富集行为如图2、图3所示.
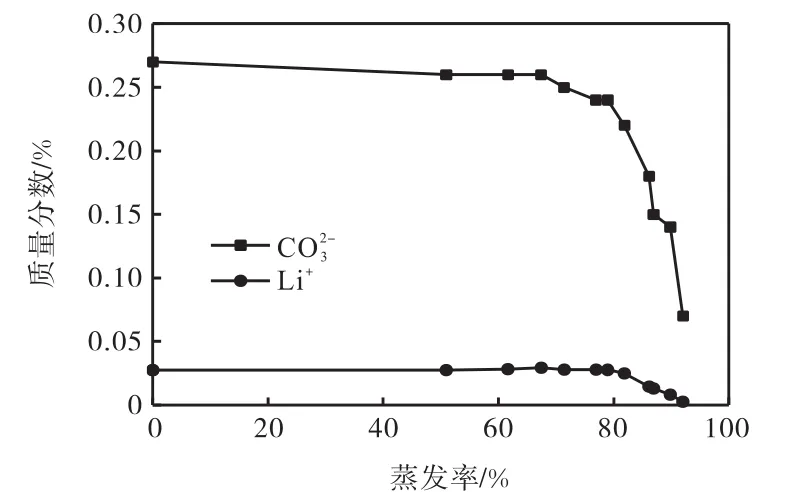
图2 母液中Li+、CO质量分数与蒸发率关系Fig. 2The relationship between mass fraction of Li+,COin the mother liquor and the rate of evaporation
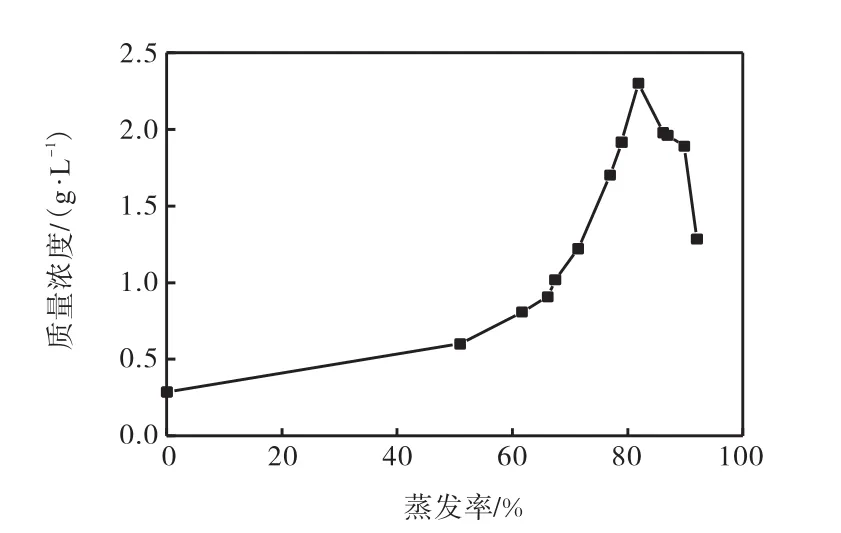
图3 母液中Li+质量浓度与蒸发率关系Fig. 3Relationship between lithium concentration in the mother liquor and the rate of evaporation
2.3.2 硼的富集行为
在蒸发过程中,液相中硼(以B2O3计)的变化行为如图4和图5所示.由图4可知:在卤水蒸发率小于67%的过程中,硼没有固相析出,当蒸发率达到67%左右,硼总量开始下降,说明有含硼固相析出.但由图5可知:随着蒸发率的增加,硼在母液中质量浓度一直在升高,说明在整个蒸发过程中,硼一直在富集,并且在实验区间质量浓度可达约15.92g/L,这主要是由于pH对溶液的影响,使得溶液中硼氧阴离子配合物的聚结形式不同.当8≤pH≤11,随着pH继续增加,硼饱和溶液中几种硼氧配阴离子的比例发生变化,硼氧配阴离子由低聚合度硼酸盐阴离子向高聚合度硼酸盐阴离子转变,为溶液中硼质量浓度的继续增加提供条件.
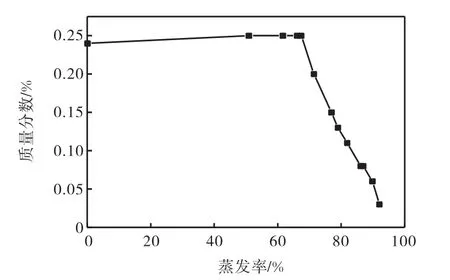
图4 母液中B2O3质量分数与蒸发率关系Fig. 4 Relationship between mass fraction of B2O3in the mother liquor and the rate of evaporation
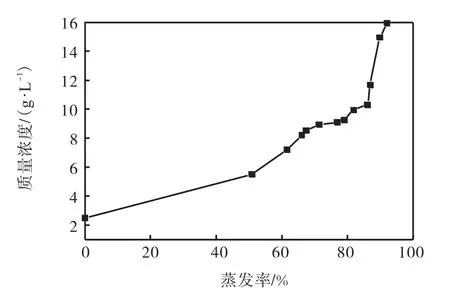
图5 母液中B2O3质量浓度与蒸发率关系Fig. 5 Relationship between B2O3concentration in the mother liquor and the rate of evaporation
2.4 相图分析
根据盐湖卤水和实验卤水的化学组成,可简化为Na+、K+//Cl-、SO–H2O四元水盐体系.由于文献没有该体系15℃相图,本文分别采用0℃和25℃,Na+、K+//Cl-、SO–H2O四元体系相图[10]来分析本实验蒸发析盐过程,结果如图6和图7所示.
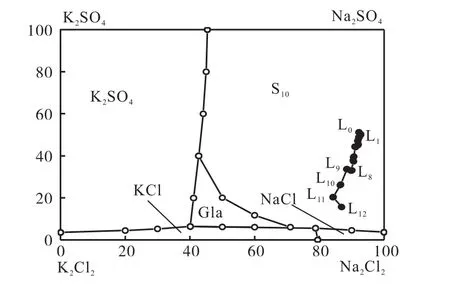
图6 Na+、K+//Cl-、SO-H2O四元体系0℃等温相图及蒸发结晶路线Fig. 6Phase diagram and crystallization path of the quinary system of Na+,K+//Cl-,SO-H2O at 0℃
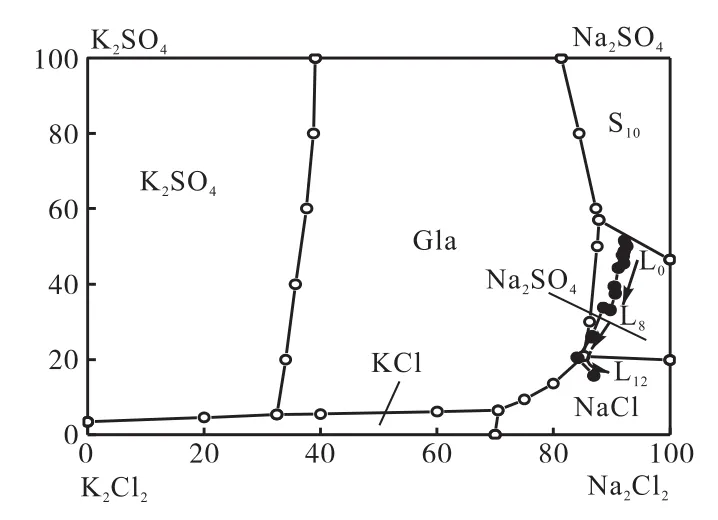
图7 Na+、K+//Cl-、SO-H2O四元体系25℃等温相图及蒸发结晶路线Fig. 7Phase diagram and cry stallization path of the quinary system Na+,K+//Cl-,SO-H2O at 25℃
由图6可见,在0℃相图中,整个系统轨迹完全处在芒硝(S10)相区,不能反映实验卤水蒸发析盐情况.通过与25℃相图(图7)比较和对实验结果分析,系统轨迹在25℃相图变化更与实验温度15℃接近,因此,实验结果采用25℃相图来分析.
从图7可以看出,Na+、K+//Cl-、SO-H2O四元水盐体系25℃相图包括6个相区,即:氯化钠、氯化钾、硫酸钠、芒硝、钾芒硝(Gla)以及硫酸钾区域.将本实验液相点标绘于该相图中,其变化趋势用箭头表示.由图7可知:实验卤水系统点L0位于Na2SO4相区,蒸发过程中多数液相点集中在Na2SO4相区内,随着蒸发率的增加,向Na2SO4、Gla和NaCl共饱点运动.而对相图进行理论分析可知,系统轨迹会沿着系统点L0与Na2SO4固相点直线连线向Na2SO4与Gla共饱线运动,两盐共析,然后沿着共饱线移动,到达Na2SO4、Gla及NaCl三相共饱点,直至蒸干.卤水实际系统轨迹与理论轨迹存在差异,主要是因为实验是在15℃条件下进行,其温度要比25℃低,实验卤水会形成自己独特的结晶路线.
3 结 论
钠盐在蒸发率达到52%时以硫酸钠形式析出,在蒸发率达到86%时氯化钠开始析出;钾盐在蒸发率87%之后才有钾盐析出,析出钾盐为硫酸钾和氯化钾.整个蒸发过程中,硼一直是处在富集状态,母液中硼的最高质量浓度可达15.92g/L;锂在蒸发率为82%时达到最高质量浓度2.30g/L,此后由于卤水中有CO存在,Li+会以Li2CO3形式析出.
[1] 昇于松. 西藏盐湖及其水系中的痕量金属[J]. 海洋与湖沼,1992,23(4):407–413.
[2] 刘俊英,郑绵平,罗健. 西藏拉果错卤虫:Ⅰ. 生物学特征[J]. 湖泊科学,1998,10(2):92–95.
[3] 姫连敏,李丽娟,张波,等. 我国硫酸盐型盐湖钾镁锂资源的分析工艺以及与犹他州合作领域的探讨[J]. 材料导报:纳米与新材料专辑,2011,25(专辑17):198–202.
[4] 程怀德,马海州. 我国硫酸盐型盐湖资源与开发现状[J]. 矿产保护与利用,2009(6):52–55.
[5] 纪律,林浩宇,程学业,等. 青海硫酸盐型钾矿资源制取硫酸钾工艺研究[J]. 化工矿物与加工,2003,32(6):5–7.
[6] 孙之南,郭绍珍. 海水蒸发浓缩析盐规律研究[J]. 海湖盐与化工,1985,14(4):1–8.
[7] Kılıc Ö,Kılıc A M. Recovery of salt co-products during the salt production from brine[J]. Desalination,2005,186(1/2/3):11–19.
[8] 左秉坚. 制盐工业手册[M]. 北京:中国轻工业出版社,1994:105–106.
[9] 中国科学院青海盐湖所分析室. 卤水和盐的分析方法[M]. 2版. 北京:科学出版社,1988.
[10] 牛自得,程芳琴. 水盐体系相图及其应用[M]. 天津:天津大学出版社,2002.
责任编辑:周建军
Salting-out Law of the Brine from the Laguocuo Salt Lake through Isothermal Evaporation at 15℃
WU Jingli,WANG Xuekui,DONG Jinggang,SHA Zuoliang
(College of Marine Science and Engineering,Tianjin University of Science & Technology,Tianjin 300457,China)
Laguocuo Salt Lake brine in Tibet was used in the research to study its enrichment behavior and the crystallization process through isothermal evaporation at 15℃,which can provide basic data for the utilization of the brine. The experiment showed that sodium sulfate began to precipitate when the evaporation rate reached 52%,and a large quantity of precipitation took place during the whole evaporation process;potassium began to precipitate when the evaporation rate reached 87%;the maximum mass concentration of Li+in the mother liquor was 2.30g/L when the evaporation rate was 82%;Li2CO3precipitated when it reached the dissolution equilibrium in the brine;boron began to precipitate when the evaporation rate reached 67% and the maximum mass concentration of B2O3in the mother liquor was 15.92g/L.
Laguouco;saltlake;salting-out law;phase diagram
TS352
A
1672-6510(2014)03-0049-04
10.13364/j.issn.1672-6510.2014.03.010
2013–09–03;
2013–12–10
天津市自然科学基金资助项目(12JCZDJC30000,12JCZDJC28200)
吴敬礼(1988—),男,山东枣庄人,硕士研究生;通信作者:董景岗,副教授,dongjinggang@tust.edu.cn.

