聚桂醇泡沫硬化剂治疗浅表静脉畸形的疗效及安全性分析
胡丽 黄惠真 马刚 仇雅璟 陈辉 金云波 胡晓洁 林晓曦 李伟
聚桂醇泡沫硬化剂治疗浅表静脉畸形的疗效及安全性分析
胡丽 黄惠真 马刚 仇雅璟 陈辉 金云波 胡晓洁 林晓曦 李伟
目的观察聚桂醇泡沫硬化剂治疗浅表静脉畸形的疗效与安全性。方法2013年1月至2014年4月,对17例浅表静脉畸形患者采用硬化治疗。采用Tessari法制作聚桂醇泡沫硬化剂(液气比为1∶4),其中聚桂醇注射液浓度为1%。治疗4周1次,末次治疗结束后1个月,根据病灶颜色和大小进行疗效评价,同时记录治疗过程中及治疗后的不良反应。结果17例患者平均治疗3.06次,治疗后5例病灶接近正常,7例明显好转,3例部分改善,2例轻度改善,无效0例;不良反应包括局部肿胀、疼痛、皮肤色素沉着。结论应用聚桂醇泡沫硬化剂治疗浅表静脉畸形,疗效肯定,无严重并发症,安全性高。
聚桂醇泡沫硬化治疗浅表静脉畸形
静脉畸形是一种较常见的先天性血管畸形,出生时表现不明显,随年龄增长而逐渐增大,不能自行消退[1]。临床表现与病灶的部位和大小相关,可表现为无症状的浅表静脉扩张,也可出现肢体肿胀、功能障碍甚至气道阻塞等[2]。血管内硬化治疗是治疗静脉畸形的一线方法[3],其中无水乙醇是目前最为有效的硬化剂,但是治疗风险高,严重并发症发生率高,用于浅表静脉畸形时易发生皮肤坏死,导致瘢痕形成[4-5]。近年来,多项研究报道应用聚桂醇泡沫硬化剂治疗静脉畸形,疗效肯定,并发症发生率低且无严重并发症出现[6-8]。本研究旨在探讨聚桂醇泡沫硬化治疗对于浅表静脉畸形的疗效和安全性。
1 资料和方法
1.1 临床资料
收集2013年1月至2013年12月,于我科血管瘤专科门诊就诊并确诊为静脉畸形,同时伴有浅表病灶的病例,统计人口学特征及病灶临床特征。所有
患者治疗前均行MRI检查,以明确病灶大小、范围和影像学特征,签署治疗知情同意书,治疗前后拍摄照片。本组共17例,男性5例,女性12例,年龄5~39岁,平均24.9岁;病灶部位包括面颈部4例,四肢7例,躯干6例,其中有3例患者同时存在深部病灶。排除标准:急性严重心脏病、急性肺部疾病以及发热患者。
1.2 配制泡沫硬化剂
使用2个5 mL注射器,分别抽取聚桂醇注射液(10 mL∶100 mg,陕西天宇制药有限公司)与空气,二者体积比为1∶4,三通管连接2个注射器,快速来回推送15~20次,使其呈现为白色细小泡沫状。现配现用。
1.3 治疗过程
治疗前开放静脉通道,滴加地塞米松5 mg,常规心电、血压及血氧饱和度监测。根据病灶位置,患者取平卧位或俯卧位,常规消毒铺巾。21号蝶翼套管针从病灶边缘进针,针尖与皮肤呈15°进入浅表病灶,可见静脉血回流,缓慢注入泡沫硬化剂,当病灶内充满泡沫、表面青紫色变浅时停止注射(图1),治疗结束后继续监测2~3 h后患者方可离开。单次用量视病灶范围而定,一般不超过10 mL。硬化治疗4周一次,治疗次数根据临床效果及患者主观满意度而定。对于3例伴有深部病灶患者同时采用无水乙醇进行血管内硬化治疗。

图1 左面部浅表VM聚桂醇泡沫硬化治疗中Fig.1Sclerotherapy with polidocanol foam for superficial VM on the left face
1.4 评价方法
根据病灶外观的改善情况将疗效分为5个等级。1级:0%清除,病灶对治疗无反应;2级:1%~25%清除,病灶颜色、体积改善不明显;3级:26%~50%清除,病灶颜色稍淡化,体积略有;4级:51%~90%清除,病灶颜色淡化明显,体积缩小明显;5级:>90%清除,病灶基本接近正常。由未参与研究的两位血管瘤专科医生根据术前术后照片进行评价。同时记录治疗过程中及治疗后出现的并发症。末次治疗结束后1个月、3个月门诊随访。
2 结果
2.1 治疗效果
所有患者均完成治疗及治疗后随访。本组患者治疗次数为1~6次,平均3.06次;聚桂醇单次用量为0.6~7.2 mL,平均3.11 mL;治疗结束后1个月评价疗效发现,17例患者中疗效达到5级有5例(29.4%),4级7例(41.2%),3级3例(17.6%),2级2例(11.8%),1级0例(0%)。治疗后3个月随访未见病灶复发(图2、3)。
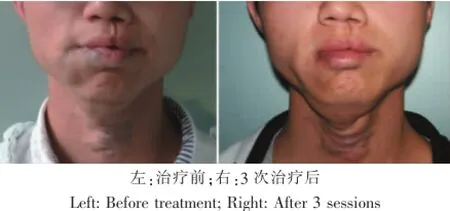
图2 典型病例:下颌颈部静脉畸形Fig.2Typical case:VM in the jaw and neck
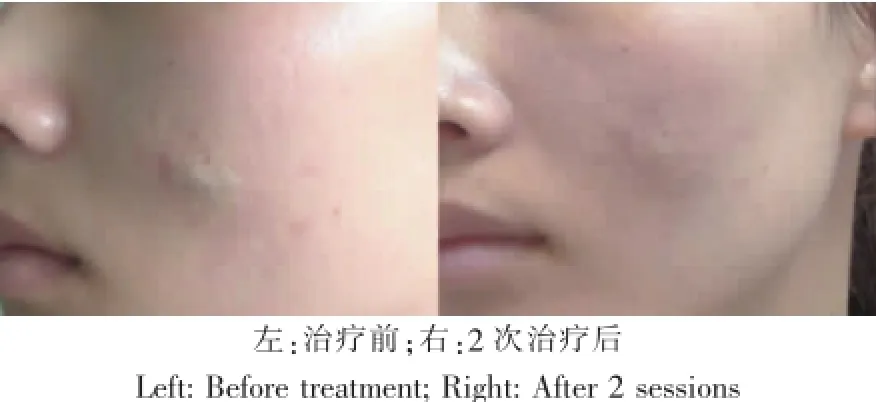
图3 典型病例:左面部浅表静脉畸形。Fig.3Typical case:Superficial VM on the left face
2.2 并发症
本组患者均未出现严重并发症。17例患者治疗后均发生局部肿胀,一般持续3~7 d,15例患者主诉治疗过程疼痛;此外,2例患者在治疗3~5次后表面出现色素沉着,3个月随访时有改善。
3 讨论
目前静脉畸形的治疗仍是一个临床难题。手术切除通常导致脉管畸形和运动功能丧失,特别当病灶累及重要结构时会导致神经损伤。事实上,受到功能和解剖结构的限制,完整切除病灶难以实现,而切除不完全容易导致病灶复发。采用血管内硬化治疗时,硬化剂可以破坏畸形血管的内皮细胞,血栓形成,最后使病灶纤维化[9]。因此,相较于手术而言,血管内硬化治疗对于静脉畸形疗效更好。
目前,临床上用于治疗静脉畸形的硬化剂多种多样,无水乙醇应用最为广泛,同时也是复发率最低的[10-11]。Svendsen等[11]使用无水乙醇治疗静脉畸形,84%患者都取得了极好或良好的疗效;Yakes等[12]应用无水乙醇治疗经其他方法失败的静脉畸形患者,其中95%病灶都得到了持续的改善。虽然无水乙醇是目前最有效的硬化剂,但其并发症应引起重视。Lee等[13]曾经报道,在30例患者的98次无水乙醇硬化治疗中,出现9例缺血性大疱,2例组织坏死,1例深静脉血栓,1例肺栓塞以及5例神经麻痹;Berenguer等[14]也报道过1例患者在治疗过程中出现一过性呼吸困难。
2000年,Tesari等[15]报道了一种能够产生稳定泡沫硬化剂的制作方法,泡沫硬化治疗逐渐获得推广。Pascarella等[16]应用聚桂醇泡沫硬化治疗14例静脉畸形,疗效肯定,治疗过程痛苦小,短期效果维持良好;Mimura等[17]应用聚桂醇泡沫硬化治疗伴有疼痛的静脉畸形,病灶体积缩小,疼痛感明显降低。聚桂醇与无水乙醇作用机理类似,效果有所不及,但并发症较少。其并发症可分为轻微并发症和严重并发症,前者包括疼痛、肿胀、血肿、皮肤坏死、可逆性神经损伤,后者包括过敏反应、肾脏衰竭、呼吸困难、胸痛和深静脉血栓等[7]。
本研究针对浅表静脉畸形,主要考虑的是皮肤副作用。硬化治疗造成的常见皮肤副作用包括皮肤结痂、破溃、坏死、瘘管以及色素沉着等,而在这些不良反应中,由无水乙醇造成的比例最高为15.5%,聚桂醇则为9.2%[18]。本研究选择聚桂醇泡沫硬化治疗,除了暂时性的肿胀、疼痛和色素沉着外,并未出现其他皮肤副作用和严重并发症。因此,掌握聚桂醇泡沫硬化剂的剂量,应不会引起额外皮肤损伤。
综上所述,我们聚桂醇泡沫硬化治疗浅表静脉畸形疗效肯定,安全性高,可成为浅表静脉畸形治疗的首选方法。
[1]Mulliken JB,Glowacki J.Hemangiomas and vascular malformations in infants and children:a classifi cation based on endothelial characteristics[J].Plast Reconstr Surg,1982,69(3):412-422.
[2]Legiehn GM,Heran MK.Venous malformations:classification, development,diagnosis,and interventional radiologic management [J].Radiol Clin North Am,2008,46(3):545-597.
[3]Gurgacz S,Zamora L,Scott NA.Percutaneous sclerotherapy for vascular malformations:a systematic review[J].Ann Vasc Surg, 2014,28(5):1335-1349.
[4]Lee CH,Chen SG.Direct percutaneous ethanol instillation for treatment of venous malformation in the face and neck[J].Br J Plast Surg,2005,58(8):1073-1078.
[5]Lee BB,Do YS,Byun HS,et al.Advanced management of venous malformation with ethanol sclerotherapy:mid-term results[J].J Vasc Surg,2003,37(3):533-538.
[6]Saito N,Sasaki S,Sekido M,et al.Efficacy of polidocanol sclerotherapy for capillary malformation with masked venous malformation[J]. Dermatol Surg,2009,35(1):161-164.
[7]Blaise S,Charavin-Cocuzza M,Riom H,et al.Treatment of low-flow vascular malformations by ultrasound-guided sclerotherapy with polidocanol foam:24 cases and literature review[J].Eur J Vasc Endovasc Surg,2011,41(3):412-417.
[8]Górriz-Gómez E,Vicente-Barrero M,Loras-Caballero ML,et al. Sclerotherapy of face and oral cavity low flow vascular malformations: our experience[J].Br J Oral Maxillofac Surg,2014,52(1):43-47.
[9]de Lorimier AA.Sclerotherapy for venous malformations[J].J Pediatr Surg,1995,30(2):188-193.
[10]Yakes WF,Haas DK,Parker SH,et al.Symptomatic vascular malformations:ethanol embolotherapy[J].Radiology,1989,170(3 Pt 2):1059-1066.
[11]Svendsen P,Wikholm G,Fogdestam I,et al.Instillation of alcohol into venous malformations of the head and neck[J].Scand J Plast Reconstr Surg Hand Surg,1994,28(4):279-284.
[12]Yakes WF,Luethke JM,Parker SH,et al.Ethanol embolization of vascular malformations[J].Radiographics,1990,10(5):787-796. [13]Lee BB,Kim DI,Huh S,et al.New experiences with absolute ethanol sclerotherapy in the management of a complex form of congenital venous malformation[J].J Vasc Surg,2001,33(4):764-772.
[14]Berenguer B,Burrows PE,Zurakowski D,et al.Sclerotherapy of craniofacial venous malformations:complications and results[J]. Plast Reconstr Surg,1999,104(1):1-11.
[15]Tessari L,Cavezzi A,Frullini A.Preliminary experience with a new sclerosing foam in the treatment of varicose veins[J].Dermatol Surg,2001,27(1):58-60.
[16]Pascarella L,Bergan JJ,Yamada C,et al.Venous angiomata: treatment with sclerosant foam[J].Ann Vasc Surg,2005,19(4): 457-464.
[17]Mimura H,Fujiwara H,Hiraki T,et al.Polidocanol sclerotherapy for painful venous malformations:evaluation of safety and efficacy in pain relief[J].Eur Radiol,2009,19(10):2474-2480.
[18]Qiu Y,Chen H,Lin X,et al.Outcomes and complications of sclerotherapy for venous malformations[J].Vasc Endovascular Surg,2013,47(6):454-461.(收稿日期:2014年6月12日;修回日期:2014年7月10日)
Efficacy and Safety of Sclerotherapy with Polidocanol Foam for Superficial Venous Malformation
ObjectiveTo investigate the efficacy and safety of sclerotherapy with polidocanol foam in the treatment of superficial venous malformation(VM).MethodsFrom January 2013 to April 2014,17 superficial VM patients were treated by sclerotherapy.The polidocanol foam was produced by Tessari’s method(liquid∶air=1∶4).The concentration of polidocanol used was 1%.Sclerotherapy was repeated at an interval of 4 weeks.Therapeutic outcomes were evaluated by color and size of lesions.Side-effects were both recorded during treatment and after treatment.ResultsThe average number of sessions was 3.06.The results were excellent in 5 cases,good in 7 cases,fair in 3 cases and poor in 2 cases.Side effects including swelling,pain and transient hyperpigmentation were observed.ConclusionSclerotherapy with polidocanol foam for superficial venous malformation is effective and safe without severe side effects.
Polidcanol;Foam sclerotherapy;Superficial venous malformation
R732.2
A
1673-0364(2014)04-0196-03
HU Li,HUANG Huizhen,MA Gang,QIU Yajing,CHEN Hui,JIN Yunbo,HU Xiaojie,LIN Xiaoxi,LI Wei.
Department of Plastic and Reconstructive Surgery,Shanghai Ninth People's Hospital,Shanghai Jiaotong University School of Medicine,Shanghai 200011,China.Corresponding author:LI Wei(E-mail:liweiboshi@163.com).
国家自然科学基金(81071565);上海市卫生系统重要系统联合攻关重点项目(2013ZYJB0014)。
200011上海市上海交通大学医学院附属第九人民医院整复外科。
李伟(E-mail:liweiboshi@163.com)。
10.3969/j.issn.1673-0364.2014.04.006

