纳米金自催化生长及其应用研究
杨西萍,展宗瑞
(兰州石化职业技术学院应用化学工程系,甘肃兰州 730060)
纳米金自催化生长及其应用研究
杨西萍,展宗瑞
(兰州石化职业技术学院应用化学工程系,甘肃兰州 730060)
介绍了纳米金基因探针的制备方法,对小尺寸纳米金的自催化性能进行了分析研究,在此基础上,探讨了纳米金自催化机理放大光学信号及其在光学传感器方面的应用价值。
纳米金;自催化生长;抗坏血酸;基因探针
21世纪,由于纳米技术的飞速发展,纳米材料被广泛的应用到各个领域,产生了巨大的经济效益和社会价值。而纳米尺寸的金颗粒(AuNPs),以其良好的粒子分散效应,纳米尺寸效应,表面效应,光谱吸收效应以及自催化效应,成为当前纳米学界乃至整个科学界的研究热点[1]。近几年,由于纳米技术的深入发展,研究发现,小尺寸的纳米金(小于10 nm)表现出较高的催化活性,打破了认为金没有催化活性的传统观念,致使人们对其催化特性产生了极大的关注兴趣[2]。而从经济角度上来看,金的价钱要远远低于铂和钯,正是由于这些原因使得金催化剂的研究已经成为催化领域中的一个新的热点。目前有关纳米金微粒的研究日趋活跃,但由于实验条件和方法的不同存在很多争议,对其催化活性影响的本质原因尚在探讨之中,关于其高催化活性的原因,较多研究工作结论将其归结于量子尺寸效应[3]。当金属粒子小到一定程度以后,金属本身的电子性质将发生变化,从而导致其化学和物理性质出现突变。例如,局域表面等离子体共振效应(LSPR),并且对光具有很强的吸收和散射特性。研究显示,纳米金所表现出来的这些独特的光学性质,与纳米颗粒的形状、结构、尺寸有直接的关系,对周围介质极其敏感,在传感技术领域的推广应用具有极为重要的意义。这里重点探讨小尺寸纳米金颗粒的自催化效应,尤以其特殊光学性质及独特的生物亲和性,被广泛用来标记细胞、DNA等生物大分子[4,5],通过纳米金自催化生长后的纳米微粒,其光学信号显著增强,可显著提高光学传感器件的检测灵敏性[6]。在用于临床诊断的光学传感器发展历程中,纳米金传感器因其灵敏性高,寿命长,功能多而被广泛应用于各种电学和光学生物检测平台。在这里,就近年关于纳米金自催化机理的本质,及其放大生物探针信号的过程进行分析,并对其在生物检测及临床诊断方面的应用价值一并进行展望。
1 纳米金
1.1 纳米金胶体的形成过程
迄今为止,已有很多关于纳米金合成方法的研究报道,较多采用柠檬酸钠还原氯酸金的方法,合成纳米金溶液[7]。通过调整还原剂量及种类,还原金盐(HAuCl4)的方法,在保护剂或者静电斥力等作用下,就可以合成出不同粒径不同形状的多分散纳米金颗粒。图1所示为金离子被还原为纳米金的过程:在加入还原剂之前,溶液为100%金盐溶液,图表的纵座标显示出,随着还原剂的加入,金离子被还原成原子的进程,金原子量在明显激增之后,会达到过度饱和状态,随后开始团聚,即所谓成核阶段,由11个金原子快速团聚形成二十面体形的金核晶体,而溶液中的其余金原子则按照能量递减的梯度一次吸附在金核外围。在定量的金盐溶液中,一开始所形成的晶核越多,最终所得到的金纳米粒子尺寸越小。所以,可以通过控制还原剂用量,来合成不同尺寸粒径的金纳米颗粒。通过控制反应条件,若能实现快速成核,就可得到尺寸均一的单分散纳米金胶体颗粒。单个胶体金颗粒由中心的纳米胶团以及其周围的负电荷层包裹而成,由于此电荷斥力,纳米金颗粒可以长期稳定的分散开来,避免团聚形成沉淀,而此电荷层的厚度则取决于周边体系中离子浓度高低。反之,若实验条件控制不当,往往得到的是不规则的多分散纳米金胶体颗粒,比如椭圆形、三角形、矩形、菱形等。

图1 金离子被还原继而形成纳米金的过程Figure 1 Process of reducing gold ions and then the formation of gold nanoparticles
1.2 纳米金颗粒尺寸优选
一般情况下,粒径越大,团聚过程中的颜色变化越明显,比如,肉眼很难观察到粒径为1 nm的金颗粒,而当粒径增大至5 nm以上,至40 nm时,则会很容易观察到桃红色。随着粒径增大,空间位阻效应越为显著。从可见性及空间位阻两方面综合考虑,一般用于生物大分子标记纳米金颗粒,粒径通常在40 nm左右,但有些情况下,为避免空间位阻的干扰,尤其是在DNA检测应用中,为保证较高的杂交效率,多选用小尺寸,因其溶液浓度高,分散性好,纳米金颗粒表面更有利于耦合生物大分子,10~20 nm的纳米金颗粒常用来修饰标记生物探针,一般可通过共价键或者吸附作用将标记核苷酸耦合在纳米金胶粒上。图2显示,通过控制还原剂加入量,可以合成出不同粒径的球状纳米金颗粒,在波长520 nm附近出现纳米金颗粒的等离子共振紫外吸收特征峰,此吸收峰的位置、形状与纳米金颗粒的大小、形状与分散状态密切相关[8]。随着还原剂柠檬酸钠用量的增大,吸收峰的位置向短波方向移动。随着粒径增大,金溶胶的紫外-可见吸收光谱峰展宽且向长波方向移动。研究结果表明,紫外-可见吸收光谱不仅可以用来表征纳米金颗粒的光学性质,其粒径大小与分布也可以体现出来。
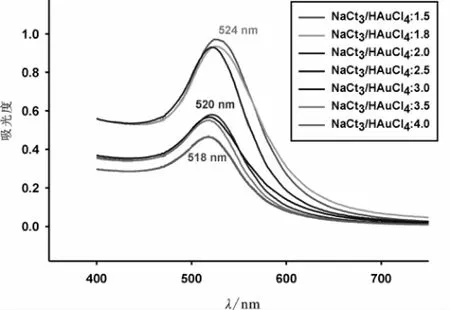
图2 不同还原条件下合成不同粒径金纳米颗粒的紫外-可见吸收光谱Figure2 UV-visible absorption spectrum of the syn thesized gold nanoparticles w ith different sizes under different reduction conditions
2 纳米金自催化生长
2.1 均相体系中纳米金自催化生长
图3显示金盐溶液被还原并形成纳米金颗粒的过程。先前关于纳米金自催化生长的报道主要集中在NH2OH,H2O2,NADH,还原剂上,这里我们分析弱还原剂AA(抗坏血酸维C)还原金离子促进纳米金生长过程,纳米金最终可增大至溶液中金离子消耗完毕,随着粒径增大,其特征吸收峰变化可通过紫外-可见光谱直接测出,最终的吸光度值依赖于纳米金核数量,当用其来标记生物探针时,即可随之确定待测标本中的目标生物分子量。利用纳米金自催化生长原理,原始纳米金胶核作为晶种,自身扮演催化剂及成核中心角色,为避免生长过程中新核的产生,在金盐生长溶液中,加入弱还原剂抗坏血酸维C,在没有加晶种溶液之前,它的还原性不足以将溶液中的Au3+先还原为Au°,当加入晶种溶液后,反应开始,抗坏血酸维C即表现出还原性,将溶液中的Au3+先还原为Au+,再随即还原为Au°,并使其沉积附着在纳米金胶核上,随着粒径增大,其吸光强度随之增强,在此自催化过程中,生长时间及体系中金离子浓度将决定最终纳米金微粒尺寸大小,以期来放大信号,提高检测灵敏度,在新型光学传感器的开发研究领域表现出良好的应用价值。可用来标记检测无机分子,有机分子,生物大分子及细胞等临床诊断中。
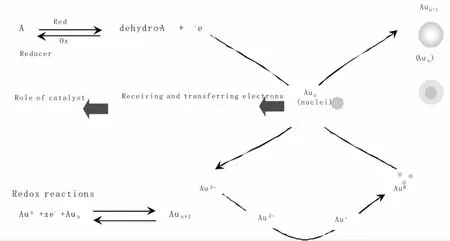
图3 还原剂还原金盐HAuCl4及其在纳米金核表面的沉积过程Figure 3 Gold salt HAuCl4reduced by reducing agent and its deposition p rocess in the nuclear surface of gold nanoparticles
2.2 纳米金自催化生长的动力学过程研究
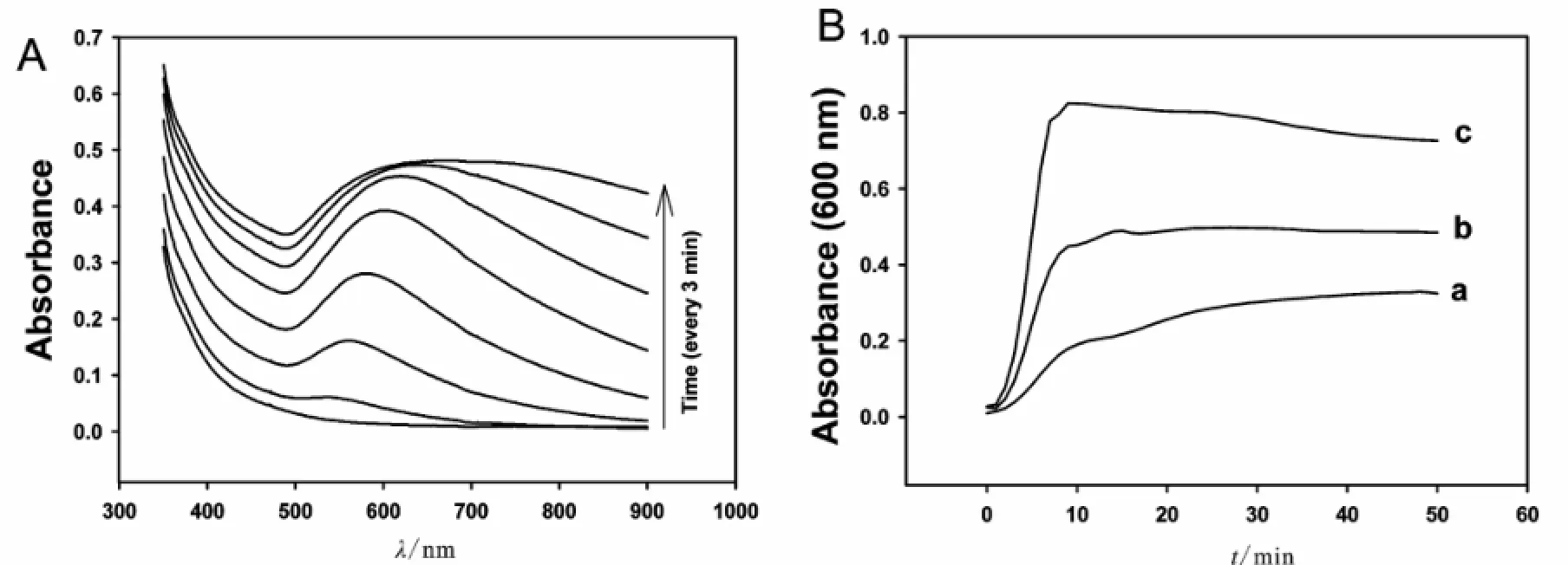
图4 A:纳米金自催化生长过程的紫外吸收光谱(间隔3m in扫描一次)。B:不同初始浓度纳米金核自催化过程的动力学行为研究。(生长溶液:0.25mmol/L HAuCl4,10mmol/L AA,and 0.1mol/L CTAB;初始浓度:a=3.5 pmol/L;b=8.75 pmol/L;c=17.5 pmol/L)Figure4 A:UV absorption spectrum of the growth process of self-catalyzed gold nanoparticles(scan interval of threeminutes).B:dynamic behavior of self catalysis process of nanogold nucleuswith different initial concentration(Growth solution:0.25mM HAuCl4,10mM AA,and 0.1M CTAB;initial concentration:a=3.5 pM;b=8.75 pM;c=17.5 pM)
图4A所示。自催化生长依赖于生长时间及金核种子初始浓度,在催化开始20 min后,吸光强度值不再上升,该过程显示纳米金颗粒的光学性质取决于其粒径及形状,相对于初始金核,显示出明显的红移,在生长过程导致少许团聚[9],而最终的吸光强度则跟初始金核浓度成正比。通过对晶种生长法反应过程的系统研究,发现恒定晶种量,通过调节生长溶液的量即可控制合成不同粒径或形貌的金纳米颗粒。该实验数据表明:pH为11时,维C作为还原剂,CTAB作为表面活性剂,纳米金微粒可快速生长成大粒径胶体金,而还原剂及金盐量则决定了生长时间和最终特征吸收峰位置,以此可以优选自催化条件,设计相关实验步骤定量分析生物大分子,将其应用于纳米金标记的光学传感器,来放大检测信号,提高其检测灵敏度。由图4B看出,当用优选出的生长时间和吸光强度去调查纳米金的自催化生长行为时,可以清楚的看到,其生长速率明显依赖于纳米金核的初始浓度,为定量分析提供了坚实的理论依据,由此可以检测出一系列不同浓度的目标分析物,做出相应的标准曲线,实现该方法的应用价值。
3 展望
综上所述,进一步探究纳米金催化剂的自催化本质并拓宽其实际应用范围,将成为新的研究热点,为开发各种新的纳米金自催化化学反应或提高光学传感器检测限提供了新的可能,实现以相对简单,价廉,易操作的紫外-可见分光光度计来快速定量分析生物大分子,尤其对于一类癌变基因序列的检测,有望开发并应用于下一代基因传感器,从而为临床诊断及前期治疗提供数据参考。
[1] 张立德,牟季美.纳米材料和纳米结构[M].北京:北京科学出版社,2001.
[2] 王路存,苏方正,黄新松,等.高性能纳米金催化剂的研究进展[J].石油化工,2007,36:869-875.
[3] Valden M.Lai X,Goodman D W.Onset of catalytic activity gold clusters on titania with appearance of nonmetallic properties[J].Science,1998,281:1647-1650.
[4] Han M S,Lytton-Jean A K R,Mirkin CA.Colorimetric Screening of DNA-Binding Molecules with Gold Nanoparticle Probes[J].Angew Chem Int Ed,2006,45:1807-1810.
[5] Zhang J,Song SP,Wang L H,et al.A gold nanoparticle-based chronocoulometric DNA sensor for amplified detection of DNA[J].Nat.Protocals.2007,2:2888-2895.
[6] Zhan Z,Cao C,Sim S J.Quantitative detection of DNA by autocatalyticenlargenment of hybridized gold nanoprobes[J],Biosens.Bioelectron,2010,26:511-516.
[7] Grabar KC,Freeman RG,Hommer M B,etal.Preparation and characterization of Au colloid monolayers[J].Anal Chem,1995,67:735-743.
[8] 谢娟,王延吉,李艳廷,等.粒径可控纳米金的制备及表征[J].黄金,2008(7):3-6.
[9] Noguez C.Surface plasmons on metal nanoparticles:The influence of shape and physical environment[J]. JPhys Chem C,2007,111:3806-3819.
Self-catalytic G row th of Gold Nanoparticles and Their Application
YANG Xi-ping,ZHAN Zong-rui
(Departmentof Applied Chemical Engineering,Lanzhou Petrochemical College of Vocational Technology,Lanzhou 730060,China)
Themethod of the preparation of gold nanoparticles was outline,and the self-catalytic mechanism of the gold nanoprobeswaswell explained.On this basis,signal enhancements in the absorbance intensity and kinetic behavior for gold enlargenment have been well investigated,and the potential contribution to the development of the optical biosensor was also expected.
Nano gold;Self-catalytic growth;Ascorbic acid;Gene probe
TP212.3;TB383.1
: A
: 1004-275X(2014)01-0030-04
12.3969/j.issn.1004-275X.2014.01.008
收稿:2013-05-14
杨西萍(1966-)女,甘肃兰州人,副教授,从事有机化工的教学及研究工作。

