类风湿关节炎相关间质性肺疾病的CT影像特点
曲 丹,徐小嫚,马 跃,赵 立
类风湿关节炎(rheumatoid arthritis,RA)是以对称性多关节炎为主要表现的异质性、系统性、自身免疫性疾病,其病理基础是滑膜炎。RA患者除关节症状外,病变还可累及皮肤、眼、心脏及肺等多器官。肺脏有丰富的结缔组织和血供,是经常受累的器官之一。19%~44%的RA患者存在肺间质病变,即类风湿关节炎相关间质性肺疾病(rheumatoid arthritis-associated interstitial lung disease,RA-ILD)[1-2]。RA-ILD早期因无明显临床表现易被忽略,晚期出现肺纤维化后常因呼吸衰竭或合并肺部感染而死亡,预后较差。因此早期诊断及治疗RA-ILD有重大的临床意义。本研究旨在探讨RA-ILD患者的CT影像特点,以提高对其认识,利于早期诊断及合理治疗,改善预后。
1 对象与方法
1.1 研究对象 选择2008—2013年中国医科大学附属盛京医院收治的确诊为RA-ILD患者32例,其中男8例,女24例;年龄56~68岁,平均(62.3±8.5)岁;病程14~36 d,平均(18.9±5.3)d;3例合并高血压,3例合并糖尿病,1例合并脑血管疾病,2例合并冠心病,1例合并肺气肿、肺大疱。
1.2 诊断标准 RA诊断符合1987年美国风湿病学会(ACR)中的RA分类标准[3]。ILD诊断符合2000年美国胸科协会/欧洲呼吸协会(ATS/ERS)中的特发性肺间质病变临床诊断标准[4],排除其他肺部并发症,如肺及胸膜感染、肺结核、慢性阻塞性肺疾病、支气管扩张和肺部肿瘤等。
1.3 CT检查 采用Philips Brilliance 40和Philips Mx8000 IDT CT扫描仪,层厚3 mm,层间距3 mm。CT图像由1名放射科专家和1名呼吸科专家分别进行回顾性分析,2名医师判断结果不同时经协商讨论达成一致意见。评价指标包括病变类型、病变部位、病变范围等。病变类型包括网格影、渗出斑片浸润/实变影、磨玻璃影、蜂窝状影、结节影、肺气肿及胸腔积液。
2 结果
2.1 病变类型 32例患者中,14例(43.8%)CT表现为网格影,12例(37.5%)渗出斑片浸润/实变影,6例(18.8%)磨玻璃影,6例(18.8%)蜂窝状影,4例(12.5%)胸腔积液,2例(6.2%)肺气肿,1例(3.1%)空洞性结节。
2.2 病变部位 患者均为双肺同时受累,各个肺叶的受累情况分别为:左肺上叶4例(12.5%),左肺下叶32例(100.0%),右肺上叶4例(12.5%),右肺中叶14例(43.8%),右肺下叶32例(100.0%)。
2.3 病变范围 12例(37.5%)累及2个肺叶,14例(43.8%)累及3个肺叶,4例(12.5%)累及5个肺叶。
2.4 治疗中的CT表现 患者最初均经系统抗炎治疗,但肺内病变均无明显吸收,16例(50.0%)患者影像呈进行性发展(见图1、2),应用糖皮质激素治疗2周后患者影像均有不同程度吸收,其中以网格影及蜂窝状影表现为主的影像仅2例(10.0%)略有吸收,而以渗出斑片浸润/实变影及磨玻璃影为主的患者有16例(88.9%)吸收明显(见图3),其中1例患者在病情好转及渗出斑片浸润/实变影明显吸收后肺内出现空洞性结节(见图4、5),1例合并肺气肿、肺大疱的患者治疗过程中出现自发性气胸,伴纵隔气肿及皮下气肿(见图6、7)。
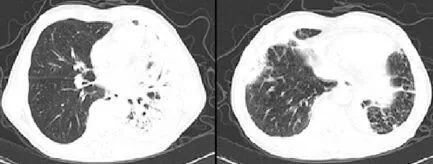
图1 入院时双肺渗出斑片浸润/实变影,左肺严重,内可见支气管充气征和肺气肿
Figure1 On admission,oozing plaques infiltration/consolidation shadows were found in both lungs,lesions in the left lung were heavier,and air bronchogram and emphysema can be seen

图2 系统抗炎后左肺影像似略有吸收,右肺下叶出现新发病变
Figure2 Mild absorption can be found in the left lung after systematic anti-inflammatory treatment,new lesions appeared in the right lower lung

图3 经激素治疗后双肺渗出斑片影/实变影明显吸收
Figure3 Oozing plaques infiltration/consolidation in both lungs was absorbed obviously after glucocorticoid hormones treatment

图4 入院时双肺多发渗出斑片影/实变影及磨玻璃影
Figure4 Bilateral pulmonary multiple oozing plaques infiltration/consolidation shadows and ground-glass opacity shadows on admission
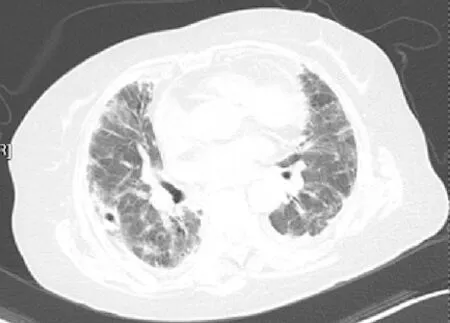
图5 激素治疗后肺内病变明显吸收,但出现空洞性结节
Figure5 The lesions in lungs were absorbed obviously after glucocorticoid hormones treatment,but an empty nodule appeared

图6 入院时双肺多发渗出影/实变影,可见肺气肿及肺大疱
Figure6 Bilateral pulmonary multiple effusion/consolidation shadows,emphysema and bullae of lung can be seen

图7 激素治疗后双肺多发渗出影及实变影明显吸收,但出现气胸,伴纵隔气肿及皮下气肿
Figure7 Bilateral pulmonary multiple effusion/consolidation shadows were absorbed obviously after glucocorticoid hormones treatment,but pneumothorax appeared,accompanied by pneumomediastinum and subcutaneous emphysema
3 讨论
RA患者可见的肺部损害有胸膜炎、间质性肺炎、类风湿结节、卡布兰综合征(Caplan′s syndrome)、肺血管炎及肺动脉高压等。RA-ILD是RA患者肺部受累常见的表现形式。RA-ILD患者早期呼吸系统症状不明显,因此容易忽略,错过早期诊断和治疗的最佳时期,晚期出现间质性肺炎后预后极差,是RA患者重要的死因之一[5]。RA-ILD发病机制尚未完全清楚,可能与遗传因素、免疫损伤、应用抗风湿药物等有关,涉及细胞、细胞因子及细胞外基质等因素间的相互作用,是多因素、多环节参与的复杂过程[6-7]。RA-ILD预后较差,诊断后的中位生存期是2.6~3.0年,故一旦发现应尽早治疗。
RA-ILD的诊断较为困难,即便已确诊为RA的患者,当出现呼吸系统症状及异常的胸部影像时,也需要鉴别是由于应用了糖皮质激素或细胞毒类药物引起的继发肺部感染还是RA本身对肺的累及。若各种抗感染药物治疗无效,而糖皮质激素治疗有效时,提示是RA-ILD而不是肺部感染。必要时可行纤维支气管镜检查、支气管肺泡灌洗及肺穿刺活检。目前肺活检是诊断RA-ILD的金标准,但由于RA-ILD患者病情在较长时间内保持稳定,且多数病理类型为寻常性间质性肺炎(UIP),不建议常规行肺活检,认为如有典型的高分辨率CT(HRCT)改变,结合RA病史,排除其他肺部疾病后即可考虑诊断为RA-ILD[8]。
本组患者均因发热、咳嗽、呼吸困难及肺CT异常影像收入呼吸科病房,1例患者因严重呼吸衰竭行有创机械通气入住呼吸科重症监护室。因患者均有RA病史,入院时均考虑到RA-ILD可能,但不能排除肺部感染或其他肺部疾病,故未直接诊断为RA-ILD,而是给予系统抗炎治疗,患者病情均无改善,肺CT影像无改善或呈进行性发展,实验室检查排除其他肺部疾病,结合患者RA病史及ILD诊断标准,诊断为RA-ILD,给予全身糖皮质激素治疗,患者病情及肺CT影像均有不同程度改善,明确诊断为RA-ILD。
RA-ILD以男性多见,男∶女为1.5~2.0∶1.0,而一般RA中,男∶女为1.0∶1.5~3.0。本研究32例患者则以女性多见,男∶女为1∶3。多数RA-ILD患者肺病变在关节炎发作3~10年后出现,少数先于关节炎。陈进伟等[9]研究显示,RA病程较长,红细胞沉降率(ESR)、C反应蛋白(CRP)、抗环胍氨酸抗体(CCP)、类风湿因子(RF)等炎性活动指标较高患者易并发ILD。Lee等[10]研究结果显示,吸烟、男性、发病年龄大、病程长、病程活动度高和病情严重时RA-ILD的危险因素。RA-ILD的主要症状是进行性呼吸困难和干咳,HRCT能清楚地显示肺部病变。网状影和蜂窝肺是RA-ILD最常见的肺CT征象,病变早期以磨玻璃影为主要征象,提示存在肺泡炎且经过恰当的治疗可以逆转,而网格影、蜂窝样改变提示不可逆的肺间质纤维化[11-12]。Tanaka等[13]提出,RA-ILD的HRCT呈现4种主要影像学模式,UIP样模式为双侧胸膜下网格影伴或不伴蜂窝样改变;非特异性间质性肺炎(NSIP)样模式以磨玻璃影为主;炎症性气道疾病模式为小叶中心性线样影伴或不伴支气管扩张;机化性肺炎(OP)样模式为实变影。Lee等[10]研究表明,UIP是RA-ILD最常见的类型,占56%,其次为NSIP(33%)、OP(11%)。本研究结果表明,32例患者中,CT表现为UIP占43.8%,NSIP占18.8%,OP占37.5%。OP特点为发热,CT表现为多发性渗出斑片浸润/实变影,患者初诊常被诊断为肺炎而收入呼吸科病房,很难直接诊断为RA-ILD,因此OP患者所占比例较大。
本研究中1例患者入院时肺部病变为双肺多发渗出实变影,予亚胺培南/西司他汀盐及莫西沙星抗炎后病情无好转,呼吸困难加重,并行气管插管机械通气治疗。加用激素后,患者退热,呼吸困难减轻,1周后脱机,复查肺CT见双肺多发渗出实变影明显吸收,但出现多个空洞性结节。患者既往无结核病史,行支气管肺泡灌洗,反复行痰结核菌培养涂片均为阴性,并积极查找其他能引起空洞性结节的疾病,如Wegener肉芽肿、肺癌及肺部真菌感染,均无证据。动态观察患者病情,无发热、咳嗽及呼吸困难,各项检查均不支持肺结核等疾病,结合患者病史,考虑空洞性结节为坏死性类风湿结节。渐进性坏死性类风湿结节一般发生于肺实质,可发生于关节症状明显严重、类风湿因子滴度很高者,也可发生于关节炎之前或不伴有关节炎表现,但只是偶尔发现。结节通常是多发性,较大的结节可有空洞形成[12]。多发性结节应与Wegener肉芽肿和肺转移癌相鉴别,有空洞形成时应与癌性空洞及结核性空洞相鉴别。
本研究中2例患者肺CT提示肺气肿,肺功能提示阻塞性肺疾病。其中1例合并肺大疱,经激素治疗后呼吸困难明显缓解,肺内病变明显吸收,但在一次进食时出现误吸,发生剧烈咳嗽,随后出现了自发性气胸,经胸腔闭式引流气体无明显吸收,并出现纵隔气肿及周身皮下气肿,行第二枚闭式引流后气体才逐渐吸收。2例患者吸烟量分别为15包/年和20包/年。RA是否引起阻塞性肺疾病一直存在争论,有研究表明,RA吸烟者比正常人或其他类型的风湿病吸烟者发生阻塞性气道疾病的概率高2~4倍,原因未明。约1/3的非吸烟RA患者发生气道阻塞性疾病[14]。
综上所述,RA-ILD的CT影像特点最常见的表现为网格影,其次为渗出斑片浸润/实变影及磨玻璃影。患者多呈双肺同时受累。少数患者可合并肺气肿及空洞性结节。当RA患者出现呼吸道症状及肺CT异常改变时,经系统抗炎治疗无效,结合影像特点应考虑为RA-ILD。对以磨玻璃样和/或实变影为主要病变者,应积极给予糖皮质激素及环磷酰胺等免疫抑制剂治疗,吸烟者应戒烟,同时应高度警惕继发肺部感染。
1 Bongartz T,Nannini C,Medina-Velasquez YF,et al.Incidence and mortality of interstitial lung disease in rheumatoid arthritis:a population-based study[J].Arthritis Rheum,2010,62(6):1583-1591.
2 Olson AL,Swigris JJ,Sprunger DB,et al.Rheumatoid arthritis-interstitial lung disease-associated mortality[J].Am J Respir Crit Care Med,2011,183(3):372-378.
3 Arnett FC,Edworthy SM,Bloch DA,et al.The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis[J].Arthritis Rheum,1988,31(3):315-324.
4 American Thoracic Society.Idiopathic pulmonary fibrosis:diagnosis and treatment.International consensus statement.American Thoracic Society(ATS),and the European Respiratory Society(ERS)[J].Am J Respir Crit Care Med,2000,161(2 pt 1):646-664.
5 O′Dwyer DN,Armstrong ME,Cooke G,et al.Rheumatoid Arthritis(RA)associated interstitial lung disease(ILD)[J].Eur J Intern Med,2013,24(7):597-603.
6 李宗英,王俊祥.类风湿关节炎并发肺间质纤维化的相关因素研究[J].中国全科医学,2013,16(1):140.
7 闫慧明,丁利芳,刘媛,等.转化生长因子-β1与结缔组织生长因子在类风湿关节炎合并肺间质病变患者血清中的表达水平及临床意义[J].中国全科医学, 2012,15(10):3268.
8 宋淑菊,马骥良,潘丽恩,等.类风湿关节炎患者肺间质病变的临床研究[J].中华风湿病学杂志,2005,9(2):81-85.
9 陈进伟,吴佩君,谢希,等.类风湿关节炎合并肺间质病变的临床特点[J].临床内科杂志,2010,27(8):554-556.
10 Lee HK,Kim DS,Yoo B,et al.Histopathologic pattern and clinical features of rheumatoid arthritis-associated interstitial lung disease[J].Chest,2005,127(6):2019-2027.
11 张艳敏,姜莉.类风湿关节炎相关性间质性肺疾病的研究进展[J].国际呼吸杂志,2011,31(6):471-475.
12 Yuksekkaya R,Celikyay F,Yilmaz A,et al.Pulmonary involvement in rheumatoid arthritis:multidetector computed tomography findings[J].Acta Radiol,2013,54(10):1138-1149.
13 Tanaka N,Kim JS,Newell JD,et al.Rheumatoid arthritis-related lung disease:CT findings[J].Radiology,2004,232(1):81-91.
14 Antoniou KM,Walsh SL,Hansell DM,et al.Smoking-related emphysema is associated with idiopathic pulmonary fibrosis and rheumatoid lung[J].Respirology,2013,18(8):1191-1196.

