Bi O(OH)/AC催化硼氢化钠还原法制备氧化偶氮苯类化合物
周惠敏,董安元,蔡可迎
(徐州工程学院化学化工学院,江苏 徐州 221018)
氧化偶氮苯类化合物是重要的有机合成中间体,其可被还原为偶氮化合物,偶氮化合物可广泛地用作染料;氧化偶氮苯类化合物也可用于制备指示剂和液晶材料。还原芳香族硝基化合物是制备氧化偶氮苯类化合物的重要方法。将芳香族硝基化合物还原为氧化偶氮苯类化合物方法有多种,其中锌粉还原法消耗锌粉较多,且生成的氧化锌回收较困难[1-3];甲醛还原法体系复杂,产生大量的含碱废水,后处理麻烦[4-5];加氢还原法需要贵金属作催化剂,对设备要求高,且具有较大的危险性[6];β-环糊精还原法[7-8]和聚乙二醇还原法[9]的收率较低;电化学还原法操作较复杂[10]。硼氢化钠还原法[11-12]具有条件温和、操作简便的优点,但该法使用的催化剂氯化铋和碱式氧化铋较难回收使用。因此,我们采用活性炭(AC)作载体,采用浸渍法制备了BiO(OH)/C催化剂,并将其用于催化硼氢化钠还原芳香族硝基化合物制备氧化偶氮苯类化合物,该催化剂具有较高的活性和较好的重复使用性。反应如下:
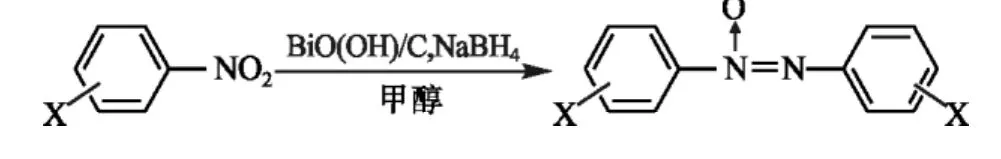
1 实验
1.1 主要试剂与仪器
AC(粒 径 0.297~0.840mm,AR),五 水 硝 酸 铋(AR),硼氢化钠(质量分数≥ 97%,AR),其余试剂均为国产分析纯,实验用水为自制蒸馏水。
岛 津 GC2014型 气 相 色 谱 仪(GC),惠 普HP6890/5973型气相色谱-质谱联用仪(GC-MS),85-2型数显恒温磁力搅拌器。
1.2 实验方法
1.2.1 Bi O(OH)/C催化剂的制备
称取0.464 g Bi(NO3)3·5H2O,放入小烧杯中,加入少量的稀硝酸至Bi(NO3)3·5H2O全溶,加蒸馏水稀释至6 mL。精确称量2 g AC,加入配制好的Bi(NO3)3溶液中,搅拌后,于室温下晾干,得到浸渍好的硝酸铋/AC。将硝酸铋/AC加入10%的氨水中,于室温搅拌4 h,充分反应后,再用蒸馏水充分洗涤至中性,于120℃干燥4 h,得10% Bi O(OH)/AC(以Bi计,下同)。按照同样的方法制备5% Bi O(OH)/AC和15% Bi O(OH)/AC催化剂。
1.2.2 氧化偶氮苯类化合物的制备
在室温下,将5mmol的芳香族硝基化合物、1.0g Bi O(OH)/C和15mL甲醇加入装有空气冷凝管的二口烧瓶,开动搅拌,于0.5h内分批加完5.5mmol NaBH4,室温下再反应约1.5h,用GC监测反应进程。反应完成后,过滤,用甲醇充分洗涤催化剂。滤液合并,旋转蒸发除溶剂后冷至室温。用蒸馏水洗涤浓缩产物至中性,抽滤。用丙酮溶解产物并用无水硫酸镁干燥,然后用GC-MS定性、GC定量。产物的收率和质谱数据见表1。
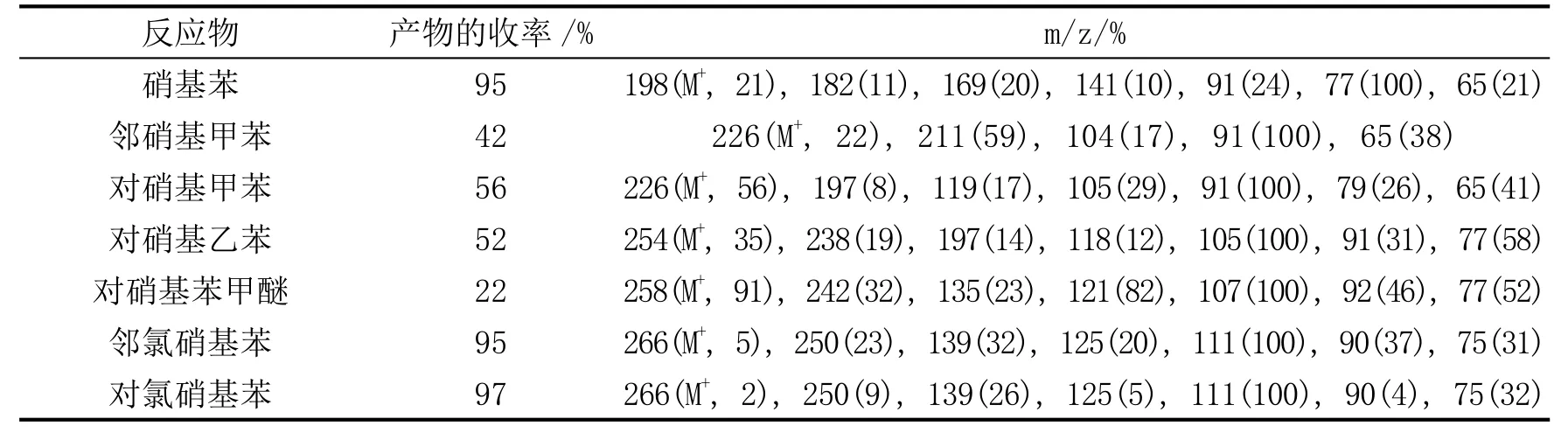
表1 氧化偶氮苯类化合物的收率和质谱数据Table1 Yields and MS data of azoxy compounds
2 结果与讨论
2.1 铋负载量对催化剂性能的影响
以硝基苯为底物,考察了不同负载量的Bi O(OH)/AC的催化活性。由图1可知,催化剂中铋的负载量较少时,活性中心较少,导致催化活性较低;提高铋的负载量可提高催化剂的活性,但铋的负载量超过10%其活性增加并不明显。因此,催化剂中铋的负载量为10%是适宜的。

图1 Bi负载量对Bi O(OH)/AC催化活性的影响Figure1 Effect of Bi loading on catalytic activity of BiO(OH)/AC
2.2 硼氢化钠用量对反应的影响
在不同条件下硝基苯可被还原为氧化偶氮苯、偶氮苯和苯胺。还原剂NaBH4的用量对产物的选择性有较大影响。因此,以硝基苯为底物,以10%Bi O(OH)/AC为催化剂考察了NaBH4的用量对反应的影响。由表2(反应2 h)可知,NaBH4的用量较少时,氧化偶氮苯的选择性较高,但硝基苯的转化率较低,因此氧化偶氮苯的收率较低;随着NaBH4用量的增加,氧化偶氮苯的收率也逐渐增大,当NaBH4的用量为5.5 mmol时,氧化偶氮苯的收率达最高为95%;进一步增大NaBH4的用量,产物中有较多偶氮苯和苯胺生成,导致氧化偶氮苯的收率下降。因此,n(NaBH4)/n(硝基苯) = 1.1∶1是适宜的。

表2 NaBH4用量对氧化偶氮苯收率的影响Table2 Eff ect of amount of NaBH4 on azoxy benzene yield
2.3 Hammet常数对反应的影响
在碱性条件下水合肼还原芳香族硝基化合物可得氧化偶氮苯,氧化偶氮苯可进一步被还原为偶氮苯,硝基化合物也可直接被还原为芳胺。底物不同,氧化偶氮苯类化合物的收率有很大差异。底物中有吸电子基,没有芳胺生成,只生成氧化偶氮苯类化合物,所以其收率较高,如邻氯硝基苯和对氯硝基苯;底物中有推电子基,易生成芳胺,所以氧化偶氮苯类化合物的收率较低,如邻硝基甲苯、对硝基甲苯、对硝基乙苯和对硝基苯甲醚。这与任平达等[11]的研究结果一致,即氧化偶氮苯类化合物收率的高低与反应底物的Hammet常数有关,取代基的吸电子能力越强,反应底物的Hammet常数越大,相应的氧化偶氮苯的收率也越高;反之,相应的氧化偶氮苯的收率越低。
2.4 催化剂的重复使用性
该催化剂易于回收,反应完成后,用甲醇洗涤并回收催化剂,重复使用。以硝基苯为底物考察了其重复使用性能,结果见表3。由表3可知,催化剂使用4次活性有一定的下降。
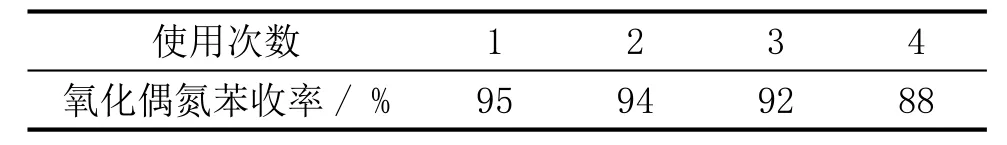
表3 催化剂的重复使用性Tabl e 3 Reusabil it y of catal yst
3 结论
采用浸渍法制备了Bi O(OH)/AC催化剂,在室温下将其用于催化硼氢化钠还原芳香族硝基化合物制备氧化偶氮苯类化合物,收率22%~97%。该方法反应条件温和,操作简单,催化剂易回收,可循环使用。硝基化合物的Hammet常数越大,氧化偶氮苯类化合物的收率越高。
[1] 李薇,陈学云,苏玉忠,等. 2,2’-二氯氢化偶氮苯合成方法进展[J]. 化工生产与技术,2000(2):16-18.
[2] 张铸勇.精细有机合成单元反应[M].上海:华东理工大学出版社, 2003: 173-175.
[3] 付春. 3,3’-二氯联苯胺合成技术进展[J].河南化工,2002(3):7-10.
[4] 张天永,张友兰,邢文康.甲醛还原法制备2,2’-二氯氢化偶氮苯[J].应用化学,2001,21(5):521-523.
[5] 催玉民,范少华,单德杰 . 3,3’-二氯 -4,4’-二氨基联苯的合成[J].化学通报,2001(11):715-717.
[6] 闫茂文,陈宏博,徐善利,等. Pd/C催化加氢法合成3,3’-二氯联苯胺[J].染料与染色,2005,42(4):64-65.
[7] 郭爱玲,尚卓镔,金硕,等. β-CD碱体系还原间二硝基苯为氧化偶氮苯[J].山西大学学报:自然科学版,2005,28(1):69-70.
[8] 刘宇芳,刘博,董振明,等.氧化偶氮苯类化合物的新法合成[J].高等学校化学学报,2010,31(12):2396-2399.
[9] Liu Yufang, Liu Bo, Guo Ailing, et al. Reduction of nitroarenes t o azoxybenzenes by NaOH-PEG 400 [J]. Synt hetic Communications, 2012(42): 2201-2206.
[10] Ohba T, Ishida H, Yamaguchi T, et al. Carbon dioxidepromoted electrochemical reduction of aromatic nitro compounds to azoxy compounds in acetonitrile [J]. J Chem Soc, Chem Commun, 1994: 263-264.
[11] 任平达,潘士峰,董庭威,等. NaBH4/Bi Cl3复合体系还原芳香族硝基化合物为氧化偶氮苯及其类似物[J]. 化学学报,1998(56):714-718.
[12] 蔡可迎,黄耀国, 宗志敏,等. Bi O(OH)-NaBH4还原法制备氧化偶氮苯类化合物[J].应用化学,2008,25(3):372-374.
[13] Wang X L, Xu M H, Lian H Z, et al. Reduction of aromatic azo-, azoxy- and nitro- compounds by ultrasonically activated nickel [J]. Synthetic Communications, 1999, 29(17): 3031-3037.

