微波萃取蓝莓中花青素获取和降解的同步模型
郑先哲,陶岩,李秀伟,刘秉欣
(东北农业大学工程学院,哈尔滨 150030)
微波萃取蓝莓中花青素获取和降解的同步模型
郑先哲,陶岩,李秀伟,刘秉欣
(东北农业大学工程学院,哈尔滨 150030)
为同步表征微波萃取蓝莓过程中花青素获取和降解过程,揭示微波萃取蓝莓中花青素的传递机理,依据Fick扩散定律和电磁场增强扩散理论,探究微波萃取温度对蓝莓花青素萃取率及降解率的影响,在低温范围内(30~60℃)花青素萃取速度高于降解速度,在高温范围内(60~70℃)花青素降解速度高于萃取速度。建立描述微波萃取过程中花青素获取与降解同步模型,为在生产实践中提高效率、实现对微波辅助萃取有效成分工艺系统的最优控制提供理论依据。
微波;萃取;蓝莓;花青素;降解;模型
萃取是指从植物性物料中获取高纯度有效成分的过程,是医药、食品、化工等行业中部分原料的主要来源和关键生产环节。微波萃取(MAE)具有萃取速度快、过程容易控制、有效成分得率高及可用酒精等对环境无污染溶剂等优势。蓝莓中含丰富的花青素和维生素,具有很高的医用和营养价值,花青素具有抗衰老、抗疲劳和增强视力等功效[1],但有效成分对热、光和氧气等外界条件有强敏感性。在微波萃取过程中,微波辐照作用使萃取体系温度迅速升高,提高目标成分传递速度,但高温又会引起热敏性成分发生氧化、聚合、缩合等反应,降解生成新的聚合物或单体物质,改变有效成分原有性质[2]。Zheng等研究发现,与常规的固-液萃取和热回流萃取工艺相比,微波萃取工艺可以提高效率3~5倍,增加有效成分得率20%~30%,但高温时引起的有效成分降解呈幂函数增加,萃取温度高于50℃时,可能有50%以上的有效成分发生降解,失去原有抗氧化、抗菌等生物活性[3]。选择合适的模型,能够同步表征花青素的萃取与降解过程,控制微波萃取过程,是当前研究关注的重点问题。
微波萃取时,目标成分扩散受到微波场、化学势场和压力场协同作用加强萃取过程[4]。根据微波萃取动力学模型,分析萃取条件对目标成分传递的影响机理,为优化高得率和效率萃取工艺参数及流程提供理论依据。Smail等研究萃取过程中的质量传递[5-7],深入分析各试验条件对萃取率影响,对试验数据回归得到萃取模型,分析各试验因素对萃取率影响;李核等根据菲克定律和电磁场增强扩散理论,建立微波萃取虎杖中白藜芦醇的动力学模型,确定微波萃取过程中有效成分在物料内部传递过程[8];Dincov等研究微波加热过程中两相多孔材料的质热传递过程,建立描述微波加热机制的模型[9];黄瑞华等在固液提取的传质扩散方程中引入温度因素,建立提取淫羊藿苷的热质传递数学模型,解释微波能强化淫羊藿苷的提取过程[10];杨俊红等建立萃取动力学方程,阐明微波促进萃取主要原因是微波引起温度升高,提高传质系数[11]。
在研究微波促进萃取同时,研究微波对热敏性物质降解作用。建立萃取过程中活性成分降解过程和动力模型,有助于分析降解机理,控制降解过程,提高有效成分得率。Hu等研究发现微波辅助萃取会造成目标成分降解[12-14];李媛等确定微波辅助提取葡萄皮中花色苷的降解过程符合指数衰减模型[15];任瑞等根据微波香菇中多糖降解特性,通过建立降解动力学方程解释微波功率对多糖降解影响理论[16]。
在MAE过程中,有效成分萃取与降解同时发生,但已有的建立微波萃取模型研究中,多数是分别考虑有效成分萃取和降解过程,难以系统、准确地表征和控制有效成分在萃取液中的变化。本文获得微波萃取条件下蓝莓中花青素的获取和降解规律;建立并验证微波萃取蓝莓中花青素获取和降解的同步模型;分析微波辐照作用对有效成分效应。以提高花青素得率和减少降解为目标,为有效控制微波萃取蓝莓过程提供理论依据。
1 材料与方法
1.1 材料
蓝莓鲜果产于黑龙江省大兴安岭地区,选择颜色均一、颗粒饱满的蓝莓置于冰箱中冻藏。试验时取出冻藏蓝莓在室温下缓慢解冻4 h,打浆,经真空冷冻干燥24 h后,磨成粉末,过40目筛,制成干燥粉末保存在避光干燥器皿中,以备后续试验使用。
试剂:花青素标样纯度95%(天津尖峰天然产物研究开发公司);香草醛、浓盐酸、甲醇、无水乙醇均为分析纯,购自天津市富宇精细化工有限公司。
1.2 仪器
ETHOS1系列T640型微波萃取仪由意大利Milestone公司生产;TD-50型冻干机由上海浦东冷冻干燥设备有限公司生产;LAMBDA35型紫外-可见分光光度计由美国Perkin Elmer公司生产。
1.3 方法
1.3.1 花青素萃取液的制备
准确称取(1.0000±0.0005)g蓝莓粉末于萃取罐中,加入30 mL 60%乙醇溶液,在微波萃取工作台中以不同水平温度(30~70℃,间隔10℃)、时间(2~10 min,间隔2 min)进行萃取试验。待萃取结束后将萃取液于室温下抽滤,并使用60%乙醇溶液将萃取液定容至100 mL容量瓶中,置于黑暗处,室温条件下保存以备后续试验所用。
收集残渣于50 mL锥形瓶中,加入30 mL 60%乙醇溶液,置于25℃、50 r·min-1水浴振荡器中继续萃取,3 h后取出溶液,室温下抽滤,得滤液。重复萃取残渣3遍,将所得滤液定容至100 mL容量瓶中,置于黑暗处,室温条件下保存以备后续试验所用。
1.3.2 标准溶液的配制和标准曲线的制作
1.3.2.1 显色剂制备
A:1%香草醛溶液(称取1.000 g香草醛溶于甲醇中,定容到100 mL);B:8%盐酸液(取8 mL浓盐酸,用甲醇定容到100 mL)。显色剂A∶B=1∶1,现配现用。
1.3.2.2 标准曲线绘制[17]
配制原花青素标准溶液,浓度为1.2 mg·mL-1。分别取1、2、3、4、5 mL,然后用乙醇定容到10 mL,各取1 mL(另取1 mL甲醇液为空白液),分别加入5 mL显色剂,摇匀,避光。在(30±1)℃恒温水浴中保持30 min,保温比色,取出比色管,在500 nm波长下,测其吸光值,绘制标准曲线。以吸光值A为纵坐标,浓度C(mg·mL-1)为横坐标作图,得到标准曲线方程为

式中,A-花青素在波长500 nm处吸光度,C-花青素标样浓度(mg·mL-1),R2=0.9989。
1.3.3 花青素含量测定
花青素含量测定采用低浓度香草醛-盐酸法[17],准确移取1.0 mL萃取液置于试管中,向试管中加入5 mL显色液,混匀后置于30℃恒温水浴锅中,保温30 min。待反应结束后使用分光光度计测定反应液在500 nm[18]处吸光值,每个样液测定3次求其平均值,利用标准曲线得出萃取液中花青素含量。
1.3.4 数据处理
应用SigmaPlot 12.0软件进行数据处理,进行方程拟合;利用Matlab 7.1软件进行数据分析,编程得到萃取动力学模型验证图。
2 萃取动力学模型的建立
2.1 花青素萃取过程传质分析
MAE是利用微波能使与固体样品接触的溶剂致热,并同时将目标成分从样品中分离出至溶剂中的过程。在微波萃取蓝莓粉内花青素过程中,如图1所示,主要包括以下阶段[19]:①在基体-溶剂交界面发生解吸,接着花青素扩散至溶剂中;②溶剂向蓝莓颗粒内部渗透,逐步润湿固体内部;③固体基质内部花青素溶解;④花青素由颗粒内部转移到表面;⑤花青素由固-液接触表面向溶液主体扩散。质热传递方向一致,能促进目标成分提取。
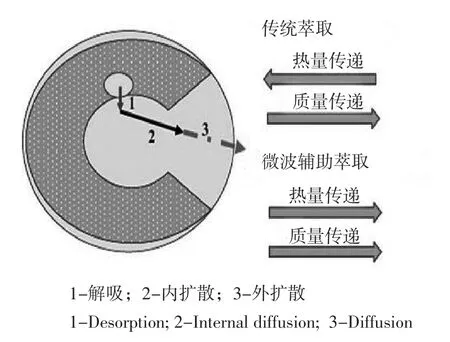
图1 萃取过程[19]Fig.1 Extraction process
2.2 模型假设
为简化MAE过程模型,提出如下假设[5,7,20]:①溶剂向基体内部渗透速度很快,可以忽略其对萃取速率的影响;②萃取过程中溶剂体积无变化;③初始状态时,花青素在基体内部分布均匀,各向同性;④溶剂向基体内部渗透是均匀的;⑤溶剂及目标萃取物向基体表面的扩散是均匀的;⑥花青素溶解速率远大于扩散速率;⑦蓝莓样品为大小均匀的球形颗粒,在MAE中粒径保持不变。根据以上假设,将整个萃取过程作为一个解吸扩散串联过程处理。由于无法测得颗粒内部不同位置的浓度,本试验只考虑蓝莓粉颗粒与溶剂接触表面处的浓度,与萃取液浓度近似相等。
2.3 萃取动力学模型建立
2.3.1 花青素在固液界面的传质通量
蓝莓中花青素的萃取过程属于溶质在固液两相中的传质过程,因此可用固液扩散公式描述蓝莓颗粒中花青素的提取过程。根据Fick第一定律[21],单位时间内传质通量J与传质表面积和浓度梯度成正比,花青素通过固液界面传质通量J为:

式中,N—τ时刻提出的溶质质量,kg,其中N=V·C(τ);τ—萃取时间,min;Dl—液相传质系数,m2·s-1;S—蓝莓颗粒表面积,m2,其中S= 4πR2;C(τ)—τ时刻溶液主体的浓度,kg·m-3;V—溶剂体积,m3。
2.3.2 浓度梯度
扩散面浓度梯度越大,扩散动力也大,扩散速度越快,浓度梯度变化越大。因而扩散面浓度随时间和空间的变化可以表示为:

m—浓度梯度的时间变化常数,m<0,m=0,m>0分别反映浓度梯度随时间衰减、恒定和增加的情况。假定原始蓝莓样品中花青素浓度为Cs,0mol·m-3。则初始条件为:

根据初始条件,由(3)式可得到:

本试验只考虑半径为R(即固液相接触面)处的浓度梯度。
2.3.3 液相传质系数Dl
液相传质系数Dl,最常用估算方法是Stokes-Einsten[22]方程,其表达式为:

式中,f—溶质的摩擦系数;kB—玻尔兹曼常数,取值1.380662×10-23J·K-1;T—液相环境温度(K);μ—溶液粘度(g·m-1·s-1);R—溶质半径(m)。
可见液相传质系数Dl与溶质分子大小R、提取溶液粘度μ及萃取温度T有关。通常情况下,随着提取溶液浓度增大,粘度随之增大,扩散系数相应减小。
2.3.4 萃取液中花青素浓度微分方程
将公式(5)带入公式(2)整理得:

假设微波对萃取过程的作用为α,微波对萃取量的影响可用(1+α)[8]表示。在微波萃取过程中,为表征微波对花青素的扩散有增强作用,引入增强因子γ1;为表征微波热效应引起花青素降解,引入降解因子γ2。增强因子增加萃取量,降解因子减少萃取量,则可设微波增强作用与微波降解作用为γ1/γ2,即微波作用α=γ1/γ2。则有:
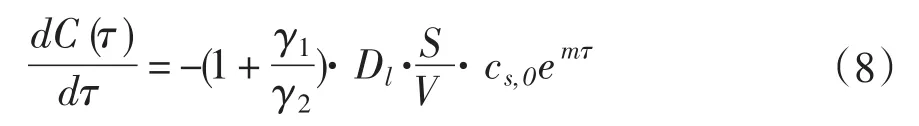
萃取过程中的固液比:

式中:M—固液比,g·mL-3;V—溶剂体积,mL3;G—称取蓝莓粉质量,1 g。
将公式(9)带入公式(8)中,可得:

公式(10)是萃取液花青素浓度随时间τ变化的微分方程,引入边界条件可以推导出τ时刻溶液中花青素浓度,是萃取动力学方程。
2.3.5 萃取动力学方程的导出
针对微分方程(8)引入边界条件:C0=0,则τ时刻萃取液中花青素浓度为:

方程(11)是萃取动力学方程,反映萃取液中花青素浓度C(τ)随着萃取时间τ的变化。
2.3.6 拟合方程
采用非线性拟合方法对试验数据进行方程拟合,通过较高的决定系数(R2)和较低的标准偏差(SEE),选择Exponential Rise to Maximu(式12)和Exponential Decay(式13)方程式描述花青素萃取率模型。在萃取过程中,微波促进花青素扩散起主导作用时,选择式(12);当微波对花青素的降解起主导作用时,选择式(13)。
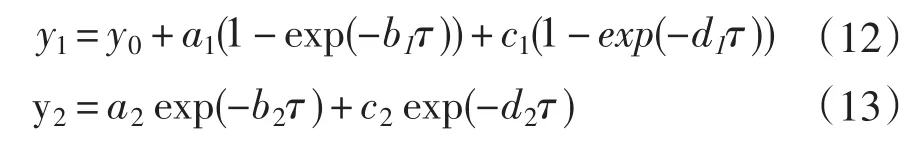
式中,y0—花青素在所设定的升温阶段(1 min后)溶液中最初花青素含量(%);a1,a2—在均衡状态下的花青素萃取率(%);b1,b2—物料传递过程中的质量系数(min-1);c1,c2—在均衡状态下物质传递过程中花青素萃取率(%);d1,d2—扩散过程的动力学常数(min-1)。
3 结果与分析
3.1 萃取温度对花青素萃取率的影响
如图1所示,萃取温度为30、40、50℃时,花青素萃取率显著提高(P<0.05)。这是由于微波辐射作用导致物料温度升高,分子热运动加快,促进花青素从蓝莓颗粒扩散到溶液中。当萃取温度在60℃时,前4 min内花青素萃取率呈上升趋势,随后开始下降。这是因为花青素是热敏性物质,当物料内热量积累到一定程度时,花青素结构被破坏,花青素萃取率下降。当萃取温度达到70℃时,花青素降解程度加剧,萃取率呈现下降趋势。此时,花青素降解为萃取过程中的主导作用。比较不同萃取温度和萃取时间下花青素的萃取率,结果表明选择合适的萃取温度和时间有利于增加花青素的萃取量。
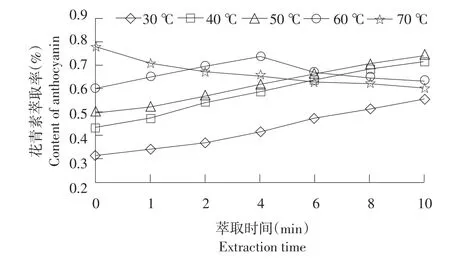
图2 萃取温度和时间对花青素萃取率的影响Fig.2 Effect of extraction temperature and extraction time on content of anthocyanin
在萃取温度30~60℃,微波萃取动力变大,萃取动力系数变大。这是因为微波作用会使基质内部结构破裂,有效成分迅速从细胞内部扩散到萃取剂中。在此过程中,溶剂在微波照射下与电磁场耦合,然后通过介电松弛机制将热传输到溶剂中致溶剂升温,从而提高花青素在溶剂中的溶解度,增大从基体解吸的动力[23],微波萃取动力系数变大。60~70℃时,微波降解动力变大,降解动力系数变大。这是因为花青素为热敏性物质,遇热易降解,此温度范围内,微波降解作用为主导作用,所以降解动力系数变大。
采用非线性拟合方法计算模型系数,结果如表1所示,方程决定系数R2均大于0.99,呈极显著水平即P=0.001。除70℃外,在其他温度条件下,蓝莓粉中花青素萃取的最初花青素含量(y0)均随萃取温度升高而升高。萃取温度70℃时质量传递系数b最高,这是由于高温有利于花青素扩散。扩散过程中动力学常数d呈现先增加后减小趋势,这是由于在微波辅助萃取过程中,低温范围(30、40、50、60℃)内,升高温度,随萃取时间的延长花青素萃取率增加,微波增强作用占主导地位,萃取动力学常数d增大;继续升温(60、70℃),微波作用破坏花青素结构,微波降解作用占主导地位,萃取动力学常数d减小。

表1 不同温度下微波辅助萃取花青素萃取率的模型系数Table 1 Regression coefficient of equation(12,13)describing the microwave extracted anthocyanin from blueberry powder under different temperatures
3.2 萃取温度对花青素降解率的影响
不同萃取温度和时间下得到的花青素降解率如图3所示。在低温范围(30、40、50℃)内,随着温度升高花青素降解率下降。这是由于低温范围内,温度上升不会对花青素造成降解,升高温度,能促进花青素扩散,微波萃取动力学系数较大,萃取为主导作用。在高温范围(60、70℃)内,花青素降解率显著上升。这是因为微波降解动力学系数较大,降解作用为主导作用。结果表明选择合适的萃取温度和萃取时间有利于减少花青素的降解量。

图3 萃取温度和时间对花青素降解率的影响Fig.3 Effect of extraction temperature and extraction time on degradation content of anthocyanin
依据指数衰减方程对图3中花青素降解率的数据进行非线性拟合,模型系数如表2所示。除70℃外,均衡状态下蓝莓粉中花青素萃取率a均随着萃取温度升高而升高。高温有利于扩散,随着萃取温度升高,质量传递系数b不断增大,萃取温度70℃时达到最高。扩散过程中动力学常数d呈现先增加后减小趋势。

表2 不同温度下微波辅助萃取花青素降解率的模型系数Table 2 Regression coefficient of equation(14)describing the degradation content of anthocyanin from blueberry powder under different temperatures
3.3 微波萃取蓝莓中花青素获取和降解的同步模型建立
为分析萃取过程中微波对目标成分的获取和降解规律,建立微波辅助萃取过程中有效成分的传递和变化过程的理论模型。
由拟合结果可知,30、40、50、60℃(0~4 min)、60℃(4~10 min)、70℃下的萃取因子γ1/γ2分别为:0.0269、0.0583、0.0870、0.3613、0.4637、0.0120。采用非线性拟合,得到温度与各因子间回归方程:

因此,微波辅助萃取蓝莓花青素过程的传质方程为:
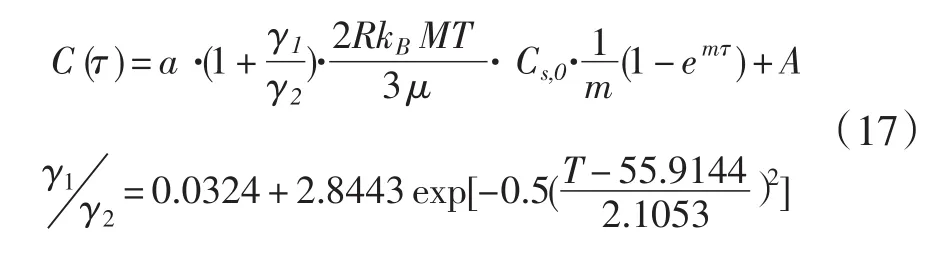
式中,a—校正系数;A—常数项。
因此,根据计算得出的微波增强因子和降解因子,获得微波辅助萃取技术的半理论-半经验公式,同步表征微波萃取蓝莓过程中花青素的获取和降解过程,从理论上揭示微波萃取蓝莓中花青素的传递机理,为在生产实践中提高萃取率、减小降解率提供理论依据,实现对微波辅助萃取有效成分工艺系统的最优控制。
3.4 萃取动力学模型的验证
验证试验的萃取工艺为:萃取时间0~10 min(间隔2 min),萃取温度为30~70℃(间隔10℃)。比较萃取液浓度C的试验值和萃取动力学模型预测值,如图4所示。试验值与模型预测值拟合较好,决定系数R2>0.95。因此萃取动力学模型能较好反应微波辅助萃取蓝莓花青素的获取和降解规律,适合表达试验范围内目标成分萃取规律。
3.5 微波强化萃取传质过程分析
蓝莓粉颗粒内部花青素含量随萃取时间和粒径变化如图5所示。半径一定时,随萃取时间延长,花青素含量减少,与萃取过程模型描述一致。这是因为在微波辐照作用下,物料吸收微波能,萃取体系内部迅速升温,分子热运动加快,目标成分快速从物料基质内部扩散到溶液中,颗粒内部花青素含量减少。微波作用能够增加基体材料空隙率,使目标成分获得非热效应能[24],促进扩散速率,颗粒内部花青素含量下降。
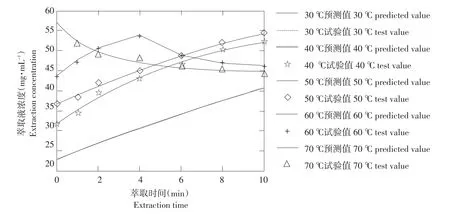
图4 萃取动力学模型的验证Fig.4 Validation of the extraction kinetics model

图5 萃取时间和粒径对花青素含量的影响Fig.5 Effect of extraction time and particle diameter on concentration of anthocyanins
萃取时间一定时,颗粒内部花青素含量随着半径增大而减小,与萃取过程模型描述一致。这是因为半径越大,溶质与溶剂的接触面积越大,扩散速率越快[19],颗粒内部花青素快速溶解,扩散到溶液中,含量减少;粒径越大,物料基体内部贮存的水分越多,加热后,水分蒸发,在细胞内部产生压力,促使细胞破裂,释放溶质,促进目标成分扩散,提高萃取率[25],蓝莓粉内部花青素含量减少。
模拟结果与提出的微波萃取过程模型结果一致,表明模型能够表征某一粒径的蓝莓粉颗粒。微波萃取过程模型可以准确表征微波对萃取物的降解与获取作用。
4 结论
本文以蓝莓为研究对象,获得微波萃取过程中花青素获取和降解的规律:在低温范围内(30~60℃)花青素萃取速度高于降解速度,在高温范围内(60~70℃)花青素降解速度高于萃取速度。考虑微波萃取过程中目标化合物的获取与降解过程,建立描述微波辅助萃取蓝莓花青素过程的理论-经验组合模型,可预测微波萃取过程中花青素获取量,为设计目标成分得率高的微波辅助萃取工艺提供理论依据。
[1]金文,王振宇,程翠林,等.叶黄素-蓝莓功能性饮料乳化性能和稳定性研究[J].东北农业大学学报,2014,45(4):123-128.
[2]李聪,霍兴荣,郑先哲,等.微波催陈条件对干红葡萄酒颜色和pH的影响[J].东北农业大学学报,2010,41(1):124-129.
[3]Zheng X Z,Xu X W,Liu C H,et al.Extraction characteristics and optimal parameters of anthocyanin from powder blueberry un⁃der microwave-assisted extraction conditions[J].Separation and Purification Technology,2013,104(5):17-25.
[4]刘海力,郭平生,宁军贤.微波强化萃取的机理及场协同分析[J].广西物理,2007,28(3):14-17.
[5]Smail M,Hocine K.Kinetics and thermodynamics of oil extrac⁃tion from olive cake[J].Journal of the American Oil Chemists′So⁃ciety,2008,85(4):391-396.
[6]Cacace J E,Mazza G.Mass transfer process during extraction of phenolic compounds from milledberries[J].Journal of Food Engi⁃neering,2003,59(4):379-389.
[7]Young S J,Eun Z L,Yun S H,et al.Kinetic study for the extrac⁃tion of succinic acid with TOA in fermentation broth effects of pH salt and contaminated acid[J].Biochemical Engineering Journal, 2007,36(1):8-13.
[8]李核,张展霞,李攻科.密闭式微波系统的微波辅助萃取动力学模型[J].中山大学学报:自然科学版,2004,43(3):40-44.
[9]Dincov D D,Parrott K A,Pericleous K A.Heat and mass transfer in two-phase porous materials under intensive microwave heating [J].Journal of Food Engineering,2004,65(3):403-412.
[10]黄瑞华,韩伟,周永传,等.微波辅助提取淫羊藿饮片中淫羊藿苷的热质同向传递数值模拟[J].化工学报,2005,56(7):1300-1304.
[11]杨俊红,段增宾,郭锦棠,等.微波预处理强化山楂回流提取的作用机理[J].天津大学学报:自然科学与工程技术版,2006,39 (7):874-880.
[12]Hu E D,Cheng H F.Rapid extraction and determination of atra⁃zine and its degradation products from microporous mineral sor⁃bents using microwave-assisted solvent extraction followed by ul⁃tra-HPLC-MS/MS[J].Microchim Acta,2013,180(7-8):703-710.
[13]Gatidou G,Zhou J L,Thomaidis N S.Microwave-assisted extrac⁃tion of Irgarol 1051 and its main degradation product from marine sedimentd using water as the extractant followed by gas chroma⁃tography-mass spectrometry determination[J].Journal of Chroma⁃tography.A,2004,1046(1-2):41-48.
[14]Marion G,Ernst L K.DDT degradation during enhanced solid-liq⁃uid extractions-A consideration[J].Journal of Chromatography A, 2005,1072(1):117-125.
[15]李媛,徐夏旸,汪俊涵,等.微波辅助提取葡萄皮中花色苷的动力学和热力学研究[J].农业工程学报,2012,28(增1):326-332.
[16]任瑞,马海乐,朱春梅,等.香菇多糖微波降解反应动力学研究[J].化工学报,2009,37(4):38-40.
[17]李春阳,许时英,于璋.香草醛-盐酸法测定葡萄籽、梗中原花青素含量的研究[J].食品科学,2004,25(2):157-161.
[18]许相雯.微波辅助萃取蓝莓中花青素及纯化的研究[D].哈尔滨:东北农业大学,2012.
[19]Veggi P C,Julian M,Angela M,et al.Fundamentals of microwave extraction[M]//Chemat F,Cravotto G.Microwave-assisted extrac⁃tion for bioactive compounds:Theory and practice,food engineer⁃ingseries,NewYork:SpringerScienceBusinessMedia,2013.
[20]Shi J,Maguer M L.Analogical cellular structure changes in sol⁃id-liquid contacting operations[J].Lebensm.-Wiss.u.-Technol, 2002,35(5):444-451.
[21]Angela M,Meireles A.Extracting bioactive compounds for food products theory and applications[M].Boca Raton FL:CRC Press, 2009.
[22]柯斯乐E L.扩散一流体系统中的传质[M].王宇新,姜忠义译.北京:化学工业出版社,2002.
[23]Jing P,Ruan S Y,Dong Y,et al.Optimization of purification con⁃ditions of radish(Raphanus sativusL.)anthocyanin-rich extracts using chitosan[J].LWT-Food Science Technology,2011,44(10): 2097-2103.
[24]郭平生,刘海力,宁军贤,等.微波辅助萃取的动力学模型[J].化工学报,2009,60(2):394-399.
[25]Wang L,Weller C L.Recent advances in extraction of nutraceuti⁃cals from plants[J].Trends Food Sci Technol,2006,17:300-312.
Simultaneous model of acquisition and degradation of anthocyanin extracted from blueberry powder by microwave technology
/ZHENG Xianzhe,TAO Yan,LI Xiuwei,LIU Bingxin
(School of Engineering,Northeast Agricultural University, Harbin 150030,China)
In order to reveal the mechanism of microwave extracting anthocyanin from powdered blueberry,the process of simultaneous acquisition and degradation of anthocyanin by microwave technology was characterized.Based on Fick's law and the theory of the electromagnetic field enhanced diffusion,the effects of extraction temperature on the acquisition and degradation of anthocyanin were analyzed as anthocyanin acquisition rate higher than its degradation in extraction temperature of 30-60℃and anthocyanin degradation rate higher than its acquisition in extraction temperature of 60-70℃.A kinetic model of microwave-assisted extraction blueberry anthocyanin was established describing simultaneous process of acquisition and degradation of anthocyanin extracted from blue berry powder.The results indicated that the model might predict the concentration of anthocyanin under the extraction system,which contributed to improving efficiency in the production practice,and provided theoretical basis for achieving optimal control of the active ingredient of microwave-assisted extraction process.
microwave;extraction;blueberry;anthocyanin;degradation;model
S663.9
A
1005-9369(2014)11-0108-08
2014-05-21
国家自然科学基金项目(31271911);黑龙江省教育厅科学技术研究重点项目(1252lz003)
郑先哲(1968-),男,教授,博士,博士生导师,研究方向为农产品加工。E-mail:zhengxz2013@163.com
时间2014-11-21 16:44:00[URL]http://www.cnki.net/kcms/detail/23.1391.S.20141121.1644.018.html
郑先哲,陶岩,李秀伟,等.微波萃取蓝莓中花青素获取和降解的同步模型[J].东北农业大学学报,2014,45(11):108-115.
Zheng Xianzhe,Tao Yan,Li Xiuwei,et al.Simultaneous model of acquisition and degradation of anthocyanin extracted from blueberry powder by microwave technology[J].Journal of Northeast Agricultural University,2014,45(11):108-115.(in Chinese with English abstract)

