126例药物性肝损害的临床特征及其预后
王思进(枣庄市薛城区人民医院消化内科,山东枣庄 277000)
药物性肝损害(Drug-induced liver injury,DILI)是指药物在治疗过程中,经呼吸道、消化道或静脉等途径进入机体而引起肝脏损害,也称之为药物性肝炎。DILI 是常见的药品不良反应。迄今为止,国内外报道大约有1 000余种药物可能导致DILI[1]。因为DILI缺乏典型的临床特征及复杂多样的病理改变,临床误诊和漏诊率较高。本研究通过回顾性分析DILI 患者的临床特征、用药及预后转归情况,旨在促进临床医师更加全面、正确认识该病,现将结果报告如下。
1 资料与方法
1.1 资料来源
选择2009年1月至2013年11月我院消化科收治的126例DILI住院患者进行研究,均与患者签署了知情同意书。126例DILI 患者的临床诊断参考1997 年Maria VA 等[2]提出的新的“药物性肝损害的诊断评分”,肝功能衰竭诊断标准参考我国2006年制订的《肝功能衰竭诊疗指南》[3]。126例患者中,男性83例,女性43例,年龄18~73岁,平均(41.5±25.5)岁;其中7例(5.56%)有药物过敏史,8例(6.35%)无基础疾病,其余患者伴有基础疾病,包括感染性疾病、心血管疾病、糖尿病、肿瘤、结缔组织疾病等,具体见表1。

表1 126例患者基础疾病情况Tab 1 Underlying diseases of 126 cases
1.2 研究方法
回顾性分析所选研究对象的性别、年龄、相关病史、用药史、肝功能检查、临床疗效及预后等指标。预后判定标准:(1)治愈:临床症状、体征完全消失或明显改善,胆红素、丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)及碱性磷酸酶等肝功能指标基本恢复正常,凝血酶原活动度(PTA)基本正常;(2)好转:临床症状好转,肝功能指标较治疗前下降50%以上或PTA 较前上升50%以上;(3)无效:症状、体征无改善,肝功能、PTA指标无明显改善或加重,其中自动出院病例判为无效;(4)死亡:住院期间死亡[4]。
1.3 统计学处理
采用SPSS 16.0统计学软件进行汇总、分析。计量资料采用x ±s表示,行t检验;计数资料选择率进行表示,行χ2检验。P<0.05为差异具有统计学意义。
2 结果
2.1 患者肝损害药物治疗情况
126 例患者中,80 例患者由西药导致肝损害,主要有大环内酯类药、调脂药、抗病毒药及抗肿瘤药等;46 例患者由中药导致,包括中成药和中药汤剂,具体见表2。
2.2 临床效果及预后
所有患者予以还原型谷胱甘肽、硫普罗宁保肝治疗,停用肝损伤药,并进行营养支持等治疗。经过7~30 d治疗后,126例患者中有31 例患者痊愈,占24.60%;84 例患者好转,占66.67%;10 例患者自愿放弃治疗出院,占7.94%;1 例患者死亡,占0.79%。将痊愈和好转患者归为A 组,放弃治疗和死亡患者归为B 组,比较两组患者间各指标,具体见表3。两组患者在ALT及AST方面比较差异无统计学意义(P>0.05);但在总胆红素(TBIL)、直接胆红素(DBIL)及白蛋白(ALB)方面比较差异有统计学意义(P<0.05),B 组患者TBIL、DBIL 水平明显增高,说明TBIL、DBIL及ALB水平与患者预后有关。

表2 药物治疗情况Tab 2 Drug treatment
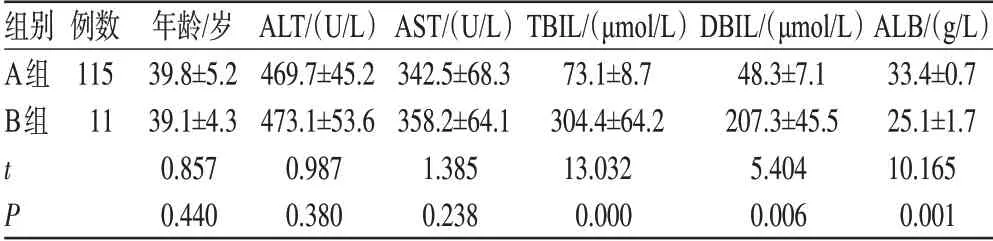
表3 两组患者间各指标比较Tab 3 Comparison of indicators between two groups
2.3 DILI的不良反应
DILI的主要不良反应表现为乏力、纳差等,具体见表4。
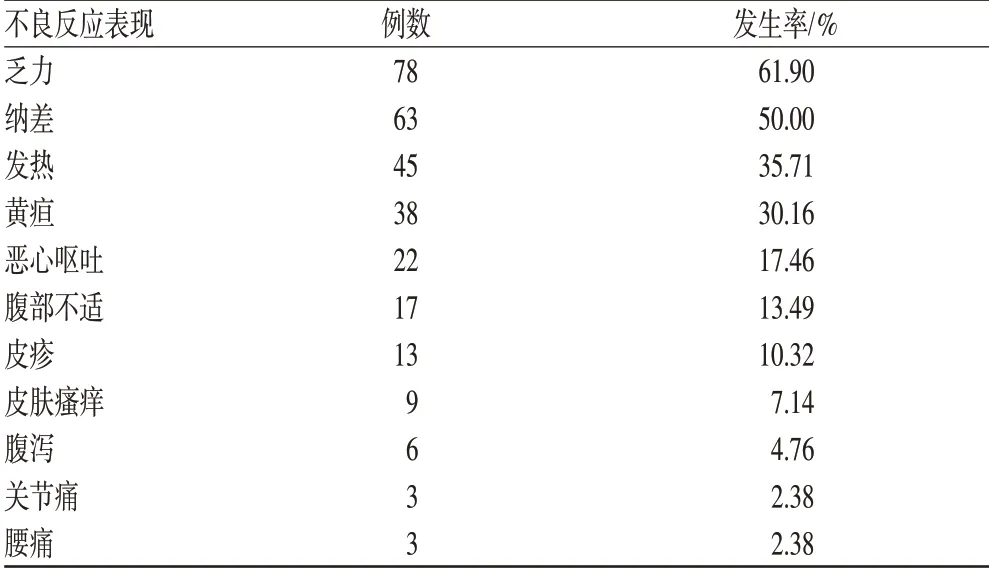
表4 DILI的不良反应Tab 4 Clinical manifestation of adverse drug reactions in drug-induced liver injury
3 讨论
引起DILI 的药物复杂多样,依照药物的毒性和宿主的易感性间的关系,分为可预测性和不可预测性肝毒性。前者与剂量和疗程相关,应用药物的大多数个体可发生DILI;后者由于个体对药物或代谢产物产生的免疫反应所致,与用药的剂量和疗程无关[5]。DILI的易感因素与患者高龄、女性、联合用药、环境因素、基础疾病及遗传易感性等多种因素有关[6-7]。近年来,DILI的发病率逐渐上升,已成为国内外常见且较严重的药源性疾病,在急性肝衰竭患者中有13%~15%是由药物引起[8]。DILI的发生机制至今尚未阐述清楚,以中毒性肝损害为主。多数学者认为,DILI的发生于细胞色素P450、CYP3A4的生物活性、氧化应激、线粒体功能受损、细胞凋亡及免疫功能异常等因素有关[9]。临床上对DILI 的治疗原则是早期诊断,立即停止损害肝功能药物并予以降黄、保肝、营养支持等对症治疗,多数患者预后良好。
3.1 西药所致DILI的临床分析
统计表明,引起DILI 的药物主要以大环内酯类药、调脂药、抗病毒药及抗肿瘤药为主,与国内多中心调研结果[10]相似。相关西药的肝损伤毒性或不良反应在药品说明书或药典中有详细描述,临床使用时须加以重视并做好防护准备[9]。用药途径多以口服为主,目前人们滥用药物是导致DILI 增加的直接原因。抗肿瘤药均有较强的细胞毒性,且大多数经由肝脏分解代谢,但不同患者肝损害程度不等,与其个体异质性有关。大环内酯类药经由解毒及药物转化而引起以胆汁淤积为主的肝损害。部分抗结核药(如利福平)直接损害肝脏,且肝损害程度与药物的剂量有关。
3.2 中药所致DILI的临床分析
中药所致肝损害的作用机制至今尚不清楚,但是近年来有关于中药所致肝损害的报道越来越多[11],使大家逐渐认识到中药并不是无毒害作用。本研究发现,中药引起DILI共46例(36.51%)。有研究已证明,川楝子、防已、木通、柴胡、雷公藤、栀子等中药成分均可造成肝功能损害[12]。中药成分及药理作用复杂多样,且纯度和精度受到当前制备工艺很大的限制,各成分间剂型、剂量、配伍多样,且受到患者年龄、体质量影响。因此,医师应谨慎用药,合理配伍,尽可能减少肝毒性药物的使用。中药致肝损害的影响因素包括药物本身的毒性作用,中药使用不当,未遵照中医药辨证施治的基本要求,乱用、误用或剂量过大等[13]。
3.3 DILI的临床特征
DILI患者多为急性肝功能损害,好发生于药物治疗后4周或8周以内[14]。本组研究患者经过治疗后,痊愈和好转率合计为91.27%;其余患者因病情进展迅速、危重,10例患者放弃治疗,1例患者因未立即停用损害肝脏的药物而发生急性肝功能衰竭,最终导致死亡。因此,医师应提高对DILI 的警惕,在对患者使用肝损害药物治疗过程中应密切监测肝功能,以便早期发现DILI。
预后佳的患者与预后差的患者在ALT及AST方面差异无统计学意义(P>0.05);但在TBIL、DBIL及ALB方面差异有统计学意义(P<0.05),预后差的患者TBIL、DBIL 水平明显增高,说明TBIL、DBIL及ALB水平与患者预后有关。
DILI 缺乏典型的临床特征,与病毒性肝炎的症状无明显区别,在临床诊断上有较大的困难[4]。本研究中患者主要的临床表现为乏力、纳差、恶心呕吐、发热等,诊断较困难,对于无明显诱因的肝损害患者,临床多采用肝穿刺检查以尽早诊断和明确肝损害程度,为临床治疗和判断预后提供客观依据。
综上所述,DILI与感染性肝炎在临床表现,在各项实验室指标等方面相似度较高,缺乏特征性,临床上大多数药物存在肝毒性。因此,用药时应加强监测,提高对DILI的早期诊断和及时正确的治疗,促进患者好转。
[1] Christina WN,Christoph S.Drug induced liver injury and its relationship to autoimmune hepatitis[J].J Hepatol,2011,55(5):747-749.
[2] Maria VA,Victorino RM.Development and validation of a clinical scale for the diagnosis of drug-induced hepatitis[J].Hepatology,1997,26(3):664-669.
[3] 中华医学会感染病学分会肝功能衰竭与人工肝学组,中华医学会肝病学分会重型肝病与人工肝学组.肝功能衰竭诊疗指南[J].中华肝脏病杂志,2006,14(9):643-646.
[4] 滕光菊,孙颖,常彬霞,等.418例药物性肝损害临床特征及预后分析[J].肝脏,2013,18(1):11-14.
[5] 张琪,彭劫,侯金林.药物性肝损害临床特点及预后相关因素分析[J].广东医学,2008,29(7):1102-1104.
[6] 刘新胜,臧红,游绍莉,等.288例药物性肝损害的临床诊断及病理学分析[J].传染病信息,2013,26(3):168-170.
[7] 陈慧,郑聘聘,王炳元.药物诱发自身免疫性肝炎的研究进展[J].传染病信息,2011,24(5):313-318.
[8] Au JS,Navarro VJ,Rossi S.Review article:drug induced liver injury-its pathophysiology and evolving diagnostic tools[J].Aliment Pharmacol Ther,2011,34(14):11-20.
[9] 胥冰,黄峰.药物性肝损害87 例临床特征分析[J].海南医学,2013,24(5):677-679.
[10] 杨桂深,李桂仙.抗结核药物致药物性肝损害100 例临床观察[J].海南医学,2010,21(11):75-76.
[11] Tafazolis,Mashregim,Obrien PJ,et al.Role of hydrazine in isoniazid-induced hepatotoxicity in a hepatocyte inflammation model[J].Toxicol Appl Pharmacol,2008,229(1):94-101.
[12] 刘翠平,邹衍泰,白岚.670 例药物性肝损害分析[J].现代消化及介入诊疗,2010,15(6):338-340.
[13] 臧红,游绍莉,柳芳芳,等.中药药物性肝损害的临床特征及预防[J].实用预防医学,2013,20(9):1025-1027.
[14] 李丰衣,李筠.中药药物性肝损害的研究现状[J].中华中医药杂志,2009,24(3):265-268.

