过渡金属离子与3-氟邻苯二甲酸和1,10-邻菲啰啉配合物的合成、结构及性质
宋 爽 查玉娥 王育丰 刘一恒 李 夏
(首都师范大学化学系,北京 100048)
近年来,配位聚合物的设计与合成越来越受到人们的关注,它们不仅结构新颖多样,而且在非线性光学材料、催化、气体储存、荧光材料、磁性材料等领域具有潜在的应用价值[1-10]。在设计配合物的过程中,选择合适的配体是人们关注的重点。邻苯二甲酸及其衍生物具有2个羧基,可以多种配位方式如单齿、鳌合、桥式等与金属离子配位,形成链状和网状等多种结构的配合物。邻苯二甲酸类分子含有较大的共轭体系,可以增强配合物的荧光性质和热稳定性。有关邻苯二甲酸类的金属配合物有较多报道[11-17]。而以氟代邻苯二甲酸作为配体的金属配合物报道得较少[18]。3-氟邻苯二甲酸作为有机配体具有邻苯二甲酸本身固有的优点,氟是电负性最高的元素,具有较强的吸电子能力,能够将其邻、对位活化,增强配合物的酸性;氟原子在3位,降低了分子的对称性,并对苯环上的2个羧基产生一定的空间位阻效应,使苯环上的2个羧基产生不同的扭转角。另外配体上的氟原子能与配合物体系中的氢原子形成H…F键;氟原子还能与体系中的π环形成F…π弱作用力,从而使配合物由低维结构构筑成高维的超分子结构。1,10-邻菲啰啉具有刚性、平面性和芳香性,具有强的配位能力,被广泛用于金属-有机配合物的合成[19-23]。1,10-邻菲啰啉的协同配位可以增强配合物的稳定性和发光性。本文中,我们选用过渡金属离子为中心,以3-氟邻苯二甲酸(H2Fpht)和1,10-邻菲啰啉(phen)为配体,通过水热法合成5个配合物:[M(Fpht)(phen)(H2O)3]·H2O(M=Ni 1,Co 2),[Cu(Fpht)(phen)(H2O)]·H2O(3),[M(Fpht)(phen)(H2O)]·H2O(M=Zn 4,Cd 5)。 本文报道配合物的合成、晶体结构及性质。
1 实验部分
1.1 试剂和仪器
3-氟 邻苯二甲 酸 , 1,10-邻 菲 啰 啉 , 3CdSO4·8H2O,Zn(Ac)2·2H2O,Cu(NO3)2·3H2O,Ni(NO3)2·6H2O和CoCl2·6H2O均为分析纯试剂。
德国Elementar公司Vario ELIII型元素分析仪。德国EQUINOX55型红外光谱仪(KBr压片)。日立F-4500型荧光分光光度仪。德国 Bruker DTG-60A H型微热-差热天平,以Al2O3为参比,空气气氛中,升温速度为10℃·min-1,由室温到800℃范围记录配合物的差热-热重分析。
1.2 配合物的合成
[Ni(Fpht)(phen)(H2O)3]·H2O(1)的合成: 将 0.2 mmol的 Ni(NO3)2·6H2O 和 0.2 mmol的 3-氟邻苯二甲酸溶于10 mL去离子水中,加热搅拌,滴加0.15 mL 2 mol·L-1的氢氧化钠溶液,再加入0.1 mmol的1,10-邻菲啰啉,倒入25 ml聚四氟乙烯反应釜中,120℃下加热3 d后,降至室温,此时得到绿色块状晶体(产率:42%)。C20H19NiFN2O8(493.06),元素分析理论 值(%):C,48.72;H,3.88;N,5.68; 实 际 值(%):C,48.34;H,4.13;N,5.98。红外光谱(KBr压片,ν/cm-1):3 398(s),1 561(s),1 470(w),1 396(s),1 242(m),1 148(w),959(w),850(m),772(m),690(w),475(w)。
[Co(Fpht)(phen)(H2O)3]·H2O(2)的合成:配合物 2的合成方法与1类似,用CoCl2·6H2O代替Ni(NO3)2·6H2O,反应温度为120℃,得到紫色块状晶体(产率:40%)。C20H19CoFN2O8(493.30),元素分析理论值(%):C,48.69;H,3.88;N,5.68;实际值(%):C,48.45;H,4.02;N,5.73。 红外光谱(KBr压片,ν/cm-1):3401(s),1906(w),1561(s),1471(m),1395(s),1242(m),1147(m),1048(w),958(m),867(s),773(s),688(m),542(w),474(m)。
[Cu(Fpht)(phen)(H2O)]·H2O(3)的合成:合成方法同配合物 1,用 Cu(NO3)2·3H2O 代替 Ni(NO3)2·6H2O,得到蓝色块状晶体 (产率:33%)。C20H15CuFN2O6(461.89),元素分析理论值(%):C,52.01;H,3.27;N,6.06;实际值(%):C,51.61;H,3.30;N,6.33。红外光谱(KBr压片,ν/cm-1):3 436(s),1 631(s),1 569(s),1 521(m),1 478(w),1 453(w),1 432(m),1 409(s),1 360(s),1 245(m),1 110(w),968(w),875(m),851(w),819(s),783(s),741(s),721(m),694(w),485(w)。
[Zn(Fpht)(phen)(H2O)]·H2O(4)的合成:合成方法同配合物 1,用 Zn(Ac)2·2H2O 代替 Ni(NO3)2·6H2O,得到无色针状晶体 (产率:36%)。C20H15ZnFN2O6(463.75),元素分析理论值(%):C,51.80;H,3.26;N,6.04;实际值(%):C,51.53;H,3.45;N,5.83。红外光谱(KBr压片,ν/cm-1):3 413(s),1 622(s),1 518(w),1 429(m),1 375(s),1 238(s),1 143(w),964(m),850(s),728(s),642(w),555(m)。
[Cd(Fpht)(phen)(H2O)]·H2O(5)的合成:将 0.1 mmol 3CdSO4·8H2O和0.1 mmol 3-氟邻苯二甲酸溶于 10 mL去离子水中,加热搅拌,滴加0.05 mL 2 mol·L-1的氢氧化钠溶液,再加入0.05 mmol 1,10-邻菲啰啉,此刻有白色沉淀生成,缓慢滴加0.5 mol·L-1的硫酸溶液,直到溶液刚好澄清,倒入25 ml聚四氟乙烯反应釜中,120℃下加热3 d后,降至室温,得到无色块状晶体 (产率:34%)。C20H15CdFN2O6(510.75),元素分析理论值 (%):C,47.03;H,2.96;N,5.48; 实际值 (%):C,46.94;H,3.27;N,5.39。红外光谱(KBr压片,ν/cm-1):3 423(s),1 618(s),1 596(s),1 573(s),1 516(m),1 477(w),1 429(w),1 381(s),1 360(s),1 238(m),1 142(w),962(w),853(m),808(w),772(s),728(m),700(m),640(w),470(w)。
1.3 晶体结构测定
选取合适大小的单晶,在Bruker Smart 1000 CCD X-射线单晶衍射仪上,使用经石墨单色器单色化的Mo Kα射线(λ=0.071 073 nm)收集衍射强度数据。晶体结构由直接法解出[24],对全部非氢原子坐标及各向异性热参数基于F2进行全矩阵最小二乘法精修[25]。水分子上的氢原子从差值傅立叶图上找到,其余氢原子均为理论加氢。主要晶体学数据列于表1中,主要键长和键角列于表2中。
CCDC:821532,1;851832,2;936807,3;806132,4;851838,5。
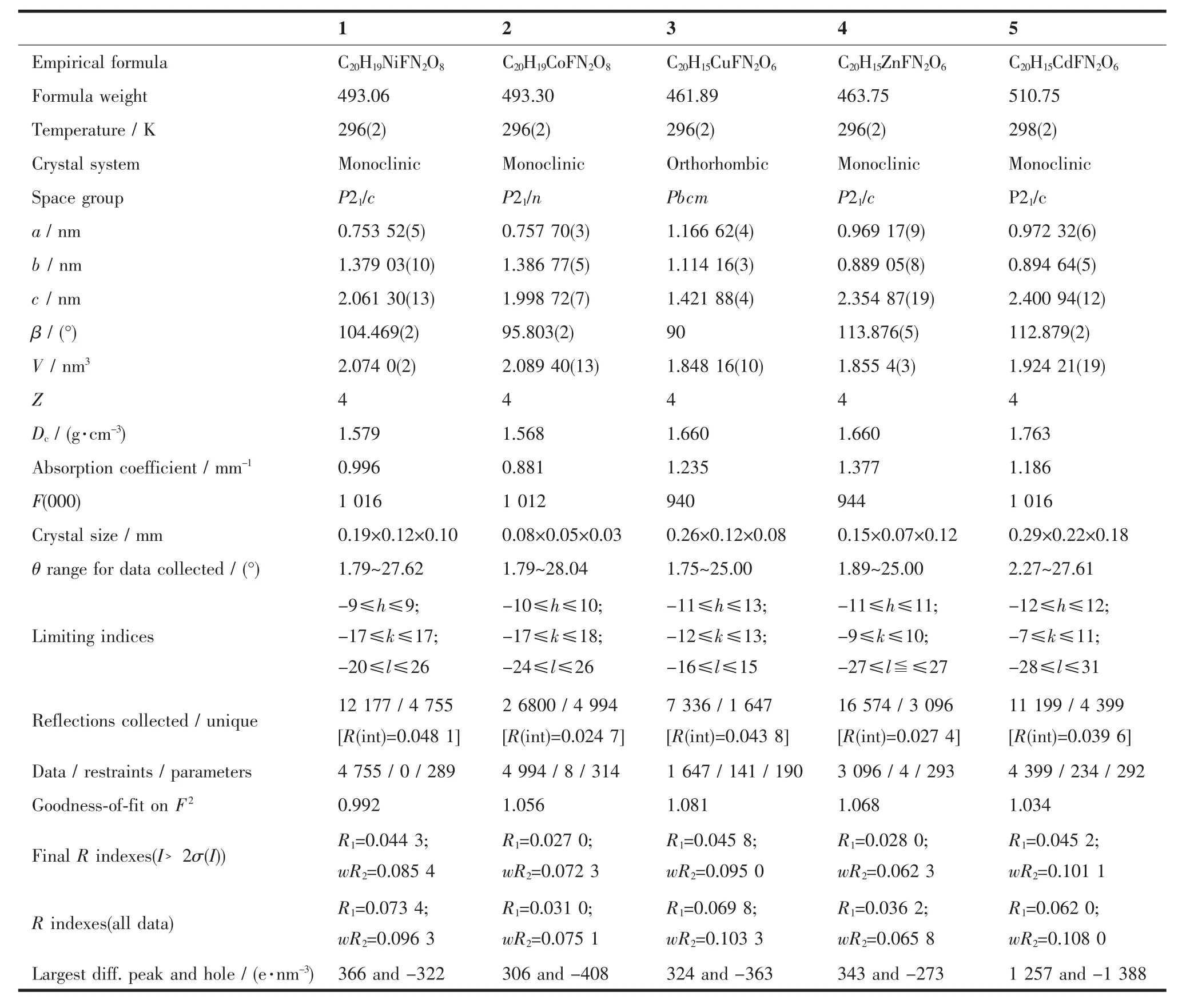
表1 配合物1~5的晶体数据Table 1 Crystallographic data of complex 1~5
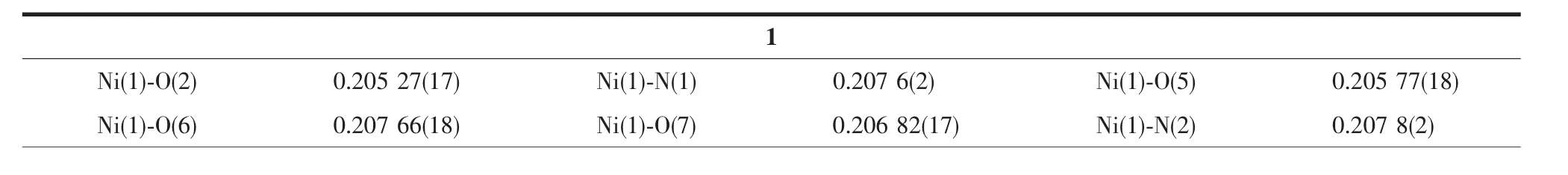
表2 配合物1~5的主要键长和键角Table 2 Selected bond lengths(nm)and bond angles(°)for complexes 1~5

Continued Table 2
2 结果与讨论
2.1 配合物[M(Fpht)(phen)(H2O)3]·H2O(M=Ni 1,Co 2)的晶体结构
配合物1与2具有相似的单核结构,仅以1为例描述其晶体结构。Ni(Ⅱ)的配位环境及原子标号如图1a所示。该配合物是由单核分子[Ni(Fpht)(phen)·(H2O)3]和1个游离水分子构成。Ni(Ⅱ)离子与3-氟邻苯二甲酸根的1个氧原子 (O2)、1,10-邻菲啰啉的2个氮原子(N1和N2)以及3个水分子氧原子(O5,O6和O7)配位,形成了六配位的扭曲八面体(图1a)。Ni-O(水)的键长范围为 0.205 8(18)~0.207 7(18)nm。 Ni-N的键长为0.207 6(2)和0.207 8(2)nm。Ni-O(羧基)的键长为0.205 3(17)nm。1,10-邻菲啰啉通过2个N原子螯合配位于Ni(Ⅱ)离子。3-氟邻苯二甲酸根的1个羧基采取单齿配位方式,另1个羧基未配位。晶格水分子(H8a-O8-H8b)与3-氟邻苯二甲酸中的羧基氧原子 (O1和O4C)形成了氢键,O8-H8a…O1和O8-H8b…O4C(对称操作 C:x+1,y,z),O…O 键长分别为0.270 2和0.275 5 nm。1,10-邻菲啰啉的C5AH5A与3-氟邻苯二甲酸根的氟原子F1,形成C-H…F氢键,C…F键长为0.333 8 nm。1,10-邻菲啰啉上的C8-H8基团与3-氟邻苯二甲酸根的苯环平面(C14B~C19B)形成C-H…π键,H到苯环质心距离为0.354 1 nm。这些弱作用将配合物分子构筑成三维超分子网状结构(图1b)。
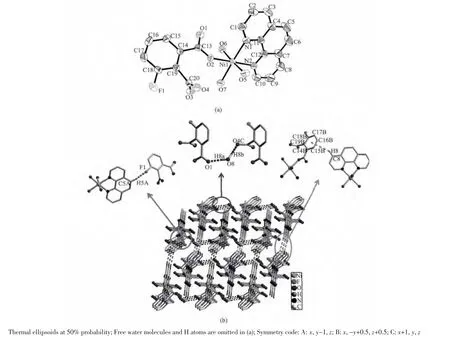
图1 配合物1的(a)不对称单元,(b)由氢键构筑的3D结构Fig.1 Structure of the complex 1:(a)asymmetric unit,(b)3D structure by hydrogen bonds
2.2 配合物[Cu(Fpht)(phen)(H2O)]·H2O(3)的晶体结构
配合物3为Z字形一维链状结构,配合物3属于正交晶系Pbcm空间群。不对称单元包括1个Cu(Ⅱ)离子,1个3-氟邻苯二甲酸根配体,1个1,10-邻菲啰啉配体,1个配位水分子和1个游离水分子。Cu(Ⅱ)离子是五配位的,配位环境及原子标号如图2a所示。Cu(Ⅱ)离子与2个3-氟邻苯二甲酸根的2个O原子(O1和 O1A),1个 1,10-邻菲啰啉的 2个N原子(N1和N1A)以及1个水分子的O原子(O1W)配位,形成四方锥构型,O1W为四方锥的顶。Cu-O1键长为0.193 1(3)nm,Cu-N键长为0.201 3(4)nm。Cu-O1W键长为0.239 5(5)nm,明显长于锥底边的Cu-O1键长,因此有Jahn-Teller扭曲。1,10-邻菲啰啉的2个氮原子螯合配位于 Cu(Ⅱ)离子,3-氟邻苯二甲酸根的2个羧基均以单齿方式配位,2个羧基所在面与苯环面的夹角为 54.118°(图 2b)。Cu(Ⅱ)离子通过 3-氟邻苯二甲酸根桥连,形成Cu-Fpht-Cu一维Z字形链,Cu…Cu…Cu键角为 133.862°,Cu…Cu的距离为0.772 7(6)nm(图 2b)。
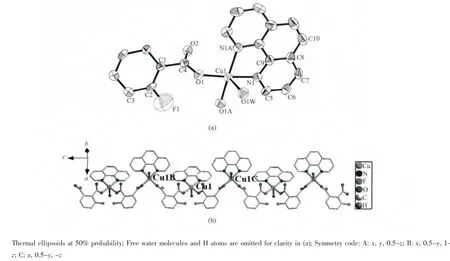
图2 配合物3的(a)不对称单元,(b)一维Z字形链Fig.2 Structure of the complex 3(a)the asymmetric units(b)1D zigzag chain
2.3 配合物[M(Fpht)(phen)(H2O)]·H2O(M=Zn 4,Cd 5)的晶体结构
配合物4与5具有相似的结构,仅以5为例描述其晶体结构。Cd(Ⅱ)的配位环境及原子标号如图3a所示。配合物是由3-氟邻苯二甲酸根配体桥联Cd(Ⅱ)离子而形成的1D螺旋链状聚合物。该配合物的1个不对称单元包括1个晶体学独立的Cd(Ⅱ)离子,1个3-氟邻苯二甲酸根配体,1个1,10-邻菲啰啉配体,1个配位水和1个自由水分子。Cd(Ⅱ)离子与2个3-氟邻苯二甲酸根的3个氧原子 (O1,O2和O4A)、1,10-邻菲啰啉的2个氮原子(N1和N2)以及1个水分子的氧原子(O5)配位,形成六配位的扭曲八面体(图 3a)。 Cd-O(羧基)的键长范围为 0.215(3)~0.265(3)nm。Cd-N的键长范围为0.233 1(3)~0.233 5(4)nm。Cd-O(水分子)的键长为0.229 9(3)nm。3-氟邻苯二甲酸根的2个羧基分别采取单齿和双齿螯合配位方式,其中1个氧原子没有参与配位。3-氟邻苯二甲酸根的2个羧基与其苯环平面分别呈112.5°和114.1°夹角。1,10-邻菲啰啉与中心金属Cd(Ⅱ)通过2个配位的N原子构成了1个五元环。3-氟邻苯二甲酸根桥连Cd(Ⅱ)离子形成了Cd-Fpht-Cd一维链,Cd…Cd…Cd键角为94.41°,Cd…Cd键长为0.609 6(4)nm。有趣的是,Cd-Fpht-Cd是沿b轴方向的一维手性螺旋链(图3b)。晶格中交替出现左手螺旋链和右手螺旋链,因此配合物5是外消旋体(图3c)。1,10-邻菲啰啉分子位于螺旋链的两侧。1,10-邻菲啰啉平面与3-氟邻苯二甲酸根的苯环平面之间的二面角为49.9°。1,10-邻菲啰啉的C-H键与3-氟邻苯二甲酸中的F原子和O原子形成了C-H…F和C-H…O氢键。螺旋链沿c轴方向堆积,并通过层间氢键相互作用进而构筑成三维网络结构。相邻邻菲啰啉平面间的面心距为0.383 7 nm。相邻螺旋链间的1,10-邻菲啰啉环互相平行,二面角为0°。1,10-邻菲啰啉N1-C1-C2-C3-C4-C11环平面与来自相邻螺旋链的1,10-邻菲啰啉C4-C5-C6-C7-C12-C11环平面间的质心间距为0.3778 nm(质心坐标:(1+x,1.5-y,0.5+z),(1-x,-0.5+x,1.5-z))。说明相邻螺旋链间的1,10-邻菲啰啉环之间存在π-π堆积弱作用力。π-π堆积弱作用力将1D链构造成2D超分子结构(图3c)。体系中的晶格水(O5)与配位水(O6)之间形成了氢键,O5-H5A…O6,O…O键长为0.288 3(5)nm。因此晶格水分子以氢键作用力键合在超分子结构中。

图3 配合物 5的 (a)不对称单元,(b)1D螺旋链,(c)左右手螺旋结构Fig.3 Structure of the complex 5:(a)asymmetric unit,(b)1D helical chain,(c)left and right helical chains
2.4 配合物的荧光光谱
室温下,在荧光分光光度仪上记录了配体和配合物的固态发射光谱。在350~650 nm范围内,分别以最大激发波长测得3-氟邻苯二甲酸、1,10-邻菲啰啉和配合物1~5的发射光谱(图4)。3-氟邻苯二甲酸在419和437 nm处存在2个发射峰 (λex=365 nm)。1,10-邻菲啰啉在420和436 nm处存在2个发射峰(λex=377 nm)。配合物1在433和458 nm处出现2个发射峰(λex=401 nm),配合物2在434 nm附近出现1个宽峰(λex=374 nm)。配合物3在419和439 nm处有2个发射峰 (λex=373 nm),配合物4在420和443 nm处出现2个发射峰(λex=389 nm),配合物5在378 nm 有一个发射峰(λex=345 nm)。 配合物 1~4的发射峰与配体相似,可认为配合物1~4的荧光来自配体的π*-π电子跃迁。配合物5相对于配体,发生了明显的蓝移,可能因为Cd(Ⅱ)离子处于第四周期,4d轨道比3d轨道发散,更容易受配体影响,是金属离子微扰的配体发光。

图4 配体和配合物的荧光光谱Fig.4 Fluorescence spectra of the ligands and complexes
2.5 配合物的差热-热重分析
以Al2O3为参比,空气气氛,在室温~800℃范围内对配合物1~5进行了差热-热重分析(图5)。配合物首先失去全部水分子。开始失重的温度为130℃(1),132 ℃ (2),93 ℃ (3),113 ℃ (4)和 110 ℃ (5);失重率为 14.66%(1),14.79%(2),8.70%(3),7.51%(4)和 6.76% (5)(理论值为 14.60% (1),14.60%(2),7.50%(3),7.76%(4)和 7.04%(5))。最终的分解产物为相应的氧化物。总失重在417℃ (1),419℃(2),437℃ (3),490℃ (4)和 497℃ (5); 失重率为83.83%(1),84.73%(2),81.56%(3),81.55%(4) 和73.74%(5)(理 论 值 为 84.85%(1),84.81%(2),83.3 3%(3),82.49%(4)和 74.94%(5))。
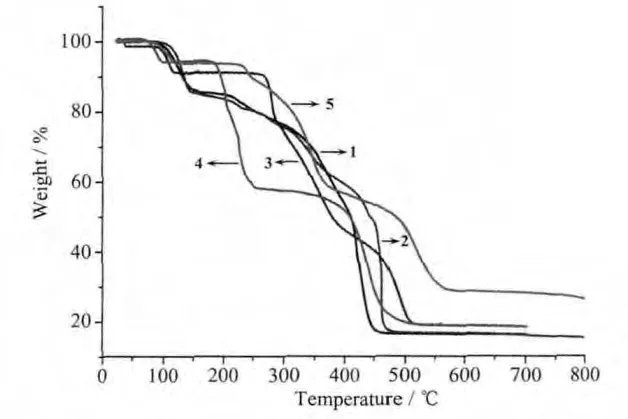
图5 配合物1~5的热分解曲线图Fig.5 TG curves of complexes 1~5
3 结 论
选择3-氟邻苯二甲酸和1,10-邻菲啰啉为配体,与二价过渡金属离子组装了5个配合物:[M(Fpht)(phen)(H2O)3]·H2O (M=Ni 1,Co 2),[Cu(Fpht)(phen)(H2O)]·H2O(3)和[M(Fpht)(phen)(H2O)]·H2O(M=Zn 4,Cd 5)。同属第三过渡相邻元素 Ni(Ⅱ)和Co(Ⅱ)离子配合物具有相似的单核分子结构,ⅡB族的Cd(Ⅱ)和Zn(Ⅱ)离子配合物具有相似的一维螺旋结构,而IB族Cu(Ⅱ)离子配合物为Z字形一维链状结构。Ni(Ⅱ)、Co(Ⅱ)和Zn(Ⅱ)、Cd(Ⅱ)离子均为六配位的八面体构型但具有不同的配位环境,而Cu(Ⅱ)离子为五配位的四方锥构型。3-氟邻苯二甲酸根在配合物1和2中采取单齿配位方式,在3中采取单齿/单齿配位方式,在4和5中采取单齿/双齿螯合配位方式。1,10-邻菲啰啉均作端基配体螯合配位于金属离子。这些结果说明,配合物的晶体结构与金属离子的配位环境和3-氟邻苯二甲酸的配位方式有关。
[1]Kitagawa S,Kitaura R,Noro S.Angew.Chem.Int.Ed.,2004,43:2334-2375
[2]Cui Y J,Yue Y F,Qian G D,et al.Chem.Rev.,2012,112:1126-1162
[3]Zhang Z J,Zhao Y G,Gong Q H,et al.Chem.Comm.,2013,49:653-661
[4]Huang Y G,Jiang F L,Hong M C.Coord.Chem.Rev.,2009,253:2814-2834
[5]Armelao L,Quici S,Barigelletti F,et al.Coord.Chem.Rev.,2010,254:487-505
[6]Xiong S S,He Y B,Krishna R,et al.Cryst.Growth Des.,2013,13:2670-2674
[7]Coronado E,Espallargas G M.Chem.Soc.Rev.,2013,42:1525-1539
[8]Wang C,Lin W B.J.Am.Chem.Soc.,2011,133:4232-4235
[9]Son H J,Jin S Y,Patwardhan S,et al.J.Am.Chem.Soc.,2013,135:862-869
[10]Horcajada P,Chalati T,Serre C,et al.Nat.Mater.,2010,9:172-178
[11]Kan W Q,Yang J,Liu Y Y,et al.CrystEngComm,2012,14:6934-6945
[12]Cheng P C,Kuo P T,Liao Y H,et al.Cryst.Growth Des.,2013,13:623-632
[13]Wang X L,Luan J,Lin H Y,et al.Dalton Trans.,2013,42:8375-8386
[14]Wan Y H,Zhang L P,Jin L P,et al.Inorg.Chem.,2003,42:4985-4994
[15]GONG Wei(巩伟),NIU Qiong(牛琼),NIU He-Lin(牛和林),et al.Chinese J.Inorg.Chem.(无机化学学报),2013,29(3):642-648
[16]TAO Zhao-Lin(陶兆林),CUI Jie-Hu(崔节虎),QIN Ling(覃玲),et al.Chinese J.Inorg.Chem.(无机化学学报),2012,28(12):2633-2637
[17]LI Kai-Hui(李凯慧),XU Kai(许凯),MEI Shi-Le(梅世乐),et al.Chinese J.Inorg.Chem.(无机化学学报),2013,29(6):1312-1318
[18]Cha Y E,Li X,Song S.J.Solid State Chem.,2012,196:40-44
[19]Gu J Z,Gao Z Q,Tang Y.Cryst.Growth Des.,2012,12:3312-3323
[20]Li Y,Zheng F K,Liu X,et al.Inorg.Chem.,2006,45:6308-6316
[21]JIANG Yong(蒋 勇),QIU Xiao(邱 晓),LI Xia(李 夏),et al.Acta Chim.Sinica(化学学报),2012,70(3):303-310
[22]HUANG Yan-Ju(黄艳菊),NI Liang(倪良),WANG Qiang(王强).Chinese J.Inorg.Chem.(无机化学学报),2012,28(5):1050-1054
[23]LI Gong-Chun(李公春),WANG Hong-Sheng(王宏胜),ZHU Lei(朱蕾),et al.Chinese J.Inorg.Chem.(无机化学学报),2012,28(11):2369-2372
[24]Sheldrick G M.SHELXS 97,Program for X-ray Crystal Structure Solution.University of Göttingen,1997.
[25]Sheldrick G M.SHELXL 97,Program for X-ray Crystal Structure Refinement.University of Göttingen,1997.

