pH 敏感型紫杉醇胶束的工艺优化
刘佳,许建国,张灿 (.江苏省苏北人民医院药剂科,江苏 扬州,500;.中国药科大学药学院,江苏 南京0009)
紫杉醇(paclitaxel,PTX)是一类具有抗微管作用机理的广谱细胞毒类抗癌药,目前广泛应用于对卵巢癌、乳腺癌、头颈部癌、非小细胞性肺癌及前列腺癌的治疗中。临床常用制剂是以聚氧乙烯蓖麻油和无水乙醇为混合溶剂的紫杉醇的油溶液。该制剂中的聚氧乙烯蓖麻油静注后会引起严重的毒副作用,如过敏、神经毒性等[1]。
聚合物胶束已经成了药物传递系统研究领域的一个热门,它由两亲性的高分子材料在水环境中自组装形成、具有均一纳米级粒径及球形的核壳结构纳米粒[2]。张灿课题组报道了多种壳聚糖衍生物胶束用于增溶难溶性药物,其中以N-辛基为疏水链,酰胺键连接的环己烷二甲酸为亲水链修饰连接在壳聚糖主链上合成了一系列pH 敏感的两亲性衍生物N-辛基-N’-(2-羧基环己甲酰基)-壳聚糖(OCCC)。将其溶于水中可自发形成具有壳核结构的胶束,而且通过酰胺键连接的亲水外层在正常生理环境(pH 7.4)下稳定存在,通过EPR(enhanced permeability and retention effect,高通透性和滞留效应)效应到达肿瘤组织进入内涵体或溶酶体后,弱酸性环境(pH 5.0~6.0)使连接臂发生水解,胶束外壳的亲水部分断裂,胶束结构被破坏并迅速释放出药物,达到提高治疗药物胞内浓度的目的,从而实现肿瘤治疗的有效性和安全性。前期研究表明胶束在正常生理环境下稳定,而在微酸性环境下敏感,细胞毒研究表明其为无毒和安全的药物载体[3]。
中心面复合设计优化法(central composite design,CCD),是一种多元非线性拟合的实验设计方法,根据非线性数学模型描绘效应面优选条件,故而模型具有精度高,预测性较好的特点[4]。因此,本实验采用此法优选pH 敏感型紫杉醇胶束的处方。
1 材料
N-辛基-N’-(2-羧基环己甲酰基)-壳聚糖(脱乙酰度97%,辛基取代度36%,自制, 批号20090805);紫杉醇(江苏红豆杉生物科技有限公司,99.66%,批号20090528);甲醇(色谱纯,江苏汉邦科技有限公司);重蒸水(自制);其他化学试剂均为分析纯。
微孔滤膜(上海新亚净化器件厂);透析袋(截留相 对 分 子 质 量10 kDa,Sigma-Aldrich 公 司);H66025T 型超声仪(无锡电子设备厂);电子天平(北京塞多利斯天平有限公司);Agilent 1050色谱仪(美国Agilent公司);Zetasizer 3000HSA 粒径电位仪。
2 方法与结果
2.1 紫杉醇胶束制剂的制备与含量测定 采用透析法制备紫杉醇胶束[5]。OCCC和紫杉醇分别溶于去离子水和无水乙醇中,随后在磁力搅拌下(室温,500r·min-1)将紫杉醇的乙醇液逐滴加入至OCCC的水溶液中,所得乳白色溶液加入透析袋中(截留相对分子质量10kDa)随后在去离子水中透析,分别过0.8,0.45,0.22μm 的微孔滤膜。滤液加入5%的甘露醇为保护剂后冻干,冻干样品在4 ℃下避光保存。用马尔文粒径仪,633nm 的He-Ne光在25℃下测定得到胶束的粒径和Zeta电位。
HPLC法测定得到胶束的载药量(drug loading rate,DL)和 包 封 产 率(entraptment efficiency,EE)。液相色谱条件为:色谱柱Lichrospher C18(4.6mm×250mm,5μm,江苏汉邦);流动相甲醇-水为75∶25(v/v);流速1mL·min-1;柱温25 ℃;进样量20μL;检测波长227nm。吸取一定量的胶束溶液用流动相稀释50倍后进样测含量。标准曲线:C=2.49×10-2A+1.299 7,r=0.999 9,线性范围10.0~100.0μg·mL-1。标准曲线的日间、日内RSD 均小于10%,精密度良好。载药量(DL)和包封产率(EE)的计算公式为:
mPTX1:被载入胶束的紫杉醇质量,mOCCC:载药时投入的OCCC质量,mPTX2:载药时投入的紫杉醇质量。

2.2 单因素试验 影响胶束载药的因素很多,首先对这些因素进行了筛选。选择胶束的载药量,包封产率,粒径以及多分散指数(polydispersity index,PI)为考察指标,比较不同因素水平对含量的影响。当改变某一因素水平时其他因素保持不变,如果各考察指标在该因素不同水平下没明显变化,则认为该因素无影响将其去除。
2.2.1 药载比(PTX/OCCC,w/w)的影响 配制溶度为50mg·mL-1的紫杉醇乙醇溶液和浓度为6 mg·mL-1的OCCC溶液。在磁力搅拌下,分别吸取0.09,0.135,0.18,0.27,0.315,0.36,0.45mL紫杉醇溶液(药载比分别是0.3,0.45,0.6,0.75,0.9,1.05,1.2,1.5)滴加入2.5mL 载体溶液中,每个药载比制备3份样品,按“2.1”项下方法制备和测定含量,计算载药量及包封产率,用粒径仪测定胶束粒径及多分散指数。
胶束的载药量、包封产率、粒径以及多分散指数的变化如图1所示。
随着药载比升高,胶束的载药量和包封产率逐渐增大,且粒径逐渐减小,多分散指数变化不大,但药载比大于1.05后,载药量及包封产率开始下降,而且粒径和多分散指数也显著升高。这可能是因为材料疏水内核对药物的容纳能力有限,药载比为0.3,0.45,0.6时其包封产率没有显著性差异,当药载比大于1.05时,包封产率开始下降,说明药载比为1.05时载体达到了载药饱和能力。

图1 药载比(PTX/OCCC,w/w)对胶束(a)载药量和包封产率以及(b)粒径和PI的影响(n=3)Fig 1 Effect of different ratios of PTX/OCCC(w/w)on micelle(a)DL and EE(b)size and PI(n=3)
2.2.2 OCCC 载体浓度的影响 配制质量浓度为3.0,6.0,9.0,12.0,15.0 mg·mL-1的OCCC 载 体溶液和50mg·mL-1的紫杉醇乙醇液,在磁力搅拌下,分别吸取0.15,0.3,0.3,0.45,0.60,0.75mL的药物溶液逐滴滴加入2.5mL载体溶液中,每个药载比制备3 份样品,按“2.1”项下方法制备和测定含量,计算载药量及包封产率,用粒径仪测定胶束粒径及多分散指数。所得结果如图2所示。

图2 载体浓度对胶束(a)载药量和包封产率以及(b)粒径和PI的影响(n=3)Fig 2 Effect of different concentration of OCCC on micelle(a)DL and EE(b)size and PI(n=3)
随着载体浓度的升高载药量和包封产率逐渐上升,在6.0mg·mL-1时达到最大,以后载药过程中有紫杉醇泄露导致载药量和包封产率迅速下降。而粒径和多分散指数也显著变化,随着载体浓度的升高,粒径和PI逐渐增大,但是大于6.0mg·mL-1时,由于载药过程中胶束的泄露和破坏,胶束粒径和多分散指数显著增加,浓度更高时无法测定。这可能由于浓度高的载体溶液中,聚合物单体大量增加,这时溶液为维持体系的稳定开始形成胶束的二次聚集[6],随着浓度的增加粒径显著增加的变化也证实了这点,而这不利于形成球形的胶束因此不能稳定载药。
2.2.3 药物浓度的影响 配制质量浓度为30,40,50,60,70 mg·mL-1紫杉醇的乙醇溶液和6 mg·mL-1的OCCC 溶液。在磁力搅拌下,分别吸取0.5,0.375,0.3,0.25,0.214mL药物溶液逐滴滴加入2.5mL载体溶液中,每个药载比制备3份样品按“2.1”项下方法制备和测定含量,计算载药量及包封产率,用粒径仪测定胶束粒径及多分散指数。
所得结果如图3所示。
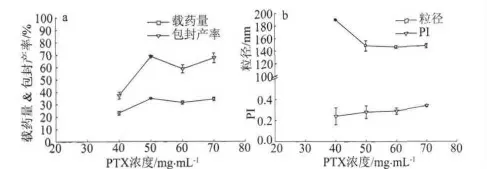
图3 药物浓度对胶束(a)载药量和包封产率以及(b)粒径和PI的影响(n=3)Fig 3 Effect of different concentration of PTX on micelle(a)DL and EE(b)size and PI(n=3)
结果表明,当紫杉醇质量浓度为30mg·mL-1时胶束载药失败,推测是由于药物溶液中的乙醇量比较多,透析过程中不易除去使得载药失败;随着浓度的增加载药量和包封产率逐渐上升,粒径和多分散指数也逐渐下降,达到50mg·mL-1后没有显著变化,因此选用紫杉醇质量浓度为50mg·mL-1后期进行处方优化。
2.2.4 透析时间的影响 配制6.0 mg·mL-1的OCCC载体溶液和50 mg·mL-1的紫杉醇乙醇液,在磁力搅拌下,将药物溶液逐滴加入至2.5mL的载体溶液中,混合后分别透析6,12,24,36h后分别过0.8,0.45,0.22μm 微孔滤膜,每个时间点制备3份样品同“2.1”项测PTX 含量和粒径及PI,计算载药量和包封产率。结果如图4所示。
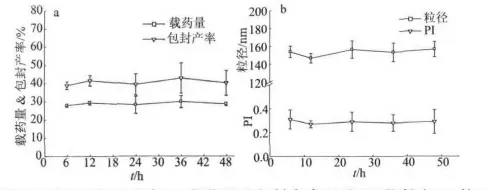
图4 透析时间对胶束(a)载药量和包封产率以及(b)粒径和PI的影响(n=3)Fig 4 Effect of dialysis time on micelle(a)DL and EE(b)size and PI(n=3)
由图可知,6h之后随着透析时间的增加,胶束的载药量、包封产率、粒径以及多分散指数无显著性差异,说明6h之后的透析时间对胶束无明显影响,选择透析时间为6h。
2.3 中心复合面设计优化处方 在单因素考察的基础上,选择对紫杉醇胶束包封产率、载药量影响显著的2个因素,药载比(A)和载体浓度(B)作为考察对象,载药量(DL%)(Y1)和包封产率(EE%)(Y2)为评价指标,利用Design Expert 8.0软件,通过中心复合设计进行实验设计[7],各因素水平代码和具体物理量见表1。应用Design Expert 8.0,对药载比和载体浓度这2个自变量进行实验设计安排结果如表2。

表1 考察因素各水平的代码值及实际操作物理量Tab 1 Independent variables and their correspondent values in code and physical form
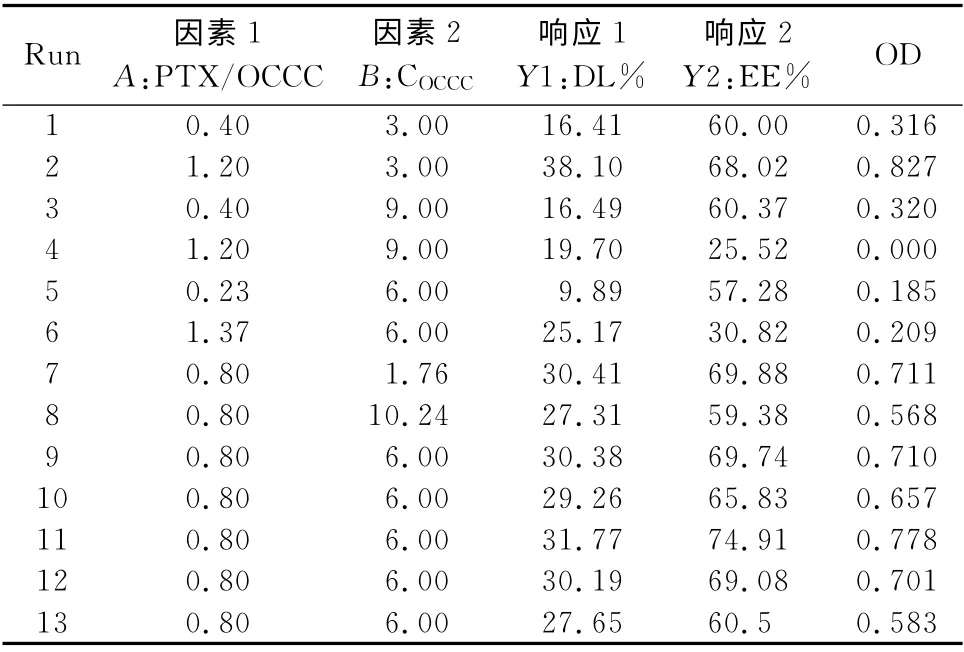
表2 实验设计安排及各考察指标的结果Tab 2 Experiment design and results
评价指标(Y1和Y2)分别对自变量(A 和B)进行多元线性拟合和多元非线性拟合,以相关系数r2和方差分析中的显著性水平P 来评定模型的优度,r2越大,P 越小,模型拟合情况越好。根据模型拟合得到的方程分别绘制2个指标对自变量的三维效应面图。
单量化指标的优化可以根据结果直接进行判断,但当指标超过一个时,指标间往往相互影响,对某一项指标有利的条件可能不利于另一个指标,最终选择条件往往根据这些指标的综合效应。我们引入“总评归一值”(overall desirability,OD)的概念,每个指标均标准化为0~1之间的“归一值”,各指标的“归一值”求几何平均数,得“总评归一值”。公式如下[8-9]:

对取值越大越好的因素(如包封产率、载药量),采用Hassan方法进行数据转化求“归一值”di,公式如下[8,9]:
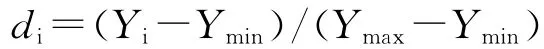
以OD 对2个自变量进行拟合绘制三位效应面图,选取最优处方。按最有处方制备紫杉醇胶束,并进行预测分析。用多元线性模型对各评价指标和自变量(A 和B)进行回归,其方程如下:
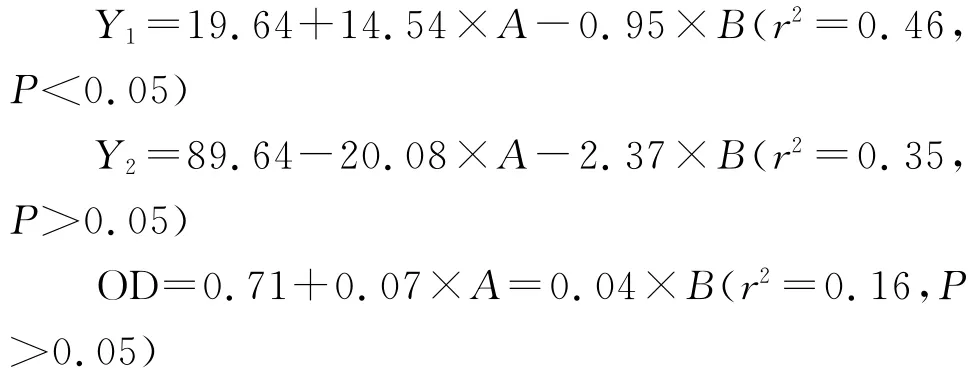
用多元非线性模型对各评价指标和自变量进行回归,各拟合的二次多项式方程为:
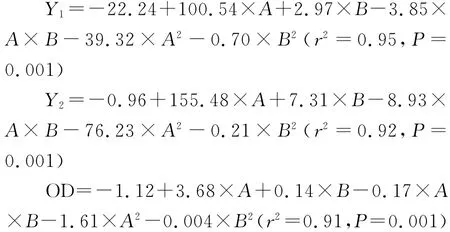
拟合结果表明,以二次多项回归方程的相关系数r高,相关性最好,根据拟合得到的二次多项式方程绘制三维效应面图,如图5 所示,分别为药载比(A)和载体浓度(B)对载药量(Y1)和包封产率(Y2)的三维效应面图。从图中可以直观地观察到最优区域,得到的最优处方为药载比为0.98,载体质量浓度为3.0mg·mL-1。

图5 载药量(Y1),包封产率(Y2)和OD 值对药载比(A),载体浓度(B)的效应面图Fig 5 The predicted response surface of the drug loading(Y1),entrapment efficiency(Y2)and OD function of drug/carrier(A)and carrier concentration(B)
根据所得最优处方,透析法制备紫杉醇胶束,测定载药量和包封产率,同时与预测值进行对比分析,结果见表3。
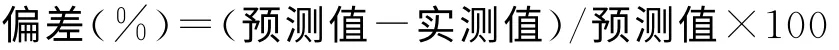

表3 PTX-胶束的预测和实测结果分析Tab 3 Predicted and measured values of PTX-loaded OCCC micelle
由表3可见,按照拟合得到的最优处方制得的紫杉醇胶束,载药量和包封产率与预测值很接近,偏差在规定范围内,表明模型预测较准确。以上优化得到了PTX-OCCC 胶束的最优工艺为:精密称取29.4mg PTX 溶于0.58mL 的无水乙醇中,OCCC载体30.0mg 溶于10mL的去离子水中,磁力搅拌下将PTX 乙醇液缓慢滴加入载体水溶液中,混合后于25 ℃下去离子水透析6h 后分别过0.8,0.45,0.22μm 微孔滤膜,得到pH 敏感型胶束的载药量为(34.8±2.5)%,包封产率为(69.8±4.4)%。粒径为(142.5±4.4)nm,Zeta电位为(-23.5±1.2)mV。
2.4 胶束冻干品的配伍稳定性 紫杉醇胶束冻干品与临床常用的5%葡萄糖溶液,0.9%生理盐水的配伍稳定性进行初步性考察。紫杉醇胶束冻干粉分别以5%葡萄糖溶液、0.9%生理盐水溶液稀释,置室温、自然光下于0,2,4,6,8h取样,测定其中药物含量、粒径、Zeta电位。含量以0h时间点溶液中的紫杉醇含量为100%,计算其他时间点相应溶液中的紫杉醇百分含量,计算出泄漏率。泄漏率按如下公式计算:
泄漏率=(1-冻干后胶束中药物浓度/冻干前胶束中药物浓度)×100%
以粒径和PTX 泄漏率为考察指标评价胶束与常用输液5%葡萄糖溶液、0.9%生理盐水在8h内的配伍稳定性,结果见表4,胶束冻干粉用5%葡萄糖和0.9%生理盐水复溶后粒径均无明显改变,但是用葡萄糖复溶的胶束中PTX 含量偏低,这可能与临床输液的pH 不同有关,5%葡萄糖溶液的pH 值为3.2~5.5,而0.9%生理盐水的pH 值为5.5~7.4,低pH 值的输液可能导致pH 敏感的胶束不稳定。因此建议临床使用时用0.9%生理盐水与之配伍。
3 讨论
近年来新型给药系统处方筛选和工艺优化主要以星点复合设计(CCD)的应用较多,根据星点设计所建立的数学模型描绘效应面,将各效应面的等高线进行重叠直接得到了较佳区域,直观方便地确定了较优处方。多个效应所选择的较佳条件通过叠加,可以进一步缩小较佳条件范围。若无重叠区时,可通过归一化,求总评“归一值”的方法进行综合评价。
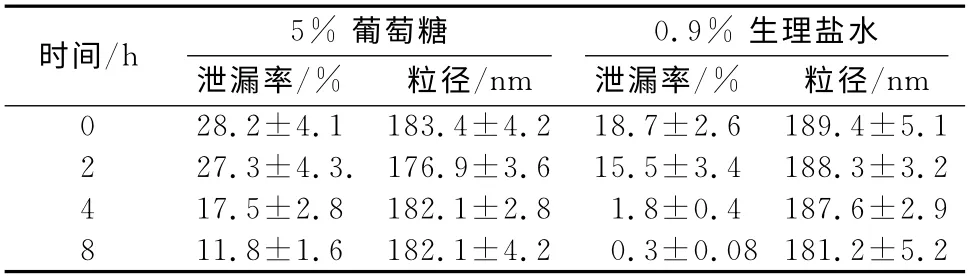
表4 PTX-胶束冻干品与5%葡萄糖和0.9%生理盐水的配伍稳定性Tab 4 The compatible stability of PTX micelle with 5%glucose infusion solution and 0.9%normal saline solution
研究结果表明,中心面复合设计适用于pH 敏感型紫杉醇胶束的工艺优化,所建立的数学模型预测性良好,PTX 胶束具有较高的载药量和包封产率。配伍稳定性研究表明胶束冻干品用pH 近中性的生理盐水复溶后稳定性好。制备过程中胶束溶液过微孔滤膜目的是为了滤除粒径过大的胶束使粒径分布趋于均一,这样保证所得胶束的粒径是纳米级别,有利于减少胶束进入体内后被RES系统摄取,延长体循环时间从而实现被动靶向作用,胶束较高的Zeta电位值使得胶束粒子互相排斥从而增强胶束在循环系统中的稳定性。
[1] 梅林,宋洪范,宋存先.紫杉醇制剂研究进展[J].中国药学杂志,2006,41(18):1366-1370.
[2] Kwon GS.Polymeric micelles for delivery of poorly water-soluble compounds[J].Critical Reviews in Therapeutic Drug Carrier Systems,2003,20(5):357-403.
[3] 刘佳,张灿,平其能.pH 敏感型紫杉醇胶束的制备[J].中国科技论文在线,2011,6(9):649-655.
[4] 吴摇伟,崔光华.星点设计原效应面优化法及其在药学中的应用[J].国外医学药学分册,2000,27(5):292.
[5] Zhang C,Ping Q,Zhang H,et al.Preparation of N-alkyl-Osulfate chitosan derivatives and micellarsolubilization of taxol[J].Carbohydrate Polymers,2003,54(2):137-144.
[6] Yin HQ,Lee ES,Kim D,et al.Physicochemical characteristics of pH-sensitive poly(L-Histidine)-b-poly(ethylene glycol)/poly(L-Lactide)-b-poly(ethylene glycol)mixed micelles[J].J Control Release,2008,12(2):130-138.
[7] 平其能.现代药剂学[M].北京:中国医药科技出版社,2001:588-607.
[8] Hassan EE,Parish KC,Gallo JM.Optimized formulation of magnetic chitosan microspheres containing the anticancer agent,oxantranzole[J].Pharm Res,1992,9(3):390-397.
[9] 吴摇伟,崔光华,陆彬.实验设计中多指标的优化:星点设计和总评“归一值”的应用[J].中国药学杂志,2000,35(8):530.

