用高效液相色普测定乳或乳制品中的乳铁蛋白
廖长保
(雅士利国际集团有限公司 广东潮州 515638)
乳铁蛋白(Lactoferrin,Lf)是1939年由Sorensen等在动物乳中发现的一种功能因子。1960年首先由Groves从牛乳中分离获得,因与铁结合而呈红色,故称之为“红蛋白”。在发现之初,LF被认为是一种与铁的转运和存储有关的蛋白质,所以又称乳转铁蛋白。乳铁蛋白是一种具有多种生物学功能的蛋白质。2004年4月12日,卫生部发布第6号号公告,首次允许乳铁蛋白可在婴幼儿配方乳粉中添中。目前生乳中的乳铁蛋白的检测方法还很少,本文建立高效液相色谱法对乳或乳制品中乳铁蛋白进行测定。
1 仪器设备
(1)Waters-600E多溶剂递送系统,-600E系统控制器,-600E带100ml泵头的溶剂递送系统;(2)Waters486可调吸光度检测器;(3)Waters基线系统控制器;(4)47mm玻璃过滤器座;(5)47mm,0.45μm纤维素滤膜;(6)锥形烧瓶;(7)真空抽吸装置;(8)25mm碟形过滤中座;(9)可设置小型过滤器,25mm醋酸纤维素(滤膜);(10)聚丙烯锁定注射针筒,容量6ml;(11)AE200型分析天平;(12)PH计;(13)磁力搅拌器;(14)烧杯(容量1L,2个);(15)贝克曼微型离心机;(16)容量瓶(容量1L,2个)。
2 材料和试剂
(1)milli-Q(超纯水,电饱18兆欧);(2)磷酸氢二钠(BDH分析级)(分子量142.0);(3)氯化钠(分子量58.44);(4)正磷酸(BDH分析级) (分子量98.00)。
3 步骤
3.1 缓冲液的制备
1)缓冲液A:50mM Na2HPO4PH7.00。①称取7.100克Na2HPO4于玻璃烧杯中,用850ml超纯水溶解;②将上述溶液用正磷酸溶液调至PH=7.00;③将调好PH值的溶液转移到1升的容量瓶中,用超纯水定容;④把定容好的缓冲液通过0.2μm乙酸纤维素过滤到锥形瓶中。
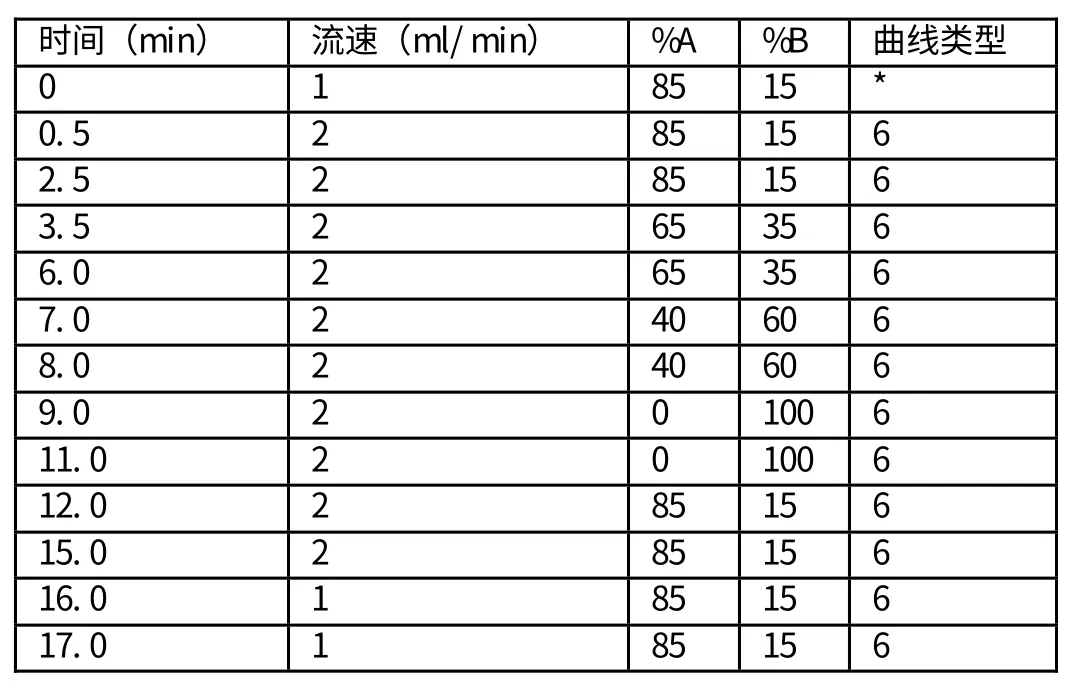
表1
2)缓冲液B:50mM NaHPO4+1.0M NaCl PH7.00。①称取7.100克Na2HPO4和58.440克NaCl于玻璃烧杯中,用850ml超纯水溶解;②将上述溶液用正磷酸溶液调至PH=7.00;③将调好PH值的溶液转移到1升的容量瓶中,并用超纯水定容;④把定容好的缓冲液通过0.2μm乙酸纤维素滤膜过滤到锥形瓶中(注:缓冲液可保存10天有效)。
3.2 标准液的制备
1)为了制备标准贮存液,将适量纯乳铁蛋白的标准物溶于超纯水中,制成蛋白浓度近似8.0mg/ml的溶液(按称的重量准确计算其浓度);
2)用超纯水将1ml标准贮存液稀释成20ml(按称量质量准确计算其浓度);
3)为确定溶液的精确浓度,将过滤过的溶液在波长280nm处测定其吸光度,按以下公式计算其浓度:

假定乳铁蛋白标准液是10%的饱和溶液,按照E1%1cm=13.0,由280nm处的吸光度可确定其纯度
纯度=X/稀释过的贮备液的浓度
标准贮存液的实际浓度等于称重计算出的浓度值乘以上面计算出的纯度;
4)每次使用HPLC之前,都必须吸取1ml的标准液,用缓冲液A稀释至0.2mg/ml,并经过0.2μm乙酸纤维素滤膜过滤。
3.3 乳样品的制备
①将乳样品离心以除去乳脂肪(5分钟);②将脱脂过的乳液用0.45μm乙酸纤维素滤膜过滤;③注入100μl(进样量100μl)。
4 分析条件
(1)梯度表:每个样品分析的时间:17分钟
(2)检测皿的设定:波长229nm,全标尺吸光度单位0.200
(3)固定相:Hi Trap Heparin
5 计算和报告
乳铁蛋白的浓度报告:通过注入不同体积(例如20μl,60μl,100μl,200μl)的乳铁标准液,以吸收峰面积对(浓度×进样体积)画图,标定曲线的斜率,Y轴截距和线性回归可以计算出。
6 结语
总之,是一种具有多种生物学功能的蛋白质,母乳中同样含有此成分,卫生部也明确规定可用于婴幼儿食品中。为确保乳铁蛋白在食品中的添加量,迫切需要建立乳或乳制品中乳铁蛋白的检测方法,本方法回收率高,结果准确,适用于乳或乳制品中乳铁蛋白的检测。
[1]Tatua生物学(1991)“用HPLC测定乳铁蛋白的浓度”.
[2]夏明,应铁进.食品科学[J].2010年第2期.

