硫酸酯化银耳多糖的制备及抗氧化性活性研究
郭晓强,何 钢,刘 嵬,杨轶浠,刘 波,苟小军*
1成都大学生物产业学院;2 成都大学药食同源植物资源开发四川省高校重点实验室,成都610106
银耳(Tremella fuciformis Berk)又称白木银耳、雪耳等,我国银耳产区主要集中在四川通江和福建漳州等地,银耳具有“补肾、润肺、生津、止咳”之功效。随着银耳功能性组分的明确以及银耳多糖(Tremella polysaccharides,TP)药理活性的研究深入,银耳所含有的酸性多糖具有广泛的生理活性,能提高机体免疫力、抗肿瘤、清除自由基,诱导人体产生抗体及干扰素,可治疗高血压、高血脂、糖尿病等多种医学中疑难病症[1,2]。
在天然多糖分子中引入某种离子基团并且具有恰当的取代度时,不仅能够显著改善多糖在水溶液中的溶解度,而且可以使多糖在水溶液中的链构象发生改变,从而使其具有某种特定的结构而提高生物活性。[3]多糖的硫酸酯化可导致原有多糖的生物活性发生明显改变,多糖的硫酸酯化成为多糖结构修饰的一个重要方向。[4]本文从银耳子实体中提取、分离纯化得到银耳多糖,采用氯磺酸-吡啶法研究在不同反应条件下对硫酸酯化银耳多糖(Sulfate Tremella polysaccharides,S-TP)取代度的影响,并且对不同取代度硫酸酯化银耳多糖在体外清除羟基自由基的情况进行研究。
1 材料与方法
1.1 实验材料与试剂
银耳子实体干品(市售),氢氧化钠、硫酸亚铁、氯化钡、水杨酸、硫酸钾、明胶、氯磺酸、吡啶、氯仿、正丁醇、乙醇(95%)、三氯乙酸、H2O2(30%)、N,N-二甲基甲酰胺(DMF)、浓盐酸(均为国产分析纯,新购置。),透析袋(MW 8000,美国联合碳化),1,1-二苯基-2-苦基肼(DPPH)购于百灵威科技公司。其中氯磺酸、吡啶、N,N-二甲基甲酰胺(DMF)按照要求进行精制和干燥处理。[5]
1.2 实验仪器
GL-21M 型高速冷冻离心机(湘仪)、UV-1800紫外分光光度计(尤尼柯仪器有限公司)、FD-1C-55型真空冷冻干机机(北京博医康实验仪器有限公司)、UV-2802PC 紫外扫描仪(尤尼柯仪器有限公司)、Spectrum TWO 红外光谱仪(Perkin Elmer 公司)。
1.3 实验方法
1.3.1 银耳多糖(TP)的制备[6]
银耳子实体于70 ℃干燥2 h,粉碎,过60 目筛。取银耳粉末50 g ,室温条件下用乙醇(80%)搅拌浸泡银耳粉末12 h,减压抽滤,滤饼用10 倍体积70 ℃的水浸提5 h,冷冻离心,取上清液,并重复浸提1次。合并提取液,减压浓缩,向残余物中加入乙醇至终浓度80%,静置2 h,离心分离,沉淀加适量蒸馏水溶解,取上清液,采用Sevage 试剂除蛋白后,80%乙醇析出沉淀经过真空冷冻干燥即得银耳多糖(TP)4.58 g,提取率为9.17%。
1.3.2 硫酸酯化银耳多糖(S-TP)的制备[7,8]
1.3.2.1 磺酰化试剂的制备
将8 mL 吡啶加入附有冷凝管和磁力搅拌装置的50 mL 干燥三颈瓶中,冰盐浴冷却和搅拌条件下,用恒压滴液漏斗慢慢加入氯磺酸2 mL,控制滴加速度,使温度保持在室温以下,反应产物为淡黄色固体,备用。
1.3.2.2 硫酸酯化银耳多糖(S-TP)的制备
室温下银耳多糖(TP)0.1 g 混悬于10 mL N,N-二甲基甲酰胺(DMF),搅拌30 min 后将其加入制备好的磺酰化试剂中,油浴加热搅拌3 h,反应结束后冷却至室温,用2.5 mol/L 的NaOH 溶液中和反应液至中性,搅拌下加入3 倍体积乙醇(95%),析出沉淀,室温搅拌过夜后离心收集沉淀,沉淀溶于适量蒸馏水中,用蒸馏水透析3 d,减压浓缩,真空冷冻干燥获得硫酸酯化银耳多糖。
1.3.3 硫酸酯化银耳多糖硫酸根离子含量的测定[9,10]
1.3.3.1 标准曲线的绘制
精确称取105 ℃干燥至恒重的硫酸钾0.2175 g,以1 mol/L 盐酸定容至50 mL 得到硫酸根标准溶液,再配制3% 三氯乙酸溶液和BaCl2-明胶溶液(BaCl21.0%,明胶0.5%),按表-1 实验条件加入具塞试管,室温静置15 min 后在360 nm 处测定其吸光值A1;再以相同体积的0. 5% 明胶溶液代替BaCl2-明胶溶液按照上述操作方法在360 nm 处测定其吸光度A2,以(A1-A2)对硫酸根浓度作标准曲线。
表1 SO含量测定标准曲线实验条件Table 1 The experiment conditions of the standard curve of assaying SO

表1 SO含量测定标准曲线实验条件Table 1 The experiment conditions of the standard curve of assaying SO
浓度梯度Concentration gradient空白组Control 1 2 3 4 5 K2SO4(mL)Potassium sulfate 0.080.160.240.320.4 HCl(mL)Hydrochloric acid0.40.320.240.160.080三氯乙酸(mL)Trichloroacetic acid7.67.67.67.67.67.6 BaCl2-明胶(mL)(A1)Barium chloride -gelatin222222明胶(mL)(A2)Gelatin 0 2 2 2 2 2 2
1.3.3.2 试样中硫酸根含量的测定
精确称取硫酸酯化银耳多糖试样20 mg 于安瓿瓶中,加入2 mL 1 mol/L HCl 溶液,N2保护下封管。沸水浴加热1 h,取0.2 mL 进行试样溶液进行分析,按照绘制标准曲线的方法,测定其吸光度A1。
根据标准曲线得到试样中SO2-4的百分含量,再按照以下公式计算硫酸酯化银耳多糖(S-TP)的取代度(DS)。[11]
DS=1.62 ×S% /(32-1.02 ×S%)
S%:试样中硫元素百分含量。
1.3.4 紫外光谱分析
将硫酸酯化银耳多糖溶液在200~400 nm 处扫描。
1.3.5 红外光谱分析
银耳多糖及硫酸酯化银耳多糖用溴化钾压片后进行红外光谱测定。
1.3.6 清除羟基自由基的测定[12,13]
向试管中加入不同浓度多糖溶液1.00 mL,Fe-SO4(1. 8 mmol/L)溶液2 mL,水杨酸-乙醇(1. 8 mmol/L)溶液1.50 mL,最后加H2O2(0.3%)0.10 mL 启动反应,振荡混合,37 ℃水浴保温30 min,在波长510 nm 处测定其吸光度值。并按下列公式计算多糖对羟基自由基的清除率。
清除率=[(A0-AS)/A0]×100%
A0:空白管的吸光度;AS:加入自由基清除剂后的吸光度。
2 实验结果与分析
2.1 硫酸酯化银耳多糖紫外光谱测定结果
硫酸酯化银耳多糖紫外扫描结果见图-1,在260 nm 附近出现一个新的吸收峰,说明银耳多糖分子可能连接上了硫酸酯基团。[14]

图1 硫酸酯化银耳多糖UV 图谱Fig.1The ultraviolet spectrogram of the sulfated Tremella polysaccharides
2.2 硫酸酯化银耳多糖红外光谱测定结果
银耳多糖的红外光谱见图2,3424 cm-1处的宽吸收峰在3600~3200 cm-1之间,表示有O-H 的伸缩振动;在3000~2800 cm-1之间,2929 cm-1处弱吸收表示C-H 的特征峰;1626 cm-1处是C =O 键的吸收峰,1413 cm-1处是C-H 键的变角振动,以上各峰均为多糖的特征吸收峰。而1074 cm-1处的强吸收峰是吡喃糖环的醚键C-O-C 的吸收峰,897 cm-1处的弱吸收表明有β-D-葡聚糖的存在。
硫酸酯化银耳多糖红外光谱(图3)中均保留了银耳多糖的特征吸收峰,而新出现的1259 cm-1左右的S=O 伸缩振动和816 cm-1左右的C-O-S 伸缩振动的特征吸收峰,说明硫酸基以酯键的形式已经连接在银耳多糖分子上。

2.3 银耳多糖硫酸酯化反应条件的确定
根据表-2 中不同反应条件按1.3.2 方法对银耳多糖进行硫酸酯化修饰,BaCl2-明胶比浊法测定硫酸根离子含量,得到标准曲线(图-4),线性关系良好,回归方程为:Y =1.4804X-0.13(R2=0.9993)。

图4 硫酸酯化银耳多糖硫酸根离子含量测定标准曲线Fig.4 The standard curve of assaying SOfor the sulfated Tremella polysaccharides
在反应温度60 ℃下吡啶与氯磺酸按照4∶1、2∶1 和1∶1 三种体积比例制备硫酸酯化银耳多糖(STP),取代度测定结果及分析见表-2、图-5。在相同反应温度下硫酸酯化银耳多糖的取代度随吡啶和氯磺酸比例的降低而减小,当吡啶与氯磺酸比例(体积)为4∶1,60 ℃反应3 h 时,DS 最大为1.32。

表2 硫酸酯化银耳多糖硫元素含量(S%)和取代度(DS)测定结果Table 2 The reaction conditions,sulfur content(S%)and degree of substitution(DS)of the sulfated Tremella polysaccharides

图5 硫酸酯化银耳多糖不同反应条件下取代度(DS)结果分析Fig.5 Assay of degree of substitution(DS)of synthetized sulfated Tremella polysaccharides under different reaction condition
2.4 S-TP 及TP 对Fenton 反应产生羟基自由基的清除作用
硫酸酯化银耳多糖试样(S-TP-1~ S-TP-3)和银耳多糖(TP)均取20 mg,分别溶于10 mL 蒸馏水中配制成2 mg/mL 试样溶液,对每个试样分别取0.2,0.4,0.6,0.8,1.0 mL,加水补足至1.0 mL。然后按照1.3.4 进行反应,测定试样在A510处的吸光值,计算试样对羟基自由基的清除率,结果见表-3 和图-6。
硫酸酯化银耳多糖(S-TP-1~ S-TP-3)和银耳多糖(TP)对羟基自由基的清除能力基本随试样浓度的升高呈量效关系,其中S-TP-2 的0.8 mg/mL 实验组除外;当S-TP 试样浓度为0.8~2.0 mg/mL时,清除率均随取代度增大而提高;高取代度试样S-TP-1 浓度1.2~2.0 mg/mL 时清除率增加趋势明显减缓,而S-TP-2 和S-TP-3 在整个实验浓度范围内清除率增大趋势相对平缓,其中S-TP-2 的0. 8 mg/mL 实验组还较0.4 mg/mL 实验组清除率低。
当试样浓度0.8~2.0 mg/mL 时高取代度试样S-TP-1 相对于对照组TP 的清除率具有明显的优势,但随浓度升高两者之间的差距逐渐缩小;当试样浓度0.8~2.0 mg/mL 时对照组TP 对羟基自由基清除率均大于S-TP-3,试样浓度1.2~2.0 mg/mL时对照组TP 对羟基自由基清除率优于S-TP-2。

表3 S-TP-1~S-TP-3 及TP 对羟基自由基的清除率.Table 3 Scavenging effect on hydroxyl radical in vitro by different concentrations of TP and sulfated derivatives
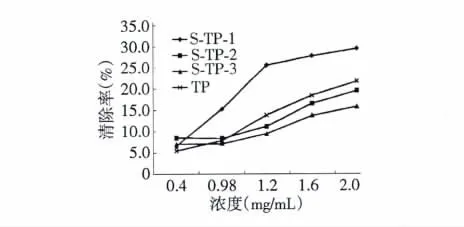
图6 S-TP 及TP 对羟基自由基的清除作用Fig.6 Assay of scavenging effect on hydroxyl radical in vitro by different concentrations of TP and sulfated derivatives
3 结论
氯磺酸-吡啶法制备硫酸酯化银耳多糖在本实验条件下最佳反应条件为吡啶与氯磺酸体积比4∶1,反应温度60 ℃,反应时间3 h;硫酸酯化银耳多糖硫元素含量S% =14.23%、取代度DS =1.32。在相同反应温度下硫酸酯化银耳多糖的取代度随吡啶和氯磺酸体积比的降低而减小,吡啶一方面作为氯磺酸与多糖发生酯化反应生成氯化氢的缚酸剂,另一方面吡啶通过与氯磺酸反应生成氯磺酸吡啶盐而起到催化作用。[15]因此在氯磺酸和吡啶对银耳多糖大大过量(本文氯磺酸为多糖的20 倍量)的情况下,吡啶与氯磺酸的体积比增加有利于硫酸酯化反应的进行。
硫酸酯化银耳多糖对Fenton 反应所产生羟基自由基均有一定的清除作用,且随多糖浓度的增加,清除率升高,呈一定的量效关系。取代度为1.32 的S-TP 在0.8~2.0 mg/mL 浓度范围内相对于对照组TP 的清除率具有明显的优势。多糖分子通过硫酸酯化引入硫酸根,引起极性增加、水溶性提高和粘度降低等理化性质变化,取代度较高的银耳多糖分子来说上述特性相对增加较多,这可能是导致硫酸酯化银耳多糖随取代度升高而体外活性提高的原因之一。[16]因此硫酸酯化修饰多糖分子可以作为天然产物改性的一个重要方法,其作用机制还有待进一步探讨。
1 Gou XJ(苟小军),Guo XQ(郭晓强),Yan J(颜军).China Tremella (中国银耳). Beijing:China Agriculture Press,2009.255-299.
2 Chen FF(陈飞飞),Cai DL(蔡东联).Research advances in primary biological effects of Tremella polysaccharides. Journal of Chinese Integrative Medicine(中西医结合学报),2008,6:862-867.
3 Adachi Y,Ohno N,Ohsawa M,et al.Change of biological activities of (1 →3)-β-D-Glucan from Grifola frondosa upon molecular weight reduction by heat treatment. Chem Pharm Bull,1990,38:477-481.
4 Talarico LB,Zibetti RGM,Faria P,et al.Anti-herpes simplex virus activity of sulfated galactans from the red seaweeds Gymnogongrus griffithsiae and Cryptonemia crenulata. Int J Biol Macromol,2004,34(12):63-71.
5 Huang S(黄枢),Xie RG(谢如刚).Handbook of preparating organic solvent,2nded(有机合成试剂制备手册).Beijing:Science Press,2006.335-336.
6 Yan J(颜军),Xu GY(徐光域),Guo XQ(郭晓强),et al.Research on the purification and anti-oxidize activity of Tremella polysaccharide. Food Sci(食品科学),2005,26:169-172.
7 Wang SC(王顺春),Fang JN(方积年). Preparation and structural analysis of sulfated derivatives of Lentinan. Acta Biochimica et Biophysica Sinica(生物化学与生物物理学报),1999,31:594-597.
8 Lu Y,Wang DY,Hu YL,et al. Sulfated modification of epimedium polysaccharide and effects of the modifiers on cellular infectivity of IBDV. Carbohydr Polymers. 2008,71:180-186.
9 Cong JB(丛建波),Wang CZ(王长振),Li Y(李妍),et al.Investigation of barium sulfate turbidimetry on determination the sulfated group of sulfated polysaccharides.Pharm J Chin PLA(解放军药学学报),2003,19:182-183.
10 Xie J(谢佳),Zhang J(张静),Liu H(柳红). Preparation and antioxidant research of pumpkin polysaccharide sulfate.Science and Technology of Food Industry(食品工业科技),2008,29(9):60-62.
11 Zhang WJ(张惟杰). Sugar Complex Biochemical Research Technology,2nded(糖复合物生化研究技术). Hangzhou:Zhejiang University Press,2006:291-292.
12 Yan J(颜军),Gou XJ(苟小军),Zou QF(邹全付),et al.Determination of hydroxyl radical generating from Fenton reaction by spectrophotometry.J Chengdu Univ Nat Sci Ed(成都大学学报),2009,28(2):89-92.
13 Wang BB(王蓓蓓),Duan YF(段玉峰),Shao HJ(邵红军),et al.Antioxidant activity of polysaccharide from Dictyophora rubrovalvata.Nat Prod Res Dev(天然产物研究与开发),2012,24:1122-1125.
14 Wang YH(王亚辉).Preparation,structural analysis and activity research of sulfated derivatives of Lentinan. Nanjing:Nanjing Normal University,MSC.2005.
15 Wen R(闻韧).Organic Reactions for Drug Synthesis,second ed(药物合成反应). Beijing:Chemical Industry Press,2004.125-126.
16 Wang YF.Structure and bioactivities of polysaccharides from sclerotium of Poria cocos and their derivatives. Wuhan:Wuhan University,PhD.2004.

