通窍鼻渊丸制备过程中栀子苷转移率的实验研究
肖正国,李喜香,刘效栓,姜玲艳
(甘肃省中医院,甘肃兰州730050)
通窍鼻渊丸为我院院内制剂,由栀子、辛夷、葛根、川芎等15味中药组成,为半粉末浓缩丸。栀子为其主药。栀子是茜草科植物Gardenia jasminoides Ellis的干燥成熟果实,性味苦寒,入心、肝、肺、三焦经,具有抗炎、镇痛、解毒之功效[1]。栀子属植物中含有黄酮类(栀子素类)、环烯醚萜类(栀子苷类)、三萜类(栀子花酸类)和有机酸脂类(绿原酸)等多种化合物,而栀子苷是栀子药材中环烯醚萜类的代表成分。2010版《中国药典》规定:栀子苷为栀子药材药效成分评价的指标[2-4]。本实验探讨了通窍鼻渊丸在制备的各个环节中,栀子苷含量变化的规律,以期为生产提供一定的理论依据。
1 药品、试剂与仪器
所用药材饮片购自兰州安泰堂中药饮片公司、兰州方正药业有限公司,经甘肃省中医院药物分析实验室检定,符合2010版《中国药典》各药材项下规定的标准。栀子苷对照品,供含量测定用,由中国药品生物制品检定所提供,批号110749-200714;甲醇(批号20100410),乙腈(批号20100410),为色谱纯,由天津市科米欧化学试剂开发中心提供;含量测定用水为娃哈哈纯净水;提取用水为饮用水。美国Waters 2695高效液相色谱仪,包括Waters 2487双通道紫外检测器;Sartorius R-200D电子天平,产地德国;HM500型电热套,北京科伟仪器公司产品;KQ2500DE型超声波清洗器,昆山超声仪器有限公司产品;HHS数显恒温水浴锅,北京科伟仪器公司产品;TYPE-YUG101型全自动速控中药制丸机、微波真空干燥仪,均为甘肃天水华圆制药设备有限公司产品。
2 方法与结果
2.1 药材细粉配料
按处方比例称取栀子、辛夷、葛根、川芎等15味药材细粉共 55.6 g,其中栀子6.3 g,辛夷3.3 g。细粉过120目筛,用倍研法混合均匀。
2.2 浸膏的制备
按处方比例称取栀子、辛夷、葛根、川芎等15味药材粗粉共209 g,其中栀子24 g,辛夷6 g。粗粉过3号筛,加水煎煮3次,加水量分别为10倍、8倍、8倍,合并滤液,减压浓缩至稠膏,收膏110 g,干燥失重45%,干膏得率52.6%。
2.3 成品总混合粉制备
浸膏与药材细粉按2∶1的比例混合,制丸成形,40℃微波真空干燥8 min,得丸剂110.5 g。取一定数量的浓缩丸粉碎,得总混合粉。
2.4 栀子苷含量测定
2.4.1 色谱条件
色谱柱(Symmetryshield RP18,4.6 mm ×250 mm,5 μm),流动相为甲醇 ∶水(13∶87),流速1 mL/min,检测波长238 nm,进样量10μL,柱温为室温。理论塔板数按栀子苷峰计,不低于1500[5-6]。
2.4.2 对照品溶液的制备
精密称取栀子苷对照品8.02 mg,加甲醇溶解,稀释定容至50 mL,制成160.4 mg/L的对照品储备液,备用。精密吸取储备液 0.2,0.6,1.0,4.0,8.0,10.0 mL置10 mL容量瓶中,用甲醇定容至刻度,分别得到 3.208,9.624,16.04,64.16,128.32,160.40 mg/L的对照品甲醇溶液。
2.4.3 供试品溶液的制备
分别精密称取2.1,2.2,2.3 项下的细粉、浸膏、总混合粉各1 g,以及栀子药材(细粉∶粗粉质量比为6∶24)0.1 g,置具塞锥形瓶中,精密加入甲醇25 mL,称定质量,超声处理20 min,放冷;再称定质量,用甲醇补足减失的质量,摇匀,滤过;精密量取续滤液10 mL,置25 mL容量瓶中,加甲醇至刻度,摇匀,0.45μm微孔滤膜过滤即得。
2.4.4 阴性对照溶液的制备
按照2.1,2.2,2.3 项下的方法制备不含栀子的浓缩丸,精密称取1 g,参照2.4.3方法,制成阴性对照溶液。
2.4.5 线性关系考察
精密吸取2.4.2项下栀子苷对照品溶液各10μL进样测定,以峰面积(A)为纵坐标,浓度(C)为横坐标进行回归,得回归方程 A=320.619C+28 277.210,r=0.999 2(n=6)。表明:栀子苷在3.208~160.40 mg/L范围内峰面积与浓度的线性关系良好。
2.4.6 精密度试验
取3.208 mg/L的栀子苷对照品溶液按2.4.1项下色谱条件,连续进样6次,峰面积的RSD值为0.18%(n=6)。
2.4.7 稳定性试验
精密吸取2.4.3项下的供试品溶液在 0,2,4,8,10,12 h各进样10μL,记录峰面积。结果峰面积的RSD=0.28%,表明供试品溶液在12 h内稳定。
2.4.8 重复性试验
分别精密称取 2.1,2.2,2.3 中的样品各 5 份,照2.4.3的方法各制备5份样品溶液,进行测定。结果:栀子苷峰面积的 RSD值分别为 0.28%、0.42%、0.29%(n=5)。
2.5 含量测定
分别精密吸取对照品溶液、供试品溶液、阴性对照品溶液各10μL进样,按上述色谱条件进行测定。结果表明,阴性对照溶液色谱图与样品溶液位置处无干扰(见图1~5),此方法可行。

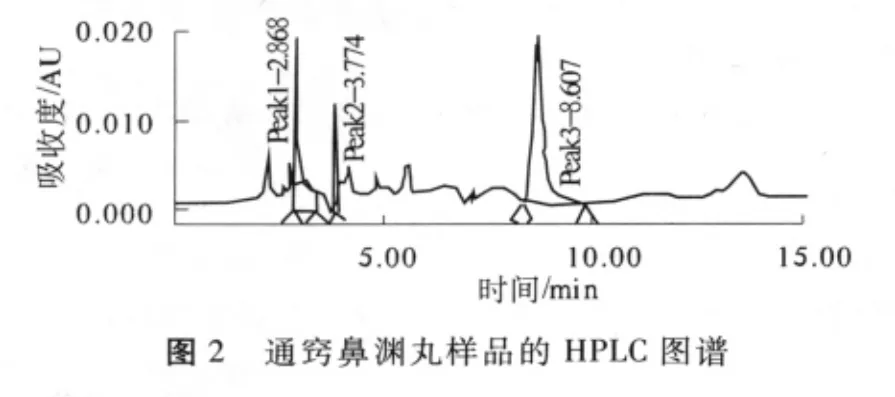



2.6 结 果
栀子原料药材中栀子苷含量以2.098%计,结果按下列公式计算[7]:
每g样品中栀子苷的含量=[实测浓度(mg/L)×25L/10 g/L]×0.025 L
每g细粉中栀子苷理论投入量=1×6.3/55.6×2.098% ×100% ×103
每g浸膏中栀子苷理论投入量=1×24/110×2.098% ×100% ×103
每g成品中栀子苷理论投入量=1×(30.3×2.098%) ×100%/110.5 ×103
栀子苷转移率=每g样品中栀子苷含量/理论投入量×100%,结果见表2。
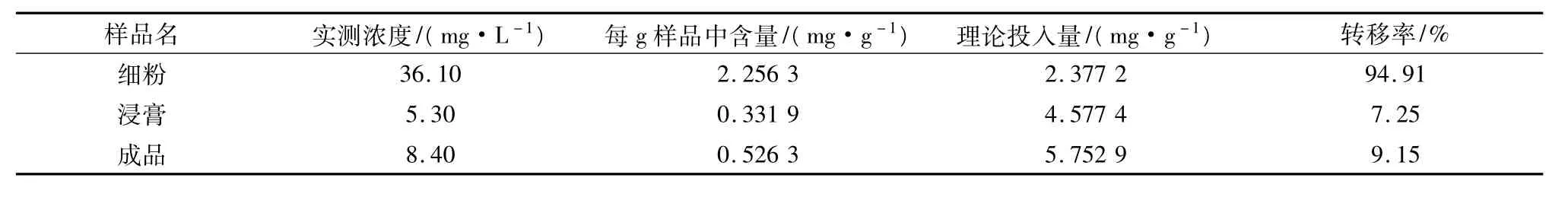
表2 实验结果
3 讨论
根据《中国药典》规定[1],栀子药材中之栀子苷的含量不低于1.8%。以此为依据,在目前的条件下,院内制剂通窍鼻渊丸中栀子苷含量应不低于0.45 mg/g;以此可作为鼻渊丸质量内控标准的依据。从表2的实验数据可知,我们以往采用的水提浓缩工艺相对落后,资源浪费较大。浸膏制作过程栀子苷只有7.25%被利用,由原料到成品转移率不到10%,究其原因,可能有以下几点:①提取不完全。据文献报道,与栀子环烯醚萜苷的溶解性相匹配的溶剂的极性,在乙酸乙酯与甲醇之间[8],而大部分文献采用500~600 g/L)的稀乙醇提取[9]。②浓缩中破坏。即使在减压条件下,水提液浓缩时温度亦在60℃以上,生产上很难控制。③干燥时的温度[10]。尽管中药复方制剂成分复杂,只使用单一有效成分分析,难以全面表达制剂质量的全面性和系统性[11],但由原料至成品,毕竟栀子苷损失了90%之多。如何提高栀子苷转移率,同时尽量减少其他有效成分的损失,是研究的关键。在进一步研究中,笔者采用乙醇为溶剂,以干膏得率和栀子苷含量结合,综合评分为考察指标,均匀设计优选出正确的提取工艺:即乙醇浓度为527.3 g/L,固液比为10.82倍,提取时间为60.91 min,提取次数为 3 次[12]。工艺验证中,栀子苷转移率提高到32.5%。
[1]国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2010:231.
[2]陈阳,贾林,蔡乐,等.四川纳溪地区栀子指纹图谱及红花苷、栀子苷含量的研究[J].华西药学杂志,2010,25(4):458-460.
[3]Wang SC,Tseng TY,Huang CM,et al.Gardenia herbal active constituents:applicable separation procedures[J].J Chromatogr B Analyt Technol Biomed Life Sci,2004,812(1-2):193-202.
[4]Chio HJ,Park YS,Kim MG,et al.Isolation and characterization of the major colorant in Gardennia fruit[J].Dyes Pigm,2001,49(1):15-20.
[5]耿立冬,石任兵,萨楚拉,等.栀蒡热毒平中栀子苷、牛蒡子苷、黄芩苷在大鼠体内血药浓度的测定[J].北京中医药大学学报,2010,33(5):350-353.
[6]Tasai TR,Tseng TY,Chen CF,et al.Identification and determination of geniposide contained in Gardenia jasminoides and in two preparations of mixed traditional Chinese medicines[J].JChromatogr A,2002,961(1):83-88.
[7]傅强,王巧,王少云,等.药物分析实验方法学[M].北京:人民卫生出版社,2008:527-532.
[8]陈芳,董志,傅亚.栀子总环稀醚萜苷纯化工艺研究[J].激光杂志,2010,31(2):95-96.
[9]谢学建,张俊慧,马爱华.中药栀子研究进展[J].时珍国医国药,2007,11(10):943-94.
[10]张海燕,程晓燕,万娜,等.栀子苷稳定性高效液相色谱法考察[J].时珍国医国药,2011,22(2):374.
[11]王雷琛,周婷婷,范国荣.中药栀子中指标性成分定量分析在其质量评价中的应用[J].药学服务与研究,2010,10(4):286-288.
[12]刘效栓,肖正国,李喜香,等.均匀设计优选通窍鼻渊丸提取工艺条件[J].中国中医药信息杂志,2011,18(10):51.

